كروم
 | |||||||||||||||
| كروم | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| المظهر | معدني فضي | ||||||||||||||
| الوزن الذري العياري Ar°(Cr) | |||||||||||||||
| كروم في الجدول الدوري | |||||||||||||||
| |||||||||||||||
| الرقم الذري (Z) | 24 | ||||||||||||||
| المجموعة | 6 | ||||||||||||||
| الدورة | period 4 | ||||||||||||||
| المستوى الفرعي | d-block | ||||||||||||||
| التوزيع الإلكتروني | [Ar] 3d5 4s1 | ||||||||||||||
| الإلكترونات بالغلاف | 2, 8, 13, 1 | ||||||||||||||
| الخصائص الطبيعية | |||||||||||||||
| الطور at د.ح.ض.ق | صلب | ||||||||||||||
| نقطة الانصهار | 2180 K (1907 °س، 3465 °F) | ||||||||||||||
| نقطة الغليان | 2944 K (2671 °س، 4840 °ف) | ||||||||||||||
| الكثافة (بالقرب من د.ح.غ.) | 7.15 ج/سم³ | ||||||||||||||
| حين يكون سائلاً (عند ن.إ.) | 6.3 ج/سم³ | ||||||||||||||
| حرارة الانصهار | 21.0 kJ/mol | ||||||||||||||
| حرارة التبخر | 339.5 kJ/mol | ||||||||||||||
| السعة الحرارية المولية | 23.35 J/(mol·K) | ||||||||||||||
ضغط البخار
| |||||||||||||||
| الخصائص الذرية | |||||||||||||||
| حالات الأكسدة | 6, 4, 3, 2 | ||||||||||||||
| الكهرسلبية | مقياس پاولنگ: 1.66 | ||||||||||||||
| طاقات التأين |
| ||||||||||||||
| نصف القطر الذري | empirical: 140 pm calculated: 166 pm | ||||||||||||||
| نصف قطر التكافؤ | 127 pm | ||||||||||||||
| خصائص أخرى | |||||||||||||||
| البنية البلورية | body-centered cubic (bcc) | ||||||||||||||
| سرعة الصوت قضيب رفيع | 5940 م/ث (عند 20 °س) | ||||||||||||||
| قضيب رفيع | 93.9 W/(m·K) | ||||||||||||||
| التمدد الحراري | 4.9 µm/(m⋅K) (عند 25 °س) | ||||||||||||||
| المقاومة الكهربائية | 125 nΩ⋅m (at 20 °C) | ||||||||||||||
| الترتيب المغناطيسي | antiferromagnetic (rather: SDW)[1] | ||||||||||||||
| القابلية المغناطيسية | +280.0·10−6 cm3/mol (273 K)[2] | ||||||||||||||
| معامل يونگ | 279 GPa | ||||||||||||||
| معامل القص | 115 GPa | ||||||||||||||
| معاير الحجم | 160 GPa | ||||||||||||||
| نسبة پواسون | 0.21 | ||||||||||||||
| صلادة موز | 8.5 | ||||||||||||||
| صلادة ڤيكرز | 1060 MPa | ||||||||||||||
| صلادة برينل | 687–6500 MPa | ||||||||||||||
| رقم كاس | 7440-47-3 | ||||||||||||||
| التاريخ | |||||||||||||||
| الاكتشاف وأول عزل | Louis Nicolas Vauquelin (1794, 1797) | ||||||||||||||
| نظائر الكروم | |||||||||||||||
| قالب:جدول نظائر كروم غير موجود | |||||||||||||||
الكروم أو الكروميوم Chromium، هو عنصر أساس من عناصر الجدول الدوري رمزه Cr فيه 24 بروتون و28 نيوترون.
ويقع الكروميوم في الدور الرابع من الجدول الدوري ضمن عناصر الفصيلة VIB (أو 6) التي تضم كلاً من التنگستن والمولبدنم، وتمتاز هذه المعادن بحجم ذري صغير، ونقطة انصهار مرتفعة وقساوة عالية ومقاومة كبيرة للتآكل، وتأخذ جميعها التكافؤ السداسي في مركباتها إضافة إلى تكافؤات أخرى.
الكروم فلز انتقالي نموذجي، تشمل بنيته الإلكترونية الخارجية المدارات d، وله حالات أكسدة عدة، ويكوّن أيونات معقّدة، مركباته ذات مغناطيسية مسايرة (طردية)، يقوم بدور حفّاز (وسيط)، يكوِّن سبائك (أشابات).[3]
إذا ما تعرض الكروم إلى الهواء الطلق فإنه يتأكسد بسرعة فتتكون طبقة خارجية من أكسيدات الكروم لكنها تعزل في نفس الوقت بقية المعدن الداخلي عن الهواء الطلق.
والكروميوم عنصر أساسي في الجسم، له مشاركة في تأيض النشويات والدهون، وأظهرت الدراسات المعملية على الفئران أن معدن الكروميوم يعمل مع هرمون الإنسولين، ويسهل دخول السكر لداخل الخلية، وقد يفيد في علاج الاكتئاب المصحوب بالنوم الزائد، والنهم للنشويات، حسب دراسة جاءت من جامعة ديوك على 15 مريضاً.
بينما يعتبر معدن الكروم وأيونات Cr(III) غير سامين، فإن الكروم السداسي التكافؤ، Cr(VI) سام ومسرطن. وفقاً لوكالة المواد الكيميائية الأوروبية (ECHA)، يعد ثالث أكسيد الكروم المستخدم في عمليات الطلاء الكهربائي الصناعية مادة ذات أهمية بالغة (SVHC).[4]
غالباً ما تتطلب مواقع إنتاج الكروم المهجورة عمليات تنظيف بيئية.[5]
وهو من العناصر التي يحتاجها جسم الإنسان لكن بكميات ضئيلة جداً في حدود تقدر من خمسة وعشرين إلى مائة مايكرو گرام يومياً.
تظهر الدراسات الحديثة إلى أن الكروم قد يكون له دورا أساسيا في تمرير الأنسولين إلى داخل الخلية وبالتالي الاستفادة منه لذلك قد يكون مفيداً جداً لمرضى السكري وللوقاية منه
الخصائص الفيزيائية
الذرية
الكروم هو رابع فلز انتقالي موجود في الجدول الدوري، وله تكوين إلكتروني لـ [Ar] 3d5 4s1. وهو أيضاً العنصر الأول في الجدول الدوري الذي ينتهك تكوينه الإلكتروني لحالة الأرض مبدأ أوفباو. يحدث هذا مرة أخرى لاحقاً في الجدول الدوري مع العناصر الأخرى وتكويناتها الإلكترونية، مثل النحاس والنيوبيوم و[[مولبدنم |المولبدنم]].[6]يحدث هذا بسبب تنافر الإلكترونات الموجودة في نفس المدار بسبب الشحنات المتشابهة. في العناصر السابقة، كانت التكلفة النشطة لنقل الإلكترون إلى مستوى الطاقة الأعلى التالي أكبر من أن تعوض عن ذلك المنطلق من خلال تقليل التنافر بين الإلكترونات. ومع ذلك، في المعادن الانتقالية 3d، تكون فجوة الطاقة بين الغلاف الفرعي 3d والأعلى من 4s صغيرة جداً، ولأن الغلاف الفرعي 3d أكثر إحكاماً من الغلاف الفرعي 4s، فإن التنافر بين الإلكترونات يكون أصغر بين الإلكترونات 4s منه بين إلكترونات 3d. هذا يقلل من التكلفة النشطة للترويج ويزيد الطاقة التي يطلقها، بحيث يصبح الترويج ممكناً بقوة ويتم دائماً ترقية إلكترون واحد أو حتى إلكترونين إلى الطبقة الفرعية 4s. (تحدث ترقيات مماثلة لكل ذرة معدنية انتقالية ما عدا واحدة، كالپلاديوم.)[7]
الكروم هو العنصر الأول في السلسلة 3d حيث تبدأ الإلكترونات 3d بالانهيار في النواة؛ وبالتالي فهي تساهم بشكل أقل في الترابط المعدني، ومن ثم تكون نقاط الانصهار والغليان والمحتوى الحراري لتذرية الكروم أقل من تلك الموجودة في العنصر السابق كالڤناديوم. الكروم (VI) هو عامل مؤكسد قوي على عكس أكاسيد المولبدنم(VI) وأكاسيد التنگستن (VI).[8]
الصب

الكروم شديد الصلادة، وهو ثالث أصلد عنصر بعد الكربون (ألماس) والبورون. تبلغ صلادة موز 8.5، مما يعني أنه يمكن خدش عينات من المرو والزبرجد، ولكن يمكن خدشها بواسطة السامور. يتميز الكروم بمقاومة عالية للتشويه، مما يجعله مفيداً كمعدن يحافظ على الطبقة الخارجية من التآكل، على عكس المعادن الأخرى مثل النحاس، المغنسيوم، والألمنيوم.
لدى الكروم نقطة انصهار 1907 °C (3465 °F)، وهي منخفضة نسبياً مقارنة بمعظم المعادن الانتقالية. ومع ذلك، لا يزال لديه ثاني أعلى نقطة انصهار من بين جميع عناصر الدورة 4، حيث يتصدرها الڤناديوم بمقدار 3 °C (5 °F) عند 1910 °C (3470 °F). ومع ذلك، فإن نقطة الغليان البالغة 2671 °C (4840 °F) أقل نسبياً، حيث تحتوي على ثالث أدنى نقطة غليان من المعادن الانتقالية من الدورة 4 وحدها خلف المنجنيز والزنك.[note 1] المقاومة الكهربائية للكروم عند 20 درجة مئوية هي 125 نانواوم - متر.
يحتوي الكروم على انعكاس منتظم مرتفع مقارنة بالمعادن الانتقالية الأخرى. في الأشعة تحت الحمراء، عند 425 μm، يمتلك الكروم أقصى انعكاس بحوالي 72٪، ويقلل إلى 62٪ على الأقل عند 750 ميكرومتر قبل أن يرتفع مرة أخرى إلى 90٪ عند 4000 ميكرومتر.[9] عند استخدام الكروم في سبائك الفولاذ المقاوم للصدأ وصقله، يتناقص الانعكاس المرآوي مع تضمين معادن إضافية، لكنه يظل مرتفعاً مقارنةً بالسبائك الأخرى. ينعكس ما بين 40٪ و60٪ من الطيف المرئي من الفولاذ المقاوم للصدأ المصقول.[9] يمكن أن يُعزى تفسير سبب عرض الكروم لمثل هذا الإقبال الكبير من موجات الفوتون المنعكسة بشكل عام، وخاصة 90٪ في الأشعة تحت الحمراء، إلى الخصائص المغناطيسية للكروم.[10]للكروم خصائص مغناطيسية فريدة - الكروم هو المادة الصلبة الوحيدة التي تظهر ترتيب الخصائص المغناطيسية المضادة في درجة حرارة الغرفة وما دونها. فوق 38 درجة مئوية، يصبح ترتيبها مغناطيسي مساير.[1] الخصائص المضادة المغناطيسية، التي تجعل ذرات الكروم تتأين وربطها مؤقتاً، موجودة لأن الخصائص المغناطيسية للمكعب المتمركز في الجسم غير متناسبة مع دورية الشبكة. هذا بسبب اللحظات المغناطيسية في زوايا المكعب ومراكز المكعب غير المتكافئة، ولكن المضادة للتوازي.[10] من هنا، السماحية النسبية المعتمد على التردد للكروم، المشتق من معادلات ماكسويل والمغناطيسية المضادة للكروم، يترك الكروم بأشعة تحت الحمراء عالية وانعكاس الضوء المرئي.[11]
التخميل
يُخمَّل معدن الكروم المتروك في الهواء فهو يشكل طبقة سطحية رفيعة ووقائية من الأكسيد. هذه الطبقة لها بنية [[لعل (جوهرة) |لعل]] بسماكة بضع طبقات ذرية؛ فهو كثيف جداً ويمنع انتشار الأكسجين في المعدن الأساسي. في المقابل، يشكل الحديد أكسيداً مسامياً يمكن للأكسجين أن يرتحل من خلاله، مما يتسبب في استمرار الصدأ.[12] يمكن تعزيز التخميل عن طريق التلامس القصير مع حمض مؤكسد مثل حمض النيتريك. الكروم المُخمَّل مستقر ضد الأحماض. يمكن إزالة التخميل باستخدام مختزل قوي يدمر طبقة الأكسيد الواقية على المعدن. معدن الكروم المعالج بهذه الطريقة يذوب بسهولة في الأحماض الضعيفة.[13]
الكروم، على عكس الحديد والنيكل، لا يعاني من التقصف الهيدروجين. ومع ذلك ، فإنه يعاني من تقصف هيدروجيني، الذي يتفاعل مع النيتروجين من الهواء ويشكل نيتريداً هشاً عند درجات الحرارة العالية اللازمة لتشغيل الأجزاء المعدنية.[14]
النظائر
يتكون الكروم الموجود طبيعياً من ثلاثة نظائر مستقرة؛ 52Cr، 53Cr و 54Cr، مع كون 52Cr الأكثر وفرة (83.789٪ من الوفرة الطبيعية). تم تمييز 19 نظير مشع، وأكثرها استقراراً هو50Cr مع عمر النصف (أكثر من) 1.8×1017 عام، و51Cr مع عمر نصف يبلغ 27.7 يوماً. جميع النظائر المشعة المتبقية لها نصف عمر أقل من 24 ساعة والأغلبية أقل من دقيقة واحدة. يحتوي الكروم أيضاً على مصاوغين نوويين شبه مستقرين.[15]
53Cr هو ناتج الاضمحلال المشع لـ 53Mn (عمر-النصف= 3.74 مليون عام).[16] عادةً ما تكون نظائر الكروم مرتبطة (ومركبة) مع نظائر المنجنيز. هذا الحالة مفيدة في جيولوجيا النظائر. حيث تعزز نسب نظائر المنجنيز والكروم الأدلة من 26Al و107Pd فيما يتعلق بالتاريخ المبكر للنظام الشمسي. الاختلافات في نسب 53Cr/52Cr وMn/Cr من عدة نيازك تشير إلى قيمة أولية 53Mn/55Mn نسبة المنجنيز التي تشير إلى التركيب النظائري للمنجنيز-Cr يجب أن تنتج عن الاضمحلال في الموقع لـ 53Mn في الأجسام الكوكبية المتباينة. ومن ثم، فإن 53Cr يوفر دليلاً إضافياً لعمليات التخليق النووي مباشرةً قبل اندماج النظام الشمسي.[17]
تتراوح نظائر الكروم في عدد الكتلة من 43 u (43Cr) إلى 67 u (67Cr). وضع الاضمحلال الأساسي قبل النظير المستقر الأكثر وفرة، 52Cr، هو التقاط الإلكترون والوضع الأساسي بعده هو اضمحلال بيتا.[15] افتُرض 53Cr كبديل لتركيز الأكسجين في الغلاف الجوي.[18]
الكيمياء والمركبات
الكروم عضو في المجموعة 6، من معدن انتقالي. تحدث حالات +3 و+6 بشكل شائع داخل مركبات الكروم، تليها +2؛ نادراً ما تكون رسوم +1 و+4 و+5 للكروم، ولكنها موجودة في بعض الأحيان.[21][22]
حالات الاكسدة الشائعة
| Oxidation states[note 2][22] | |
|---|---|
| −4 (d10) | Na4[Cr(CO)4][23] |
| −2 (d8) | Na 2[Cr(CO) 5] |
| −1 (d7) | Na 2[Cr 2(CO) 10] |
| 0 (d6) | Cr(C 6H 6) 2 |
| +1 (d5) | K 3[Cr(CN) 5NO] |
| +2 (d4) | CrCl 2 |
| +3 (d3) | CrCl 3 |
| +4 (d2) | K 2CrF 6 |
| +5 (d1) | K 3CrO 8 |
| +6 (d0) | K 2CrO 4 |
الكروم (0)
العديد من مركبات Cr(0) معروفة. مضاعف (بنزين) الكروم وسداسي كربونيل الكروم هما عنصران بارزان في كيمياء الكروم العضوي.
الكروم (II)

مركبات الكروم (II) غير شائعة، ويرجع ذلك جزئياً إلى أنها تتأكسد بسهولة إلى مشتقات الكروم (III) في الهواء. كلوريد الكروم (II) CrCl 2 المستقر بالماء يمكن تصنيعه عن طريق اختزال كلوريد الكروم (III) بالزنك. يكون المحلول الأزرق اللامع الناتج من إذابة كلوريد الكروم (II) مستقراً عند درجة حموضة متعادلة.[13] تتضمن بعض مركبات الكروم (II) البارزة الأخرى أكسيد الكروم (II) CrO، وكبريتات الكروم (II) CrSO 4. العديد من الكربوكسيلات الكروم (II) معروفة. أسيتات الكروم (II) الأحمر (Cr2(O2CCH3)4) مشهور إلى حد ما. ويتميز Cr-Cr برابطة رباعية.[24]
الكروم (III)

يُعرف عدد كبير من مركبات الكروم (III)، مثل نترات الكروم (III)، أسيتات الكروم (III)، وأكسيد الكروم (III).[25]يمكن الحصول على الكروم (III) بإذابة عنصر الكروم في أحماض مثل حمض الهيدروكلوريك أو حمض الكبريتيك، ولكن يمكن أيضاً تكوينه من خلال اختزال الكروم (VI) بواسطة السيتوكروم c7.[26]الأيون Cr3+ له نصف قطرها (50 pm) pm) لـ Al3+ (نصف قطرها 50 pm)، ويمكنهما استبدال كل منهما البعض الآخر في بعض المركبات، مثل شب الكروم والشب.
يميل الكروم (III) إلى تكوين مركبات ثماني السطوح. الهيدرات المتاح تجارياً هي هيدرات كلوريد الكروم (III) هو المركب الأخضر الداكن [CrCl2(H2O)4]Cl. المركبات وثيقة الصلة هي الأخضر الباهت [CrCl(H2O)5]Cl2 والبنفسجي [Cr(H2O)6]Cl3 إذا أُذيب البنفسج اللامائي[27] كلوريد الكروم (III) يذوب في الماء، المحلول البنفسجي يتحول إلى اللون الأخضر بعد بعض الوقت حيث يتم استبدال الكلوريد في مجال التنسيق الداخلي بالماء. لوحظ هذا النوع من التفاعل أيضاً مع محاليل شب الكروم وأملاح الكروم (III) الأخرى القابلة للذوبان في الماء. تم الإبلاغ عن بنية رباعيةالسطوح الكروم (III) لأنيون كگن المتمركز في [α-CrW12O40]5–.[28]
هيدروكسيد الكروم (III) Cr(OH)3 هو مذبذب، يتحلل في المحاليل الحمضية لتشكيل [Cr(H2O)6]3+، وفي المحاليل الأساسية لتشكيل [Cr(OH) 6]3− . يتم تجفيفه بالتسخين لتكوين أكسيد الكروم (III) الأخضر (Cr2O3)، وهو أكسيد مستقر له بنية بلورية مماثلة لتلك الموجودة في السامور.[13]
الكروم (VI)
مركبات الكروم (VI) هي مواد مؤكسدة عند درجة حموضة منخفضة أو متعادلة. الأنيونات كرومات (CrO2−4) و ثنائي كرومات (Cr2O72−) الأنيونات هي الأيونات الرئيسية في حالة الأكسدة هذه. توجد في حالة توازن يحدده الرقم الهيدروجيني:
- 2 [CrO4]2− + 2 H+
 [Cr2O7]2− + H2O
[Cr2O7]2− + H2O
أوكسياليد الكروم (VI) معروفة أيضاً وتشمل فلوريد الكروميل (CrO2F2) وكلوريد الكروميل(CrO 2Cl 2).[13]ومع ذلك، على الرغم من العديد من الادعاءات الخاطئة، لا يزال سداسي فلوريد الكروم (بالإضافة إلى جميع سداسي الهكساليدات الأعلى) غير معروف، اعتباراً من عام 2020.[29]

يتم إنتاج كرومات الصوديوم صناعياً عن طريق التحميص التأكسدي للكروميت الخام مع كربونات الصوديوم. يمكن رؤية التغيير في التوازن من خلال التغيير من اللون الأصفر (كرومات) إلى البرتقالي (ثنائي كرومات)، كما هو الحال عند إضافة حمض إلى محلول متعادل من كرومات الپوتاسيوم. عند قيم الأس الهيدروجيني الأقل بعد، من الممكن حدوث مزيد من التكثيف إلى أكسانيونات الكروم الأكثر تعقيداً.
كل من الأنيونات الكرومات وثنائي كرومات عبارة عن كواشف مؤكسدة قوية عند درجة حموضة منخفضة:[13]
- Cr 2O2−7 + 14 H 3O+ + 6 e− → 2 Cr3+ + 21 H 2O (ε0 = 1.33 V)
ومع ذلك، فهي تتأكسد بشكل معتدل فقط عند ارتفاع درجة الحموضة:[13]
- CrO2−4 + 4 H 2O + 3 e− → Cr(OH) 3 + 5 OH− (ε0 = −0.13 V)

يمكن الكشف عن مركبات الكروم (VI) في المحلول عن طريق إضافة محلول حمضي بيروكسيد الهيدروجين. يتشكل اللون الأزرق الداكن غير المستقر بيروكسيد الكروم (VI) (CrO5)، والذي يمكن تثبيته كمقرب إيثر CrO 5·OR 2.[13]
حمض الكروميك لها الصيغة الافتراضيةH 2CrO 4. وهي مادة كيميائية موصوفة بشكل غامض، على الرغم من معرفة العديد من الكرومات وثنائي كرومات جيداً. يباع أكسيد الكروم (VI) الأحمر الداكن CrO 3، حمض أنهيدريد لحمض الكروميك، صناعياً على أنه "حمض الكروميك".[13] يمكن إنتاجه عن طريق خلط حامض الكبريتيك مع ثنائي كرومات وهو عامل مؤكسد قوي.
حالات أكسدة أخرى
مركبات الكروم (V) نادرة نوعاً ما؛ تتحقق حالة الأكسدة +5 فقط في مركبات قليلة ولكنها تكون وسيطة في العديد من التفاعلات التي تنطوي على أكسدة بالكرومات. المركب الثنائي الوحيد هو فلوريد الكروم (V) (CrF5). هذه المادة الصلبة الحمراء لها نقطة انصهار تبلغ 30 درجة مئوية ونقطة غليان تبلغ 117 درجة مئوية. يمكن تحضيره بمعالجة معدن الكروم بالفلور عند 400 درجة مئوية وضغط 200 بار. يعتبر البيروكسكرومات (V) مثالاً آخر على حالة الأكسدة +5. پيروكسكرومات الپوتاسيوم (K3[Cr(O2)4]) مصنوع عن طريق تفاعل كرومات الپوتاسيوم مع بيروكسيد الهيدروجين عند درجات حرارة منخفضة. هذا المركب البني الأحمر مستقر في درجة حرارة الغرفة ولكنه يتحلل تلقائياً عند 150-170 درجة مئوية.[30]
مركبات الكروم (IV) أكثر شيوعاً من تلك الموجودة في الكروم (V). رباعي الهاليدات، CrF4، CrCl4، وCrBr4، عن طريق معالجة ثلاثي الهاليدات (CrX 3) مع الهالوجين المقابل في درجات حرارة مرتفعة. هذه المركبات عرضة لتفاعلات غير متكافئة وليست مستقرة في الماء. المركبات العضوية التي تحتوي على حالة الكروم (IV) مثل رباعي الكروم تي-بوتوكسيد المعروف أيضاً أن أكسيد البوتوكسيد.[31]
يتم الحصول على معظم مركبات الكروم (I) فقط عن طريق أكسدة مركبات الكروم الغنية بالإلكترون ثمانية السطوح (0). تحتوي مركبات الكروم (I) الأخرى على روابط cyclopentadienyl. كما تم التحقق منه بواسطة حيود الأشعة السينية، تم أيضاً وصف Cr-Cr برابطة خماسية (طول 183.51(4) pm).[32]تعمل الروابط أحادية الكتلة الضخمة للغاية على تثبيت هذا المركب عن طريق حماية الرابطة الخماسية من المزيد من التفاعلات.
التواجد


الكروم هو العنصر الحادي والعشرون[33] الأكثر وفرة في قشرة الأرض بمتوسط تركيز 100 ppm. توجد مركبات الكروم في البيئة من تآكل الصخور المحتوية على الكروم، ويمكن إعادة توزيعها عن طريق الانفجارات البركانية. التركيزات النموذجية للكروم في الخلفية في الوسط البيئي هي: الغلاف الجوي <10 ng/m3; التربة <500 mg/kg؛ الغطاء النباتي <0.5 mg/kg مياه عذبة <10 μg/L; مياه بحرية <1 μg/L; رواسب.<80 mg/kg.[34] يتم استخراج الكروم كخام كروميت (FeCr2O4).[35]
يتم إنتاج حوالي خمسي خامات ومركزات الكروميت في العالم في جنوب إفريقيا، وحوالي الثلث في قزخستان،[36] بينما تعد الهند وروسيا وتركيا منتجين مهمين أيضاً. توجد رواسب الكروميت غير المستغلة بوفرة، ولكنها تتركز جغرافياً في قزخستان وجنوب إفريقيا.[37]على الرغم من ندرتها، توجد رواسب من الكروم الأصلي.[38][39]ينتج أنبوب أوداتشنايا في روسيا عينات من المعدن الأصلي. هذا المنجم عبارة عن أنبوب كمبرلايت غني بألماس، وساعدت البيئة المختزلة في إنتاج كل من عنصر الكروم والماس.[40]
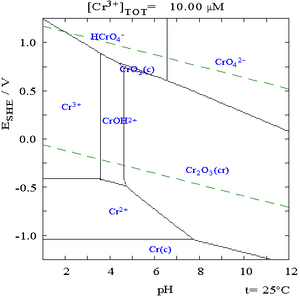
تعتمد العلاقة بين Cr(III) وCr(VI) بشدة على pH وخصائص الأكسدة للموقع. في معظم الحالات، Cr(III) هو النوع المهيمن،[19] ولكن في بعض المناطق، يمكن أن تحتوي المياه الجوفية على ما يصل إلى 39 ميكروغرام/لتر من إجمالي الكروم، منها 30 ميكروغرام/لتر هي Cr(VI).[41]
التاريخ

اكتشف الكيميائي يوهان گوتليب مركب كرومات الرصاص الاحمر المائل إلى البرتقالي سنة 1761 في الأورال، وأسماه الرصاص الأحمر. وحيث أنه اعتقد بأنه مركب رصاص-سيلين، بقي الكروم غير مكتشف.
سنة 1770 وجد پيتر سيمون پالاس في نفس المكان مركب رصاص أحمر أطلق عليه اسم كروكويت (من كروكوس باليونانية وتعني "لون الزعفران"). على أثر ذلك تزايد استعمال مركب الرصاص الأحمر كخضاب. ومن الأخضاب المستخلصة خضاب الكروم الأصفر المستخدم كلون خاص بخدمات البريد.
عام 1797 تمكن لويس-نيكولاس فوكولين من استخلاص ثالث أكسيد الكروم (Cr2O3) من الكروكويت وحمض الكلور. وفي عام 1798 توصل لاستخلاص العنصر كروم بشكل غير نقي عبر اختزال أكسيد الكروم الثالث بالفحم الخشبي. هذا العنصر المكتشف حديثا سمي كروم (من كروما باليونانية وتعني لون) نظراً لخصائص املاحه الملونة. كذلك تمكن فوكولين من برهان تواجد اثار من الكروم في بعض الاحجار الكريمة كالروبين والزمرد.
في القرن التاسع عشر ساد استخدام مركبات الكروم كأخضاب غالباً. وفي القرن العشرين تم استخدام الكروم ومركباته بصورة أساسية في تصنيع مستحضرات للوقاية من الصدأ والحرارة.
الإنتاج

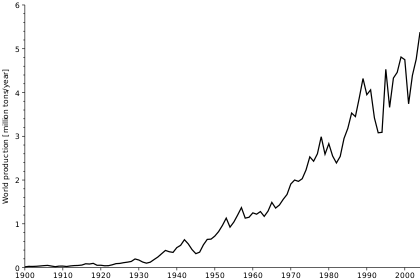

أُنتج ما يقرب من 28.8 مليون طن متري من خام الكروميت القابل للتسويق في عام 2013، وتحويلها إلى 7.5 مليون طن من الحديد والكروم.[37]وفقاً لجون پپ، الذي يكتب لـ USGS "Ferrochromium هو الاستخدام النهائي الرائد لخام الكروميت، [و] الفولاذ المقاوم للصدأ هو الاستخدام النهائي الرائد للحديد الكروم.""[37]
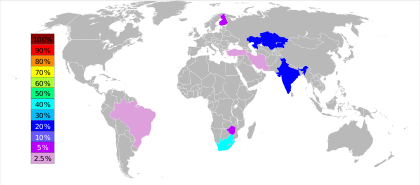
أكبر منتجي خام الكروم في عام 2013 هم جنوب إفريقيا (48٪)، قزخستان (13٪)، تركيا (11٪)، والهند (10٪)، مع العديد من البلدان الأخرى التي تنتج بقية حوالي 18٪ من العالم إنتاج.[37]
المنتجان الرئيسيان لتكرير خام الكروم هما فروكروم والكروم الفلزي. وتختلف عملية صهر الخام إلى حد كبير بالنسبة لتلك المنتجات. لإنتاج حديد الكروم، يتم تقليل خام الكروميت (FeCr2O4) على نطاق واسع في فرن القوس الكهربي أو في مصاهر أصغر باستخدام إما الألومنيوم أو السيليكون في تفاعل الألمنيوم.[42]
لإنتاج الكروم النقي، يجب فصل الحديد عن الكروم في خطوتين من عملية التحميص والترشيح. يتم تسخين خام الكروميت بمزيج من كربونات الكالسيوم وكربونات الصوديوم في وجود الهواء. يتأكسد الكروم إلى الشكل السداسي التكافؤ، بينما يشكل الحديد الحديد المستقر Fe2O3. النض اللاحق عند درجات حرارة مرتفعة يذيب كرومات ويترك أكسيد الحديد غير القابل للذوبان. يتم تحويل الكرومات بواسطة حامض الكبريتيك إلى ثنائي كرومات.[42]
- 4 FeCr2O4 + 8 Na2CO3 + 7 O2 → 8 Na2CrO4 + 2 Fe2O3 + 8 CO2
- 2 Na2CrO4 + H2SO4 → Na2Cr2O7 + Na2SO4 + H2O
يُحوَّل ثنائي كرومات إلى أكسيد الكروم (III) عن طريق الاختزال بالكربون ثم يتم تقليله في تفاعل الألمنيوم مع الكروم.[42]
- Na2Cr2O7 + 2 C → Cr2O3 + Na2CO3 + CO
- Cr2O3 + 2 Al → Al2O3 + 2 Cr
الاستخدامات
يمثل إنشاء السبائك المعدنية 85٪ من استخدام الكروم المتاح. يستخدم ما تبقى من الكروم في الصناعات الكيميائية، المواد الحرارية، والمسابك.[44]
علم الفلزات

إن التأثير المعزز لتشكيل كربيدات معدنية مستقرة عند حدود الانتزاع، والزيادة القوية في مقاومة التآكل جعلت الكروم مادة مهمة في صناعة السبائك للصلب. يحتوي أدوات فولاذ عالي السرعة على ما بين 3 و 5٪ كروم. صلب مقاوم للصدأ، سبيكة معدنية أولية مقاومة للتآكل، تتشكل عند إدخال الكروم إلى الحديد بتركيزات أعلى من 11٪.[45] لتشكيل الفولاذ المقاوم للصدأ، يضاف الحديد الكروم إلى الحديد المصهور. أيضاً، زادت السبائك القائمة على النيكل من القوة بسبب تكوين جزيئات كربيد منفصلة ومستقرة ومعدنية عند حدود الحبوب. على سبيل المثال، يحتوي إنكونل 718 على 18.6٪ كروم. نظراً لخصائص درجات الحرارة العالية الممتازة لهذه السبائك الفائقة من النيكل، فإنها تُستخدم في المحركات النفاثة والتوربينات الغازية بدلاً من المواد الهيكلية الشائعة.[46] يعتمد ASTM B163 على الكروم لأنابيب المكثف والمبادل الحراري، بينما المسبوكات ذات القوة العالية في درجات الحرارة المرتفعة التي تحتوي على الكروم تكون معيارية مع ASTM A567.[47]يستخدم AISI يستخدم النوع 332 حيث تؤدي درجة الحرارة المرتفعة عادةً إلى الكربنة، الأكسدة أو التآكل.[48]Incoloy 800 "قادر على الحفاظ على استقراره والحفاظ على هيكله الأوستنيتي حتى بعد التعرض لوقت طويل لدرجات حرارة عالية".[49]يستخدم النيكروم كسلك مقاومة لعناصر التسخين في أشياء مثل المحمصات والسخانات الفراغية. هذه الاستخدامات تجعل الكروم مادة استراتيجية. وبالتالي، خلال الحرب العالمية الثانية، صدرت تعليمات لمهندسي الطرق الأمريكيين بتجنب الكروم المطلي باللون الأصفر للطرق، لأنه "قد يصبح مادة بالغة الأهمية أثناء حالة الطوارئ".[50] وبالمثل اعتبرت الولايات المتحدة الكروم "ضرورياً للصناعة في الحرب الألمانية" وبذلت جهوداً دبلوماسية مكثفة لإبقائه بعيداً عن أيدي ألمانيا النازية.[51]

إن الصلابة العالية ومقاومة التآكل للكروم غير المخلوط تجعله معدناً موثوقاً به لطلاء السطح؛ لا يزال المعدن الأكثر شيوعاً لطلاء الألواح، بمتانة أعلى من المتوسط، مقارنة بمعادن الطلاء الأخرى.[52] يتم ترسيب طبقة من الكروم على الأسطح المعدنية المعالجة مسبقاً بواسطة تقنيات الطلاء الكهربائي. هناك طريقتان للترسيب: رقيقة وسميكة. يتضمن الترسيب الرقيق طبقة من الكروم أقل من 1 ميكرومتر يتم ترسيبها بواسطة طلاء الكروم، ويستخدم للأسطح الزخرفية. يتم ترسيب طبقات الكروم السميكة إذا كانت هناك حاجة إلى أسطح مقاومة للتآكل. تستخدم كلتا الطريقتين الكرومات الحمضية أو محاليل ثنائي كرومات. لمنع التغيير المستهلك للطاقة في حالة الأكسدة، فإن استخدام كبريتات الكروم (III) قيد التطوير؛ بالنسبة لمعظم تطبيقات الكروم، يتم استخدام العملية المحددة مسبقاً.[53]
في عملية طلاء تحويل الكرومات، تُستخدم الخصائص المؤكسدة القوية للكرومات لإيداع طبقة أكسيد واقية على معادن مثل الألومنيوم والزنك والكادميوم. هذا التخميل وخصائص الإصلاح الذاتي للكرومات المخزنة في طلاء تحويل الكرومات، القادر على الانتقال إلى عيوب محلية، هي فوائد طريقة الطلاء هذه.[54]بسبب اللوائح البيئية والصحية على الكرومات، يجري تطوير طرق طلاء بديلة.[55]
أنودة حمض الكروميك (أو أنودة من النوع الأول) للألمنيوم هو عملية كهروكيميائية أخرى لا تؤدي إلى ترسب الكروم، ولكنها تستخدم حمض الكروميك كإلكتروليت في المحلول. أثناء عملية الأنودة، تتكون طبقة أكسيد على الألومنيوم. يؤدي استخدام حمض الكروميك، بدلاً من حمض الكبريتيك المستخدم عادةً، إلى اختلاف طفيف في طبقات الأكسيد هذه.[56] تتطلب السمية العالية لمركبات Cr(VI)، المستخدمة في عملية الطلاء الكهربائي بالكروم المعمول بها، وتقوية اللوائح التنظيمية للسلامة والبيئة، البحث عن بدائل للكروم، أو على الأقل تغيير إلى مركبات الكروم (III) الأقل سمية.[53]
الخضاب
استُخدم المعدن كروكويت (كرومات الرصاص PbCrO4) كصبغة صفراء بعد وقت قصير من اكتشافه. بعد أن أصبحت طريقة التوليف متاحة بدءاً من الكروميت الأكثر وفرة، كان أصفر الكروم، مع أصفر الكادميوم، أحد أكثر الأصباغ الصفراء استخداماً. لا تتحلل الصبغة ضوئياً، ولكنها تميل إلى التغميق بسبب تكوين أكسيد الكروم(III). له لون قوي، وكان يستخدم للحافلات المدرسية في الولايات المتحدة وللخدمة البريدية (على سبيل المثال، البريد الألماني) في أوروبا. انخفض استخدام الكروم الأصفر منذ ذلك الحين بسبب مخاوف تتعلق بالبيئة والسلامة وتم استبداله بأصباغ عضوية أو بدائل أخرى خالية من الرصاص والكروم. الأصباغ الأخرى التي تعتمد على الكروم، على سبيل المثال، الظل العميق للصبغة الحمراء أحمر الكروم، والتي هي مجرد كرومات الرصاص مع هيدروكسيد الرصاص (II) (PbCrO4·Pb(OH)2). كان كرومات الزنك أحد أصباغ الكرومات المهمة جداً، والذي تم استخدامه على نطاق واسع في تركيبات المعدن التمهيدي، والذي تم استبداله الآن بفوسفات الزنك. تمت صياغة أساس غسيل ليحل محل الممارسة الخطيرة المتمثلة في المعالجة المسبقة لهيئات الطائرات المصنوعة من الألومنيوم بمحلول حمض الفوسفوريك. يستخدم هذا الزنك رباعي كرومات مشتت في محلول پولي ڤينيل بوتيرال. تمت إضافة محلول 8٪ من حامض الفوسفوريك في مذيب قبل التطبيق مباشرة. وجد أن الكحول المؤكسد كان عنصراً أساسياً. تم تطبيق طبقة رقيقة من حوالي 10-15 ميكرومتر، والتي تحولت من الأصفر إلى الأخضر الداكن عند الشفاء. لا يزال هناك سؤال حول الآلية الصحيحة. الكروم الأخضر هو خليط من أزرق پروسيا وأصفر الكروم، بينما أكسيد الكروم الأخضر هو أكسيد الكروم (III).[57]
ُُتُستخدم أكاسيد الكروم أيضاً كصبغة خضراء في مجال صناعة الزجاج وأيضاً كطلاء زجاجي للسيراميك.[58] أكسيد الكروم الأخضر شديد ثبات الضوء وعلى هذا النحو يستخدم في طلاءات الكسوة. وهو أيضاً المكون الرئيسي في الدهانات العاكسة بالأشعة تحت الحمراء، التي تستخدمها القوات المسلحة لطلاء المركبات ومنحها نفس انعكاس الأشعة تحت الحمراء مثل الأوراق الخضراء.[59]
استخدامات أخرى

تتسبب أيونات الكروم (III) الموجودة في بلورات السامور (أكسيد الألمنيوم) في جعلها ملونة باللون الأحمر؛ عندما يظهر السامور على هذا النحو، فإنه يُعرف باسم الياقوت. إذا كان السامور ينقصه أيونات الكروم (III)، فإنه يُعرف باسم الزفير.[note 3]يمكن أيضاً الحصول على ياقوت صناعي أحمر اللون عن طريق تعاطي المنشطات من الكروم (III) في بلورات السامور الاصطناعية، مما يجعل الكروم مطلباً لصنع الياقوت الصناعي.[note 4][60] مثل بلورة الياقوت الاصطناعية كانت الأساس لأول ليزر، تم إنتاجه في عام 1960، والذي اعتمد على الانبعاث المحفَّز للضوء من ذرات الكروم في مثل هذه البلورة. لدى الياقوت انتقال ليزر عند 694.3 نانومتر، بلون أحمر غامق.[61]
بسبب سميتها، تستخدم أملاح الكروم (VI) للحفاظ على الخشب. على سبيل المثال، يتم استخدام زرنيخات النحاس الكروماتية (CCA) في معالجة الأخشاب لحماية الخشب من الفطريات المتحللة والحشرات التي تهاجم الأخشاب، بما في ذلك [[نمل أبيض |النمل الأبيض]] والحفريات البحرية.[62]تحتوي التركيبات على الكروم على أساس أكسيد CrO3 بين 35.3٪ و65.5٪. في الولايات المتحدة، تم استخدام 65300 طن متري من محلول CCA في عام 1996.[62]
تستخدم أملاح الكروم (III)، وخاصة شب الكروم وكبريتات الكروم (III)، في دباغة الجلود. يقوم الكروم (III) بتثبيت الجلد عن طريق ربط ألياف الكولاجين.[63] يمكن أن يحتوي الجلد المدبوغ بالكروم على ما بين 4 و5٪ من الكروم، وهو مرتبط بإحكام بالبروتينات.[35] على الرغم من أن شكل الكروم المستخدم للدباغة ليس النوع السداسي التكافؤ السام، فلا يزال هناك اهتمام بإدارة الكروم في صناعة الدباغة. الاستعادة وإعادة الاستخدام، التدوير المباشر/غير المباشر،[64] ويتم ممارسة الدباغة "الخالية من الكروم" أو "الخالية من الكروم" لإدارة استخدام الكروم بشكل أفضل.[65]
المقاومة العالية للحرارة ونقطة الانصهار العالية تجعل الكروميت وأكسيد الكروم(III) مادة لتطبيقات مقاومة الحرارة العالية، مثل الفرن العالي، فرن الأسمنت، قوالب لخبز الطوب وكرمال مسبك لصب المعادن. في هذه التطبيقات، تصنع المواد المقاومة للصهر من خليط من الكروميت والمغنسيت. كما يتناقص الاستخدام بسبب اللوائح البيئية بسبب إمكانية تكوين الكروم (VI).[42] [66]
تُستخدم العديد من مركبات الكروم كمحفزات لمعالجة الهيدروكربونات. على سبيل المثال، محفز فلپس، المحضر من أكاسيد الكروم، يستخدم لإنتاج حوالي نصف پوليإثيلين في العالم.[67] كما تُستخدم أكاسيد الحديد والكروم المختلطة كمحفزات عالية الحرارة من أجل تفاعل انزياح ماء-غاز.[68][69] كما أن كروميت النحاس هو محفز مفيد للهدرجة.[70]
استخدامات المركبات
- أكسيد الكروم الرباعي (CrO2) هو مركب مغناطيسي. تباين الخواص في شكله المثالي، يضفي مقاومة مغناطيسية وبقايا مغنطة، مما جعله مركباً متفوقاً على γ-Fe2O3. يستخدم أكسيد الكروم (IV) لتصنيع الشرائط المغناطيسية المستخدمة في الشرائط الصوتية عالية الأداء والأشرطة الصوتية القياسية.[71]
- أكسيد الكروم الثلاثي (Cr2O3) عبارة عن ملمع معدني يعرف باسم الأحمر المصقول المخضر.[72][73]
- حمض الكروميك هو عامل مؤكسد قوي ومركب مفيد لتنظيف الأواني الزجاجية للمختبر من أي أثر للمركبات العضوية.[74]يتم تحضيره عن طريق إذابة ثنائي كرومات الپوتاسيوم في حمض الكبريتيك المركز، والذي يستخدم بعد ذلك لغسل الجهاز. يستخدم ثنائي كرومات الصوديوم أحياناً بسبب قابلية ذوبانه العالية (50 غ/لتر مقابل 200 غ/لتر على التوالي). تم الآن التخلص التدريجي من استخدام محاليل التنظيف ثنائية الكرومات بسبب السمية العالية والمخاوف البيئية. حلول التنظيف الحديثة فعالة للغاية وخالية من الكروم.[75]
- ثنائي كرومات الپوتاسيوم مادة كيميائية كاشفة، تستخدم كعامل معايرة.[76]
- تضاف الكرومات إلى طين الحفر لمنع تآكل الفولاذ في الظروف الرطبة.[77]
- شب الكروم هو كبريتات الكروم الثلاثي الپوتاسيوم ويستخدم كمادة مرسخة (على سبيل المثال، عامل تثبيت) للأصباغ في النسيج وفي الدباغة.[78]
الدور الحيوي
نوقشت الآثار المفيدة حيوياً للكروم الثلاثي.[79][80] كما تمت الموافقة على الكروم من قبل المعاهد الوطنية الأمريكية للصحة كعنصر تتبع لدوره في عمل الإنسولين، وهو هرمون يتوسط عملية التمثيل الغذائي وتخزين الكربوهيدرات والدهون والبروتين.[81] ومع ذلك، لم يتم تحديد آلية أفعاله في الجسم، مما يترك موضع تساؤل حول أهمية الكروم.[82][83]
في المقابل، الكروم السداسي التكافؤ (Cr(VI) or Cr6+) شديد السمية ومطفّر.[84] رُبط تناول الكروم السداسي في الماء بأورام المعدة، وقد يسبب أيضاً حساسية التهاب الجلد التماسي (ACD).[85]
"نقص الكروم"، الذي ينطوي على نقص Cr (III) في الجسم، أو ربما بعض معقدة منه، مثل عامل تحمل الگلوكوز، أمر مثير للجدل.[81] تشير بعض الدراسات إلى أن الشكل النشط بيولوجياً للكروم (III) يتم نقله في الجسم عبر قليل الپپتيد يسمى مادة ربط الكروم منخفضة الوزن الجزيئي (LMWCr)، والتي قد تلعب دوراً في مسار إشارات الأنسولين.[86]
محتوى الكروم في الأطعمة الشائعة منخفض بشكل عام (1-13 ميكروغرام لكل حصة).[81][87]يختلف محتوى الكروم في الطعام بشكل كبير، بسبب الاختلافات في محتوى التربة من المعادن، وموسم النمو، وزريعات النبات، والتلوث أثناء المعالجة.[87] يتسرّب الكروم (والنيكل) في الطعام المطبوخ من الفولاذ المقاوم للصدأ، ويكون التأثير أكبر عندما تكون أواني الطهي جديدة. كما تؤدي الأطعمة الحمضية التي يتم طهيها لعدة ساعات أيضاً إلى تفاقم هذا التأثير.[88][89]
التوصيات الغذائية
الكروم من العناصر التي يحتاجها جسم الانسان لكن بكميات ضئيلة جداً في حدود تقدر من خمسة وعشرين إلى مائة مايكرو گرام يومياً.
تظهر الدراسات الحديثة إلى أن الكروم قد يكون له دوراً أساسياً في تمرير الأنسولين إلى داخل الخلية وبالتالي الاستفادة منه لذلك قد يكون مفيداً جداً لمرضى السكري وللوقاية منه. عنصر الكروميوم هو أحد العناصر المعدنية الأساسية اللازمة لعمل الإنسولين، كما أنه ضروري لتأيض النشويات والدهون والبروتين في الجسم.
في دراسة عشوائية مقارنة تستغرق 7 أشهر، وهي الأولى من نوعها لدراسة تأثير عنصر الكروميوم المضاف لأطعمة الأطفال المصابين بالسكري (النوع الأول)، ويعانون من عدم السيطرة على مستوى السكر في الدم. وقد استندت الدراسة على توفر أكثر من 15 دراسة سبق وأن دعمت مأمونية ودور عنصر الكروميوم في تحسين عمل الإنسولين، وتأيض سكر الدم في المرضى المصابين بداء السكري - النوع الثاني. وأن هناك شاهداً قوياً على أن إضافة الكروميوم إلى جانب أدوية السكري يحسن مستقبلات الإنسولين، ويضبط مستوى سكر الدم، بالإضافة إلى تقليل المخاطر التي تحيط بالقلب لدى مرضى داء السكري – النوع الثاني.
تشمل الدراسة 30 مريضا بداء السكري – النوع الأول من الجنسين، وبأعمار تتراوح بين 12إلى 18 عاماً، كلهم من ذوي الأوزان الزائدة، ويعطي الواحد منهم 600 ميكروجرام (نصف ملجم تقريباً) من معدن كروميوم يومياً. إن الهدف من الدراسة معرفة تأثير الكروميوم على مستوى سكر الهيموجلوبين، لأنه يدل على معدل مستوى سكر الدم خلال الأشهر الأخيرة، ثم مستوى الجلوكوز في الدم، والوزن، ومؤشر وزن الكتلة، والأخطار المحيطة بالقلب، وتتوقع الدراسة نتائج إيجابية في استخدام عنصر الكروم في تحسين وضبط داء السكري في الأطفال.
عنصر الكروميوم موجود في معظم الأغذية، إلا أنه قليل في الأغذية المكررة، ولا يتوقع نقصه في الجسم، إلا إذا كان هناك سوء امتصاص لعنصر الكروميوم في الأمعاء، كما أن الكمية اليومية اللازمة للإنسان العادي لم تحدد بعد، وقد تبدأ بـ 200 إلى 600 ميكروجرام (نحو نصف ملجم) يومياً. يوجد معدن الكروميوم في الكبد، وخميرة البيرة، والبيض، واللحم، والحبوب الكاملة، ونخالة القمح، والبطاطا، والمكسرات، والجبن ويوجد كذلك في الأرز البني، والبقول الجافة، والدجاج، والذرة، وعرق السوس.
من الصعب معرفة الأعراض التي تدل على نقص عنصر الكروميوم، لكن فعالية الإنسولين تصبح مضطربة بشكل شديد عندما ينقص الكروميوم في الغذاء، ويظهر على المريض أعراض مرض السكري، وقد يرتبط نقص الكروميوم باضطراب النمو في الأطفال الذين يعانون سوء التغذية، والشعور بالتعب، وعدم تأيض الأحماض الأمينية بشكل ملائم، وقد يؤدي نقصه إلى تصلب الشرايين، وقد تظهر أعراض الإصابة بقصور شرايين القلب التاجية.
| النوع | الكروميوم (ملجم) |
|---|---|
| التفاح ثمرة متوسطة بدون قشر | 1 |
| الموزثمرة متوسطة | 1 |
| عنب أحمر 5 أوقية | 1-13 |
| الفول الأخضر نصف كوب | 1 |
| الريحان المجفف معلقة طعام | 2 |
| عصير البرتقالكوب | 2 |
| خبز حبة القمح الكاملةشريحتان | 2 |
| صدور الديك الرومي3 أوقية | 2 |
| مكعبات اللحم البقري3 أوقية | 2 |
| البطاطس مهروسة، 1 كوب | 3 |
| ثوم مجفف، 1 معلقة | 3 |
| كعكات المافن الإنگليزية | 4 |
| عصير العنب1 كوب | 8 |
| البروكلينصف كوب | 11 |
وضع العلامات
لأغراض وضع العلامات على المواد الغذائية والمكملات الغذائية في الولايات المتحدة، يتم التعبير عن كمية المادة في الوجبة كنسبة مئوية من القيمة اليومية (٪ DV). لأغراض وضع العلامات على الكروم، كانت 100٪ من القيمة اليومية 120 ميكروغرام. اعتباراً من 27 مايو 2016، تم تعديل النسبة المئوية للقيمة اليومية إلى 35 ميكروغرام لجعل تناول الكروم في توافق مع المسؤول الكمية الغذائية الموصى بها.[91][92]يتوفر جدول بالقيم اليومية القديمة والجديدة للبالغين في الكمية الغذائية المرجعية.
مصادر الطعام
لا تحتوي قواعد بيانات مكونات الأغذية مثل تلك التي تحتفظ بها وزارة الزراعة الأمريكية على معلومات عن محتوى الكروم في الأطعمة.[93]تحتوي مجموعة متنوعة من الأطعمة الحيوانية والنباتية على الكروم.[94] يتأثر المحتوى لكل حصة بمحتوى الكروم في التربة التي تزرع فيها النباتات، وبالمواد الغذائية التي يتم تغذيتها للحيوانات، وبطرق المعالجة، حيث يتم ترشيح الكروم في الأطعمة إذا تمت معالجته أو طهيه في معدات من الفولاذ المقاوم للصدأ.[95]أفادت إحدى دراسات تحليل النظام الغذائي التي أجريت في المكسيك عن متوسط مدخول يومي من الكروم يبلغ 30 ميكروغرام.[96]ما يقدر بنحو 31 ٪ من البالغين في الولايات المتحدة يستهلكون مكملات غذائية متعددة من الفيتامينات/المعادن،[97]والتي غالباً ما تحتوي على 25 إلى 60 ميكروغرام من الكروم.
المكملات
يعد الكروم عنصراً في التغذية بالحقن (TPN)، لأن النقص يمكن أن يحدث بعد شهور من التغذية الوريدية باستخدام TPN الخالي من الكروم. [98] يُضاف أيضاً إلى المنتجات الغذائية لـ الخدج.[99] على الرغم من أن آلية العمل في الأدوار البيولوجية للكروم غير واضحة، إلا أن المنتجات المحتوية على الكروم في الولايات المتحدة تُباع كمكملات غذائية بدون وصفة طبية بكميات تتراوح من 50 إلى 1000 ميكروغرام. غالباً ما يتم أيضاً دمج كميات أقل من الكروم في مكملات الفيتامينات المتعددة والمعادن التي يستهلكها ما يقدر بنحو 31٪ من البالغين في الولايات المتحدة.[97]تشمل المركبات الكيميائية المستخدمة في المكملات الغذائية كلوريد الكروم، وسيترات الكروم، پيكولينات الكروم الثلاثي، پولينيكوتينات الكروم الثلاثي، والتركيبات الكيميائية الأخرى.[81] ولم يتم إثبات فائدة المكملات.[81][100]
الادعاءات الصحية المعتمدة والمرفوضة
في عام 2005، وافقت إدارة الغذاء والدواء الأمريكية على مطالبة صحية مؤهلة لپيكولينات الكروم مع شرط صياغة ملصق محدد للغاية: "تشير إحدى الدراسات الصغيرة إلى أن پيكولينات الكروم قد تقلل من مخاطر مقاومة الأنسولين، وبالتالي قد تقلل من داء السكريالمخاطر من النوع 2. ومع ذلك، خلصت إدارة الغذاء والدواء الأمريكية إلى أن وجود مثل هذه العلاقة بين الكروم پيكولينات ومقاومة الأنسولين أو داء السكري من النوع 2 أمر غير مؤكد إلى حد كبير". في الوقت نفسه، رداً على أجزاء أخرى من الالتماس، رفضت إدارة الغذاء والدواء الأمريكية المطالبات المتعلقة بپيكولينات الكروم وأمراض القلب والأوعية الدموية، واعتلال الشبكية أو أمراض الكلى الناتجة عن ارتفاع غير طبيعي في مستويات السكر في الدم.[101]في عام 2010، وافقت وزارة الصحة الكندية على استخدام پيكولينات الكروم (III) في المكملات الغذائية. كما عبارات الملصقات المعتمدة: عامل في الحفاظ على صحة جيدة، ويوفر الدعم لعملية التمثيل الغذائي الصحي للگلوكوز، ويساعد الجسم على استقلاب الكربوهيدرات ويساعد الجسم على استقلاب الدهون.[102]وقد وافقت الهيئة الأوروپية لسلامة الأغذية (EFSA) في عام 2010 على الادعاءات القائلة بأن الكروم يساهم في التمثيل الغذائي الطبيعي للمغذيات الكبيرة والحفاظ على تركيز گلوكوز الدم الطبيعي، لكنها رفضت المطالبات بالحفاظ على وزن الجسم الطبيعي أو تحقيقه، أو تقليل التعب أو الإرهاق.[103]
بالنظر إلى الأدلة على نقص الكروم الذي يسبب مشاكل في إدارة الگلوكوز في سياق منتجات التغذية الوريدية المصنوعة بدون الكروم،[98]تحول الاهتمام البحثي إلى ما إذا كانت مكملات الكروم ستفيد الأشخاص المصابين بداء السكري من النوع 2 ولكنهم لا يعانون من نقص الكروم. بالنظر إلى نتائج أربعة تحليلات تلوية، أبلغ أحدهم عن انخفاض معتد به إحصائياً في مستويات الصيام گلوكوز الپلازما (FPG) واتجاه غير مهم في الهموگلوبين A1C.[104] وقد أفاد تقرير ثانٍ بذات الموضوع[105] وأبلغ ثالث عن انخفاض كبير في كلا المقياسين،[106]بينما أفاد رابع بعدم وجود فائدة لأي منهما.[107]وقد أدرجت مراجعة نُشرت في عام 2016 53 تجارب سريرية عشوائية تم تضمينها في واحد أو أكثر من ستة تحليلات تلوية. وخلصت إلى أنه في حين قد يكون هناك انخفاض طفيف في FPG و/أو HbA1C التي تحقق أهمية إحصائية في بعض هذه التحليلات التلوية، فإن القليل من التجارب التي تحققت تتناقص بشكل كبير بما يكفي لتوقع أن تكون ذات صلة بالنتائج السريرية.[108]
نظرت مراجعتين منهجيتين في مكملات الكروم كوسيلة للتحكم في وزن الجسم لدى الأشخاص الذين يعانون من زيادة الوزن والسمنة. الأولى، تقتصر على پيكولينات الكروم، وهو مكون مكمل شائع، أبلغ عن فقدان وزن معتد به إحصائياً 1.1 kg (2.4 lb) في التجارب التي تزيد مدتها عن 12 أسبوع.[109]وقد تضمن الآخر جميع مركبات الكروم وأبلغ عن تغير معتد به إحصائياً −0.50 kg (1.1 lb).[110] ولم يصل التغيير في نسبة الدهون في الجسم إلى دلالة إحصائية. وقد اعتبر مؤلفو كلا المراجعتين أن الملاءمة السريرية لفقدان الوزن المتواضع هذا غير مؤكد/غير موثوق به.[109][110]كما قامت الهيئة الأوروپية لسلامة الأغذية بمراجعة الأدبيات وخلصت إلى عدم وجود أدلة كافية لدعم المطالبة.[103]
يُروَّج للكروم كمكمل غذائي للأداء الرياضي، بناءً على النظرية القائلة بأنه يقوي نشاط الأنسولين، مع النتائج المتوقعة لزيادة كتلة العضلات، واستعادة أسرع لتخزين الگليكوجين أثناء التعافي بعد التمرين.[100][111][112]وقد أفادت مراجعة للتجارب السريرية أن مكملات الكروم لم تحسن أداء التمرين أو تزيد من قوة العضلات.[113] وقد استعرضت اللجنة الأولمبية الدولية المكملات الغذائية للرياضيين ذوي الأداء العالي في عام 2018 وخلصت إلى عدم وجود حاجة لزيادة تناول الكروم للرياضيين، ولا دعم مزاعم فقدان الدهون في الجسم.[114]
أسماك المياه العذبة
يوجد الكروم بشكل طبيعي في البيئة بكميات ضئيلة، ولكن الاستخدام الصناعي في صناعة المطاط والفولاذ المقاوم للصدأ والطلاء بالكروم والأصباغ للمنسوجات والمدابغ وغيرها من الاستخدامات تلوث الأنظمة المائية. في بنگلادش، تظهر الأنهار في المناطق الصناعية أو في اتجاه مجرى النهر منها تلوثاً بالمعادن الثقيلة. معايير مياه الري للكروم هي 0.1 mg/L، لكن بعض الأنهار تزيد عن خمسة أضعاف هذه الكمية. معيار الأسماك للاستهلاك البشري أقل من 1 mg/kg، لكن العديد من العينات المختبرة كانت أكثر من خمسة أضعاف هذه الكمية.[115] الكروم، وخاصة الكروم سداسي التكافؤ، شديد السمية للأسماك لأنه يسهل امتصاصه عبر الخياشيم، ويدخل الدورة الدموية بسهولة، ويتقاطع مع أغشية الخلايا، ويتركز في السلسلة الغذائية. في المقابل، فإن سمية الكروم ثلاثي التكافؤ منخفضة للغاية، ويعزى ذلك إلى ضعف نفاذية الأغشية وقلة التضخم الأحيائي.[116]
يؤثر التعرض الحاد والمزمن للكروم (VI) على سلوك الأسماك وعلم وظائف الأعضاء والتكاثر والبقاء على قيد الحياة. تم الإبلاغ عن فرط النشاط والسباحة غير المنتظمة في البيئات الملوثة. يتأثر فقس البيض وبقاء الإصبعيات. في الأسماك البالغة، هناك تقارير عن حدوث أضرار نسيجية مرضية للكبد، والكلى، والعضلات، والأمعاء، والخياشيم. تشمل الآليات تدمير الجينات المطفرة واضطراب وظائف الإنزيم.[116]
هناك دليل على أن الأسماك قد لا تحتاج إلى الكروم، ولكنها تستفيد من كمية محددة في النظام الغذائي. في إحدى الدراسات، اكتسبت الأسماك الصغيرة وزناً عند اتباع نظام غذائي خالٍ من الكروم، ولكن إضافة 500 ميكروغرام من الكروم على شكل كلوريد الكروم أو أنواع أخرى من المكملات الغذائية، لكل كيلوغرام من الطعام (الوزن الجاف)، أدى إلى زيادة الوزن. عند 2000 ميكروغرام/كغ، لم يكن اكتساب الوزن أفضل من النظام الغذائي الخالي من الكروم، وكانت هناك زيادة في فواصل شرائط الحمض النووي.[117]
الاحتياطات
 مقالة مفصلة: تسمم الكروم
مقالة مفصلة: تسمم الكروم
لا تعرف أي أعراض سمية ناجمة عن تناول أغذية غنية بعنصر الكروميوم، ولكن المبالغة في تناول المستحضرات التي تحتوي على عنصر الكروميوم قد تضر بالكلى وغيرها لأن المعلومات عن عنصر الكروميوم غير كافية حتى الآن، لذا يجب الانتباه عند تناول أكثر من مستحضر، فقد يحتوي كل منها على جرعات عالية من عنصر الكروميوم.
يتعرض الإنسان لهذا التسمم بالتلامس الجلدى لمعدن الكروم أو مركباته. معدلات الكروم في المياه أو الهواء بوجه عام قليلة جداً، إلا ن مياه الآبار الملوثة به تحتوى على الكروم معظم ما يتناوله الفرد من هذا المعدن من خلال الأطعمة هو الكروم والمتوافر بشكل طبيعى في الخضراوات والفاكهة واللحوم والخميرة والحبوب. وطريقة تحضير الأطعمة والتخزين من الممكن أن تغير محتوى الكروم ونسبه، فإذا تم تخزين الكروم في تنكات أو علب حديدية فإن تركيزاته قد ترتفع.[118]:
هذا النوع من الكروم هام لصحة الإنسان، وعدم حصول الإنسان على القدر الكافى منه يسبب اضطرابات للقلب، اضطرابات في عملية الآيض (التمثيل الغذائى)، الإصابة بالسكر. والكميات الزائدة منه تسبب اضطرابات صحية أيضاً مثل الطفح الجلدي.
الكروم ضار لصحة الإنسان ويمثل خطورة على الأشخاص التى تعمل في مجال صناعة الصلب والمنسوجات. أما الأشخاص التى تدخن التبغ تتعرض لنسب كبيرة من معدن الكروم، وعند استخدامه في الجلود قد يكون هناك رد فعل من الحساسية عند بعض الأشخاص مثل الطفح الجلدى. كما أن تنفسه يسبب اهتياج للأنف ونزيف منها.
أما المخاطر الأخرى المرتبطة بهذا المعدن:
- الطفح الجلدى
- اضطرابات المعدة والقرح
- اضطرابات في التنفس
- ضعف في كفاءة الجهاز المناعي
- ضمور في الكلى والكبد
- تغير في المواد الجينية
- سرطان الرئة
- الموت
وهذه المخاطر تعتمد على حالة التأكسد. والصورة المعدنية له تكون درجة سميتها ضئيلة، أما النوع السادس فهو سام. وتأثير هذا النوع على الجلد يتمثل في صورة حدوث الأعراض التالية: القرح، التهاب طبقة الجلد الخارجية، حساسية الجلد والاضطرابات المختلفة.
أما تنفسه من خلال الهواء فقد يسبب الآتى: ثقب في الغشاء المخاطى للحاجز الأنفى، اهتياج الحلق والحنجرة، التهاب الشعب الهوائية مسبباً أزمة الصدر، تشنجات الشعب الهوائية، الأوديما. ومن الأعراض التنفسية الأخرى: السعال، الأزيز، قصر التنفس، هرش بالأنف.
سمية الكروم (VI)
تتراوح درجة السمية الفموية الحادة للكروم (VI) بين 1.5 و3.3 ملغ/كغ.[119] في الجسم، يتم تقليل الكروم (VI) بعدة آليات إلى الكروم (III) الموجود بالفعل في الدم قبل أن يدخل الخلايا. يتم إخراج الكروم (III) من الجسم، في حين يتم نقل أيون الكرومات إلى الخلية بواسطة آلية نقل، والتي بواسطتها تدخل أيونات كبريتات وفوسفات إلى الخلية. ترجع السمية الحادة للكروم (VI) إلى خصائصه المؤكسدة القوية. بعد وصوله إلى مجرى الدم، يتلف الكلى والكبد وخلايا الدم من خلال تفاعلات الأكسدة. نتيجة انحلال الدم، الفشل الكلوي، وفشل الكبد. يمكن أن يكون غسيل الكلى العنيف علاجياً.[120]
عُرفت سرطنة غبار الكرومات منذ فترة طويلة، وفي عام 1890 وصف المنشور الأول ارتفاع مخاطر الإصابة بالسرطان لدى العاملين في شركة صبغ الكرومات.[121][122] اقتُرحت ثلاث آليات لوصف السمية الجينية للكروم (VI). تشتمل الآلية الأولى على جذور الهيدروكسيل شديدة التفاعل والجذور التفاعلية الأخرى التي تكون عن طريق منتجات اختزال الكروم (VI) إلى الكروم (III). تتضمن العملية الثانية الارتباط المباشر للكروم (V)، الناتج عن الاختزال في الخلية، ومركبات الكروم (IV) إلى DNA. عزت الآلية الأخيرة السمية الجينية إلى الارتباط بالحمض النووي للمنتج النهائي لاختزال الكروم (III).[123][124]
أملاح الكروم (كرومات) هي أيضاً سبب رد الفعل التحسسي لدى بعض الأشخاص. غالباً ما يستخدم الكرومات لتصنيع المنتجات الجلدية والدهانات والأسمنت والملاط والمواد المضادة للتآكل، من بين أشياء أخرى. يمكن أن يؤدي التلامس مع المنتجات المحتوية على كرومات إلى التهاب الجلد التماسي والتهاب الجلد التحسسي، مما يؤدي إلى تقرح الجلد، والذي يشار إليه أحياناً باسم "قرح الكروم". غالباً ما توجد هذه الحالة في العمال الذين تعرضوا لمحاليل كرومات قوية في شركات تصنيع الطلاء الكهربائي والدباغة وإنتاج الكروم.[125][126]
قضايا بيئية
نظراً لاستخدام مركبات الكروم في الصباغ والطلاء و دباغة الجلود، غالباً ما توجد هذه المركبات في التربة والمياه الجوفية في المواقع الصناعية النشطة والمهجورة، التي تحتاج إلى تنظيف بيئي ومعالجة. لا يزال الطلاء التمهيدي المحتوي على الكروم سداسي التكافؤ مستخدماً على نطاق واسع في تطبيقات الطيران والسيارات لإعادة الصقل.[127]
في عام 2010، قامت مجموعة العمل البيئي بدراسة مياه الشرب في 35 مدينة أمريكية في أول دراسة وطنية. وجدت الدراسة الكروم سداسي التكافؤ القابل للقياس في مياه الصنبور في 31 مدينة تم أخذ عينات منها، مع نورمان، اوكلاهوما، على رأس القائمة؛ 25 مدينة لديها مستويات تجاوزت حدود كاليفورنيا المقترحة.[128]
يمكن اختزال شكل الكروم سداسي التكافؤ الأكثر سمية إلى حالة الأكسدة ثلاثية التكافؤ الأقل قابلية للذوبان في التربة بواسطة المواد العضوية والحديدية والكبريتيدات وعوامل الاختزال الأخرى، حيث تكون معدلات هذا الاختزال أسرع في ظل الظروف الحمضية أكثر من الظروف القلوية. في المقابل، يمكن أكسدة الكروم ثلاثي التكافؤ إلى الكروم سداسي التكافؤ في التربة بواسطة أكاسيد المنجنيز، مثل مركبات Mn (III) وMn (IV). نظراً لأن قابلية ذوبان الكروم (VI) وسميته أكبر من تلك الموجودة في الكروم (III)، فإن تحويلات الأكسدة والاختزال بين حالتي الأكسدة لها آثار على الحركة والتوافر الحيوي للكروم في التربة والمياه الجوفية والنباتات.[129]
انظر أيضاً
- مركبات الكروم
- فلزات الكروم
- Chromium-vanadium steel
- Nichrome
- Lake Chichoj، بحيرة ملوثة بالكروم
الهوامش
- ^ The melting/boiling point of transition metals are usually higher compared to the alkali metals, alkaline earth metals, and nonmetals, which is why the range of elements compared to chromium differed between comparisons
- ^ Most common oxidation states of chromium are in bold. The right column lists a representative compound for each oxidation state.
- ^ Any color of corundum (disregarding red) is known as a sapphire. If the corundum is red, then it is a ruby. Sapphires are not required to be blue corundum crystals, as sapphires can be other colors such as yellow and purple
- ^ When Cr3+ replaces Al3+ in corundum (aluminium oxide, Al2O3), pink sapphire or ruby is formed, depending on the amount of chromium.
المصادر
- ^ أ ب Fawcett, Eric (1988). "Spin-density-wave antiferromagnetism in chromium". Reviews of Modern Physics. 60: 209. Bibcode:1988RvMP...60..209F. doi:10.1103/RevModPhys.60.209.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. pp. E110. ISBN 0-8493-0464-4.
- ^ "الكروم". الموسوعة العربية.
- ^ "Substance Information - ECHA". echa.europa.eu (in الإنجليزية البريطانية). Retrieved 17 يناير 2022.
- ^ EPA (أغسطس 2000). "Abandoned Mine Site Characterization and Cleanup Handbook" (PDF). United States Environmental Protection Agency. Retrieved 8 سبتمبر 2019.
- ^ "The Nature of X-Ray Photoelectron Spectra". CasaXPS. Casa Software Ltd. 2005. Retrieved 10 مارس 2019.
- ^ Schwarz, W. H. Eugen (أبريل 2010). "The Full Story of the Electron Configurations of the Transition Elements" (PDF). Journal of Chemical Education. 87 (4): 444–8. Bibcode:2010JChEd..87..444S. doi:10.1021/ed8001286. Retrieved 9 نوفمبر 2018.
- ^ Greenwood and Earnshaw, pp. 1004–5
- ^ أ ب خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةNIST specular reflection - ^ أ ب Lind, Michael Acton (1972). "The infrared reflectivity of chromium and chromium-aluminium alloys". Iowa State University Digital Repository. Iowa State University. Bibcode:1972PhDT........54L. Retrieved 4 نوفمبر 2018.
- ^ Bos, Laurence William (1969). "Optical properties of chromium-manganese alloys". Iowa State University Digital Repository. Iowa State University. Bibcode:1969PhDT.......118B. Retrieved 4 نوفمبر 2018.
- ^ Wallwork, GR (1976). "The oxidation of alloys". Reports on Progress in Physics. 39 (5): 401–485. Bibcode:1976RPPh...39..401W. doi:10.1088/0034-4885/39/5/001.
- ^ أ ب ت ث ج ح خ د Holleman, Arnold F; Wiber, Egon; Wiberg, Nils (1985). "Chromium". Lehrbuch der Anorganischen Chemie (in الألمانية) (91–100 ed.). Walter de Gruyter. pp. 1081–1095. ISBN 978-3-11-007511-3.
- ^ National Research Council (U.S.). Committee on Coatings (1970). High-temperature oxidation-resistant coatings: coatings for protection from oxidation of superalloys, refractory metals, and graphite. National Academy of Sciences. ISBN 978-0-309-01769-5.
- ^ أ ب Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties", Nuclear Physics A 729: 3–128, doi:, Bibcode: 2003NuPhA.729....3A, https://hal.archives-ouvertes.fr/in2p3-00020241/document
- ^ "Live Chart of Nuclides". International Atomic Energy Agency - Nuclear Data Section. Retrieved 18 أكتوبر 2018.
- ^ Birck, JL; Rotaru, M; Allegre, C (1999). "53Mn-53Cr evolution of the early solar system". Geochimica et Cosmochimica Acta. 63 (23–24): 4111–4117. Bibcode:1999GeCoA..63.4111B. doi:10.1016/S0016-7037(99)00312-9.
- ^ Frei, Robert; Gaucher, Claudio; Poulton, Simon W; Canfield, Don E (2009). "Fluctuations in Precambrian atmospheric oxygenation recorded by chromium isotopes". Nature. 461 (7261): 250–253. Bibcode:2009Natur.461..250F. doi:10.1038/nature08266. PMID 19741707. S2CID 4373201.
- ^ أ ب Kotaś, J.; Stasicka, Z. (2000). "Chromium occurrence in the environment and methods of its speciation". Environmental Pollution. 107 (3): 263–283. doi:10.1016/S0269-7491(99)00168-2. PMID 15092973.
- ^ Puigdomenech, Ignasi Hydra/Medusa Chemical Equilibrium Database and Plotting Software Archived 5 يونيو 2013 at the Wayback Machine (2004) KTH Royal Institute of Technology
- ^ Clark, Jim. "Oxidation states (oxidation numbers)". Chemguide. Retrieved 3 أكتوبر 2018.
- ^ أ ب Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ Theopold, Klaus H.; Kucharczyk, Robin R. (2011-12-15), Scott, Robert A., ed. (in en), Chromium: Organometallic Chemistry, John Wiley & Sons, Ltd, pp. eibc0042, doi:, ISBN 978-1-119-95143-8.
- ^ Cotton, FA; Walton, RA (1993). Multiple Bonds Between Metal Atoms. Oxford: Oxford University Press. ISBN 978-0-19-855649-7.
- ^ "Chromium(III) compounds". National Pollutant Inventory. Commonwealth of Australia. Retrieved 8 نوفمبر 2018.
- ^ Assfalg, M; Banci, L; Bertini, I; Bruschi, M; Michel, C; Giudici-Orticoni, M; Turano, P (31 يوليو 2002). "NMR structural characterization of the reduction of chromium(VI) to chromium(III) by cytochrome c7". Protein Data Bank (1LM2). doi:10.2210/pdb1LM2/pdb. Retrieved 8 نوفمبر 2018.
- ^ Luther, George W. (2016). "Introduction to Transition Metals". Inorganic Chemistry for Geochemistry & Environmental Sciences: Fundamentals & Applications. Hydrate (Solvate) Isomers. John Wiley & Sons. p. 244. ISBN 978-1118851371. Retrieved 7 أغسطس 2019.
- ^ Gumerova, Nadiia I.; Roller, Alexander; Giester, Gerald; Krzystek, J.; Cano, Joan; Rompel, Annette (19 فبراير 2020). "Incorporation of CrIII into a Keggin Polyoxometalate as a Chemical Strategy to Stabilize a Labile {CrIIIO4} Tetrahedral Conformation and Promote Unattended Single-Ion Magnet Properties". Journal of the American Chemical Society. 142 (7): 3336–3339. doi:10.1021/jacs.9b12797. ISSN 0002-7863. PMC 7052816. PMID 31967803.
- ^ Seppelt, Konrad (28 يناير 2015). "Molecular Hexafluorides". Chemical Reviews (in الإنجليزية). 115 (2): 1296–1306. doi:10.1021/cr5001783. ISSN 0009-2665. PMID 25418862.
- ^ Haxhillazi, Gentiana (2003). Preparation, Structure and Vibrational Spectroscopy of Tetraperoxo Complexes of CrV+, VV+, NbV+ and TaV+ (PhD thesis). University of Siegen.
- ^ Thaler, Eric G.; Rypdal, Kristin; Haaland, Arne; Caulton, Kenneth G. (1 يونيو 1989). "Structure and reactivity of chromium(4+) tert-butoxide". Inorganic Chemistry. 28 (12): 2431–2434. doi:10.1021/ic00311a035. ISSN 0020-1669.
- ^ Nguyen, T; Sutton, AD; Brynda, M; Fettinger, JC; Long, GJ; Power, PP (2005). "Synthesis of a stable compound with fivefold bonding between two chromium(I) centers". Science. 310 (5749): 844–847. Bibcode:2005Sci...310..844N. doi:10.1126/science.1116789. PMID 16179432. S2CID 42853922.
- ^ Emsley, John (2001). "Chromium". Nature's Building Blocks: An A–Z Guide to the Elements. Oxford, England, UK: Oxford University Press. pp. 495–498. ISBN 978-0-19-850340-8.
- ^ John Rieuwerts (14 يوليو 2017). The Elements of Environmental Pollution. Taylor & Francis. ISBN 978-1-135-12679-7.
- ^ أ ب National Research Council (U.S.). Committee on Biologic Effects of Atmospheric Pollutants (1974). Chromium. National Academy of Sciences. ISBN 978-0-309-02217-0.
- ^ Champion, Marc (11 يناير 2018). "How a Trump SoHo Partner Ended Up With Toxic Mining Riches From Kazakhstan". Bloomberg.com. Bloomberg L.P. Retrieved 21 يناير 2018.
- ^ أ ب ت ث Papp, John F. "Mineral Yearbook 2015: Chromium" (PDF). United States Geological Survey. Retrieved 3 يونيو 2015.
- ^ Fleischer, Michael (1982). "New Mineral Names" (PDF). American Mineralogist. 67: 854–860.
- ^ Chromium (with location data), Mindat.
- ^ Chromium from Udachnaya-Vostochnaya pipe, Daldyn, Daldyn-Alakit kimberlite field, Saha Republic (Sakha Republic; Yakutia), Eastern-Siberian Region, Russia, Mindat.
- ^ Gonzalez, A. R.; Ndung'u, K.; Flegal, A. R. (2005). "Natural Occurrence of Hexavalent Chromium in the Aromas Red Sands Aquifer, California". Environmental Science and Technology. 39 (15): 5505–5511. Bibcode:2005EnST...39.5505G. doi:10.1021/es048835n. PMID 16124280.
- ^ أ ب ت ث Papp, John F. & Lipin, Bruce R. (2006). "Chromite". Industrial Minerals & Rocks: Commodities, Markets, and Uses (7th ed.). SME. ISBN 978-0-87335-233-8.
- ^ Papp, John F. "Mineral Yearbook 2002: Chromium" (PDF). United States Geological Survey. Retrieved 16 فبراير 2009.
- ^ Morrison, RD; Murphy, BL (4 أغسطس 2010). Environmental Forensics: Contaminant Specific Guide (in الإنجليزية). Academic Press. ISBN 9780080494784.
- ^ Davis, JR (2000). Alloy digest sourcebook : stainless steels (in الأفريقانية). Materials Park, OH: ASM International. pp. 1–5. ISBN 978-0-87170-649-2. OCLC 43083287.
- ^ Bhadeshia, HK. "Nickel-Based Superalloys". University of Cambridge. Archived from the original on 25 أغسطس 2006. Retrieved 17 فبراير 2009.
- ^ "Chromium, Nickel and Welding". IARC Monographs. International Agency for Research on Cancer. 49: 49–50. 1990.
- ^ "Stainless Steel Grade 332 (UNS S33200)". AZoNetwork. 5 مارس 2013.
- ^ "Super Alloy INCOLOY Alloy 800 (UNS N08800)". AZoNetwork. 3 يوليو 2013.
- ^ "Manual On Uniform Traffic Control Devices (War Emergency Edition)" (PDF). Washington, DC: American Associan of State Highway Officials. نوفمبر 1942. p. 52. Retrieved 8 يوليو 2021.
- ^ State Department, United States. "Allied Relations and Negotiations with Turkey" (PDF). Archived (PDF) from the original on 9 نوفمبر 2020.
- ^ Breitsameter, M (15 أغسطس 2002). "Thermal Spraying versus Hard Chrome Plating". Azo Materials. AZoNetwork. Retrieved 1 أكتوبر 2018.
- ^ أ ب خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةCrplating - ^ Edwards, J (1997). Coating and Surface Treatment Systems for Metals. Finishing Publications Ltd. and ASMy International. pp. 66–71. ISBN 978-0-904477-16-0.
- ^ Zhao J, Xia L, Sehgal A, Lu D, McCreery RL, Frankel GS (2001). "Effects of chromate and chromate conversion coatings on corrosion of aluminum alloy 2024-T3". Surface and Coatings Technology. 140 (1): 51–57. doi:10.1016/S0257-8972(01)01003-9. hdl:1811/36519.
- ^ Cotell, CM; Sprague, JA; Smidt, FA (1994). ASM Handbook: Surface Engineering. ASM International. ISBN 978-0-87170-384-2. Retrieved 17 فبراير 2009.
- ^ Gettens, Rutherford John (1966). "Chrome yellow". Painting Materials: A Short Encyclopaedia. Courier Dover Publications. pp. 105–106. ISBN 978-0-486-21597-6.
- ^ Gerd Anger et al. "Chromium Compounds" Ullmann's Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a07_067
- ^ Marrion, Alastair (2004). The chemistry and physics of coatings. Royal Society of Chemistry. pp. 287–. ISBN 978-0-85404-604-1.
- ^ Moss, SC; Newnham, RE (1964). "The chromium position in ruby" (PDF). Zeitschrift für Kristallographie. 120 (4–5): 359–363. Bibcode:1964ZK....120..359M. doi:10.1524/zkri.1964.120.4-5.359.
- ^ Webb, Colin E; Jones, Julian DC (2004). Handbook of Laser Technology and Applications: Laser design and laser systems. CRC Press. pp. 323–. ISBN 978-0-7503-0963-9.
- ^ أ ب Hingston, J; Collins, CD; Murphy, RJ; Lester, JN (2001). "Leaching of chromated copper arsenate wood preservatives: a review". Environmental Pollution. 111 (1): 53–66. doi:10.1016/S0269-7491(00)00030-0. PMID 11202715.
- ^ Brown, EM (1997). "A Conformational Study of Collagen as Affected by Tanning Procedures". Journal of the American Leather Chemists Association. 92: 225–233.
- ^ Sreeram, K.; Ramasami, T. (2003). "Sustaining tanning process through conservation, recovery and better utilization of chromium". Resources, Conservation and Recycling. 38 (3): 185–212. doi:10.1016/S0921-3449(02)00151-9.
- ^ Qiang, Taotao; Gao, Xin; Ren, Jing; Chen, Xiaoke; Wang, Xuechuan (9 ديسمبر 2015). "A Chrome-Free and Chrome-Less Tanning System Based on the Hyperbranched Polymer". ACS Sustainable Chemistry & Engineering. 4 (3): 701–707. doi:10.1021/acssuschemeng.5b00917.
- ^ Barnhart, Joel (1997). "Occurrences, Uses, and Properties of Chromium". Regulatory Toxicology and Pharmacology. 26 (1): S3–S7. doi:10.1006/rtph.1997.1132. ISSN 0273-2300. PMID 9380835.
- ^ Weckhuysen, Bert M; Schoonheydt, Robert A (1999). "Olefin polymerization over supported chromium oxide catalysts" (PDF). Catalysis Today. 51 (2): 215–221. doi:10.1016/S0920-5861(99)00046-2. hdl:1874/21357.
- ^ Twigg, MVE (1989). "The Water-Gas Shift Reaction". Catalyst Handbook. ISBN 978-0-7234-0857-4.
- ^ Rhodes, C; Hutchings, GJ; Ward, AM (1995). "Water-gas shift reaction: Finding the mechanistic boundary". Catalysis Today. 23: 43–58. doi:10.1016/0920-5861(94)00135-O.
- ^ Lazier, WA & Arnold, HR (1939). "Copper Chromite Catalyst". Organic Syntheses. 19: 31; Collected Volumes, 2, pp. 142.
- ^ Mallinson, John C. (1993). "Chromium Dioxide". The foundations of magnetic recording. Academic Press. p. 32. ISBN 978-0-12-466626-9.
- ^ Toshiro Doi; Ioan D. Marinescu; Syuhei Kurokawa (30 نوفمبر 2011). Advances in CMP Polishing Technologies. William Andrew. pp. 60–. ISBN 978-1-4377-7860-1.
- ^ Baral, Anil; Engelken, Robert D. (2002). "Chromium-based regulations and greening in metal finishing industries in the USA". Environmental Science & Policy. 5 (2): 121–133. doi:10.1016/S1462-9011(02)00028-X.
- ^ Soderberg, Tim (3 يونيو 2019). "Oxidizing Agents". LibreTexts. MindTouch. Retrieved 8 سبتمبر 2019.
- ^ Roth, Alexander (1994). Vacuum Sealing Techniques. Springer Science & Business Media. pp. 118–. ISBN 978-1-56396-259-2.
- ^ Lancashire, Robert J (27 أكتوبر 2008). "Determination of iron using potassium dichromate: Redox indicators". The Department of Chemistry UWI, Jamaica. Retrieved 8 سبتمبر 2019.
- ^ Garverick, Linda (1994). Corrosion in the Petrochemical Industry. ASM International. ISBN 978-0-87170-505-1.
- ^ Shahid Ul-Islam (18 يوليو 2017). Plant-Based Natural Products: Derivatives and Applications. Wiley. pp. 74–. ISBN 978-1-119-42388-1.
- ^ Vincent, JB (2013). "Chapter 6. Chromium: Is It Essential, Pharmacologically Relevant, or Toxic?". In Astrid Sigel; Helmut Sigel; Roland KO Sigel (eds.). Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. Vol. 13. Springer. pp. 171–198. doi:10.1007/978-94-007-7500-8_6. ISBN 978-94-007-7499-5. PMID 24470092.
- ^ Maret, Wolfgang (2019). "Chapter 9. Chromium Supplementation in Human Health, Metabolic Syndrome, and Diabetes". In Sigel, Astrid; Freisinger, Eva; Sigel, Roland K. O.; Carver, Peggy L. (eds.). Essential Metals in Medicine:Therapeutic Use and Toxicity of Metal Ions in the Clinic. Vol. 19. Berlin: de Gruyter GmbH. pp. 231–251. doi:10.1515/9783110527872-015. ISBN 978-3-11-052691-2. PMID 30855110.
{{cite book}}:|journal=ignored (help) - ^ أ ب ت ث ج خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةods - ^ European Food Safety Authority (2014). "Scientific Opinion on Dietary Reference Values for chromium". EFSA Journal. 12 (10): 3845. doi:10.2903/j.efsa.2014.3845.
- ^ Di Bona KR, Love S, Rhodes NR, McAdory D, Sinha SH, Kern N, Kent J, Strickland J, Wilson A, Beaird J, Ramage J, Rasco JF, Vincent JB (2011). "Chromium is not an essential trace element for mammals: effects of a "low-chromium" diet". J Biol Inorg Chem. 16 (3): 381–390. doi:10.1007/s00775-010-0734-y. PMID 21086001. S2CID 22376660.
- ^ Wise, SS; Wise, JP, Sr (2012). "Chromium and genomic stability". Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis. 733 (1–2): 78–82. doi:10.1016/j.mrfmmm.2011.12.002. PMC 4138963. PMID 22192535.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ^ "ToxFAQs: Chromium". Agency for Toxic Substances & Disease Registry, Centers for Disease Control and Prevention. فبراير 2001. Archived from the original on 8 يوليو 2014. Retrieved 2 أكتوبر 2007.
- ^ Vincent, JB (2015). "Is the Pharmacological Mode of Action of Chromium(III) as a Second Messenger?". Biological Trace Element Research. 166 (1): 7–12. doi:10.1007/s12011-015-0231-9. PMID 25595680. S2CID 16895342.
- ^ أ ب Thor, MY; Harnack, L; King, D; Jasthi, B; Pettit, J (2011). "Evaluation of the comprehensiveness and reliability of the chromium composition of foods in the literature". Journal of Food Composition and Analysis. 24 (8): 1147–1152. doi:10.1016/j.jfca.2011.04.006. PMC 3467697. PMID 23066174.
- ^ Kamerud KL; Hobbie KA; Anderson KA (2013). "Stainless steel leaches nickel and chromium into foods during cooking". Journal of Agricultural and Food Chemistry. 61 (39): 9495–9501. doi:10.1021/jf402400v. PMC 4284091. PMID 23984718.
- ^ Flint GN; Packirisamy S (1997). "Purity of food cooked in stainless steel utensils". Food Additives and Contaminants. 14 (2): 115–126. doi:10.1080/02652039709374506. PMID 9102344.
- ^ "Chromium Food Sources, Chromium: Diabetes & Weight Loss". dietbites.com. Retrieved 25 مارس 2013.
- ^ "Federal Register May 27, 2016 Food Labeling: Revision of the Nutrition and Supplement Facts Labels. FR page 33982" (PDF).
- ^ "Daily Value Reference of the Dietary Supplement Label Database (DSLD)". Dietary Supplement Label Database (DSLD). Archived from the original on 7 أبريل 2020. Retrieved 16 مايو 2020.
- ^ "USDA Food Composition Databases". United States Department of Agriculture Agricultural Research Service. أبريل 2018. Retrieved 4 أكتوبر 2018.
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةIOM-Chromium - ^ Kumpulainen, JT (1992). "Chromium content of foods and diets". Biological Trace Element Research. 32 (1–3): 9–18. doi:10.1007/BF02784582. PMID 1375091. S2CID 10189109.
- ^ Grijalva Haro, MI; Ballesteros Vázquez, MN; Cabrera Pacheco, RM (2001). "Chromium content in foods and dietary intake estimation in the Northwest of Mexico". Arch Latinoam Nutr (in الإسبانية). 51 (1): 105–110. PMID 11515227.
- ^ أ ب Kantor, Elizabeth D; Rehm, Colin D; Du, Mengmeng; White, Emily; Giovannucci, Edward L (11 أكتوبر 2017). "Trends in Dietary Supplement Use Among US Adults From 1999-2012". JAMA. 316 (14): 1464–1474. doi:10.1001/jama.2016.14403. PMC 5540241. PMID 27727382.
- ^ أ ب Stehle, P; Stoffel-Wagner, B; Kuh, KS (6 أبريل 2014). "Parenteral trace element provision: recent clinical research and practical conclusions". European Journal of Clinical Nutrition. 70 (8): 886–893. doi:10.1038/ejcn.2016.53. PMC 5399133. PMID 27049031.
- ^ Finch, Carolyn Weiglein (فبراير 2015). "Review of trace mineral requirements for preterm infants: What are the current recommendations for clinical practice?". Nutrition in Clinical Practice. 30 (1): 44–58. doi:10.1177/0884533614563353. PMID 25527182.
- ^ أ ب Vincent, John B (2010). "Chromium: Celebrating 50 years as an essential element?". Dalton Transactions. 39 (16): 3787–3794. doi:10.1039/B920480F. PMID 20372701.
- ^ FDA Qualified Health Claims: Letters of Enforcement Discretion, Letters of Denial U.S. Food and Drug Administration, Docket #2004Q-0144 (August 2005).
- ^ "Monograph: Chromium (from Chromium picolinate)". Health Canada. 9 ديسمبر 2009. Retrieved 18 أكتوبر 2018.
- ^ أ ب Scientific Opinion on the substantiation of health claims related to chromium and contribution to normal macronutrient metabolism (ID 260, 401, 4665, 4666, 4667), maintenance of normal blood glucose concentrations (ID 262, 4667), contribution to the maintenance or achievement of a normal body weight (ID 339, 4665, 4666), and reduction of tiredness and fatigue (ID 261) pursuant to Article 13(1) of Regulation (EC) No 1924/2006 Archived 21 أبريل 2020 at the Wayback Machine European Food Safety Authority EFSA J 2010;8(10)1732.
- ^ San Mauro-Martin I, Ruiz-León AM, Camina-Martín MA, Garicano-Vilar E, Collado-Yurrita L, Mateo-Silleras B, Redondo P (2016). "[Chromium supplementation in patients with type 2 diabetes and high risk of type 2 diabetes: a meta-analysis of randomized controlled trials]". Nutr Hosp (in الإسبانية). 33 (1): 27. doi:10.20960/nh.27. PMID 27019254.
- ^ Abdollahi, M; Farshchi, A; Nikfar, S; Seyedifar, M (2013). "Effect of chromium on glucose and lipid profiles in patients with type 2 diabetes; a meta-analysis review of randomized trials". J Pharm Pharm Sci. 16 (1): 99–114. doi:10.18433/J3G022. PMID 23683609.
- ^ Suksomboon, N; Poolsup, N; Yuwanakorn, A (17 مارس 2013). "Systematic review and meta-analysis of the efficacy and safety of chromium supplementation in diabetes". J Clin Pharm Ther. 39 (3): 292–306. doi:10.1111/jcpt.12147. PMID 24635480. S2CID 22326435.
- ^ Bailey, Christopher H (يناير 2014). "Improved meta-analytic methods show no effect of chromium supplements on fasting glucose". Biol Trace Elem Res. 157 (1): 1–8. doi:10.1007/s12011-013-9863-9. PMID 24293356. S2CID 2441511.
- ^ Costello, Rebecca B; Dwyer, Johanna T; Bailey, Regan L (30 مايو 2016). "Chromium supplements for glycemic control in type 2 diabetes: limited evidence of effectiveness". Nutrition Reviews. 74 (7): 455–468. doi:10.1093/nutrit/nuw011. PMC 5009459. PMID 27261273.
- ^ أ ب Tian, Honglian; Guo, Xiaohu; Wang, Xiyu; He, Zhiyun; Sun, Rao; Ge, Sai; Zhang, Zongjiu (2013). "Chromium picolinate supplementation for overweight or obese adults". Cochrane Database Syst Rev (11): CD010063. doi:10.1002/14651858.CD010063.pub2. PMC 7433292. PMID 24293292.
- ^ أ ب Onakpoya, I; Posadzki, P; Ernst, E (2013). "Chromium supplementation in overweight and obesity: a systematic review and meta-analysis of randomized clinical trials". Obes Rev. 14 (6): 496–507. doi:10.1111/obr.12026. PMID 23495911. S2CID 21832321.
- ^ Lefavi RG, Anderson RA, Keith RE, Wilson GD, McMillan JL, Stone MH (1992). "Efficacy of chromium supplementation in athletes: emphasis on anabolism". International Journal of Sport Nutrition. 2 (2): 111–122. doi:10.1123/ijsn.2.2.111. PMID 1299487.
- ^ Vincent JB (2003). "The potential value and toxicity of chromium picolinate as a nutritional supplement, weight loss agent and muscle development agent". Sports Med. 33 (3): 213–230. doi:10.2165/00007256-200333030-00004. PMID 12656641. S2CID 9981172.
- ^ Jenkinson DM, Harbert AJ (2008). "Supplements and sports". Am Fam Physician. 78 (9): 1039–1046. PMID 19007050.
- ^ Maughan RJ, Burke LM, et al. (2018). "IOC Consensus Statement: Dietary Supplements and the High-Performance Athlete". International Journal of Sport Nutrition and Exercise Metabolism. 28 (2): 104–125. doi:10.1123/ijsnem.2018-0020. PMC 5867441. PMID 29589768.
- ^ Islam MM, Karim MR, Zheng X, Li X (2018). "Heavy Metal and Metalloid Pollution of Soil, Water and Foods in Bangladesh: A Critical Review". International Journal of Environmental Research and Public Health. 15 (12): 2825. doi:10.3390/ijerph15122825. PMC 6313774. PMID 30544988.
- ^ أ ب Bakshi A, Panigrahi AK (2018). "A comprehensive review on chromium induced alterations in fresh water fishes". Toxicol Rep. 5: 440–447. doi:10.1016/j.toxrep.2018.03.007. PMC 5977408. PMID 29854615.
- ^ Ahmed AR, Jha AN, Davies SJ (2012). "The efficacy of chromium as a growth enhancer for mirror carp (Cyprinus carpio L): an integrated study using biochemical, genetic, and histological responses". Biol Trace Elem Res. 148 (2): 187–197. doi:10.1007/s12011-012-9354-4. PMID 22351105. S2CID 16154712.
- ^ المعادن الثقيلة.. سموم بيئية، فيدو
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةKatz - ^ Dayan, AD; Paine, AJ (2001). "Mechanisms of chromium toxicity, carcinogenicity and allergenicity: Review of the literature from 1985 to 2000". Human & Experimental Toxicology. 20 (9): 439–451. doi:10.1191/096032701682693062. PMID 11776406. S2CID 31351037.
- ^ Newman, D. (1890). "A case of adeno-carcinoma of the left inferior turbinated body, and perforation of the nasal septum, in the person of a worker in chrome pigments". Glasgow Medical Journal. 33: 469–470.
- ^ Langard, S (1990). "One Hundred Years of Chromium and Cancer: A Review of Epidemiological Evidence and Selected Case Reports". American Journal of Industrial Medicine. 17 (2): 189–214. doi:10.1002/ajim.4700170205. PMID 2405656.
- ^ Cohen, MD; Kargacin, B; Klein, CB; Costa, M (1993). "Mechanisms of chromium carcinogenicity and toxicity". Critical Reviews in Toxicology. 23 (3): 255–281. doi:10.3109/10408449309105012. PMID 8260068.
- ^ Methods to Develop Inhalation Cancer Risk Estimates for Chromium and Nickel Compounds. Research Triangle Park, NC: U.S. Environmental Protection Agency, Office of Air Quality Planning and Standards, Health and Environmental Impacts Division. 2011. Retrieved 19 مارس 2015.
- ^ Ngan, V (2002). "Chrome Allergy". DermNet NZ.
- ^ Basketter, David; Horev, L; Slodovnik, D; Merimes, S; Trattner, A; Ingber, A (2000). "Investigation of the threshold for allergic reactivity to chromium". Contact Dermatitis. 44 (2): 70–74. doi:10.1034/j.1600-0536.2001.440202.x. PMID 11205406. S2CID 45426346.
- ^ Baselt, Randall C (2008). Disposition of Toxic Drugs and Chemicals in Man (8th ed.). Foster City: Biomedical Publications. pp. 305–307. ISBN 978-0-9626523-7-0.
- ^ "US water has large amounts of likely carcinogen: study". Yahoo News. 19 ديسمبر 2010. Archived from the original on 23 ديسمبر 2010. Retrieved 19 ديسمبر 2010.
- ^ James, Bruce (1996). "The challenge of remediating chromium-contaminated soil". Environmental Science and Technology. 30 (6): 248A–251A. doi:10.1021/es962269h. PMID 21648723.
وصلات خارجية
- ATSDR Case Studies in Environmental Medicine: Chromium Toxicity U.S. Department of Health and Human Services
- IARC Monograph "Chromium and Chromium compounds"
- It's Elemental – The Element Chromium
- National Pollutant Inventory – Chromium (III) compounds fact sheet
- The Merck Manual – Mineral Deficiency and Toxicity
- National Institute for Occupational Safety and Health – Chromium Page
- The periodic table of videos: Chromium
| الجدول الدوري | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Uub | Uut | Uuq | Uup | Uuh | Uus | Uuo | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||
- CS1 الإنجليزية البريطانية-language sources (en-gb)
- CS1 الألمانية-language sources (de)
- CS1 الأفريقانية-language sources (af)
- CS1 errors: periodical ignored
- CS1 الإسبانية-language sources (es)
- Short description is different from Wikidata
- Pages using infobox element with unknown parameters
- Articles with hatnote templates targeting a nonexistent page
- مقالات جيدة
- Use dmy dates from November 2011
- كروم
- عناصر كيميائية
- فلزات إنتقالية
- معادن غذائية
- سلامة وصحة مهنية
- علم الأحياء وعلم الصيدلة من العناصر الكيميائية


