بروم
 Liquid and gas bromine inside transparent cube | |||||||||||||||
| البروم | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| المظهر | بني مائل للحمرة | ||||||||||||||
| الوزن الذري العياري Ar°(Br) | |||||||||||||||
| البروم في الجدول الدوري | |||||||||||||||
| |||||||||||||||
| الرقم الذري (Z) | 35 | ||||||||||||||
| المجموعة | 17 | ||||||||||||||
| الدورة | period 4 | ||||||||||||||
| المستوى الفرعي | p-block | ||||||||||||||
| التوزيع الإلكتروني | [Ar] 3d10 4s2 4p5 | ||||||||||||||
| الإلكترونات بالغلاف | 2, 8, 18, 7 | ||||||||||||||
| الخصائص الطبيعية | |||||||||||||||
| الطور at د.ح.ض.ق | liquid | ||||||||||||||
| نقطة الانصهار | 265.8 K (−7.2 °س، 19 °F) | ||||||||||||||
| نقطة الغليان | 332.0 K (58.8 °س، 137.8 °ف) | ||||||||||||||
| الكثافة (بالقرب من د.ح.غ.) | Br2، السائل: 3.1028 ج/سم³ | ||||||||||||||
| النقطة الثلاثية | 265.90 K, 5.8 kPa[1] | ||||||||||||||
| النقطة الحرجة | 588 K, 10.34 MPa[1] | ||||||||||||||
| حرارة الانصهار | (Br2) 10.571 kJ/mol | ||||||||||||||
| حرارة التبخر | (Br2) 29.96 kJ/mol | ||||||||||||||
| السعة الحرارية المولية | (Br2) 75.69 J/(mol·K) | ||||||||||||||
ضغط البخار
| |||||||||||||||
| الخصائص الذرية | |||||||||||||||
| الكهرسلبية | مقياس پاولنگ: 2.96 | ||||||||||||||
| طاقات التأين |
| ||||||||||||||
| نصف القطر الذري | empirical: 120 pm | ||||||||||||||
| نصف قطر التكافؤ | 120±3 pm | ||||||||||||||
| نصف قطر ڤان در ڤالز | 185 pm | ||||||||||||||
| خصائص أخرى | |||||||||||||||
| البنية البلورية | orthorhombic | ||||||||||||||
| سرعة الصوت | 206 م/ث (at 20 °س) | ||||||||||||||
| قضيب رفيع | 0.122 W/(m·K) | ||||||||||||||
| المقاومة الكهربائية | 7.8×1010 Ω⋅m (at 20 °C) | ||||||||||||||
| الترتيب المغناطيسي | مغناطيسي معاكس[2] | ||||||||||||||
| القابلية المغناطيسية | −56.4×10−6 cm3/mol[3] | ||||||||||||||
| رقم كاس | 7726-95-6 | ||||||||||||||
| التاريخ | |||||||||||||||
| الاكتشاف وأول عزل | أنطوان جيروم بالارد كارل ياكوب لوڤيگ (1825) | ||||||||||||||
| نظائر الالبروم | |||||||||||||||
| قالب:جدول نظائر البروم غير موجود | |||||||||||||||
البروم (إنگليزية: Bromine)، هو عنصر كيميائي يحمل الرمز Br ورقمه الذري 35. وهو سائل أحمر-بني متطاير في درجة حرارة الغرفة ويتبخر بسهولة ليشكل بخارًا بنفس اللون. خصائصه متوسطة بين خصائص الكلور واليود. عزله كيميائيان، كلٌ على حدة، كارل ياكوب لوڤيگ (عام 1825) وأنطوان جيروم بالار (عام 1826)، وقد اشتق اسمه من اليونانية القديمة βρῶμος (بروموس)، وتعني "الرائحة الكريهة"، في إشارة إلى رائحته الحادة والنفاذة.
البروم العنصري تفاعلي للغاية، وبالتالي لا يتواجد كعنصر حر في الطبيعة. بدلاً من ذلك، يمكن عزله من أملاح هاليدة معدنية بلورية قابلة للذوبان عديم اللون مشابهة لملح الطعام، وهي خاصية يشترك فيها مع الهالوجينات الأخرى. على الرغم من ندرة وجوده في القشرة الأرضية، إلا أن قابلية ذوبان أيون البروميد العالية (Br−) قد تسببت في تراكمه في المحيطات. تجاريًا، يستخر العنصر بسهولة من برك تبخر المياه المالحة، معظمها في الولايات المتحدة وإسرائيل. تبلغ كتلة البروم في المحيطات حوالي واحد على ثلاثمائة من كتلة الكلور.
في الظروف القياسية لدرجة الحرارة والضغط يكون سائلاً؛ والعنصر الوحيد الآخر الذي يكون سائلاً في ظل هذه الظروف هو الزئبق. عند درجات الحرارة المرتفعة، ينفصل مركب البروم العضوي بسهولة لينتج ذرات البروم الحرة، وهي تفاعلات متسلسلة كيميائية توقف الجذور الحرة. هذا التأثير يجعل مركبات البروم العضوية مفيدة كمثبطات للحريق، وأكثر من نصف البروم الذي يتم إنتاجه في جميع أنحاء العالم سنوياً يستخدم لهذا الغرض. تتسبب الخاصية نفسها في قيام الأشعة فوق البنفسجية في ضوء الشمس بفصل مركبات البروم العضوية المتطايرة في الغلاف الجوي لإنتاج ذرات البروم الحرة، مما يسبب استنفاد الأوزون. نتيجة لذلك، فإن العديد من مركبات البروم العضوية - مثل المبيدات الحشرية بروميد الميثيل - لم تعد تُستخدم. لا تزال مركبات البروم تستخدم في سوائل حفر الآبار، وفي الأفلام الفوتوغرافية، وكمادة وسيطة في تصنيع الكيماويات العضوية.
تعتبر الكميات الكبيرة من أملاح البروميد سامة بسبب عمل أيونات البروميد القابلة للذوبان، مما يسبب تسمم البروم. ومع ذلك، فإن البروم مفيد للخلايا الحمضية البشرية،[4] وهو عنصر تتبع أساسي لتطور الكولاجين في جميع الحيوانات.[5] تُخلق المئات من مركبات البروم العضوية المعروفة بواسطة النباتات والحيوانات البرية والبحرية، وبعضها يؤدي أدوارًا حيوية هامة.[6] باعتباره مركباً صيدلانياً، فإن أيون البروميد البسيط (Br−) ) له تأثيرات مثبطة على الجهاز العصبي المركزي، وكانت الأملاح البروميد من المهدئات الطبية الرئيسية، قبل استبدالها بأدوية ذات مفعول أقصر. لا تزال تستخدم في صناعة أدوية متخصصة مثل مضادات الصرع.
التاريخ

اكتشف البروم بشكل مستقل بواسطة اثنين من الكميائيين، كارل ياكوب لوڤيگ[7] وأنطوان بالار،[8][9] عامي 1825 و1826، بالترتيب.[10]
قام لوڤيگ بعزل البروم من نبع مياه معدنية من مسقط رأسه باد كرويتسناخ عام 1825. استخدم لوڤيگ محلول الملح المعدني المشبع بالكلور واستخرج البروم مع ثنائي إيثيل الإيثر. وبعد تبخر الأثير بقي سائل بني. باستخدام هذا السائل كعينة من عمله تقدم لوظيفة في مختبر ليوپولد گملين في هايدلبرگ. تأخر نشر النتائج ونشر بالار نتائجه أولاً.[11]
عثر بالار على مواد كيميائية من البروم في رماد الأعشاب البحرية من المستنقعات المالحة في مونپلييه. استخدمت الأعشاب البحرية لإنتاج اليود، لكنها تحتوي أيضًا على البروم. قام بالار بتقطير البروم من محلول رماد الأعشاب البحرية المشبع بالكلور. وكانت خواص المادة الناتجة متوسطة بين خواص الكلور واليود؛ فحاول أن يثبت أن المادة هي أحادي كلوريد اليود (ICl)، لكنه بعد أن فشل في ذلك تيقن أنه وجد عنصراً جديداً وأطلق عليه اسم موريد، مشتق من الكلمة اللاتينية muria ("محلول ملحي").[9][12][13]
بعد موافقة الكيميائيون الفرنسيون لوي نيكولا ڤاوكلان، لوي جاك ثينار، ولوي-جوزيف گي-لوساك على تجارب الصيدلي الشاب بالار، عُرضت النتائج في محاضرة في أكاديمية العلوم الفرنسية ونشرت في حوليات الكيمياء والفيزياء.[8] في منشوره، ذكر بالار أنه غير الاسم من muride إلى brôme باقترات من م. أنگلادا. اسم brôme (بروم) مشتق من الكلمة اليونانية βρῶμος (brômos، "كريه الرائحة").[8][14][12][15] بينما تذكر مصادر أخرى أن الكيميائي والفيزيائي الفرنسي لوي-جوزيف گي-لوساك قد اقترح اسم "بروم" نظراً لأبخرته ذات الرائحة النفاذة.[16][17] لم يُنتج البروم بكميات كبيرة حتى عام 1858، عند اكتشاف رواسب الملح في ستاسفورت مكن من إنتاجه كمنتج ثانوي لملح القلي (البوتاس).[18]
بصرف النظر عن بعض التطبيقات الطبية البسيطة، كان أول استخدام تجاري للبروم هو الداجيرية (نوع مبكر من التصوير). عام 1840، اكتشف أن البروم يتمتع ببعض المزايا مقارنة ببخار اليود المستخدم سابقًا لإنشاء طبقة هاليد الفضة الحساسة للضوء المستخدمة في الداجيرية.[19]
استخدم بروميد الپوتاسيوم وبروميد الصوديوم كمضادات اختلاج ومهدئات في أواخر القرن التاسع عشر وأوائل القرن العشرين، لكنها استبدلت تدريجيًا بهيدرات الكلورال ثم بالباربيتيورات.[20] في السنوات الأولى من الحرب العالمية الأولى، استخدمت مركبات البروم مثل بروميد الزايليل كغاز سام.[21]
الخصائص
البروم هو الهالوجين الثالث، كونه عنصراً لافلزياً في المجموعة 17 من الجدول الدوري. وبالتالي فإن خصائصه تشبه خصائص الفلور، الكلور، واليود، وتميل إلى أن تكون متوسطة بين خصائص الهالوجينين المتجاورين، الكلور واليود. يحتوي البروم على التكوين الإلكتروني [Ar]4s23d104p5، حيث تعمل الإلكترونات السبعة الموجودة في الغلاف الرابع والأبعد كإلكترون تكافؤ خاص به. مثل جميع الهالوجينات، فهو ينقصه إلكترون واحد عن الثمانية الكاملة، وبالتالي فهو عامل مؤكسد قوي، يتفاعل مع العديد من العناصر لإكمال غلافه الخارجي.[22] يتوافق البروم مع الاتجاهات الدورية، وهو متوسط في الكهرسلبية بين الكلور واليود (F: 3.98, Cl: 3.16, Br: 2.96, I: 2.66)، وهو أقل تفاعلاً من الكلور وأكثر تفاعلاً من اليود. وهو أيضًا عامل مؤكسد أضعف من الكلور، لكنه أقوى من اليود. وعلى العكس من ذلك، فإن أيون البروميد هو عامل اختزال أضعف من اليوديد، ولكنه أقوى من الكلوريد.[22] أدت أوجه التشابه هذه إلى تصنيف الكلور والبروم واليود معًا كأحد الثلاثيات الأصلية ليوهان ڤولفگانگ دوبراينر، الذي تنبأ عمله بالقانون الدوري للعناصر الكيميائية.[23][24] وهو ذو نصف قطري ذري متوسط بين الكلور واليود، وهذا يؤدي إلى أن العديد من خصائصه الذرية تكون متوسطة بالمثل في القيمة بين الكلور واليود، مثل طاقة التأين الأولى، الألفة الإلكترونية، المحتوى الحراري للتفكك جزيء X2 (X = Cl, Br, I)، نصف القطر الأيوني، وطول الحزمةX–X.[22] يبرز تطاير البروم رائحته النفاذة والخانقة والكريهة.[25]
تتمتع جميع الهالوجينات الأربعة المستقرة بقوى ڤان در ڤالز الجاذبة بين الجزئيات، وتزداد قوتها مع عدد الإلكترونات بين جميع جزيئات الهالوجين ثنائية الذرة متجانسة النواة. وبالتالي فإن درجات انصهار وغليان البروم تكون متوسطة بين درجتي الكلور واليود. نتيجة لزيادة الوزن الجزيئي للهالوجينات أسفل المجموعة، فإن كثافة وحرارة اندماج وتبخر البروم تكون متوسطة مرة أخرى بين كثافة الكلور واليود، على الرغم من أن جميع درجات حرارة تبخرها منخفضة إلى حد ما (مما يؤدي إلى تطاير عالي). بفضل تركيبها الجزيئي ثنائي الذرة.[22] يصبح لون الهالوجينات داكنًا مع نزول المجموعة: الفلور غاز أصفر شاحب جدًا، والكلور أصفر مخضر، والبروم سائل متطاير بني محمر ينصهر عند -7.2 درجة مئوية ويغلي عند درجة حرارة 58.8 درجة مئوية (اليود مادة صلبة سوداء لامعة) ويحدث هذا الاتجاه لأن الأطوال الموجية للضوء المرئي التي تمتصها الهالوجينات تزداد أسفل المجموعة.[22] على وجه التحديد، لون الهالوجين، مثل البروم، ينتج عن انتقال الإلكترون بين الأعلى شغلًا للترابط المضاد πg في المدار الجزيئي والمدار الجزيئي الأدنى الشاغر σu.[26] يتلاشى اللون عند درجات الحرارة المنخفضة بحيث يصبح البروم الصلب عند -195 درجة مئوية أصفر باهتًا.[22]
مثل الكلور الصلب واليود، يتبلور البروم الصلب في نظام بلوري معيني قائم، في ترتيب طبقات من جزيئات Br2. المسافة Br-Br هي 227pm (بالقرب من المسافة Br-Br الغازية البالغة 228pm) والمسافة Br···Br بين الجزيئات هي 331pm داخل الطبقة و399pm بين الطبقات (قارن الشاحنة نصف قطر دير فالس للبروم، 195 ميكرومتر). تعني هذه البنية أن البروم موصل رديء جدًا للكهرباء، مع موصلية تبلغ حوالي 5 × 10−13 Ω−1 سم −1 أقل بقليل من نقطة الانصهار، على الرغم من أن هذا أعلى من الموصلية غير القابلة للاكتشاف للكلور.[22]
عند ضغط 55 GPa (حوالي 540.000 مرة الضغط الجوي) يخضع البروم لعملية تحول من عازل إلى معدن. عند 75 GPa يتحول إلى بنية عظمية محورها الوجه. عند 100 GPa يتحول إلى شكل أحادي الذرة متمركز حول الجسم.[27]
النظائر
للبروم نظيرين مستقريين، 79Br و 81Br. هذان هما النظيران الطبيعيان الوحيدان، حيث يشكل 79Br 51% من البروم الطبيعي و81Br يشكل 49% المتبقية. كلاهما لهما دوران نووي 3/2− وبالتالي يمكن استخدامهما في الرنين المغناطيسي النووي، على الرغم من أن 81Br أكثر ملاءمة. إن التوزيع النسبي 1:1 للنظيرين في الطبيعة مفيد في تحديد المركبات التي تحتوي على البروم باستخدام التحليل الطيفي الشامل. . نظائر البروم الأخرى كلها مشعة، مع نصف عمر قصير جدًا بحيث لا يمكن أن تتواجد في الطبيعة. من بينها، أهمها 80Br (t1/2 = 17.7 min)، 80mBr (t' '1/2 = 4.421 h)، و82Br (t1/2 = 35.28 h)، والتي قد يتم إنتاجه من التنشيط النيوتروني للبروم الطبيعي.[22] النظائر المشعة الأكثر استقرارًا للبروم هي 77Br (t1/2 = 57.04 h). وضع الاضمحلال الأساسي للنظائر الأخف من 79Br هو الاصطياد الإلكتروني لنظائر السلنيوم؛ النظائر الأثقل من 81Br هي اضمحلال بيتا إلى نظائر الكريپتون؛ و80 قد يتحلل Br بأي من الوضعين إلى مستقر 80Se أو 80Kr. نظائر البروم من Br-87 والأثقل تخضع لاضمحلال بيتا مع انبعاث النيوترونات ولها أهمية عملية لأنها منتجات انشطارية؛ يُعد Br-87 الذي يبلغ عمر النصف له 55 ثانية ملحوظًا باعتباره باعث النيوترونات الأطول عمرًا.[28]
الكيمياء والمركبات
| X | XX | HX | BX3 | AlX3 | CX4 |
|---|---|---|---|---|---|
| F | 159 | 574 | 645 | 582 | 456 |
| Cl | 243 | 428 | 444 | 427 | 327 |
| Br | 193 | 363 | 368 | 360 | 272 |
| I | 151 | 294 | 272 | 285 | 239 |
يعتبر البروم وسيطا في التفاعل بين الكلور واليود، وهو من أكثر العناصر تفاعلاُ. تميل طاقات الروابط للبروم إلى أن تكون أقل من تلك الخاصة بالكلور لكنها أعلى من تلك الخاصة باليود، والبروم عامل مؤكسد أضعف من الكلور لكنه أقوى من اليود. يمكن ملاحظة ذلك من [[|جهود القطب القياسي|جهد القطب القياسي]] للأزواج X2/X− (F، +2.866 V; Cl، +1.395 V ؛ Br، +1.087 V؛ I، +0.615 V؛ عند، تقريبًا +0.3 V). غالبًا ما تؤدي المعالجة بالبروم إلى حالات أكسدة أعلى من المعالجة باليود، ولكنها تؤدي إلى حالات أكسدة أقل أو مساوية للكلورة. يميل البروم إلى التفاعل مع المركبات بما في ذلك روابط M–M أو M–H أو M–C لتكوين روابط M–Br.[26]
بروميد الهيدروجين
أبسط مركب للبروم هو بروميد الهيدروجين، HBr. يستخدم بشكل رئيسي في إنتاج البروميد الغير عضوي وبروميدات الألكيل، وكمحفز للعديد من التفاعلات في الكيمياء العضوية. صناعيًا، يُنتج بشكل أساسي عن طريق تفاعل غاز الهيدروجين مع غاز البروم عند درجة حرارة 200-400 درجة مئوية مع محفز البلاتين. ومع ذلك، يعد اختزال البروم باستخدام الفسفور الأحمر طريقة عملية أكثر لإنتاج بروميد الهيدروجين في المختبر:[29]
- 2 P + 6 H2O + 3 Br2 → 6 HBr + 2 H3PO3
- H3PO3 + H2O + Br2 → 2 HBr + H3PO4
في درجة حرارة الغرفة، يكون بروميد الهيدروجين غازًا عديم اللون، مثل جميع هاليدات الهيدروجين باستثناء فلوريد الهيدروجين، نظرًا لأن الهيدروجين لا يمكنه تكوين روابط هيدروجينية قوية مع ذرة البروم الكبيرة ذات السالبية الكهربية المعتدلة فقط؛ ومع ذلك، فإن الروابط الهيدروجينية الضعيفة موجودة في بروميد الهيدروجين البلوري الصلب عند درجات حرارة منخفضة، على غرار بنية فلوريد الهيدروجين، قبل أن يبدأ الاضطراب في الانتشار مع ارتفاع درجة الحرارة.[29] يُعرف بروميد الهيدروجين المائي بحمض الهيدروبروميك، وهو حمض قوي (pKa = −9) لأن الروابط الهيدروجينية مع البروم أضعف من أن تمنع تفككها. يشتمل نظام HBr/H2O أيضًا على العديد من الهيدرات HBr·nH2O for n = 1، 2، 3، 4، و6، وهي في الأساس أملاح أنيونات وهيدرونيومات كاتيونات البروم. يشكل حمض الهيدروبروميك ثابت غليان بنقطة غليان 124.3 درجة مئوية عند 47.63 جم HBr لكل 100 جم محلول؛ وبالتالي لا يمكن تركيز حمض الهيدروبروميك بعد هذه النقطة بالتقطير.[30]
على عكس فلوريد الهيدروجين، من الصعب العمل مع بروميد الهيدروجين السائل اللامائي كمذيب، لأن نقطة غليانه منخفضة، وله نطاق سائل صغير، وثابت العزل الكهربائي منخفض ولا ينفصل بشكل ملحوظ إلى أيونات H2Br+ وHBr−2 - الأخيرة، على أية حال، أقل استقرارًا بكثير من أيونات ثنائي الفلورايد (HF−2) بسبب الرابطة الهيدروجينية الضعيفة جدًا بين الهيدروجين والبروم، على الرغم من أن أملاحها تحتوي على كاتيونات كبيرة جدًا وضعيفة الاستقطاب مثل Cs+ وNR+4 (R = Me، Et، بوn) ربما لا يزال معزولاً. بروميد الهيدروجين اللامائي هو مذيب ضعيف، قادر فقط على إذابة المركبات الجزيئية الصغيرة مثل كلوريد النتروسيل والفينول، أو الأملاح ذات طاقات شبكية مثل هاليدات رباعي ألكيل الأمونيوم.[30]
بروميدات ثنائية أخرى

تشكل جميع العناصر الموجودة في الجدول الدوري تقريبًا بروميدات ثنائية. الاستثناءات هي بالتأكيد أقلية وتنبع في كل حالة واحد من ثلاثة أسباب: الخمول الشديد والتردد في المشاركة في التفاعلات الكيميائية (الغازات النبيلة، باستثناء الزينون في الغازات غير المستقرة للغاية. XeBr2)؛ عدم الاستقرار النووي الشديد الذي يعيق البحث الكيميائي قبل الاضمحلال والتحويل (العديد من العناصر الأثقل بعد البيزموث)؛ ولها سالبية كهربية أعلى من البروم (الأكسجين، النيتروجين، الفلور، والكلور)، بحيث تكون المركبات الثنائية الناتجة رسميًا ليست بروميدات بل أكاسيد ونيتريدات، فلوريدات أو كلوريدات البروم. (ومع ذلك، يُسمى ثلاثي بروميد النيتروجين على أنه بروميد لأنه يشبه ثلاثي هاليدات النيتروجين الأخرى.)[31]
تميل معالجة المعادن بالبروم (البرومة "Bromination" باستخدام Br2 إلى إنتاج حالات أكسدة أقل من المعالجة بالكلور باستخدام Cl2 عند توفر مجموعة متنوعة من حالات الأكسدة. يمكن تصنيع البروميدات عن طريق تفاعل العنصر أو أكسيده أو هيدروكسيده أو كربوناته مع حمض الهيدروبروميك، ثم يُجفف بدرجات حرارة مرتفعة بشكل معتدل مقترنة إما بالضغط المنخفض أو غاز بروميد الهيدروجين اللامائي. تعمل هذه الطرق بشكل أفضل عندما يكون منتج البروميد مستقرًا للتحلل المائي؛ بخلاف ذلك، تشتمل الاحتمالات على برومة تأكسدية عند درجة حرارة عالية للعنصر مع البروم أو بروميد الهيدروجين، أو برومة عند درجة حرارة عالية لأكسيد فلز أو هاليد آخر بواسطة البروم، أو بروميد فلز متطاير، رباعي بروميد الكربون، أو بروميد عضوي. على سبيل المثال، يتفاعل أكسيد النيوبيوم (الخماسي) مع رباعي بروميد الكربون عند درجة حرارة 370 درجة مئوية لتكوين بروميد النيوبيوم (الخماسي).[31] هناك طريقة أخرى وهي تبادل الهالوجين في وجود "كاشف الهالوجين" الزائد، على سبيل المثال:[31]
- FeCl3 + BBr3 (excess) → FeBr3 + BCl3
عند الرغبة في الحصول على بروميد أقل، يمكن اختزال هاليد أعلى باستخدام الهيدروجين أو المعدن كعامل اختزال، أو يمكن استخدام التحلل الحراري أو تفاعل عدم التناسب، على النحو التالي:[31]
- 3 WBr5 + Al 3 WBr4 + AlBr3
- EuBr3 + 1/2 H2 → EuBr2 + HBr
- 2 TaBr4 TaBr3 + TaBr5
معظم بروميدات المعادن التي يكون المعدن فيها في حالات أكسدة منخفضة (+1 إلى +3) تكون أيونية. تميل اللافلزات إلى تكوين بروميدات جزيئية تساهمية، كما تفعل المعادن في حالات الأكسدة العالية من +3 وما فوق. يُعرف كل من البروميدات الأيونية والتساهمية بالمعادن في حالة الأكسدة +3 (على سبيل المثال، بروميد السكانديوم في الغالب أيوني، لكن بروميد الألومنيوم ليس كذلك). بروميد الفضة غير قابل للذوبان في الماء، وبالتالي يستخدم غالبًا كاختبار نوعي للبروم.[31]
هاليدات البروميد
تشكل الهالوجينات العديد من المركبات الثنائية البين هالوجينية المغناطيسية المعاكسة ذات العناصر الكيميائية XY، XY3، XY5، وXY7 (حيث X أثقل من Y)، والبروم ليس استثناءً. يشكل البروم أحادي الفلوريد وأحادي الكلوريد، بالإضافة إلى ثلاثي الفلوريد وخماسي الفلوريد. يتم أيضًا تمييز بعض المشتقات الكاتيونية والأنيونية، مثل BrF−2، BrCl−2، BrF+2، BrF+4، وBrF+6. وبصرف النظر عن ذلك، فإن بعض الهاليدات الكاذبة معروفة أيضًا، مثل بروميد السيانوجين (BrCN)، وثيوسيانات البروم (BrSCN)، وأزيد البروم (BrN3).[32]
أحادي فلوريد البروم (BrF) ذو اللون البني الشاحب غير مستقر في درجة حرارة الغرفة، ويتغير بسرعة وبشكل لا رجعة فيه إلى البروم، وثلاثي فلوريد البروم، وخماسي فلوريد البروم. وبالتالي لا يمكن الحصول عليه نقياً. يمكن تحضيره عن طريق التفاعل المباشر للعناصر، أو عن طريق تناسب البروم مع ثلاثي فلوريد البروم عند درجات حرارة عالية.[32] أحادي كلوريد البروم (BrCl)، وهو غاز بني محمر، ينفصل بسهولة تامة بشكل عكسي إلى البروم والكلور في درجة حرارة الغرفة وبالتالي لا يمكن الحصول عليه نقيًا، على الرغم من أنه يمكن تحضيره عن طريق التفاعل المباشر العكسي لعناصره في الطور الغازي أو في رابع كلوريد الكربون.[31] يؤدي أحادي فلوريد البروم في تحويل الإيثانول بسهولة إلى المركبات أحادية البروم الأروماتية PhX (تحدث المعالجة بالبروم لـ X = Me, But , OMe, Br؛ تحدث المعالجة بالبروم فوقية عند التعطيل X = –CO2Et, –CHO, –NO2)؛ ويرجع ذلك إلى الانشطار غير المتجانس للرابطة Br-F، مما يؤدي إلى المعالجة السريعة بالبروم الكهربي بواسطة Br+.[31]
في درجة حرارة الغرفة، يكون ثلاثي فلوريد البروم (BrF3) سائلًا بلون القش. ويمكن تحضيره عن طريق فلورة البروم مباشرة في درجة حرارة الغرفة ويتم تنقيته من خلال التقطير. يتفاعل بعنف مع الماء وينفجر عند ملامسته للمواد القابلة للاشتعال، لكنه كاشف فلورة أقل قوة من ثلاثي فلوريد الكلور. يتفاعل بقوة مع البورون، الكربون، السليكون، الزرنيخ، الأنتيمون، واليود، والكبريت ليعطي الفلوريدات، وسيحول أيضًا معظم المعادن والعديد من المركبات المعدنية إلى الفلوريدات؛ على هذا النحو، يستخدم لأكسدة اليورانيوم إلى سداسي فلوريد اليورانيوم في صناعة الطاقة النووية. تميل الأكاسيد المقاومة للحرارة إلى أن تكون مفلورة جزئيًا فقط، لكن هنا تظل المشتقات KBrF4 وBrF2SbF6 تفاعلية. يعتبر ثلاثي فلوريد البروم مذيباً مؤينًا غير مائي مفيدًا، لأنه يتفكك بسهولة ليشكل BrF+2 وBrF−4 وبالتالي يوصل الكهرباء.[33]
تم تحضير خماسي فلوريد البروم (BrF5) لأول مرة عام 1930. ويُنتج على نطاق واسع عن طريق التفاعل المباشر للبروم مع الفلور الزائد عند درجات حرارة أعلى من 150 درجة مئوية، وعلى نطاق صغير. مقياس بواسطة فلورة بروميد الپوتاسيوم عند 25 درجة مئوية. كما أنه يتفاعل بعنف مع الماء وهو عامل فلورة قوي للغاية، على الرغم من أن ثلاثي فلوريد الكلور لا يزال أقوى.[34]
مركبات متعددة البروم
على الرغم من أن ثنائي البروم هو عامل مؤكسد قوي يتمتع بطاقة تأين أولى عالية، إلا أن المؤكسدات القوية جدًا مثل فلوريد پيروكسي ديسولفوريل (S2O6F2 ) يمكنه أكسدته ليشكل الكاتيون Br+2 ذو اللون الأحمر الكرزي. هناك عدد قليل من كاتيونات البروم الأخرى معروفة، وهي Br+3 البني و Br+5 البني الداكن.[35] تم أيضًا توصيف أنيون ثلاثي بروميد Br−3؛ إنه مشابه لثلاثي اليوديد.[32]
أكاسيد البروم والأحماض الأكسجينية
| E°(couple) | a(H+) = 1 (acid) |
E°(couple) | a(OH−) = 1 (base) |
|---|---|---|---|
| Br2/Br− | +1.052 | Br2/Br− | +1.065 |
| HOBr/Br− | +1.341 | BrO−/Br− | +0.760 |
| BrO−3/Br− | +1.399 | BrO−3/Br− | +0.584 |
| HOBr/Br2 | +1.604 | BrO−/Br2 | +0.455 |
| BrO−3/Br2 | +1.478 | BrO−3/Br2 | +0.485 |
| BrO−3/HOBr | +1.447 | BrO−3/BrO− | +0.492 |
| BrO−4/BrO−3 | +1.853 | BrO−4/BrO−3 | +1.025 |
لا تتميز أكاسيد البروم بشكل جيد مثل أكسيد الكلور أو أكسيد اليود، لأنها جميعها غير مستقرة إلى حد ما: كان يُعتقد في السابق أنها لا يمكن أن توجد على الإطلاق. أول أكسيد ثنائي البروم هو مادة صلبة ذات لون بني غامق، وعلى الرغم من ثباتها بشكل معقول عند -60 درجة مئوية، فإنها تتحلل عند نقطة انصهارها البالغة -17.5 درجة مئوية؛ فهو مفيد في تفاعلات البرومة[37] ويمكن تحضيره من تحلل ثاني أكسيد البروم في درجة حرارة منخفضة في الفراغ. فهو يؤكسد اليود إلى خامس أكسيد اليود والبنزين إلى 1،4-بنزوكينون؛ وفي المحاليل القلوية يعطي أنيون الهيپوكلوريت.[38]
ما يسمى "ثاني أكسيد البروم"، وهو مادة صلبة بلورية صفراء شاحبة، يمكن صياغتها بشكل أفضل على شكل بروم الپربرومات، BrOBrO3. وهو غير مستقر حرارياً فوق -40 درجة مئوية، ويتحلل بشدة إلى عناصره عند درجة حرارة 0 درجة مئوية. ثالث أكسيد ثنائي البروم، syn-BrOBrO2، معروف أيضًا؛ وهو أنهيدريد حمض الهيبوبروموس وحمض البروميك. وهي مادة صلبة بلورية برتقالية تتحلل فوق -40 درجة مئوية؛ إذا تم تسخينه بسرعة كبيرة، فإنه ينفجر حوالي 0 درجة مئوية. ومن المعروف أيضًا وجود عدد قليل من الأكاسيد الجذرية غير المستقرة، وكذلك بعض الأكسيدات ذات الخصائص السيئة، مثل خامس أكسيد ثنائي البروم، ثالث أكسيد ثلاثي البروم، وثالث أكسيد البروم.[38]
الأحماض الأكسجينية الأربعة، حمض الهيپوبروموس (HOBr)، حمض البروموس (HOBrO)، حمض البروميك (HOBrO2)، وحمض الپربروميك (HOBrO3)، دُرست بشكل أفضل بسبب ثباتها الأكبر، على الرغم من أنها تتواجد فقط في المحاليل المائية. عندما يذوب البروم في محلول مائي تحدث التفاعلات التالية:[36]
Br2 + H2O  HOBr + H+ + Br−
HOBr + H+ + Br−Kac = 7.2 × 10−9 mol2 l−2 Br2 + 2 OH−  OBr− + H2O + Br−
OBr− + H2O + Br−Kalk = 2 × 108 mol−1 l
حمض الهيپوبروموس غير مستقر نتيجة تفاعلات عدم التناسب. وبالتالي تتشكل أيونات الهيپوبروميت بشكل غير متناسبة بسهولة لتعطي البروميد والبرومات:[36]
3 BrO−  2 Br− + BrO−3
2 Br− + BrO−3K = 1015
أحماض البروموس والبروميت غير مستقرة للغاية، على الرغم من أن بروميت السترونشيوم والباريوم معروفان.[39] والأهم من ذلك هي البرومات، والتي تُحضر على نطاق صغير عن طريق أكسدة البروميد بواسطة الهيپوكلوريت المائي، وهي عوامل مؤكسدة قوية. على عكس الكلورات، التي لا تتناسب ببطء شديد مع الكلوريد والپيركلورات، فإن أنيون البرومات يكون ثابتًا بالنسبة لعدم التناسب في كل من المحاليل الحمضية والمائية. حمض البروميك هو حمض قوي. يمكن أن تتناسب البروميدات والبرومات مع البروم على النحو التالي:[39]
- BrO−3 + 5 Br− + 6 H+ → 3 Br2 + 3 H2O
كانت هناك العديد من المحاولات الفاشلة للحصول على الپيبرومات وحمض الپيبروميك، مما أدى إلى بعض التبريرات حول سبب عدم وجودهما، حتى عام 1968 عند تحضير الأنيون لأول مرة من اضمحلال بيتا من مادة 83 SeO2−4 الغير مستقرة كيميائياً. اليوم، يتم إنتاج البيبرومات عن طريق أكسدة محاليل البرومات القلوية بواسطة غاز الفلور. يتم ترسيب البرومات والفلورايد الزائد على شكل برومات الفضة وفلوريد الكالسيوم، ويمكن تنقية محلول حمض الپيربروميك. يكون أيون الپيبرومات خاملًا إلى حد ما في درجة حرارة الغرفة لكنه مؤكسد للغاية من الناحية الديناميكية الحرارية، مع وجود عوامل مؤكسدة قوية للغاية مطلوبة لإنتاجه، مثل الفلور أو ثنائي فلوريد الزينون. رابطة Br–O في BrO−4 ضعيفة إلى حد ما، وهو ما يتوافق مع المقاومة العامة لعناصر 4p الزرنيخ، السلنيوم، والبروم لتحقيق الأكسدة الجماعية. الحالة، لأنها تأتي بعد انكماش السكانديد الذي يتميز بالحماية الضعيفة التي توفرها المدارات ثلاثية الأبعاد التي لا عقد لها.[40]
مركبات البروم العضوي
مثل روابط الكربون والهالوجين الأخرى، فإن رابطة C-Br هي مجموعة وظيفية شائعة تشكل جزءًا من الكيمياء العضوية. رسميًا، يمكن اعتبار المركبات التي تحتوي على هذه المجموعة الوظيفية مشتقات عضوية لأنيون البروميد. بسبب اختلاف السالبية الكهربية بين البروم (2.96) والكربون (2.55)، فإن ذرة الكربون في رابطة C-Br تعاني من نقص الإلكترون وبالتالي محبة للإلكترونات. تفاعلية مركبات البروم العضوي تشبه تفاعلية مركب الكلور العضوي ومركب اليود العضوي لكنها تكون متوسطة. بالنسبة للعديد من التطبيقات، تمثل البروميدات العضوية حلاً وسطًا للتفاعلية والتكلفة.[41]
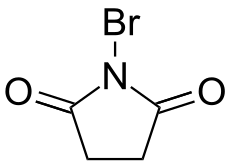
تُنتج البروميدات العضوية عادة عن طريق المعالجة بالبروم المضافة أو البديلة للسلائف العضوية الأخرى. يمكن استخدام البروم نفسه، ولكن نظرًا لسميته وتطايره، يتم عادةً استخدام كواشف البرمنة الأكثر أمانًا، مثل N-بروموسوكسينيميد. تشمل التفاعلات الرئيسية للبروميدات العضوية نزع البروم، تفاعلات گرينيار، الاقتران الاختزالي، والاستبدال المحب للنواة.[41]
تعد البروميدات العضوية أكثر الهاليدات العضوية شيوعًا في الطبيعة، على الرغم من أن تركيز البروميد لا يتجاوز 0.3% من تركيز الكلوريد في مياه البحر، وذلك بسبب سهولة أكسدة البروميد إلى ما يعادل Br+، وهو محب كهربائي قوي. . يقوم الإنزيم بروموبيروكسيديز بتحفيز هذا التفاعل.[42] تشير التقديرات إلى أن المحيطات تطلق ما بين مليون إلى مليوني طن من البروموفورم و56000 طن من البروموميثان سنويًا.[6]
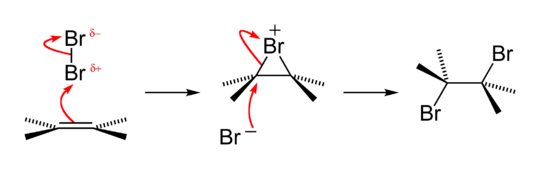
اختبار نوعي قديم لوجود مجموعة الألكين الوظيفية هو أن الألكينات تحول محاليل البروم المائية البنية إلى عديمة اللون، وتشكل البروموهيدرين مع إنتاج بعض ثنائي البروموألكان أيضًا. يمر التفاعل عبر وسيط كهربائي قصير العمر بقوة البرومونيوم. هذا مثال على تفاعل إضافة الهالوجين.[43]
التواجد والإنتاج

البروم أقل وفرة بشكل ملحوظ في القشرة الأرضية من الفلور أو الكلور، ويتكون فقط من 2.5 جزء في المليون من صخور القشرة الأرضية، وبعد ذلك فقط على شكل أملاح بروميد. وهو العنصر السادس والأربعون الأكثر وفرة في القشرة الأرضية. وهو أكثر وفرة بشكل ملحوظ في المحيطات، نتيجة الارتشاح على المدى الطويل. وهناك، يشكل 65 جزءًا في المليون، أي ما يعادل حوالي ذرة بروم واحدة لكل 660 ذرة كلور. قد تحتوي البحيرات المالحة والآبار المالحة على تركيزات أعلى من البروم: على سبيل المثال، يحتوي البحر الميت على 0.4% من أيونات البروميد.[44] ومن هذه المصادر يكون استخراج البروم مجدياً اقتصاديًا في الغالب.[45][46][47]
المصادر الرئيسية لإنتاج البروم هي إسرائيل والأردن.[48]
يتم تحرير العنصر عن طريق تبادل الهالوجين، وذلك باستخدام غاز الكلور لأكسدة Br− إلى Br2. يزال بعد ذلك بدفعة من البخار أو الهواء، ثم يتم تكثيفه وتنقيته.[49] اليوم، يُنقل البروم في براميل معدنية كبيرة السعة أو في صهاريج مبطنة بالرصاص يمكنها استيعاب مئات الكيلوجرامات أو حتى أطنان من البروم. تبلغ صناعة البروم حوالي مائة من حجم صناعة الكلور. الإنتاج المعملي غير ضروري لأن البروم متوفر تجاريًا وله مدة صلاحية طويلة.[50]
التطبيقات
تستخدم مجموعة واسعة من مركبات البروم العضوي في الصناعة. يتم تحضير بعضها من البروم والبعض الآخر من بروميد الهيدروجين، والذي يتم الحصول عليه عن طريق حرق الهيدروجين في البروم.[51]
مثبطات اللهب
تمثل مثبطات اللهب المبرومة سلعة ذات أهمية متزايدة، وتشكل أكبر استخدام تجاري للبروم. عندما تحترق المادة المبرومة، ينتج مثبط اللهب حمض الهيدروبروميك الذي يتدخل في التفاعل المتسلسل الجذري لتفاعل أكسدة النار. وتتمثل الآلية في أن جذور الهيدروجين شديدة التفاعل، وجذور الأكسجين، وجذور الهيدروكسي تتفاعل مع حمض الهيدروبروميك لتكوين جذور بروم أقل تفاعلاً (أي ذرات البروم الحرة). قد تتفاعل ذرات البروم أيضًا بشكل مباشر مع الجذور الأخرى للمساعدة في إنهاء التفاعلات المتسلسلة للجذور الحرة التي تميز الاحتراق.[52][53]
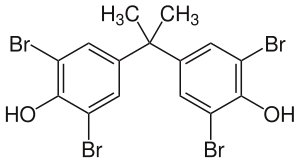
لتصنيع الپوليمرات واللدائن المبرومة، يمكن دمج المركبات المحتوية على البروم في الپوليمر أثناء الپلمرة. تتمثل إحدى الطرق في تضمين كمية صغيرة نسبيًا من المونومر المبروم أثناء عملية الپلمرة. على سبيل المثال، يمكن استخدام بروميد الڤينيل في إنتاج الپوليإثيلين، كلوريد الپوليڤينيل أو الپوليپروپلين. يمكن أيضًا إضافة جزيئات محددة عالية البرومة تشارك في عملية الپلمرة. على سبيل المثال، يمكن إضافة رباعي البروم ثنائي الفينول A إلى الپوليإسترات أو راتنجات الإيپوكسي، حيث يصبح جزءًا من الپوليمر. الإيپوكسيات المستخدمة في لوحات الدارات مطبوعة عادة ما تكون مصنوعة من الراتنجات المقاومة للهب، والمشار إليها بواسطة FR في اختصار المنتجات (FR-4 وFR-2). في بعض الحالات، يمكن إضافة المركب المحتوي على البروم بعد الپلمرة. على سبيل المثال، يمكن إضافة الإيثر ثنائي الفينيل عشاري البروم إلى الپوليمرات النهائية.[54]
عدد من مركبات الهالوميثان الغازية أو شديدة التقلب هي مركبات غير سامة وتصنع عوامل إخماد حرائق متفوقة بهذه الآلية نفسها، وتكون فعالة بشكل خاص في الأماكن المغلقة مثل الغواصات والطائرات والمركبات الفضائية. ومع ذلك، فهي باهظة الثمن وقد تم تقليص إنتاجها واستخدامها بشكل كبير بسبب تأثيرها كعوامل مستنفدة للأوزون. لم تعد تُستخدم في طفايات الحريق الروتينية، ولكنها تحتفظ باستخدامات متخصصة في تطبيقات إخماد الحرائق الآلية الفضائية والعسكرية. وهي تشمل البروموكلوروميثان (هالون 1011، CH2BrCl)، بروموكلورو ثنائي فلورو ميثان (هالون 1211، CBrClF2)، وبرومو ثلاثي فلورو ميثان (هالون 1301)، CBrF 3).[55]
استخدامات أخرى

يستخدم بروميد الفضة سواء بمفرده أو مع كلوريد الفضة ويوديد الفضة، كمكون حساس للضوء في مستحلبات التصوير الضوئي.[50]
بروميد الإيثيلين هو مادة تضاف للگازولين تحتوي على عوامل مضادة لخبط المحرك تحتوي على الرصاص. فهو يتخلص من الرصاص عن طريق تكوين بروميد الرصاص المتطاير، والذي يستنفد من المحرك. يمثل هذا التطبيق 77% من استخدام البروم عام 1966 في الولايات المتحدة. انخفض هذا التطبيق منذ السبعينيات بسبب اللوائح البيئية (انظر أدناه).[56]
الزيت النباتي المبروم (BVO)، وهو خليط معقد من الدهون الثلاثية المشتقة من النباتات والتي تم تفاعلها لتحتوي على ذرات عنصر البروم المرتبط بالجزيئات، يستخدم في المقام الأول للمساعدة في استحلاب المشروبات الغازية بنكهة الحمضيات، مما يمنعها من الفصل أثناء التوزيع.
استخدم البروموميثان السام على نطاق واسع كمبيد للآفات في تعقيم التربة والمساكن بالبخار، عن طريق طريقة الخيام. كما استخدم بروميد الإيثيلين بالمثل.[57] يتم الآن تنظيم جميع مركبات البروم العضوية المتطايرة هذه كعوامل استنفاد الأوزون. حدد پروتوكول مونتريال بشأن المواد المستنفدة لطبقة الأوزون التخلص التدريجي من المواد الكيميائية المستنفدة للأوزون بحلول عام 2005، ولم تعد مبيدات الآفات العضوية البروميدية تستخدم (في تعقيم المساكن بالبخار استبدلت بمثل هذه المبيدات الحشرية). مركبات مثل فلوريد السلفوريل، والتي لا تحتوي على مواد عضوية الكلور أو البروم التي تضر بالأوزون). قبل پروتوكول مونتريال في عام 1991 (على سبيل المثال) تم استخدام ما يقدر بنحو 35000 طن من المادة الكيميائية لمكافحة الديدانات الاسطوانية، الفطريات، الحشائش وغيرها من الأمراض المنقولة عن طريق التربة.[58][59]
في علم الأدوية، استُخدمت مركبات البروميد غير العضوية، وخاصة بروميد البوتاسيوم، بشكل متكرر كمهدئات عامة في القرن التاسع عشر وأوائل القرن العشرين. لا يزال البروميدات على شكل أملاح بسيطة تستخدم كمضادات للاختلاج في كل من الطب البيطري والطب البشري، على الرغم من أن الاستخدام الأخير يختلف من بلد إلى آخر. على سبيل المثال، لا توافق إدارة الغذاء والدواء الأمريكية على استخدام البروميد لعلاج أي مرض، وقد تمت إزالته من المنتجات المهدئة التي لا تستلزم وصفة طبية مثل برومو-سلتزر، عام 1975.[60] تشتمل مستحضرات البروم العضوية الصيدلانية المتوفرة تجاريًا على موسع الأوعية الدموية نيسيرجولين، ودواء بروتيزولام المهدئ، والعامل المضاد للسرطان پيپوبرومان، والمطهر ميربرومين. بخلاف ذلك، نادرًا ما تكون مركبات البروم العضوية مفيدة من الناحية الصيدلانية، على عكس الوضع بالنسبة لمركبات الفلور العضوية. تُنتج العديد من الأدوية كأملاح البروميد (أو ما يعادلها، هيدروبروميد)، لكن في مثل هذه الحالات، يعمل البروميد كمضاد غير ضار ليس له أي أهمية حيوية.[41]
تشمل الاستخدامات الأخرى لمركبات البروم العضوي سوائل الحفر عالية الكثافة، والأصباغ (مثل أرجوان صور والمؤشر أزرق البروموثيمول)، والمستحضرات الدوائية. يستخدم البروم نفسه، وكذلك بعض مركباته، في معالجة المياه، وهو مقدمة لمجموعة متنوعة من المركبات غير العضوية مع عدد هائل من التطبيقات (مثل بروميد الفضة للتصوير الفوتوغرافي).[50] بطاريات الزنك-البروم هي بطاريات تدفق هجينة تستخدم لدعم وتخزين الطاقة الكهربائية الثابتة؛ من النطاق المنزلي إلى النطاق الصناعي.[61]
ونظرًا لاحتوائه على خصائص مطهرة مماثلة للكلور، يمكن استخدام البروم بنفس طريقة الكلور كمطهر أو مضاد للميكروبات في تطبيقات مثل حمامات السباحة. ومع ذلك، لا يستخدم البروم عادةً في الأماكن المكشوفة لهذه التطبيقات نظرًا لكونه أغلى نسبيًا من الكلور وعدم وجود عامل استقرار لحمايته من أشعة الشمس. بالنسبة لحمامات السباحة الداخلية، يمكن أن يكون خيارًا جيدًا لأنه فعال في نطاق درجة حموضة أوسع. كما أنه أكثر استقرارًا في حمام السباحة الساخن أو حوض الاستحمام الساخن.
الدور الحيوي والسمية
| المخاطر | |
|---|---|
| ن.م.ع. مخطط تصويري |   
|
| ن.م.ع. كلمة الاشارة | خطر |
| H314, H330, H400 | |
| P260, P273, P280, P303+P361+P353, P304+P340+P310, P305+P351+P338 | |
| NFPA 704 (معيـَّن النار) | |
تشير دراسة أجريت عام 2014 إلى أن البروم (على شكل أيون البروميد) هو عامل مساعد ضروري في التخليق الحيوي للكولاجين الرابع، مما يجعله أساسياً لبنية الغشاء القاعدي وتطور الأنسجة في الحيوانات.[5] ومع ذلك، لم يتم توثيق أي أعراض أو متلازمات نقص واضحة في الثدييات.[64] في الوظائف الحيوية الأخرى، قد يكون البروم غير أساسي لكنه لا يزال مفيدًا عندما يحل محل الكلور. على سبيل المثال، في وجود پيروكسيد الهيدروجين، H2O2، الذي تكون من الخلايا الحمضية، وأيونات الكلوريد أو البروميد، يوفر پيروكسيداز الخلايا الحمضية آلية فعالة تقتل بها الخلايا الحمضية الطفيليات متعددة الخلايا (مثل الديدان الإسطوانية المسببة لداء الخيطيات) وبعض الجراثيم (مثل جرثومة السل). پيروكسيداز الخلايا الحمضية هو هالوپروكسيداز يستخدم البروميد بشكل تفضيلي على الكلوريد لهذا الغرض، ويولد الهيپوبروميت (حمض الهيپوبروموس)، على الرغم من أن استخدام الكلوريد ممكناً.[4]
يُنظر عمومًا إلى هالويسترات-ألفا على أنها شديدة التفاعل وبالتالي فهي مواد وسيطة سامة في التخليق العضوي. ومع ذلك، يبدو أن الثدييات، بما في ذلك البشر والقطط والجرذان، تقوم بتكوين آثار من بروموستر-ألفا، 2-أوكتيل 4-برومو-3-أوكسوبوتانوات، الموجود في السائل الدماغي الشوكي ويبدو أنه يلعب دورًا غير واضح حتى الآن في تحفيز حركة العين السريعة أثناء النوم.[6] يمكن للـ Neutrophil myeloperoxidase استخدام H2O2 وBr− لبرومة الديوكسي سيتيدين، مما قد يؤدي إلى طفرات الحمض النووي.[65] العضيات البحرية هي المصدر الرئيسي لمركبات البروم العضوية، وفي هذه العضيات تبين أن البروم ضروري بشكل أكبر. تم التعرف على أكثر من 1600 من مركبات بروم عضوية بحلول عام 1999. وأكثرها وفرة هو بروميد الميثيل (CH3Br)، والتي تنتج الطحالب البحرية منه ما يقدر بنحو 56000 طن سنوياً.[6] يتكون الزيت العطري لطحالب هاواي Asparagopsis Taxiformis من 80% البروموفورم.[66] تُخلق معظم مركبات البروم العضوية الموجودة في البحر بفعل إنزيم طحلبي فريد من نوعه، بروموپيروكسيداز الڤانديوم.[67]
أنيون البروميد ليس ساماً للغاية: الاستهلاك اليومي الطبيعي هو 2 إلى 8 ملليجرام.[64] ومع ذلك، فإن المستويات العالية من البروميد تؤدي إلى إضعاف غشاء الخلايا العصبية بشكل مزمن، مما يضعف بشكل تدريجي انتقال الخلايا العصبية، مما يؤدي إلى التسمم، المعروف باسم التسمم بالبروم. يبلغ عمر النصف الحيوي للبروميد من 9 إلى 12 يومًا، مما قد يؤدي إلى تراكم مفرط. قد تؤدي جرعات من 0.5 إلى 1 جرام يوميًا من البروميد إلى التسمم بالبروم. تاريخيًا، تبلغ الجرعة العلاجية بالبروميد حوالي 3 إلى 5 جرامات من البروميد، مما يفسر سبب شيوع السمية المزمنة (البروميد) في السابق. على الرغم من حدوث اضطرابات كبيرة وخطيرة في بعض الأحيان في الوظائف العصبية والنفسية والجلدية والجهاز الهضمي، إلا أن الوفاة بسبب التسمم بالبروم نادرة.[68] يحدث التسمم بالبروم بسبب تأثير سمي عصبي على المخ مما يؤدي إلى النعاس، الذهان، النوبات والهذيان.[69]
عنصر البروم سام ويسبب حروق كيميائية للحم البشري. يؤدي استنشاق غاز البروم إلى تهيج مماثل في الجهاز التنفسي، مما يسبب السعال والاختناق وضيق التنفس والوفاة إذا تم استنشاقه بكميات كبيرة بكميات كبيرة. قد يؤدي التعرض المزمن إلى التهابات الشعب الهوائية المتكررة وتدهور عام في الصحة. باعتباره عامل مؤكسد قوي، فإن البروم غير متوافق مع معظم المركبات العضوية والغير عضوية.[70] يجب توخي الحذر عند نقل البروم؛ وعادة ما يُنقل في صهاريج فولاذية مبطنة بالرصاص ومدعومة بإطارات معدنية قوية.[50] حددت إدارة الصحة والسلامة المهنية (OSHA) في الولايات المتحدة حد التعرض المسموح به (PEL) للبروم بمتوسط مرجح زمنيًا (TWA) قدره 0.1 جزء في المليون. قام المعهد الوطني للسلامة والصحة المهنية (NIOSH) بوضع حد التعرض الموصى به (REL) بقيمة TWA تبلغ 0.1 جزء في المليون وحدًا قصير المدى قدره 0.3 جزء في المليون. التعرض للبروم خطر مباشر على الحياة والصحة (IDLH) هو 3 جزء في المليون.[71] يُصنف البروم على أنه مادة شديدة الخطورة في الولايات المتحدة كما هو موضح في القسم 302 من قانون التخطيط لحالات الطوارئ حق المجتمع في المعرفة (42 U.S.C. 11002)، ويخضع لمتطلبات الإبلاغ الصارمة من قبل المنشآت التي تنتجه أو تخزنه أو تستخدمه بكميات كبيرة.[72]
المصادر
- ^ أ ب Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton, FL: CRC Press. p. 4.121. ISBN 1439855110.
- ^ Lide, D. R., ed. (2005). "Magnetic susceptibility of the elements and inorganic compounds". CRC Handbook of Chemistry and Physics (PDF) (86th ed.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. pp. E110. ISBN 0-8493-0464-4.
- ^ أ ب Mayeno AN; Curran AJ; Roberts RL; Foote CS (1989). "Eosinophils preferentially use bromide to generate halogenating agents". J. Biol. Chem. 264 (10): 5660–8. doi:10.1016/S0021-9258(18)83599-2. PMID 2538427.
- ^ أ ب McCall AS; Cummings CF; Bhave G; Vanacore R; Page-McCaw A; et al. (2014). "Bromine Is an Essential Trace Element for Assembly of Collagen IV Scaffolds in Tissue Development and Architecture". Cell. 157 (6): 1380–92. doi:10.1016/j.cell.2014.05.009. PMC 4144415. PMID 24906154.
- ^ أ ب ت ث Gribble, Gordon W. (1999). "The diversity of naturally occurring organobromine compounds". Chemical Society Reviews. 28 (5): 335–346. doi:10.1039/a900201d.
- ^ Löwig, Carl Jacob (1829). Das Brom und seine chemischen Verhältnisse [Bromine and its chemical relationships] (in الألمانية). Heidelberg: Carl Winter.
- ^ أ ب ت Balard, A. J. (1826). "Mémoire sur une substance particulière contenue dans l'eau de la mer" [Memoir on a peculiar substance contained in sea water]. Annales de Chimie et de Physique. 2nd series (in الفرنسية). 32: 337–381. Archived from the original on 5 May 2016. Retrieved 5 January 2016.
- ^ أ ب Balard, Antoine (1826). "Memoir on a peculiar Substance contained in Sea Water". Annals of Philosophy. 28: 381–387 and 411–426. Archived from the original on 17 July 2021. Retrieved 5 June 2020.
- ^ Weeks, Mary Elvira (1932). "The discovery of the elements: XVII. The halogen family". Journal of Chemical Education. 9 (11): 1915. Bibcode:1932JChEd...9.1915W. doi:10.1021/ed009p1915.
- ^ Landolt, Hans Heinrich (1890). "Nekrolog: Carl Löwig". Berichte der deutschen chemischen Gesellschaft. 23 (3): 905–909. doi:10.1002/cber.18900230395. Archived from the original on 9 February 2022. Retrieved 24 February 2022.
- ^ أ ب Harper, Douglas. "bromine". Online Etymology Dictionary.
- ^ muria. Charlton T. Lewis and Charles Short. A Latin Dictionary on Perseus Project.
- ^ Vauquelin, L. N.; Thenard, L.J.; Gay-Lussac, J.L. (1826). "Rapport sur la Mémoire de M. Balard relatif à une nouvelle Substance" [Report on a memoir by Mr. Balard regarding a new substance]. Annales de Chimie et de Physique. 2nd series (in الفرنسية). 32: 382–384. Archived from the original on 11 May 2016. Retrieved 5 January 2016.
- ^ βρῶμος. Liddell, Henry George; Scott, Robert; A Greek–English Lexicon at the Perseus Project.
- ^ On page 341 of his article, A. J. Balard (1826) "Mémoire sur une substance particulière contenue dans l'eau de la mer" [Memoir on a peculiar substance contained in sea water], Annales de Chimie et de Physique, 2nd series, vol. 32, pp. 337–381 Archived 5 مايو 2016 at the Wayback Machine, Balard states that Mr. Anglada persuaded him to name his new element brôme. However, on page 382 of the same journal – "Rapport sur la Mémoire de M. Balard relatif à une nouvelle Substance" [Report on a memoir by Mr. Balard regarding a new substance], Annales de Chimie et de Physique, series 2, vol. 32, pp. 382–384. Archived 11 مايو 2016 at the Wayback Machine – a committee of the French Academy of Sciences claimed that they had renamed the new element brôme.
- ^ Wisniak, Jaime (2004). "Antoine-Jerôme Balard. The discoverer of bromine" (PDF). Revista CENIC Ciencias Químicas. 35 (1): 35–40. Archived (PDF) from the original on 25 March 2016. Retrieved 24 February 2022.
- ^ Greenwood and Earnshaw, p. 790
- ^ Barger, M. Susan; White, William Blaine (2000). "Technological Practice of Daguerreotypy". The Daguerreotype: Nineteenth-century Technology and Modern Science. JHU Press. pp. 31–35. ISBN 978-0-8018-6458-2.
- ^ Shorter, Edward (1997). A History of Psychiatry: From the Era of the Asylum to the Age of Prozac. John Wiley and Sons. p. 200. ISBN 978-0-471-24531-5.
- ^ Corey J Hilmas; Jeffery K Smart; Benjamin A Hill (2008). "Chapter 2: History of Chemical Warfare (pdf)" (PDF). Medical Aspects of Chemical Warfare. Borden Institute. pp. 12–14. Archived from the original (PDF) on 26 August 2012. Retrieved 20 November 2016.
- ^ أ ب ت ث ج ح خ د Greenwood and Earnshaw, pp. 800–4
- ^ "Johann Wolfgang Dobereiner". Purdue University. Archived from the original on 2014-11-14. Retrieved 2008-03-08.
- ^ "A Historic Overview: Mendeleev and the Periodic Table" (PDF). NASA. Archived (PDF) from the original on 7 April 2021. Retrieved 2008-03-08.
- ^ Greenwood and Earnshaw, p. 793–4
- ^ أ ب ت Greenwood and Earnshaw, pp. 804–9
- ^ Duan, Defang; et al. (2007-09-26). "Ab initio studies of solid bromine under high pressure". Physical Review B. 76 (10): 104113. Bibcode:2007PhRvB..76j4113D. doi:10.1103/PhysRevB.76.104113.
- ^ Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties", Nuclear Physics A 729: 3–128, doi:, Bibcode: 2003NuPhA.729....3A, https://hal.archives-ouvertes.fr/in2p3-00020241/document
- ^ أ ب Greenwood and Earnshaw, pp. 809–12
- ^ أ ب Greenwood and Earnshaw, pp. 812–6
- ^ أ ب ت ث ج ح خ Greenwood and Earnshaw, pp. 821–4
- ^ أ ب ت Greenwood and Earnshaw, pp. 824–8
- ^ Greenwood and Earnshaw, pp. 828–31
- ^ Greenwood and Earnshaw, pp. 832–5
- ^ Greenwood and Earnshaw, pp 842–4
- ^ أ ب ت Greenwood and Earnshaw, pp. 853–9
- ^ Perry, Dale L.; Phillips, Sidney L. (1995), Handbook of Inorganic Compounds, CRC Press, pp. 74, ISBN 978-0-8493-8671-8, https://books.google.com/books?id=0fT4wfhF1AsC&q=%22Bromine+dioxide%22&pg=PA74, retrieved on 25 August 2015
- ^ أ ب Greenwood and Earnshaw, pp. 850–1
- ^ أ ب Greenwood and Earnshaw, pp. 862–5
- ^ Greenwood and Earnshaw, pp. 871–2
- ^ أ ب ت Ioffe, David and Kampf, Arieh (2002) "Bromine, Organic Compounds" in Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons. DOI:10.1002/0471238961.0218151325150606.a01 10.1002/0471238961.0218151325150606.a01.
- ^ Carter-Franklin, Jayme N.; Butler, Alison (2004). "Vanadium Bromoperoxidase-Catalyzed Biosynthesis of Halogenated Marine Natural Products". Journal of the American Chemical Society. 126 (46): 15060–6. doi:10.1021/ja047925p. PMID 15548002.
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart (2012). Organic Chemistry (2nd ed.). Oxford University Press. pp. 427–9. ISBN 978-0-19-927029-3.
- ^ Greenwood and Earnshaw, pp. 795–6
- ^ Tallmadge, John A.; Butt, John B.; Solomon Herman J. (1964). "Minerals From Sea Salt". Ind. Eng. Chem. 56 (7): 44–65. doi:10.1021/ie50655a008.
- ^ Oumeish, Oumeish Youssef (1996). "Climatotherapy at the Dead Sea in Jordan". Clinics in Dermatology. 14 (6): 659–664. doi:10.1016/S0738-081X(96)00101-0. PMID 8960809.
- ^ Al-Weshah, Radwan A. (2008). "The water balance of the Dead Sea: an integrated approach". Hydrological Processes. 14 (1): 145–154. Bibcode:2000HyPr...14..145A. doi:10.1002/(SICI)1099-1085(200001)14:1<145::AID-HYP916>3.0.CO;2-N.
- ^ "Major countries in worldwide bromine production from 2018 to 2022". Statista. Retrieved 26 April 2023.
- ^ "Process operations at Octel Amlwch". Octel Bromine Works. Archived from the original on 27 July 2021. Retrieved 27 July 2021.
- ^ أ ب ت ث Greenwood and Earnshaw, pp. 798–9
- ^ Mills, Jack F. (2002). "Bromine". Bromine: in Ullmann's Encyclopedia of Chemical Technology. Weinheim: Wiley-VCH Verlag. doi:10.1002/14356007.a04_391. ISBN 978-3527306732.
- ^ Green, Joseph (1996). "Mechanisms for Flame Retardancy and Smoke suppression – A Review". Journal of Fire Sciences. 14 (6): 426–442. doi:10.1177/073490419601400602. S2CID 95145090.
- ^ Kaspersma, Jelle; Doumena, Cindy; Munrob Sheilaand; Prinsa, Anne-Marie (2002). "Fire retardant mechanism of aliphatic bromine compounds in polystyrene and polypropylene". Polymer Degradation and Stability. 77 (2): 325–331. doi:10.1016/S0141-3910(02)00067-8.
- ^ Weil, Edward D.; Levchik, Sergei (2004). "A Review of Current Flame Retardant Systems for Epoxy Resins". Journal of Fire Sciences. 22: 25–40. doi:10.1177/0734904104038107. S2CID 95746728.
- ^ Siegemund, Günter; Schwertfeger, Werner; Feiring, Andrew; Smart, Bruce; Behr, Fred; Vogel, Herward; McKusick, Blaine (2002) "Fluorine Compounds, Organic" Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a11_349
- ^ Alaeea, Mehran; Ariasb, Pedro; Sjödinc, Andreas; Bergman, Åke (2003). "An overview of commercially used brominated flame retardants, their applications, their use patterns in different countries/regions and possible modes of release". Environment International. 29 (6): 683–9. doi:10.1016/S0160-4120(03)00121-1. PMID 12850087.
- ^ Lyday, Phyllis A. (May 2010). "Mineral Yearbook 2007: Bromine" (PDF). United States Geological Survey. Archived (PDF) from the original on 19 October 2017. Retrieved 2008-09-03.
- ^ Messenger, Belinda; Braun, Adolf (2000). "Alternatives to Methyl Bromide for the Control of Soil-Borne Diseases and Pests in California" (PDF). Pest Management Analysis and Planning Program. Archived from the original (PDF) on 2010-04-21. Retrieved 2008-11-17.
- ^ Decanio, Stephen J.; Norman, Catherine S. (2008). "Economics of the "Critical Use" of Methyl bromide under the Montreal Protocol". Contemporary Economic Policy. 23 (3): 376–393. doi:10.1093/cep/byi028.
- ^ Adams, Samuel Hopkins (1905). The Great American fraud. Press of the American Medical Association. Retrieved 2011-06-25.
- ^ Buecker, Brad (1998-01-07) Choose the Right Cooling Tower Chemicals. Power Engineering. Archived 10 أغسطس 2021 at the Wayback Machine Choose the Right Cooling Tower Chemicals | Power Engineering |1998
- ^ "Bromine 207888". Sigma-Aldrich. 2019-10-17. Archived from the original on 25 July 2021. Retrieved 2021-12-21.
- ^ "Msds – 207888". Sigma Aldrich. Archived from the original on 27 October 2020. Retrieved 3 October 2018.
- ^ أ ب Nielsen, Forrest H. (2000). "Possibly Essential Trace Elements". Clinical Nutrition of the Essential Trace Elements and Minerals. pp. 11–36. doi:10.1007/978-1-59259-040-7_2. ISBN 978-1-61737-090-8.
- ^ Henderson JP; Byun J; Williams MV; Mueller DM (2001). "Production of brominating intermediates by myeloperoxidase". J. Biol. Chem. 276 (11): 7867–75. doi:10.1074/jbc.M005379200. PMID 11096071.
- ^ Burreson, B. Jay; Moore, Richard E.; Roller, Peter P. (1976). "Volatile halogen compounds in the alga Asparagopsis taxiformis (Rhodophyta)". Journal of Agricultural and Food Chemistry. 24 (4): 856–861. doi:10.1021/jf60206a040.
- ^ Butler, Alison; Carter-Franklin, Jayme N. (2004). "The role of vanadium bromoperoxidase in the biosynthesis of halogenated marine natural products". Natural Product Reports. 21 (1): 180–8. doi:10.1039/b302337k. PMID 15039842. S2CID 19115256.
- ^ Olson, Kent R. (1 November 2003). Poisoning & drug overdose (4th ed.). Appleton & Lange. pp. 140–141. ISBN 978-0-8385-8172-8. Archived from the original on 24 December 2016. Retrieved 5 November 2016.
- ^ Galanter, Marc; Kleber, Herbert D. (1 July 2008). The American Psychiatric Publishing Textbook of Substance Abuse Treatment (4th ed.). United States of America: American Psychiatric Publishing Inc. p. 217. ISBN 978-1-58562-276-4. Archived from the original on 27 April 2021. Retrieved 5 November 2016.
- ^ Science Lab.com. "Material Safety Data Sheet: Bromine MSDS". sciencelab.com. Archived from the original on 15 November 2017. Retrieved 27 October 2016.
- ^ NIOSH Pocket Guide to Chemical Hazards 0064
- ^ "40 C.F.R.: Appendix A to Part 355—The List of Extremely Hazardous Substances and Their Threshold Planning Quantities" (PDF). Federal Register (1 July 2008 ed.). Government Printing Office. Archived from the original (PDF) on 25 February 2012. Retrieved 29 October 2011.
مراجع عامة
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
| Diatomic Elements | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
هيدروجين |
| |
نيتروجين |
| |
أكسجين |
| |
فلور |
|||||||||||||||||||||||||
|
كلور |
| |
بروم |
| |
يود |
| |
أستاتين |
|||||||||||||||||||||||||
- CS1 الألمانية-language sources (de)
- CS1 الفرنسية-language sources (fr)
- Articles containing Ancient Greek (to 1453)-language text
- Short description is different from Wikidata
- WikiProject Elements pages using ENGVAR
- Articles containing إنگليزية-language text
- Pages using Lang-xx templates
- Articles containing لاتينية-language text
- Articles with hatnote templates targeting a nonexistent page
- Chemical articles with unknown parameter in Chembox
- Chembox container only
- عناصر كيميائية
- هالوجينات
- بروم
- مواد كيميائية عالية الخطورة