صناعة الدواء
صناعة الدواء هي صناعة كيميائية متخصصة في صناعة الدواء، وهي تقوم بابتكار أدوية جديدة وبيعها في السوق ويكون لها حق اختراعها وابتكارها، بمعنى أنه لا يجوز لأي مصنع آخر ‘إنتاج دواء معين إلا بعد موافقة الشركة صاحبة الاختراع.[1]
تاريخها
أول صيدلية أنشت كانت في العصور الوسطى. أول مخزن دوائي إسلامي تم إنشاؤه في بغداد عام 754 وتقوم مصانع الدواء بإنتاج أدوية طبية تسمى أدوية جنيسة، وهي أدوية طبية تستخدم منذ مدة طويلة ومضت فترة احتفاظها بحق الاختراع ، وبذلك يمكن للمصانع الأخرى إنتاجها وبيعها في السوق من دون الرجوع إلى صاحب الاختراع، كما تقوم بابتكار أدوية جديدة يفوق مفعولها عادة مفعول الأدوية المعتادة وتحتفظ بحق الاختراع لها.
منتصف القرن التاسع عشر - 1945: من النباتات إلى أول العقاقير الاصطناعية
بدأت صناعة المستحضرات الصيدلانية الحديثة بعلماء محليين امتدوا من دورهم التقليدي في توزيع الأدوية النباتية مثل المورفين و الكينين إلى تصنيع الجملة في منتصف القرن التاسع عشر ، ومن الاكتشافات الناتجة عن الأبحاث التطبيقية. بدأ اكتشاف المخدرات المتعمد من النباتات بعزل ما بين 1803 و 1805 من المورفين - وكيل مسكن ومسبب للنوم - من الأفيون من قبل مساعد الصيدليات الألمانية فريدريش سيرتورنر ، الذي أطلق اسم المركب على اسم الإله اليوناني من الأحلام ، Morpheus. <المرجع> الشركات متعددة الجنسيات بما في ذلك Merck ، Hoffman-La Roche ، Burroughs-Wellcome (جزء من [[Glaxo] الآن سميث كلاين]] ، معامل Abbott ، Eli Lilly و Upjohn (جزء الآن من Pfizer) بدأت كمحلات تجارية محلية في منتصف القرن التاسع عشر . </ ref> بحلول أواخر ثمانينيات القرن التاسع عشر ، كان صانعو الأصباغ الألمان قد أتموا تنقية الفرد المركبات العضوية من القطران والمصادر المعدنية الأخرى ، كما أنشأوا طرقًا بدائية في التوليف الكيميائي العضوي.[2] أتاح تطوير الأساليب الكيميائية الصناعية للعلماء تغيير هيكل المواد الكيميائية بشكل منهجي ، كما وسّع النمو في علم الصيدلة الناشئ قدرتها على تقييم الآثار البيولوجية لهذه التغيرات الهيكلية.
ادرينالين ، بافراز ، والأمفيتامين
بحلول التسعينيات من القرن التاسع عشر ، تم اكتشاف التأثير العميق لمستخلصات الغدة الكظرية على العديد من أنواع الأنسجة المختلفة ، مما أدى إلى البحث عن آلية الإشارات الكيميائية وجهود استغلال هذه الملاحظات لتطوير عقاقير جديدة. كان لارتفاع ضغط الدم والتأثيرات المضيقة للأوعية لمستخلصات الغدة الكظرية أهمية خاصة للجراحين كعوامل مرقئي وكعلاج للصدمة ، وقام عدد من الشركات بتطوير منتجات تستند إلى مقتطفات من الغدة الكظرية تحتوي على أنواع مختلفة من المواد الفعالة. في عام 1897 ، جون أبيل من جامعة جونز هوبكنز حدد المبدأ النشط باعتباره الإيبينيفرين ، والذي عزله في حالة نجاسة مثل الكبريتات ملح. طور الكيميائي الصناعي Jōkichi Takamine فيما بعد طريقة للحصول على الإيبينيفرين في حالة نقية ، ورخص التكنولوجيا لـ Parke-Davis. قام Parke-Davis بتسويق الإيبينيفرين تحت الاسم التجاري الأدرينالين. أثبت الإيبينيفرين الذي تم حقنه أنه فعال بشكل خاص لعلاج نوبات [الربو] الحادة ، وتم بيع نسخة مستنشقة في الولايات المتحدة حتى 2011 (Primatene Mist).[3][4] بحلول عام 1929 ، تم صياغة الإيبينيفرين في جهاز استنشاق لاستخدامه في علاج احتقان الأنف. على الرغم من الفعالية العالية ، إلا أن متطلبات الحقن حدت من استخدام الإيبينيفرين [مطلوب توضيح] وتم البحث عن مشتقات نشطة شفهياً. تم التعرف على مركب مشابه هيكليا ، الايفيدرين ، (في الواقع يشبه بافراز]) من قبل الكيميائيين اليابانيين في مصنع ما هوانغ وتسويقه بواسطة ايلي ليلي كعلاج شفوي للربو. في أعقاب عمل هنري ديل وجورج بارجر في بوروز ويلكوم ، قام الكيميائي الأكاديمي جوردون أليس بتركيب الأمفيتامين واختباره في مرضى الربو في عام 1929. أثبت الدواء أنه لم يكن له سوى آثار متواضعة مضادة للربو ، لكنه أنتج إحساسات بالبهجة والخفقان. تم تطوير الأمفيتامين بواسطة Smith، Kline and French كمضاد احتقان للأنف تحت الاسم التجاري Benzedrine Inhaler. ]] ، وارتفاع المزاج في الاكتئاب وغيرها من المؤشرات النفسية. حصلت على موافقة كعلاج جديد وغير رسمي من الجمعية الطبية الأمريكية لهذه الاستخدامات في عام 1937 وظلت شائعة الاستخدام للاكتئاب حتى تطور مضادات الاكتئاب ثلاثية الحلقات في الستينيات. [4]
اكتشاف وتطوير الباربيتورات
في عام 1903 ، كشف Hermann Emil Fischer و Joseph von Mering عن اكتشافهما بأن حامض ثنائي إيثيل باربيتوريك ، الذي يتكون من تفاعل حمض ثنائي إيثيل المونيك وفوسفور أوكسي كلوريد ويوريا ، يحث على النوم في الكلاب. تم اكتشاف براءة اختراع ومرخصة لـ Bayer Pharmaceuticals ، التي قامت بتسويق المجمع تحت الاسم التجاري Veronal كوسيلة مساعدة للنوم تبدأ في عام 1904. تم إجراء تحقيقات منهجية حول تأثير التغييرات الهيكلية على الفاعلية ومدة العمل التي أدت لاكتشاف الفينوباربيتال في باير عام 1911 واكتشاف نشاطه القوي المضاد للصرع في عام 1912. كان الفينوباربيتال من بين أكثر الأدوية المستخدمة على نطاق واسع لعلاج الصرع حتى سبعينيات القرن العشرين ، وحتى 2014 ، لا يزال على قائمة منظمات الصحة العالمية بالأدوية الأساسية.[5][6]شهدت الخمسينيات والستينيات من القرن العشرين زيادة الوعي بالخصائص التي تسبب الإدمان وإساءة استعمال الباربيتورات والأمفيتامينات وأدت إلى زيادة القيود المفروضة على استخدامها وتزايد الرقابة الحكومية على الوصفات الطبية. اليوم ، يقتصر استخدام الأمفيتامين في علاج اضطراب نقص الانتباه والفينوباربيتال في علاج الصرع.[7][8]
الأنسولين
كشفت سلسلة من التجارب التي أجريت من أواخر القرن التاسع عشر إلى أوائل القرن العشرين أن مرض السكري ناجم عن عدم وجود مادة ينتجها البنكرياس عادة. في عام 1869 ، وجد [أوسكار مينكوفسكي] و جوزيف فون مرينغ أن مرض السكري يمكن أن يحدث في الكلاب عن طريق الاستئصال الجراحي للبنكرياس. في عام 1921 ، كرر الأستاذ الكندي [[فريدريك بانتنج] وطالبته تشارلز بيست هذه الدراسة ، ووجدوا أن حقن مستخلص البنكرياس عكس الأعراض الناتجة عن إزالة البنكرياس. بعد فترة وجيزة ، تم إثبات أن المستخلص يعمل في الأشخاص ، ولكن تم تأخير تطوير علاج الأنسولين كإجراء طبي روتيني بسبب الصعوبات في إنتاج المادة بكمية كافية وبنقاء متكرر. طلب الباحثون المساعدة من المتعاونين الصناعيين في Eli Lilly and Co. بناءً على تجربة الشركة في مجال تنقية المواد البيولوجية على نطاق واسع. وجد الكيميائي George B. Walden من Eli Lilly and Company أن التعديل الدقيق لدرجة الحموضة في المستخلص سمح بإنتاج درجة نقية نسبياً من الأنسولين. تحت ضغط من جامعة تورنتو وتحدي براءات الاختراع المحتملة من قبل العلماء الأكاديميين الذين طوروا بشكل مستقل طريقة تنقية مماثلة ، تم التوصل إلى اتفاق لإنتاج الأنسولين غير الحصري من قبل شركات متعددة. قبل اكتشاف العلاج بالأنسولين وتوافره على نطاق واسع ، كان العمر المتوقع لمرضى السكر بضعة أشهر فقط.[9]
الأبحاث المبكرة المضادة للعدوى: السلفارسان ، البرونتوسيل ، البنسلين واللقاحات
كان تطوير العقاقير لعلاج الأمراض المعدية محورًا رئيسيًا لجهود البحث والتطوير المبكرة ؛ في عام 1900 كانت الالتهاب الرئوي والسل والإسهال هي الأسباب الرئيسية الثلاثة للوفاة في الولايات المتحدة وتجاوز معدل الوفيات في السنة الأولى من العمر 10٪.[10][11] في عام 1911 تم تطوير أرسفينامين ، أول دواء اصطناعي مضاد للعدوى ، من قبل بول إيرليك والكيميائي ألفريد بيرثيم من معهد العلاج التجريبي في برلين. أعطيت الدواء الاسم التجاري سالفارسان .[12] مع الإشارة إلى كل من السمية العامة لـ الزرنيخ والامتصاص الانتقائي لبعض الأصباغ بواسطة البكتيريا ، افترض أنه يمكن استخدام صبغة تحتوي على الزرنيخ مع خصائص امتصاص انتقائية مماثلة لعلاج الالتهابات البكتيرية. تم إعداد أرسفينامين كجزء من حملة لتوليف سلسلة من هذه المركبات ، ووجد أنه يحمل سمية انتقائية جزئيًا. أثبت أرسفينامين أنه أول علاج فعال لمرض [الزهري] ، وهو مرض كان قبل ذلك الوقت غير قابل للشفاء وأدى بشكل لا يرحم إلى تقرح شديد في الجلد وتلف عصبي وموت.[بحاجة لمصدر] تم اتباع نهج إيرليش في تغيير الهيكل الكيميائي للمركبات الاصطناعية بشكل منهجي وقياس آثار هذه التغييرات على النشاط البيولوجي على نطاق واسع من قبل علماء الصناعة ، بما في ذلك باير العلماء جوزيف كلارر ، فريتز ميتزك ، و جيرهارد دوماجك. هذا العمل ، الذي يستند أيضًا إلى اختبار المركبات المتاحة من صناعة الأصباغ الألمانية ، أدى إلى تطوير Prontosil ، الممثل الأول للفئة سلفوناميد من المضادات الحيوية. مقارنة بأرسفينام ، كان للسلفوناميدات طيف أوسع من النشاط وكان أقل سمية بكثير ، مما يجعلها مفيدة للعدوى التي تسببها مسببات الأمراض مثل المكورات العقدية.[13]في عام 1939 ، تلقى دوماجك جائزة نوبل في الطب لهذا الاكتشاف.[14][15]ومع ذلك ، فإن الانخفاض الحاد في الوفيات الناجمة عن الأمراض المعدية التي حدثت قبل الحرب العالمية الثانية كان في المقام الأول نتيجة لتحسين تدابير الصحة العامة مثل المياه النظيفة والسكن الأقل ازدحاما ، وكان تأثير الأدوية واللقاحات المضادة للعدوى مهم بشكل رئيسي بعد الحرب العالمية الثانية.[16][17]في عام 1928 ، ألكسندر فليمنج اكتشف التأثيرات المضادة للبكتيريا لـ البنسلين ، لكن استغلاله لعلاج الأمراض التي تصيب الإنسان انتظر تطوير أساليب لإنتاجه وتنقيته على نطاق واسع. تم تطوير هذه من قبل كونسورتيوم بقيادة الولايات المتحدة وبريطانيا لشركات الأدوية خلال الحرب العالمية الثانية.[18]
حدث تقدم مبكر نحو تطوير اللقاحات طوال هذه الفترة ، بشكل أساسي في شكل أبحاث أساسية تمولها الأكاديمية والحكومية والموجهة نحو تحديد مسببات الأمراض المسؤولة عن الأمراض المعدية الشائعة. في عام 1885 قام لويس باستور و [[بيير بول إميل رو] بإنشاء أول لقاح داء الكلب. تم إنتاج أول لقاح الدفتريا في عام 1914 من مزيج من ذيفان الدفتريا و أنتيتوكسين (تم إنتاجه من مصل حيوان تلقيح) ، ولكن كانت سلامة التلقيح هامشي ولم يكن يستخدم على نطاق واسع. سجلت الولايات المتحدة 206،000 حالة من مرض الدفتيريا في عام 1921 مما أدى إلى وفاة 152020. في عام 1923 ، أدت الجهود الموازية التي بذلها غاستون رامون في معهد باستور و ألكسندر جليني في مختبرات ويلكوم للأبحاث (جزء لاحق من جلاكسو سميث كلاين) إلى اكتشاف إمكانية إنتاج لقاح أكثر أمانًا عن طريق العلاج ذيفان الخناق مع الفورمالديهايد.[19] In 1944, Maurice Hilleman of Squibb Pharmaceuticals developed the first vaccine against Japanese encephelitis.[20]ينتقل هيلمان لاحقًا إلى Merck حيث سيؤدي دورًا رئيسيًا في تطوير لقاحات ضد الحصبة ، النكاف ، جدري الماء ، روبيلا و التهاب الكبد A و التهاب الكبد B و التهاب السحايا.
المخدرات غير الآمنة والتنظيم المبكر للصناعة
[[File:Elixir Sulfanilamide.jpg|thumb|upright|In 1937 over 100 people died after ingesting a solution of the antibacterial sulfanilamide formulated in the toxic solvent diethylene glycol قبل القرن العشرين ، تم إنتاج الأدوية بشكل عام من قبل الشركات المصنعة صغيرة الحجم مع القليل من الرقابة التنظيمية على التصنيع أو مطالبات السلامة والفعالية. وبقدر وجود مثل هذه القوانين ، فإن التطبيق كان متساهلاً. في الولايات المتحدة ، حفزت زيادة تنظيم اللقاحات والأدوية البيولوجية الأخرى على تفشي مرض الكزاز والوفيات الناجمة عن توزيع لقاح الجدري الملوث ومضادات الدفتيريا المضادة للسموم..[21]يشترط قانون مراقبة البيولوجيا لعام 1902 أن تمنح الحكومة الفيدرالية الموافقة قبل التسويق لكل عقار بيولوجي ولعملية ومرفق إنتاج هذه الأدوية. وأعقب ذلك في عام 1906 قانون الأغذية والعقاقير النقية ، الذي حظر التوزيع السريع للأغذية والأدوية المغشوشة أو التي تحمل علامات تجارية خاطئة. تم اعتبار العقار خاطئًا إذا كان يحتوي على الكحول أو المورفين أو الأفيون أو الكوكايين أو أي من الأدوية الأخرى التي قد تكون خطيرة أو مسببة للإدمان ، وإذا لم تتم الإشارة إلى كميتها أو نسبتها. إن محاولات الحكومة لاستخدام القانون لمقاضاة الشركات المصنعة لقيامها بتقديم ادعاءات غير مدعومة من الفعالية قد تم تقويضها بقرار من المحكمة العليا يقصر سلطات إنفاذ الحكومة الفيدرالية على حالات المواصفات غير الصحيحة لمكونات الدواء.[22] في عام 1937 توفي أكثر من 100 شخص بعد تناول "Elixir Sulfanilamide" من إنتاج S.E. شركة ماسينجيل تينيسي. تم تصنيع المنتج في diethylene glycol ، وهو مذيب شديد السمية يستخدم الآن على نطاق واسع كمضاد للتجمد.[23]بموجب القوانين الموجودة في ذلك الوقت ، لم يكن من الممكن مقاضاة الشركة المصنعة إلا بموجب التقنية التي أطلق عليها اسم المنتج "الإكسير" ، والذي يعني حرفيًا حلاً في الإيثانول. استجابةً لهذه الحلقة ، أقر الكونجرس الأمريكي القانون الفيدرالي للأغذية والعقاقير ومستحضرات التجميل لعام 1938 ، والذي يتطلب لأول مرة مظاهرة السلامة قبل السوق قبل الدواء. يمكن بيعها ، ويحظر صراحة المطالبات العلاجية كاذبة.[24]
سنوات ما بعد الحرب ، 1945-1970
مزيد من التقدم في الأبحاث المضادة للعدوى
شهدت أعقاب الحرب العالمية الثانية انفجارًا في اكتشاف فئات جديدة من الأدوية المضادة للبكتيريا[25] including the cephalosporins (developed by Eli Lilly based on the seminal work of Giuseppe Brotzu and Edward Abraham),[26][27] streptomycin (discovered during a Merck-funded research program in Selman Waksman's laboratory[28]), the tetracyclines[29](اكتشف في معامل ليدرل ، والآن جزء من فايزر) ، الإريثروميسين (اكتشف في إيلي ليلي وشركاه)[30] وتمديدها إلى مجموعة واسعة من مسببات الأمراض البكتيرية. أصبح الستربتومايسين ، الذي اكتشف خلال برنامج بحثي ممول من شركة ميرك في مختبر سلمان واكسمان في روتجرز عام 1943 ، أول علاج فعال لمرض السل. في وقت اكتشافه ، كانت المصحات الخاصة بعزل المصابين بالسل سمة في كل مكان في المدن في البلدان المتقدمة ، حيث يموت 50 ٪ في غضون 5 سنوات من القبول.[28][31]حاول تقرير لجنة التجارة الفيدرالية الصادر عام 1958 تحديد تأثير تطور المضادات الحيوية على الصحة العامة الأمريكية. وجد التقرير أنه خلال الفترة 1946-1955 ، كان هناك انخفاض بنسبة 42 ٪ في حدوث الأمراض التي كانت المضادات الحيوية فعالة فيها ونسبة 20 ٪ فقط في تلك التي لم تكن المضادات الحيوية فعالة. وخلص التقرير إلى أنه "يبدو أن استخدام المضادات الحيوية والتشخيص المبكر وعوامل أخرى قد حد من انتشار الوباء وبالتالي عدد هذه الأمراض التي حدثت". وبحثت الدراسة كذلك معدلات الوفيات الناجمة عن ثمانية أمراض شائعة قدمت المضادات الحيوية علاجًا فعالًا لها (الزهري والسل والدرنة والحمى القرمزية والسعال الديكي والتهابات المكورات السحائية والالتهاب الرئوي) ، ووجدت انخفاضًا بنسبة 56٪ خلال نفس الفترة[32] وكان من بين هذه الانخفاضات بنسبة 75 ٪ في الوفيات بسبب السل. [33] [[File:Measles US 1944-2007 inset.png| alt=Measles cases 1944-1964 follow a highly variable epidemic pattern, with 150,000-850,000 cases per year. A sharp decline followed introduction of the vaccine in 1963, with fewer than 25,000 cases reported in 1968. Outbreaks around 1971 and 1977 gave 75,000 and 57,000 cases, respectively. Cases were stable at a few thousand per year until an outbreak of 28,000 in 1990. Cases declined from a few hundred per year in the early 1990s to a few dozen in the 2000s. | thumb | Measles cases reported in the United States before and after introduction of the vaccine.]]
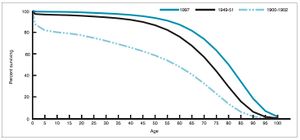
خلال الأعوام 1940-1955 ، تسارع معدل الانخفاض في الولايات المتحدة معدل الوفيات من 2 ٪ سنويًا إلى 8 ٪ سنويًا ، ثم عاد إلى المعدل التاريخي البالغ 2 ٪ سنويًا. يعزى الانخفاض الحاد في سنوات ما بعد الحرب المباشرة إلى التطور السريع للعلاجات واللقاحات الجديدة للأمراض المعدية التي حدثت خلال هذه السنوات.[16][17]استمر تطور اللقاح في التسارع ، وكان من أبرز الإنجازات التي تحققت خلال هذه الفترة تطوير جوناس سالك عام 1954 لقاح شلل الأطفال في ظل تمويل من المؤسسة الوطنية غير الربحية لشلل الأطفال. لم تكن براءة اختراع عملية اللقاح أبدًا ، ولكن تم منحها بدلاً من ذلك لشركات الأدوية لتصنيعها كعقار منخفض التكلفة دواء عام . في عام 1960 ، حددت موريس هيلمان من Merck Sharp & Dohme فيروس SV40 ، الذي ظهر لاحقًا أنه يسبب الأورام في العديد من أنواع الثدييات. وقد تقرر فيما بعد أن SV40 كان موجودًا كملوث في لقاحات شلل الأطفال التي كانت تدار إلى 90٪ من الأطفال في الولايات المتحدة..[34][35] يبدو أن التلوث قد نشأ في مخزون الخلية الأصلي وفي أنسجة القرود المستخدمة في الإنتاج. في عام 2004 ، أعلن معهد الولايات المتحدة للسرطان أنه قد خلص إلى أن SV40 لا يرتبط بالسرطان لدى الناس.[36]وتشمل اللقاحات الجديدة الأخرى البارزة في تلك الفترة تلك الخاصة بالحصبة (1962 ، وجون فرانكلين إيندرز من المركز الطبي للأطفال في بوسطن ، ثم صقلها موريس هيلمان في شركة ميرك) ، وروبيلا (1969 ، وهيليمان ، وميرك) والنكاف (1967 ، وهيلمان ، وميرك)[37]The United States incidences of rubella, congenital rubella syndrome, measles, and mumps all fell by >95% in the immediate aftermath of widespread vaccination.[38] أول 20 عامًا من ترخيص تلقيح الحصبة في الولايات المتحدة منعت ما يقدر بنحو 52 مليون حالة من حالات المرض ، و 17400 حالة من التخلف العقلي ، و 5،200 حالة وفاة.[39]
تطوير وتسويق الأدوية الخافضة للضغط
ارتفاع ضغط الدم هو عامل خطر لتصلب الشرايين ،[40]heart failure,[41] coronary artery disease,[42][43] stroke,[44] renal disease,[45][46] and peripheral arterial disease,[47][48] and is the most important risk factor for cardiovascular morbidity and mortality, in industrialized countries.[49] Prior to 1940 approximately 23% of all deaths among persons over age 50 were attributed to hypertension. Severe cases of hypertension were treated by surgery.[50] شملت التطورات المبكرة في مجال علاج ارتفاع ضغط الدم عوامل انسداد الجهاز العصبي الوبائي أيوني الأمونيوم ، ولكن هذه المركبات لم تستخدم على نطاق واسع بسبب آثارها الجانبية الشديدة ، لأن الآثار الصحية الطويلة الأجل لارتفاع ضغط الدم لم تتحدد بعد ، ولأن كان يجب أن تدار عن طريق الحقن. في عام 1952 ، اكتشف الباحثون في Ciba أول موسع للأوعية الفموية ، .[51] كان أحد أوجه القصور الرئيسية في حيد الهيدرالازين أنه فقد فعاليته مع مرور الوقت (tachyphylaxis). في منتصف الخمسينيات من القرن العشرين اكتشف كل من كارل هـ. باير ، وجيمس سبراغ ، وجون إ. باير ، وفريدريك سي نوفيللو من ميرك وشركاه كلوروثيازيد ، والذي لا يزال الأكثر ارتفاعًا في ضغط الدم. المخدرات اليوم.[52] ارتبط هذا التطور بانخفاض كبير في معدل الوفيات بين المصابين بارتفاع ضغط الدم.[53]تم الاعتراف بالمخترعين من قبل الصحة العامة جائزة Lasker في عام 1975 ل "إنقاذ الآلاف من الأرواح وتخفيف معاناة الملايين من ضحايا ارتفاع ضغط الدم".[54]
خلصت مراجعة كوكرين لعام 2009 إلى أن أدوية ثيازيد الخافضة للضغط تقلل من خطر الوفاة ( RR 0.89) والسكتة الدماغية (RR 0.63) وأمراض القلب التاجية (RR 0.84) وأحداث القلب والأوعية الدموية (RR 0.70) في الأشخاص الذين يعانون من ضغط دم مرتفع.[55][needs update] In the ensuring years other classes of antihypertensive drug were developed and found wide acceptance in combination therapy, including loop diuretics (Lasix/furosemide, Hoechst Pharmaceuticals, 1963),[56] beta blockers (ICI Pharmaceuticals, 1964)[57] ACE inhibitors, and angiotensin receptor blockers. ACE inhibitors reduce the risk of new onset kidney disease [RR 0.71] and death [RR 0.84] in diabetic patients, irrespective of whether they have hypertension.[58]
وسائل منع الحمل عن طريق الفم
قبل الحرب العالمية الثانية ، كان منع النسل محظورًا في العديد من البلدان ، وفي الولايات المتحدة حتى مناقشة أساليب منع الحمل أدت أحيانًا إلى مقاضاة بموجب قوانين كومستوك. يرتبط تاريخ تطوير وسائل منع الحمل عن طريق الفم ارتباطًا وثيقًا بـ حركة تحديد النسل وجهود الناشطين مارغريت سانجر ، ماري دينيت ، و [ [إيما جولدمان]]. استنادًا إلى الأبحاث الأساسية التي أجراها غريغوري بينكوس والأساليب الاصطناعية للبروجسترون التي طورها كارل جيراسي في سينكتيكس و فرانك كولتون في G.D. Searle & Co. ، وهي أول وسيلة لمنع الحمل عن طريق الفم ، Enovid ، تم تطويرها بواسطة E.D. Searle and Co. ووافقت عليها إدارة الأغذية والعقاقير في عام 1960. تضمنت الصيغة الأصلية جرعات زائدة من الهرمونات وتسببت في آثار جانبية حادة. ومع ذلك ، بحلول عام 1962 ، كانت 1.2 مليون امرأة أمريكية على حبوب منع الحمل ، وبحلول عام 1965 ارتفع العدد إلى 6.5 مليون.[59][60][61][62] The availability of a convenient form of temporary contraceptive led to dramatic changes in social mores including expanding the range of lifestyle options available to women, reducing the reliance of women on men for contraceptive practice, encouraging the delay of marriage, and increasing pre-marital co-habitation.[63]
Thalidomide وتعديلات Kefauver-Harris
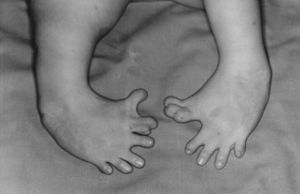
في الولايات المتحدة ، ظهرت دفعة لمراجعات قانون FD&C من جلسات الاستماع في الكونجرس بقيادة السناتور Estes Kefauver من ولاية تينيسي في عام 1959. شملت جلسات الاستماع مجموعة واسعة من قضايا السياسة العامة ، بما في ذلك انتهاكات الإعلانات ، وفعالية الأدوية المشكوك فيها ، و الحاجة إلى تنظيم أكبر لهذه الصناعة. في حين تم الإشارة إلى زخم التشريع الجديد مؤقتًا في ظل نقاش مطول ، ظهرت مأساة جديدة أكدت الحاجة إلى تنظيم أكثر شمولًا ووفرت القوة الدافعة لإصدار قوانين جديدة. في 12 سبتمبر 1960 ، قدمت شركة مرخصة أمريكية ، وهي شركة William S. Merrell التابعة لشركة Cincinnati ، طلبًا جديدًا للدواء لصالح Kevadon (thalidomide) ، وهو مهدئ تم تسويقه في أوروبا منذ عام 1956. المسؤول الطبي في FDA مراجعة المجمع ، فرانسيس كيلسي ، يعتقد أن البيانات الداعمة لسلامة تاليدوميد غير كاملة. استمرت الشركة في الضغط على كيلسي وإدارة الأغذية والعقاقير (FDA) للموافقة على الطلب حتى نوفمبر 1961 ، عندما تم سحب الدواء من السوق الألمانية بسبب ارتباطه بتشوهات خلقية خطيرة. عانى عدة آلاف من المواليد الجدد في أوروبا وفي أماكن أخرى من آثار [المسبب للمرض] من الثاليدومايد. من دون موافقة إدارة الأغذية والعقاقير ، قامت الشركة بتوزيع Kevadon على أكثر من 1000 طبيب هناك تحت ستار الاستخدام البحثي. تلقى أكثر من 20،000 أمريكي تاليدوميد في هذه "الدراسة" ، بما في ذلك 624 مريضا حاملا ، وحوالي 17 حديثي الولادة المعروف عانى من آثار المخدرات.[بحاجة لمصدر]
أعادت مأساة thalidomide إحياء مشروع قانون Kefauver لتعزيز تنظيم العقاقير التي توقفت في الكونغرس ، وأصبح Kefauver-Harris Amendment قانونًا في 10 أكتوبر 1962. وعلى الشركات المصنعة أن تثبت لـ FDA أن عقاقيرها كانت فعالة كذلك آمنة قبل أن يتمكنوا من الذهاب في السوق الأمريكية. حصلت إدارة الأغذية والعقاقير (FDA) على سلطة تنظيم الإعلان عن العقاقير الطبية وتأسيس ممارسات التصنيع الجيدة. يشترط القانون أن تكون جميع الأدوية التي أدخلت بين عامي 1938 و 1962 فعالة. أظهرت دراسة تعاونية أجرتها FDA - الأكاديمية الوطنية للعلوم أن ما يقرب من 40 في المائة من هذه المنتجات لم تكن فعالة. بدأت دراسة شاملة مماثلة للمنتجات التي تباع بدون وصفة طبية بعد عشر سنوات.[64]
1970-1980s
الستاتين
في عام 1971 ، حدد أكيرا إندو ، عالم الكيمياء الحيوية الياباني الذي يعمل لصالح شركة الأدوية سانكيو ، الميفاستاتين (ML-236B) ، وهو جزيء أنتجته الفطريات Penicillium citrinum ، كمثبط لإنزيم HMG-CoA المختزل ، وهو إنزيم مهم يستخدمه الجسم في إنتاج الكوليسترول. التجارب على الحيوانات أظهرت تأثيرًا مثبطًا جيدًا كما هو الحال في التجارب السريرية ، ومع ذلك وجدت دراسة طويلة المدى أجريت على الكلاب آثارًا سامة بجرعات أعلى ونتيجة لذلك كان يعتقد أن الميفاستاتين شديد السمية للإنسان استعمال. لم يتم تسويق ميفاستاتين أبدًا بسبب آثاره الضارة على الأورام وتدهور العضلات وأحيانًا الموت في الكلاب المختبرية. [[P. كان روي فاجيلوس] ، كبير العلماء والرئيس التنفيذي لاحقًا لـ Merck & Co ، مهتمًا ، وقام بعدة رحلات إلى اليابان بدءًا من عام 1975. بحلول عام 1978 ، كانت Merck قد عزلت لوفاستاتين (ميفينولين ، MK803) عن الفطريات Aspergillus terreus ، تم تسويقها لأول مرة في عام 1987 باسم Mevacor .[65][66][67] في أبريل 1994 ، تم الإعلان عن نتائج دراسة رعتها شركة ميرك ، دراسة بقاء الاسكندنافية سيمفاستاتين. قام الباحثون باختبار سيمفاستاتين ، الذي تم بيعه لاحقًا من قِبل شركة ميرك باسم زوكور ، على 4444 مريضًا يعانون من ارتفاع الكوليسترول في الدم وأمراض القلب. بعد خمس سنوات ، خلصت الدراسة إلى أن المرضى شهدوا انخفاضًا بنسبة 35٪ في نسبة الكوليسترول في الدم لديهم ، كما تقلصت فرصهم في الوفاة بأزمة قلبية بنسبة 42٪.[68] In 1995, Zocor and Mevacor both made Merck over US$1 billion. Endo was awarded the 2006 Japan Prize, and the Lasker-DeBakey Clinical Medical Research Award in 2008. For his "pioneering research into a new class of molecules" for "lowering cholesterol,"قالب:Fragment[69][70]
البحث والتطوير
"اكتشاف المخدرات" هي العملية التي يتم من خلالها اكتشاف أو تصميم المخدرات المحتملة. في الماضي ، تم اكتشاف معظم الأدوية إما عن طريق عزل العنصر النشط عن العلاجات التقليدية أو عن طريق اكتشاف الصدفة. يركز الحديث التكنولوجيا الحيوية غالبًا على فهم المسار الأيضي المرتبط بالحالة المرض أو الممرض ، ومعالجة هذه المسارات باستخدام البيولوجيا الجزيئية أو [[الكيمياء الحيوية] ]. عادة ما يتم إجراء الكثير من اكتشاف الأدوية في المراحل المبكرة من قبل الجامعات والمؤسسات البحثية. يشير مصطلح "تطوير العقاقير" إلى الأنشطة التي يتم تنفيذها بعد تحديد المركب كدواء محتمل من أجل إثبات ملاءمته كدواء. أهداف تطوير الدواء هي تحديد الصيغة و الجرعات ، وكذلك تحديد السلامة. تتضمن الأبحاث في هذه المناطق عمومًا مزيجًا من الدراسات "في المختبر" ، و "في الجسم الحي" ، و التجارب السريرية. تكلفة تطوير المرحلة المتأخرة تعني أن ذلك يتم عادة بواسطة شركات الأدوية الكبرى.[71] غالبًا ما تعرض الشركات الكبيرة متعددة الجنسيات التكامل الرأسي ، وتشارك في مجموعة واسعة من اكتشاف الأدوية وتطويرها ، ومراقبة التصنيع والجودة ، والتسويق ، والمبيعات ، والتوزيع. المنظمات الأصغر ، من ناحية أخرى ، غالباً ما تركز على جانب محدد مثل اكتشاف مرشحي المخدرات أو تطوير المستحضرات. في كثير من الأحيان ، يتم تشكيل اتفاقيات تعاون بين المنظمات البحثية وشركات الأدوية الكبيرة لاستكشاف إمكانات المواد الدوائية الجديدة. في الآونة الأخيرة ، يعتمد العديد من الجنسيات بشكل متزايد على [[منظمة الأبحاث التعاقدية] لإدارة تطوير الأدوية.[72]
تكلفة الابتكار
المخدرات اكتشاف وتطوير غالية جدا. من بين جميع المركبات التي تم فحصها لاستخدامها في البشر ، هناك جزء صغير فقط في نهاية المطاف المعتمدة في معظم الدول من قبل المؤسسات الطبية أو المجالس الطبية المعينة من قبل الحكومة ، والتي يتعين عليها الموافقة على دواء جديد قبل تسويقه في تلك البلدان. في عام 2010 ، تمت الموافقة على 18 NMEs (كيانات جزيئية جديدة) وثلاثة البيولوجيات من قبل إدارة الأغذية والعقاقير ، أو 21 في المجموع ، أي أقل من 26 في عام 2009 و 24 في عام 2008. من ناحية أخرى ، كان هناك 18 موافقة فقط في إجمالي في عام 2007 و 22 مرة في عام 2006. منذ عام 2001 ، بلغ متوسط مركز تقييم الأدوية والبحوث 22.9 الموافقات سنويا.[73]لا تأتي هذه الموافقة إلا بعد الاستثمار الكبير في تطوير ما قبل السريرية و تجربة سريرية ، بالإضافة إلى الالتزام المستمر مراقبة السلامة. غالبًا ما تتحمل الأدوية التي تفشل جزئيًا في هذه العملية تكاليف كبيرة ، بينما لا تحقق إيرادات في المقابل. إذا تم أخذ تكلفة هذه الأدوية الفاشلة في الاعتبار ، فقد قدرت تكلفة تطوير دواء جديد ناجح (كيان كيميائي جديد أو NCE) بحوالي 1.3 مليار دولار أمريكي[74](not including marketing expenses).أورد الأستاذان لايت و Lexchin في عام 2012 ، أن معدل الموافقة على الأدوية الجديدة كان معدل ثابت نسبيا من 15 إلى 25 لعقود.[75] وصلت البحوث والاستثمارات على مستوى الصناعة إلى مستوى قياسي بلغ 65.3 مليار دولار في عام 2009.[76] While the cost of research in the U.S. was about $34.2 billion between 1995 and 2010, revenues rose faster (revenues rose by $200.4 billion in that time).[75] أفادت دراسة أجرتها شركة الاستشارات Bain & Company أن تكلفة اكتشاف وتطوير وإطلاق (التي تؤخذ في الاعتبار في مصاريف التسويق وغيرها من الأعمال) دواء جديد (إلى جانب العقاقير المحتملة التي تفشل) قد ارتفعت أكثر من خمسة السنة إلى ما يقرب من 1.7 مليار دولار في عام 2003.[77] According to Forbes, by 2010 development costs were between $4 billion to $11 billion per drug.[78] تأخذ بعض هذه التقديرات في الاعتبار تكلفة الفرصة البديلة لاستثمار رأس المال قبل سنوات عديدة من تحقيق الإيرادات (انظر القيمة الزمنية للنقود). نظرًا للوقت الطويل للغاية اللازم لاكتشاف الأدوية وتطويرها والموافقة عليها ، يمكن أن تتراكم هذه التكاليف إلى ما يقرب من نصف إجمالي النفقات. من النتائج المباشرة في سلسلة قيمة صناعة الأدوية أن الشركات متعددة الجنسيات الدوائية تميل إلى الاستعانة بمصادر خارجية بشكل متزايد للمخاطر المتعلقة بالبحوث الأساسية ، والتي تعيد تشكيل النظام الإيكولوجي للصناعة إلى حد ما مع شركات التكنولوجيا الحيوية تلعب دوراً متزايد الأهمية ، ويتم إعادة تحديد الاستراتيجيات الشاملة وفقاً لذلك.[79] بعض الأدوية المعتمدة ، مثل تلك التي تعتمد على إعادة صياغة مكون حالي العنصر النشط (يشار إليه أيضًا باسم امتدادات الخط) هي أقل تكلفة بكثير لتطويرها.
الخلافات
نظرًا للاتهامات والنتائج المتكررة التي تشير إلى أن بعض التجارب السريرية التي تجريها أو تمولها شركات الأدوية قد تبلغ عن نتائج إيجابية فقط عن الدواء المفضل ، فقد تم النظر في هذه الصناعة عن كثب من قبل مجموعات مستقلة ووكالات حكومية.[80] استجابةً للحالات المحددة التي لم تنشر فيها بيانات غير مواتية من الأبحاث التي ترعاها شركة الأدوية ، نشر Research Pharmaceutical and Manufacturers of America إرشادات جديدة تحث الشركات على الإبلاغ عن جميع النتائج والحد من المشاركة المالية في شركات الأدوية للباحثين.[81] US congress signed into law a bill which requires phase II and phase III clinical trials to be registered by the sponsor on the clinicaltrials.gov website run by the NIH.[82] غالبًا ما يبحث باحثو الأدوية الذين لا تستخدمهم شركات الأدوية بشكل مباشر عن الشركات للحصول على المنح ، وغالبًا ما تبحث الشركات عن الباحثين في الدراسات التي تجعل منتجاتهم تبدو مواتية. تتم مكافأة الباحثين الذين ترعاهم شركات الأدوية ، على سبيل المثال بدعم تكاليف المؤتمرات / الندوات. قد تكون نصوص المحاضرات وحتى مقالات المجلات التي قدمها الباحثون الأكاديميون "مكتوبة بالأشباح" من قبل شركات الأدوية.[83] توصلت دراسة أجرتها ProPublica إلى أن 21 طبيباً على الأقل قد حصلوا على أكثر من 500000 دولار مقابل الخطب والاستشارات من قبل الشركات المصنعة للأدوية منذ عام 2009 ، حيث يعمل نصف كبار العاملين في الطب النفسي ، وحوالي 2 مليار دولار في المجموع دفعت للأطباء مقابل هذه الخدمات. دفعت AstraZeneca و Johnson & Johnson و Eli Lilly مليارات الدولارات في التسويات الفيدرالية بسبب مزاعم بأنهم دفعوا للأطباء للترويج للعقاقير للاستخدامات غير الموافق عليها. ومنذ ذلك الحين شددت بعض كليات الطب البارزة قواعد قبول أعضاء هيئة التدريس لهذه المدفوعات من قبل شركات الأدوية.[84] على النقيض من وجهة النظر هذه ، أكد مقال وافتتاحيات مرتبطة به في New England Journal of Medicine في مايو 2015 على أهمية التفاعلات بين الأطباء والصناعات الدوائية لتطوير علاجات جديدة ، وجادلوا بأن الغضب الأخلاقي بسبب سوء الصناعة قادت الكثيرين بشكل غير مبرر إلى المبالغة في تقدير المشاكل الناجمة عن تضارب المصالح المالية. أشار المقال إلى أن منظمات الرعاية الصحية الكبرى مثل المركز الوطني لتقدم علوم الترجمة في المعاهد الوطنية للصحة ، ومجلس المستشارين للرئيس المعني بالعلوم والتكنولوجيا ، والمنتدى الاقتصادي العالمي ، ومؤسسة غيتس ، ومؤسسة ويلكوم ترست ، والغذاء والدواء شجعت الإدارة تفاعلات أكبر بين الأطباء والصناعة من أجل تحقيق فوائد أكبر للمرضى.[85][86]
موافقة المنتج
في الولايات المتحدة ، يجب اعتماد المنتجات الصيدلانية الجديدة من قبل إدارة الغذاء والدواء (FDA) باعتبارها آمنة وفعالة على حد سواء. تتضمن هذه العملية عمومًا تقديم دواء استقصائي جديد للدواء يحتوي على بيانات ما قبل سريرية كافية لدعم مواصلة التجارب على البشر. بعد موافقة IND ، يمكن إجراء ثلاث مراحل من التجارب السريرية البشرية الأكبر تدريجياً. تدرس المرحلة الأولى عمومًا السمية باستخدام متطوعين أصحاء. يمكن أن تشمل المرحلة الثانية الدوائية و الجرعات في المرضى ، والمرحلة الثالثة هي دراسة كبيرة جدا للفعالية في السكان المريض المقصود. بعد الانتهاء بنجاح من اختبار المرحلة الثالثة ، يتم تقديم تطبيق دواء جديد إلى إدارة الأغذية والعقاقير. تقوم إدارة الأغذية والأدوية FDA بمراجعة البيانات وإذا كان المنتج ينظر إليه على أنه تقييم إيجابي لمخاطر المنافع ، يتم منح الموافقة على تسويق المنتج في الولايات المتحدة.[87] غالبًا ما تكون هناك حاجة أيضًا إلى مرحلة رابعة من المراقبة بعد الموافقة نظرًا لحقيقة أنه حتى أكبر التجارب السريرية لا يمكنها التنبؤ بفعالية بانتشار الآثار الجانبية النادرة. مراقبة ما بعد التسويق يضمن أنه بعد التسويق يتم مراقبة سلامة الدواء عن كثب. في بعض الحالات ، قد تحتاج الإشارة إلى قصرها على مجموعات معينة من المرضى ، وفي حالات أخرى يتم سحب المادة من السوق تمامًا.
توفر إدارة الأغذية والعقاقير (FDA) معلومات حول الأدوية المعتمدة في موقع Orange Book.[88] في المملكة المتحدة ، هيئة تنظيم الأدوية ومنتجات الرعاية الصحية توافق على الأدوية للاستخدام ، على الرغم من أن التقييم يتم بواسطة وكالة الأدوية الأوروبية ، وهي وكالة تابعة لـ الاتحاد الأوروبي ومقرها لندن. عادةً ما تأتي الموافقة في المملكة المتحدة ودول أوروبية أخرى بعد موافقة واحدة في الولايات المتحدة الأمريكية. ومن ثم ، المعهد الوطني للتميز في الرعاية الصحية (NICE) ، لإنكلترا وويلز ، هو الذي يقرر ما إذا كان الخدمة الصحية الوطنية (NHS) وكيف سيسمح (بمعنى الدفع مقابل) استخدامها. National National Formulary هو الدليل الأساسي للصيادلة والأطباء. في العديد من الدول الغربية غير الأمريكية ، تطورت "العقبة الرابعة" لـ تحليل فعالية التكلفة قبل تقديم التقنيات الجديدة. يركز هذا على كفاءة (من حيث التكلفة لكل QALY) من التقنيات المعنية بدلاً من كفاءتها. في إنجلترا وويلز ، تقرر NICE ما إذا كانت الأدوية والتكنولوجيات ستتاح من قبل NHS وفي أي ظرف من الظروف ، في حين توجد ترتيبات مماثلة مع اتحاد الأدوية الإسكتلندية في اسكتلندا ، و اللجنة الاستشارية للفوائد الدوائية في أستراليا . يجب أن يتجاوز المنتج عتبة الفعالية من حيث التكلفة إذا كان سيتم اعتماده. يجب أن تمثل العلاجات "القيمة مقابل المال" وفائدة صافية للمجتمع.
المخدرات اليتيمة
هناك قواعد خاصة لبعض الأمراض النادرة ("أمراض الأيتام") في العديد من المناطق التنظيمية الرئيسية للأدوية. على سبيل المثال ، تخضع الأمراض التي تشمل أقل من 200000 مريض في الولايات المتحدة ، أو عدد أكبر من السكان في ظروف معينة لقانون الأيتام المخدرات.[89]نظرًا لأن البحوث الطبية وتطوير العقاقير لعلاج هذه الأمراض غير مواتية من الناحية المالية ، فإن الشركات التي تفعل ذلك تُكافأ بتخفيض الضرائب وإعفائها من الرسوم وحصريتها في السوق لفترة محدودة (سبع سنوات) ، بغض النظر عما إذا كان الدواء محميًا بواسطة براءات الاختراع.
المبيعات العالمية
في عام 2011، تجاوز الإنفاق العالمي على الأدوية بوصفة طبية 954 مليار دولار ، حتى مع تباطؤ النمو إلى حد ما في أوروبا وأمريكا الشمالية. تستحوذ الولايات المتحدة على أكثر من ثلث سوق الأدوية العالمي، حيث بلغت المبيعات السنوية 340 مليار دولار يليها الاتحاد الأوروبي واليابان.[90] Emerging markets such as China, Russia, South Korea and Mexico outpaced that market, growing a huge 81 percent.[91][92] بلغ إجمالي مبيعات الأدوية العشرة الأولى مبيعًا في عام 2013 ما قيمته 75.6 مليار دولار ، مع كون العقار المضاد للالتهابات هوميرا أكثر الأدوية مبيعًا في جميع أنحاء العالم حيث بلغ مبيعاته 10.7 مليار دولار. أما ثاني وثالث الأكثر مبيعاً فكانا Enbrel و Remicade ، على التوالي.[93] The top three best-selling drugs in the United States in 2013 were Abilify ($6.3 billion,) Nexium ($6 billion) and Humira ($5.4 billion).[94] كان الدواء الأكثر مبيعًا على الإطلاق ، Lipitor ، حيث بلغ متوسطه 13 مليار دولار سنويًا ، وحقق 141 مليار دولار إجماليًا على مدار حياته قبل انتهاء صلاحية براءة فايزر في نوفمبر 2011.
IMS Health تنشر تحليلًا للاتجاهات المتوقعة في صناعة المستحضرات الصيدلانية في عام 2007 ، بما في ذلك زيادة الأرباح في معظم القطاعات على الرغم من فقدان بعض براءات الاختراع ، والأدوية الجديدة "الرائجة" في الأفق.[95]
براءات الاختراع والأدوية
بناءً على عدد من الاعتبارات ، يجوز لشركة التقدم بطلب للحصول على براءة اختراع للحصول على الدواء أو عملية إنتاج الدواء ، مع منح حقوق الحصرية عادةً لنحو 20 عامًا[96]ومع ذلك ، فقط بعد الدراسة والاختبارات الصارمة ، والتي تستغرق من 10 إلى 15 عامًا في المتوسط ، ستسمح السلطات الحكومية بإذن للشركة لتسويق الدواء وبيعه.[97]تمكّن حماية براءات الاختراع مالك البراءة من استرداد تكاليف البحث والتطوير من خلال هوامش ربح عالية للدواء العلامة التجارية. عند انتهاء حماية براءة الدواء ، عادة ما يتم تطوير دواء عام وبيعه من قبل شركة منافسة. يعد تطوير الأدوية غير المعتمدة والموافقة عليها أقل تكلفة ، مما يسمح ببيعها بسعر أقل. غالبًا ما يقدم مالك العقار الذي يحمل علامة تجارية نسخة عامة قبل انتهاء صلاحية براءة الاختراع من أجل البدء في السوق العامة.[98] Restructuring has therefore become routine, driven by the patent expiration of products launched during the industry's "golden era" in the 1990s and companies' failure to develop sufficient new blockbuster products to replace lost revenues.[99]
الوصفات
في الولايات المتحدة، زادت قيمة الوصفات الطبية خلال الفترة من 1995 إلى 2005 بمقدار 3.4 مليار سنويًا ، بزيادة قدرها 61 بالمائة. مبيعات التجزئة للأدوية الموصوفة قفزت بنسبة 250 في المائة من 72 مليار دولار إلى 250 مليار دولار ، بينما ارتفع متوسط سعر الوصفات الطبية بأكثر من الضعف من 30 دولارًا إلى 68 دولارًا.[100]
أكبر شركات الأدوية العالمية بدخل أكبر من 10 بليون
| ترتيب | شعار | الشركة | 2019 بليون$ |
2018 بليون$ |
2017 بليون$ |
2016 بليون$ |
2015 بليون$ |
2014 بليون$ |
2013 بليون$ |
2012 بليون$ |
2011 بليون$ | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | NYSE: JNJ |
82.06[101] | 81.60[102] | 76.50[103] | 71.89[104] | 70.10[105] | 74.30[106] | 71.31[107] | 67.20[108] | 65.00[109] | ||

|
2 | SIX: ROG |
63.85[110] | 56.86[111] | 57.37[112] | 50.11[113] | 47.70[114] | 49.86[115] | 48.53[116] | 47.80[117] | 45.21[118] | |

|
3 | NYSE: PFE |
51.75[119] | 53.60[120] | 52.54[121] | 52.82[122] | 48.85[123] | 49.61[124] | 51.58[125] | 58.99[126] | 65.26[127] | |
| 4 | NYSE: NVS |
47.45[128] | 44.75[129] | 49.11[130] | 48.52[131] | 49.41[132] | 58.00[133] | 57.36[134] | 56.67[135] | 58.57[136] | ||

|
5 | ▲ 4 | FWB: BAYN |
38.24 Q3[137] | 45.06[138] | 37.94[139] | 25.27[140] | 24.09[141] | 25.47[142] | 24.17[143] | 24.30[144] | 23.11[145] |

|
6 | LSE: GSK |
32.22 Q3[146] | 43.14[147] | 42.05[148] | 34.79[149] | 29.84[150] | 37.96[151] | 41.61[152] | 39.93[153] | 41.39[154] | |
| 7 | NYSE: MRK |
34.98 Q3[155] | 42.30[156] | 40.10[157] | 39.80[158] | 39.50[159] | 42.24[160] | 44.03[161] | 47.27[162] | 48.05[163] | ||

|
8 | NYSE: SNY |
29.57 Q3[164] | 39.07[165] | 42.91[166] | 36.57[167] | 36.73[168] | 43.07[169] | 42.08[170] | 46.41[171] | 44.34[172] | |
| 9 | ▲ 1 | NYSE: ABBV |
24.56 Q3[173] | 32.75[174] | 28.22[175] | 25.56[176] | 22.82[177] | 19.96[178] | 18.79[179] | – | – | |
| 10 | NASDAQ: ABT |
31.90[180] | 30.60[181] | 27.39[182] | 20.85[183] | 20.41[184] | 20.25[185] | 21.85[186] | 39.87[187] | 38.85[188] | ||
| 11 | NYSE: TMO |
25.54[189] | 24.36[190] | 20.92[191] | 18.27[192] | 16.97[193] | 16.89[194] | 13.09[195] | 12.51[196] | 11.56[197] | ||

|
11 | ▲ 1 | NYSE: LLY |
22.32[198] | 21.49[199] | 22.90[200] | 21.22[201] | 20.00[202] | 19.62[203] | 23.11[204] | 22.60[205] | 24.29[206] |
| 12 | ▲ 1 | NASDAQ: AMGN |
23.40[207] | 23.70[208] | 22.80[209] | 22.99[210] | 21.66[211] | 20.06[212] | 18.68[213] | 17.30[214] | 15.58[215] | |
| 13 | ▲ 4 | NASDAQ: BMY |
18.32 Q3[216] | 22.56[217] | 20.80[218] | 19.43[219] | 16.56[220] | 15.88[221] | 16.39[222] | 17.62[223] | 21.24[224] | |
| 14 | NASDAQ: GILD |
16.32 Q3[225] | 22.13[226] | 25.70[227] | 30.39[227] | 32.15[227] | 24.47[227] | 10.80[227] | 9.70[227] | 8.39[227] | ||
| 15 | LSE: AZN |
17.72 Q3[228] | 22.09[229] | 22.47[230] | 23.00[231] | 24.71[232] | 26.10[233] | 25.71[234] | 27.97[235] | 33.59[236] | ||
| 16 | NASDAQ: TEVA |
4.30 Q1[237] | 18.90[238] | 22.40[239] | 21.90[240] | 20.00[241] | 20.27[242] | 20.31[243] | 18.31[244] | 16.12[245] | ||
| 17 | خاصة |
19.48[246] | 21.67[247] | 17.54[248] | 16.41[248] | 17.70[248] | 18.68[248] | 18.89[248] | 18.34[248] | |||
| 18 | TYO: 4502[N 1] |
19.10[249] | 16.70[250] | 15.96 | 14.93 | 16.84 | 17.36 | 18.91 | 17.80 | |||
| 19 | ETR: MRK |
8.66 Q2[251] | 16.48[252] | 18.70[253] | 16.62[254] | 14.25[255] | 15.29[256] | 14.73[253] | 14.36[253] | 14.31[253] | ||

|
20 | NYSE: NVO |
13.39 Q3[257] | 16.99[258] | 18.77[259] | 16.61[260] | 16.06[261] | 15.83[262] | 14.88[263] | 13.48[264] | 11.56[265] | |
| 21 | NYSE: AGN |
7.69 Q2[266] | 15.78[267] | 15.94[268] | 14.57[268] | 15.07[268] | 12.88[269] | 8.68[270] | 5.91[271] | 4.58[272] | ||
| 22 | NYSE: DHR |
15.07 Q3[273] | 19.89[274] | 18.33[275] | 16.88[276] | 20.56[277] | 19.91[278] | 19.12[279] | 18.26[280] | 16.09[281] | ||

|
23 | NASDAQ: CELG |
12.95 Q3[282] | 15.28[283] | 13.00 | 11.23 | 9.26 | 7.67 | 6.49 | 5.51 | 4.84 | |
| 24 | NASDAQ: BIIB |
10.71 Q3[284] | 13.45[285] | 12.30[286] | 11.40[287] | 10.80[288] | 9.70[289] | 6.90[290] | 5.50[291] | 5.00[292] | ||
| 25 | TYO: 4503 |
12.27[293] | 12.07 | 12.63 | 11.48 | 10.49 | 9.25 | 8.92 | 8.78 | |||
| 26 | NYSE: LH |
8.60 Q3[294] | 11.33[295] | 10.31[295] | 9.55[295] | 8.51[295] | 6.01[295] | 5.81[296] | 5.67[296] | 5.54[296] | ||
| 27 | NYSE: BAX |
8.28 Q3[297] | 11.13 [298] | 10.56 [298] | 10.16 [299] | 9.97 [300] | 10.72 [301] | 14.97 [302] | 14.19 [303] | 13.89 [303] | ||
| 28 | NASDAQ: MYL |
5.35 Q2[304] | 11.43 [305] | 11.91 [305] | 11.08 [305] | 9.43 [305] | 7.72 [305] | 6.91 [306] | 6.80 [306] | 6.13 [306] |
التسويق
الإعلان شائع في مجلات الرعاية الصحية وكذلك من خلال وسائل الإعلام الرئيسية. في بعض البلدان ، ولا سيما الولايات المتحدة ، يُسمح لهم بالإعلان مباشرةً للجمهور العام. توظف شركات الأدوية عمومًا أشخاص مبيعات (يُطلق عليهم غالبًا اسم "ممثلو الأدوية" أو "كبار السن من الرجال") للتسويق المباشر والشخصي للأطباء ومقدمي الرعاية الصحية الآخرين. في بعض البلدان ، ولا سيما الولايات المتحدة ، شركات الأدوية تستخدم أيضًا جماعات الضغط للتأثير على السياسيين. يتم تنظيم تسويق أدوية الوصفات الطبية في الولايات المتحدة بواسطة القانون الفيدرالي قانون تسويق أدوية الوصفات الطبية لعام 1987.
للعاملين في الرعاية الصحية
يناقش كتاب "Bad Pharma" أيضًا تأثير ممثلي المخدرات ، وكيف يتم توظيف رماة الأشباح من قبل شركات الأدوية لكتابة أوراق للأكاديميين لنشرها ، ومدى استقلالية المجلات الأكاديمية ، وكيف تقوم شركات الأدوية بتمويل الأطباء "التعليم المستمر ، وكيف يتم تمويل مجموعات المرضى في كثير من الأحيان من قبل الصناعة.[307]
مباشرة إلى الإعلان المستهلك
منذ الثمانينات من القرن العشرين ، أصبحت الطرق الجديدة لتسويق الأدوية التي تصرف بوصفة طبية للمستهلكين مهمة. تم إضفاء الشرعية على الإعلان الإعلامي المباشر للمستهلك في دليل إدارة الأغذية والعقاقير الخاص بإعلانات البث الموجهة للمستهلك.
الجدل حول تسويق المخدرات وكسب التأييد
كان هناك جدل متزايد حول التسويق الدوائي والنفوذ. كانت هناك اتهامات ونتائج للتأثير على الأطباء وغيرهم من المهنيين الصحيين من خلال ممثلين عن المخدرات بما في ذلك توفير "هدايا" تسويقية ومعلومات متحيزة باستمرار للمهنيين الصحيين ؛[308]الإعلان واسع الانتشار في المجلات والمؤتمرات ؛ تمويل منظمات الرعاية الصحية المستقلة وحملات الترويج الصحي ؛ الضغط على الأطباء والسياسيين (أكثر من أي صناعة أخرى في الولايات المتحدة)[309]); sponsorship of medical schools or nurse training; sponsorship of continuing educational events, with influence on the curriculum;[310] وتوظيف الأطباء كمستشارين مدفوعين في المجالس الاستشارية الطبية. انتقدت بعض مجموعات المناصرة ، مثل No Lunch Lunch و AllTrials ، تأثير تسويق الأدوية للأطباء لأنهم يقولون إنه يحيز الأطباء على وصف الأدوية التي يتم تسويقها حتى عندما يكون الآخرون قد يكون أرخص أو أفضل للمريض.[311] كانت هناك اتهامات ذات صلة بـ الترويج للمرض[312](الإفراط في الطب) لتوسيع السوق للأدوية. عُقد مؤتمر افتتاحي حول هذا الموضوع في أستراليا عام 2006.[313]في عام 2009 ، أطلقت National Prescribing Service التي تمولها الحكومة برنامج "العثور على أدلة - التعرف على الضجيج" ، يهدف إلى تثقيف الممارسين العامين حول طرق الاستقلالية.[314] توصلت مراجعة عام 2005 من قبل لجنة خاصة من المملكة المتحدة إلى جميع الاستنتاجات المذكورة أعلاه في سياق الاتحاد الأوروبي[315]مع تسليط الضوء أيضا على مساهمات واحتياجات الصناعة. أظهرت التحاليل التلوية أن الدراسات النفسية التي ترعاها شركات الأدوية هي أكثر عرضة للإبلاغ عن نتائج إيجابية عدة مرات ، وإذا كان العامل في شركة أدوية يشارك في التأثير ، فإن التأثير يكون أكبر.[316][317][318]امتد التأثير أيضًا إلى تدريب الأطباء والممرضات في كليات الطب ، التي يتم قتالها. لقد قيل إن تصميم الدليل التشخيصي والإحصائي للاضطرابات العقلية وتوسيع المعايير يمثلان طابعًا طبيًا متزايدًا للطبيعة البشرية ، أو "الترويج للمرض" ، مدفوعًا بتأثير شركة الأدوية على الطب النفسي.[319]لقد أثيرت إمكانية حدوث تضارب المصالح مباشرة ، ويرجع ذلك جزئيًا إلى أن ما يقرب من نصف المؤلفين الذين اختاروا وحددوا الاضطرابات النفسية DSM-IV كانوا أو لديهم علاقات مالية سابقة مع صناعة المستحضرات الصيدلانية.[320] في الولايات المتحدة ، ابتداءً من عام 2013 ، بموجب تقارير الشفافية المالية للطبيب (جزء من قانون Sunshine Act) ، يتعين على مراكز خدمات Medicaid و Medicaid الطبية جمع معلومات من الشركات المصنعة المعمول بها ومنظمات الشراء الجماعية من أجل الإبلاغ عن معلومات حول علاقاتها المالية مع الأطباء والمستشفيات. يتم نشر البيانات للجمهور في موقع مراكز خدمات الرعاية الطبية والخدمات الطبية. من المتوقع أن تصبح العلاقة بين الأطباء والصناعة الدوائية شفافة تمامًا.[321] في تقرير أصدره مركز السياسة المستجيبة ، كان هناك أكثر من 1100 عضو في جماعات الضغط يعملون في بعض القدرات في مجال صناعة الأدوية في عام 2017. في الربع الأول من عام 2017 ، أنفقت صناعة المنتجات الصيدلانية والصيدلانية 78 مليون دولار على الضغط أعضاء كونغرس الولايات المتحدة.[322]
المسائل التنظيمية
Ben Goldacre جادل بأن المنظمين - مثل هيئة تنظيم الأدوية ومنتجات الرعاية الصحية (MHRA) في المملكة المتحدة ، أو إدارة الغذاء والدواء (FDA) في الولايات المتحدة - تقدم مصالح شركات الأدوية بدلاً من مصالح الجمهور بسبب تبادل الباب الدوار للموظفين بين الجهة المنظمة والشركات وتنمية الصداقات بين موظفي الهيئة التنظيمية وموظفي الشركة.[323] He argues that regulators do not require that new drugs offer an improvement over what is already available, or even that they be particularly effective.[323] جادل آخرون بأن التنظيم المفرط يقمع الابتكار العلاجي ، وأن التكلفة الحالية للتجارب السريرية التي تتطلبها الجهة المنظمة تمنع الاستغلال الكامل للمعرفة الوراثية والبيولوجية الجديدة لعلاج الأمراض التي تصيب الإنسان. قدم تقرير أصدره عام 2012 من قبل مجلس مستشاري الرئيس للعلوم والتكنولوجيا عدة توصيات رئيسية لتقليل الأعباء التنظيمية على تطوير عقاقير جديدة ، بما في ذلك 1) توسيع استخدام إدارة الأغذية والعقاقير لعمليات الموافقة السريعة ، 2) إنشاء مسار موافقة سريع للعقاقير المعدة للاستخدام في مجموعات محددة بدقة ، و 3) الاضطلاع بمشاريع رائدة تهدف إلى تقييم جدوى عملية جديدة للموافقة على الدواء.[324]
الاحتيال الدوائي
الاحتيال الدوائي ينطوي على الخداع الذي يحقق مكاسب مالية لشركة أدوية. إنه يؤثر على الأفراد و العام و التأمين الخاص. هناك العديد من المخططات المختلفة[325]تستخدم للاحتيال على نظام الرعاية الصحية التي تعتبر خاصة لصناعة الأدوية. وتشمل هذه: انتهاكات ممارسات التصنيع الجيدة (GMP) ، التسويق خارج الملصقات ، احتيال أفضل الأسعار ، احتيال CME ، الإبلاغ عن أسعار المعونة الطبية ، والأدوية المركبة المصنعة.[326]من هذا المبلغ ، تم استرداد 2.5 مليار دولار من خلال قضايا "قانون المطالبات الزائفة" في السنة المالية 2010. وتشمل أمثلة حالات الاحتيال تسوية GlaxoSmithKline بقيمة 3 مليارات دولار ، Pfizer وتسوية 2.3 مليار دولار و [[Merck & Co] ]] تسوية 650 مليون دولار. يمكن استرداد الأضرار الناتجة عن الاحتيال عن طريق استخدام قانون الدعاوى الخاطئة ، والأكثر شيوعًا بموجب الأحكام qui tam التي تكافئ الفرد على كونه "المبلغين عن المخالفات" ، أو [ [relator (القانون)]].[327]
كل شركة كبرى تبيع مضادات الذهان - بريستول مايرز سكويب ، إيلي ليلي وشركاه ، فايزر ، أسترا زينيكا و جونسون آند جونسون - إما استقرت على الحكومة الأخيرة الحالات ، بموجب قانون الادعاءات الخاطئة ، لمئات الملايين من الدولارات أو قيد التحقيق حاليًا بسبب الاحتيال المحتمل في الرعاية الصحية. بعد اتهامات بالتسويق غير القانوني ، سجلت اثنتان من المستوطنات أرقامًا قياسية العام الماضي لأكبر غرامات جنائية تم فرضها على الشركات. أحدهما شمل مضادات الذهان إيلي ليلي Zyprexa ، والآخر مشارك Bextra. في قضية Bextra ، اتهمت الحكومة شركة Pfizer أيضًا بتسويق مضادات الذهان الأخرى بطريقة غير مشروعة ، Geodon ؛ قامت شركة Pfizer بتسوية هذا الجزء من المطالبة بمبلغ 301 مليون دولار ، دون الاعتراف بأي مخالفات.[328]
في 2 يوليو 2012 ، GlaxoSmithKline أقر بأنه مذنب في تهم جنائية ووافق على تسوية بقيمة 3 مليارات دولار لأكبر قضية احتيال في مجال الرعاية الصحية في الولايات المتحدة وأكبر مدفوعات شركة أدوية.[329] تتعلق التسوية بالترويج غير القانوني للشركة للعقاقير الطبية ، وفشلها في الإبلاغ عن بيانات السلامة ،[330]
رشوة الأطباء ، وترويج الأدوية للاستخدامات التي لم تكن مرخصة. كانت الأدوية المعنية Paxil ، Wellbutrin ، Advair ، Lamictal ، و Zofran للاستخدامات غير الملصقة وغير المغطاة. هؤلاء والمخدرات Imitrex و Lotronex و Flovent و Valtrex شاركوا في | kickback plan).[331][332][333]
فيما يلي قائمة بأربع أكبر مستوطنات تم التوصل إليها مع شركات الأدوية من 1991 إلى 2012 ، مرتبة مرتبة حسب حجم التسوية الإجمالية. تباينت الادعاءات القانونية ضد صناعة المستحضرات الصيدلانية على نطاق واسع خلال العقدين الماضيين ، بما في ذلك الغش في الرعاية الطبية والرعاية الطبية ، خارج الملصق ، وعدم كفاية ممارسات التصنيع.[334][335]
| Company | Settlement | Violation(s) | Year | Product(s) | Laws allegedly violated (if applicable) |
|---|---|---|---|---|---|
| GlaxoSmithKline[336] | $3 billion | Off-label promotion/ failure to disclose safety data |
2012 | Avandia/Wellbutrin/Paxil | False Claims Act/FDCA |
| Pfizer[337] | $2.3 billion | Off-label promotion/kickbacks | 2009 | Bextra/Geodon/ Zyvox/Lyrica |
False Claims Act/FDCA |
| Abbott Laboratories[338] | $1.5 billion | Off-label promotion | 2012 | Depakote | False Claims Act/FDCA |
| Eli Lilly[339] | $1.4 billion | Off-label promotion | 2009 | Zyprexa | False Claims Act/FDCA |
العالم النامي
براءات الاختراع
تم انتقاد براءات الاختراع في العالم النامي ، حيث يُعتقد أنها تقلل من الوصول إلى الأدوية الموجودة.[340]إن التوفيق بين براءات الاختراع والوصول الشامل إلى الدواء يتطلب سياسة دولية فعالة من التمييز في الأسعار. علاوة على ذلك ، بموجب اتفاقية TRIPS المبرمة من منظمة التجارة العالمية ، يجب على البلدان أن تسمح ببراءة المنتجات الصيدلانية. في عام 2001 ، اعتمدت منظمة التجارة العالمية إعلان الدوحة ، الذي يشير إلى أنه ينبغي قراءة اتفاق تريبس مع وضع أهداف الصحة العامة في الاعتبار ، وتسمح ببعض الأساليب للتحايل على الاحتكارات الدوائية: عن طريق الترخيص الإجباري أو [ [الواردات الموازية]] ، حتى قبل انتهاء صلاحية البراءة.[341]
في مارس 2001 ، رفعت 40 شركة أدوية متعددة الجنسيات دعاوى ضد جنوب إفريقيا بسبب قانون الأدوية ، والذي سمح بالإنتاج العام للأدوية المضادة للفيروسات القهقرية علاج فيروس نقص المناعة البشرية ، على الرغم من حقيقة أن هذه الأدوية كانت على براءة اختراع. خطأ استشهاد: إغلاق </ref> مفقود لوسم <ref>
في عام 2016 ، أعلنت GlaxoSmithKline (سادس أكبر شركة أدوية في العالم) أنها ستتخلى عن براءات اختراعها في البلدان الفقيرة ، وذلك للسماح للشركات المستقلة بإنتاج وبيع الأدوية الخاصة بها في تلك المناطق ، مما يوسع من وصول الجمهور إليها..[342]نشرت شركة GlaxoSmithKline قائمة تضم 50 دولة لم تعد تمتلك براءات اختراع فيها ، مما أثر على مليار شخص حول العالم.
البرامج الخيرية
في عام 2011 ، جاءت أربعة من أكبر 20 تبرعًا خيريًا للشركات وثمانية من أفضل 30 تبرعًا خيريًا من الشركات المصنعة للأدوية. يأتي الجزء الأكبر من التبرعات الخيرية للشركات (69٪ اعتبارًا من عام 2012) عن طريق التبرعات الخيرية غير النقدية ، والتي كان معظمها مرة أخرى تبرعات من شركات الأدوية. بعض هذه الشركات الصيدلانية الكبيرة هي مؤسسات "مساعدة المرضى" ، حيث تقدم الدعم المالي للأفراد في شراء الأدوية التي تصرف بوصفة طبية ، ولكن شركات الأدوية هي أيضًا من يقدمون منتجات عينية ضخمة ، أي الأدوية الخاصة بهم. يقول باتريك روني من Giving USA في مقابلة مع Nonpritit Quarterly ، إن التبرعات غير النقدية للمنتجات يمكن أن "تزيد الأرباح ... كجزء من قضية مراقبة المخزون عندما يكون لديها مخزونات زائدة" لبعض الشركات ،[343]
تشمل البرامج الخيرية وجهود اكتشاف وتطوير الأدوية التي تقوم بها شركات الأدوية ما يلي:
- "هدية Merck" ، حيث تم التبرع بمليارات من عمى النهر من المخدرات في إفريقياref>"Merk". Archived from the original on 26 August 2006. Retrieved 30 August 2006.</ref>
- Pfizer's gift of free/discounted fluconazole and other drugs for AIDS in South Africa[344]
- GSK's commitment to give free albendazole tablets to the WHO for, and until, the elimination of lymphatic filariasis worldwide.
- In 2006, Novartis committed US$755 million in corporate citizenship initiatives around the world, particularly focusing on improving access to medicines in the developing world through its Access to Medicine projects, including donations of medicines to patients affected by leprosy, tuberculosis, and malaria; Glivec patient assistance programs; and relief to support major humanitarian organisations with emergency medical needs.[345]
أنظر أيضا
- Big Pharma conspiracy theory
- Clinical trial
- Drug development
- Drug discovery
- Legal drug trade
- List of pharmaceutical companies
- Pharmaceutical marketing
- Pharmacy
المصادر
- ^ John L. McGuire, Horst Hasskarl, Gerd Bode, Ingrid Klingmann, Manuel Zahn "Pharmaceuticals, General Survey" Ullmann's Encyclopedia of Chemical Technology" Wiley-VCH, Weinheim, 2007.DOI: 10.1002/14356007.a19_273.pub2
- ^ "Top Pharmaceuticals: Introduction: EMERGENCE OF PHARMACEUTICAL SCIENCE AND INDUSTRY: 1870-1930".
- ^ Walter Sneader (31 October 2005). Drug Discovery: A History. John Wiley & Sons. pp. 155–156. ISBN 978-0-470-01552-0.
- ^ أ ب Rasmussen, Nicolas (2006). "Making the First Anti-Depressant: Amphetamine in American Medicine, 1929-1950". J Hist Med Allied Sci. 61 (3): 288–323. doi:10.1093/jhmas/jrj039. PMID 16492800.
- ^ Yasiry Z, Shorvon SD (December 2012). "How phenobarbital revolutionized epilepsy therapy: the story of phenobarbital therapy in epilepsy in the last 100 years". Epilepsia. 53 Suppl 8: 26–39. doi:10.1111/epi.12026. PMID 23205960.
- ^ López-Muñoz F, Ucha-Udabe R, Alamo C (December 2005). "The history of barbiturates a century after their clinical introduction". Neuropsychiatr Dis Treat. 1 (4): 329–43. PMC 2424120. PMID 18568113.
- ^ "Drug Abuse Control Amendments of 1965". NEJM. 273 (22): 1222–1223. 1965-11-25. doi:10.1056/NEJM196511252732213.
Officers of the Food and Drug Administration,إدراكًا لخطورة المشكلة ، قدّر أن ما يقرب من نصف الكبسولات والأقراص التي تحتوي على 9000.000.000 من الباربيتورات والأمفيتامين المصنعة سنويًا في هذا البلد يتم تحويلها إلى استخدام غير قانوني. لقد أثبتت الأرباح التي يمكن جنيها من البيع غير المشروع لهذه الأدوية جاذبية الجريمة المنظمة ، حيث يمكن شراء الأمفيتامين بالجملة بسعر يقل عن دولار واحد لكل 1000 كبسولة ، ولكن عند بيعه في السوق غير القانوني ، فإنه يجمع ما بين 30 إلى 50 دولارًا لكل 1000 وعندما يتم إعادة بيعها للمشتري الفردي ، قد يجلب الجهاز اللوحي ما يصل إلى 10 إلى 25 سنتًا.
- ^ "Sedative-Hypnotic Drugs — The Barbiturates — I". NEJM. 255: 1150–1151. 1956. doi:10.1056/NEJM195612132552409.
THE barbiturates, introduced into medicine by E. Fischer and J. فون Mering1 في عام 1903 ، هي بالتأكيد من بين العقاقير الأكثر استخدامًا وتعاطيًا على نطاق واسع في مجال الطب. يتم تصنيع ما يقرب من 400 طن من هذه العوامل كل عام. هذا يكفي لوضع حوالي 9000.000 شخص للنوم كل ليلة لتلك الفترة إذا تم إعطاء كل منهم 0.1 جم. جرعة
{{cite journal}}: Unknown parameter|قضية=ignored (help) - ^ Rosenfeld L (December 2002). "Insulin: discovery and controversy". Clin. Chem. 48 (12): 2270–88. doi:10.1093/clinchem/48.12.2270. PMID 12446492.
- ^ أ ب "www.cdc.gov" (PDF).
- ^ "www.cdc.gov" (PDF).
- ^ Sepkowitz KA (July 2011). "One hundred years of Salvarsan". N. Engl. J. Med. 365 (4): 291–3. doi:10.1056/NEJMp1105345. PMID 21793743.
- ^ Aminov RI (2010). "A brief history of the antibiotic era: lessons learned and challenges for the future". Front Microbiol. 1: 134. doi:10.3389/fmicb.2010.00134. PMC 3109405. PMID 21687759.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Hager, Thomas (2006). The demon under the microscope : from battlefield hospitals to Nazi labs, one doctor's heroic search for the world's first miracle drug (1st ed.). New York: Harmony Books. ISBN 978-1-4000-8213-1.
- ^ "Nobel Prize Facts". www.nobelprize.org. Retrieved 19 May 2016.
- ^ أ ب Cutler, David; Meara, Ellen (October 2001). "Changes in the Age Distribution of Mortality Over the 20th Century" (PDF). NBER Working Paper No. 8556. doi:10.3386/w8556.
- ^ أ ب Klein, Herbert (2012). A Population History of the United States. Cambridge University Press. p. 167.
- ^ John Parascandola (1980). The History of antibiotics: a symposium. American Institute of the History of Pharmacy No. 5. ISBN 978-0-931292-08-8.
- ^ "Diphtheria — Timelines — History of Vaccines".
- ^ Ii, Thomas H. Maugh (2005-04-13). "Maurice R. Hilleman, 85; Scientist Developed Many Vaccines That Saved Millions of Lives - Los Angeles Times". Los Angeles Times.
- ^ "Significant Dates in U.S. Food and Drug Law History".
- ^ "FDAReview.org, a project of The Independent Institute".
- ^ "Sulfanilamide Disaster".
- ^ "FDA History - Part II".
- ^ Zaffiri L, Gardner J, Toledo-Pereyra LH (April 2012). "History of antibiotics. From salvarsan to cephalosporins". J Invest Surg. 25 (2): 67–77. doi:10.3109/08941939.2012.664099. PMID 22439833.
- ^ Hamilton-Miller JM (March 2008). "Development of the semi-synthetic penicillins and cephalosporins". Int. J. Antimicrob. Agents. 31 (3): 189–92. doi:10.1016/j.ijantimicag.2007.11.010. PMID 18248798.
- ^ Abraham EP (1987). "Cephalosporins 1945-1986". Drugs. 34 Suppl 2 (Supplement 2): 1–14. doi:10.2165/00003495-198700342-00003. PMID 3319494.
- ^ أ ب Kingston W (July 2004). "Streptomycin, Schatz v. Waksman, and the balance of credit for discovery". J Hist Med Allied Sci. 59 (3): 441–62. doi:10.1093/jhmas/jrh091. PMID 15270337.
- ^ Nelson ML, Levy SB (December 2011). "The history of the tetracyclines". Ann. N. Y. Acad. Sci. 1241 (1): 17–32. Bibcode:2011NYASA1241...17N. doi:10.1111/j.1749-6632.2011.06354.x. PMID 22191524.
- ^ "ERYTHROMYCIN". Br Med J. 2 (4793): 1085–6. November 1952. doi:10.1136/bmj.2.4793.1085. PMC 2022076. PMID 12987755.
- ^ Anderson, Rosaleen (2012). Antibacterial agents chemistry, mode of action, mechanisms of resistance, and clinical applications. Oxford: WiBlackwell. ISBN 9780470972458.
- ^ تقرير لجنة التجارة الفيدرالية عن تصنيع المضادات الحيوية ، يونيو 1958 (واشنطن العاصمة ، مكتب الطباعة الحكومي ، 1958) الصفحات 98-120
- ^ Federal Trade تقرير لجنة تصنيع المضادات الحيوية ، يونيو 1958 (واشنطن العاصمة ، مكتب الطباعة الحكومي ، 1958) صفحة 277
- ^ SWEET BH, HILLEMAN MR (November 1960). "The vacuolating virus, S.V. 40". Proc. Soc. Exp. Biol. Med. 105 (2): 420–7. doi:10.3181/00379727-105-26128. PMID 13774265.
- ^ Shah K, Nathanson N (January 1976). "Human exposure to SV40: review and comment". Am. J. Epidemiol. 103 (1): 1–12. doi:10.1093/oxfordjournals.aje.a112197. PMID 174424.
- ^ "Studies:No Evidence That SV40 is Related to Cancer - National Cancer Institute". Archived from the original on 28 أكتوبر 2014.
- ^ "History of Vaccines — A Vaccine History Project of The College of Physicians of Philadelphia".
- ^ "Prevention of Measles, Rubella, Congenital Rubella Syndrome, and Mumps, 2013".
- ^ Bloch AB, Orenstein WA, Stetler HC, et al. (1985). "Health impact of measles vaccination in the United States". Pediatrics. 76 (4): 524–32. PMID 3931045.
- ^ Insull W (January 2009). "The pathology of atherosclerosis: plaque development and plaque responses to medical treatment". The American Journal of Medicine. 122 (1 Suppl): S3–S14. doi:10.1016/j.amjmed.2008.10.013. PMID 19110086.
- ^ Gaddam KK, Verma A, Thompson M, Amin R, Ventura H (May 2009). "Hypertension and cardiac failure in its various forms". The Medical Clinics of North America. 93 (3): 665–80. doi:10.1016/j.mcna.2009.02.005. PMID 19427498. Retrieved 2009-06-20.
- ^ Agabiti-Rosei E (September 2008). "From macro- to microcirculation: benefits in hypertension and diabetes". Journal of Hypertension. 26 (Suppl 3): S15–21. doi:10.1097/01.hjh.0000334602.71005.52. PMID 19363848.
- ^ Murphy BP, Stanton T, Dunn FG (May 2009). "Hypertension and myocardial ischemia". The Medical Clinics of North America. 93 (3): 681–95. doi:10.1016/j.mcna.2009.02.003. PMID 19427499. Retrieved 2009-06-20.
- ^ White WB (May 2009). "Defining the problem of treating the patient with hypertension and arthritis pain". The American Journal of Medicine. 122 (5 Suppl): S3–9. doi:10.1016/j.amjmed.2009.03.002. PMID 19393824.
- ^ Truong LD, Shen SS, Park MH, Krishnan B (February 2009). "Diagnosing nonneoplastic lesions in nephrectomy specimens". Archives of Pathology & Laboratory Medicine. 133 (2): 189–200. doi:10.1043/1543-2165-133.2.189 (inactive 2020-01-25). PMID 19195963. Retrieved 2009-06-20.
{{cite journal}}: CS1 maint: DOI inactive as of يناير 2020 (link) - ^ Tracy RE, White S (February 2002). "A method for quantifying adrenocortical nodular hyperplasia at autopsy: some use of the method in illuminating hypertension and atherosclerosis". Annals of Diagnostic Pathology. 6 (1): 20–9. doi:10.1053/adpa.2002.30606. PMID 11842376.
- ^ Aronow WS (August 2008). "Hypertension and the older diabetic". Clinics in Geriatric Medicine. 24 (3): 489–501, vi–vii. doi:10.1016/j.cger.2008.03.001. PMID 18672184. Retrieved 2009-06-20.
- ^ Gardner AW, Afaq A (2008). "Management of Lower Extremity Peripheral Arterial Disease". Journal of Cardiopulmonary Rehabilitation and Prevention. 28 (6): 349–57. doi:10.1097/HCR.0b013e31818c3b96. PMC 2743684. PMID 19008688.
- ^ Novo S, Lunetta M, Evola S, Novo G (January 2009). "Role of ARBs in the blood hypertension therapy and prevention of cardiovascular events". Current Drug Targets. 10 (1): 20–5. doi:10.2174/138945009787122897. PMID 19149532. Retrieved 2009-06-20.
- ^ Craig WM (1939). "Surgical Treatment of Hypertension". Br Med J. 2 (4120): 1215–9. doi:10.1136/bmj.2.4120.1215. PMC 2178707. PMID 20782854.
- ^ Sneader, Walter (2005). Drug Discovery. A History. New York: Wiley. p. 371.
- ^ Beyer KH (1993). "Chlorothiazide. How the thiazides evolved as antihypertensive therapy". Hypertension. 22 (3): 388–91. doi:10.1161/01.hyp.22.3.388. PMID 8349332.
- ^ BORHANI NO, HECHTER HH (1964). "Recent Changes in CVR Disease Mortality in California: An Epidemiologic Appraisal". Public Health Rep. 79 (2): 147–60. doi:10.2307/4592077. JSTOR 4592077. PMC 1915335. PMID 14119789.
- ^ "The Lasker Foundation - Awards".
- ^ Wright JM, Musini VM (2009). "First-line drugs for hypertension". Cochrane Database Syst Rev (3): CD001841. doi:10.1002/14651858.CD001841.pub2. PMID 19588327.
- ^ Stason WB, Cannon PJ, Heinemann HO, Laragh JH (November 1966). "Furosemide. A clinical evaluation of its diuretic action". Circulation. 34 (5): 910–20. doi:10.1161/01.cir.34.5.910. PMID 5332332.
- ^ Black JW, Crowther AF, Shanks RG, Smith LH, Dornhorst AC (1964). "A new adrenergic betareceptor antagonist". The Lancet. 283 (7342): 1080–1081. doi:10.1016/S0140-6736(64)91275-9. PMID 14132613.
- ^ Lv J, Perkovic V, Foote CV, Craig ME, Craig JC, Strippoli GF (2012). "Antihypertensive agents for preventing diabetic kidney disease". Cochrane Database Syst Rev. 12: CD004136. doi:10.1002/14651858.CD004136.pub3. PMID 23235603.
- ^ "A brief history of the birth control pill - The pill timeline | Need to Know | PBS". 7 May 2010.
- ^ "Why the Oral Contraceptive Is Just Known as "The Pill"". www.smithsonianmag.com.
- ^ "BBC News | HEALTH | A short history of the pill".
- ^ "FDA's Approval of the First Oral Contraceptive, Enovid".
- ^ Cafe, Rebecca (2011-12-04). "BBC News - How the contraceptive pill changed Britain". BBC News.
- ^ "Brochure: The History of Drug Regulation in the United States".
- ^ Tobert, Jonathan A. (July 2003). "Lovastatin and beyond: the history of the HMG-CoA reductase inhibitors". Nature Reviews Drug Discovery. 2 (7): 517–526. doi:10.1038/nrd1112. ISSN 1474-1776. PMID 12815379.
- ^ Endo A (1 November 1992). "The discovery and development of HMG-CoA reductase inhibitors". Journal of Lipid Research. 33 (11): 1569–82. PMID 1464741.
- ^ Endo, Akira (2004). "The origin of the statins". International Congress Series. 1262: 3–8. doi:10.1016/j.ics.2003.12.099.
- ^ Scandinaviansimvastatinsurvival (November 1994). "Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S)". Lancet. 344 (8934): 1383–9. doi:10.1016/S0140-6736(94)90566-5. PMID 7968073.
- ^ "National Inventors Hall of Fame Honors 2012 Inductees". PRNewswire. Retrieved 11 May 2014.
- ^ "How One Scientist Intrigued by Molds Found First Statin". Wall Street Journal. Retrieved 11 May 2014.
- ^ "Annual Impact Report". Tufts Center for the Study of Drug Development.
{{cite journal}}: Cite journal requires|journal=(help) - ^ Outsourcing-Pharma.com. "Pfizer teams with Parexel and Icon in CRO sector's latest strategic deals". Outsourcing-Pharma.com.
- ^ "How Many New Drugs Did FDA Approve Last Year?". pharmalot.com.
- ^ "Research".
- ^ أ ب Perry, Susan (8 August 2012). "Donald Light and Joel Lexchin in BMJ 2012;345:e4348, quoted in: Big Pharma's claim of an 'innovation crisis' is a myth, BMJ authors say". MinnPost. Retrieved 8 August 2012.
- ^ "About PhRMA - PhRMA".
- ^ "Has the Pharmaceutical Blockbuster Model Gone Bust?". www.bain.com. Retrieved 19 May 2016.
- ^ Matthew Harper (2012-02-10). "The Truly Staggering Cost Of Inventing New Drugs". Forbes.
- ^ IMS Health (2015-06-18). "Are European biotechnology companies sufficiently protected?". Portal of Competitive Intelligence.
- ^ Bhandari M, Busse JW, Jackowski D, Montori VM, Schunemann H, Sprague S, Mears D, Schemitsch EH, Heels-Ansdell D, Devereaux PJ (2004-02-17). "Association between industry funding and statistically significant pro-industry findings in medical and surgical randomized trials". Canadian Medical Association Journal. 170 (4): 477–480. doi:10.1016/0006-291x(75)90506-9. PMID 4.
- ^ Moynihan, R. (29 May 2003). "Who pays for the pizza? Redefining the relationships between doctors and drug companies. 2: Disentanglement". BMJ. 326 (7400): 1193–1196. doi:10.1136/bmj.326.7400.1193. PMC 1126054. PMID 12775622.
- ^ "Hogan & Hartson Update on Pharmaceutical Trial Registration" (PDF). 3 مارس 2008. Archived from the original (PDF) on 25 يونيو 2008. Retrieved 2 يونيو 2008.
- ^ Barnett, Antony (7 December 2003). "Revealed: how drug firms 'hoodwink' medical journals". the Guardian. Retrieved 19 May 2016.
- ^ Ornstein, Tracy Weber, Charles (11 March 2013). "Dollars for Docs Mints a Millionaire". ProPublica. Retrieved 19 May 2016.
{{cite news}}: CS1 maint: multiple names: authors list (link) - ^ Drazen, Jeffrey M. (2015). "Revisiting the Commercial–Academic Interface — NEJM". New England Journal of Medicine. 372 (19): 1853–1854. doi:10.1056/NEJMe1503623. PMID 25946285.
- ^ Rosenbaum, Lisa (2015). "Reconnecting the Dots — Reinterpreting Industry–Physician Relations — NEJM". New England Journal of Medicine. 372 (19): 1860–1864. doi:10.1056/NEJMms1502493. PMID 25946288.
- ^ Liberti L, McAuslane JN, Walker S (2011). "Standardizing the Benefit-Risk Assessment of New Medicines: Practical Applications of Frameworks for the Pharmaceutical Healthcare Professional". Pharm Med. 25 (3): 139–46. doi:10.1007/BF03256855.
- ^ "Electronic Orange Book". U.S. Food and Drug Administration. Retrieved 2007-05-31.
- ^ "The Orphan Drug Act (as amended)". U.S. Food and Drug Administration. Retrieved 2007-09-24.
- ^ (pdf)
- ^ Herper, Matthew; Kang, Peter (2006-03-22). "The World's Ten Best-Selling Drugs". Forbes. Retrieved 2007-05-31.
{{cite news}}: Unknown parameter|lastauthoramp=ignored (|name-list-style=suggested) (help) - ^ "Creating Connected Solutions for Better Healthcare Performance" (PDF). IMS Health.
- ^ Julia Kollewe (2014-03-27). "World's 10 bestselling prescription drugs made $75bn last year". the Guardian.
- ^ "Top 100 Drugs for 2013 by Sales - U.S. Pharmaceutical Statistics".
- ^ "IMS Health Forecasts 5 to 6 Percent Growth for Global Pharmaceutical Market in 2007". IMS Health. 2006-10-24. Retrieved 2007-06-19.
- ^ Frequently Asked Questions (FAQs) Archived 25 فبراير 2013 at the Wayback Machine
- ^ "New Drug Approvals in 2006" (PDF). March 2007. Archived from the original (PDF) on 2008-02-28. Retrieved 2008-02-23.
- ^ "Assessment of Authorized Generics in the U.S" (PDF). IMS Consulting. June 2006. Archived from the original (PDF) on 2008-02-28. Retrieved 2008-02-23.
- ^ "Sanofi Laying Off 1,700 in US". Drug Discovery & Development.
- ^ "2007 Health and Nutrition - Census" (PDF). U.S. Census Bureau. Retrieved 19 May 2016.
- ^ https://www.biospace.com/article/releases/johnson-and-amp-johnson-reports-2019-fourth-quarter-and-full-year-results-/?s=72
- ^ "Johnson & Johnson Reports 2018 Fourth-Quarter Results:". Content Lab - U.S.
- ^ "Johnson & Johnson Reports 2017 Fourth-Quarter Results: - Johnson & Johnson". www.jnj.com.
- ^ "Johnson & Johnson Reports 2016 Fourth-Quarter Results - Johnson & Johnson". www.jnj.com.
- ^ "Johnson & Johnson Reports 2015 Fourth-Quarter Results:".
- ^ "Johnson & Johnson Reports 2014 Fourth-Quarter and Full-Year Results - Johnson & Johnson". www.jnj.com.
- ^ "Johnson & Johnson Reports 2013 Fourth-Quarter and Full-Year Results - Johnson & Johnson". www.jnj.com.
- ^ "Johnson & Johnson Reports 2012 Fourth-Quarter and Full-Year Results:".
- ^ "Johnson & Johnson Reports 2011 Fourth-Quarter and Full-Year Results:".
- ^ https://www.roche.com/dam/jcr:e49f6995-e813-43c1-9302-c9b7d0bddbc8/en/irp200130-a.pdf
- ^ https://www.roche.com/dam/jcr:af865dfd-50fb-458b-9cac-34097db9d3ec/en/ar18e.pdf
- ^ "Roche reports good results in 2017". www.roche.com.
- ^ https://www.roche.com/dam/jcr:ee2f197f-5487-4629-9e28-66b77c9cbbab/en/ar16e.pdf
- ^ https://www.roche.com/dam/jcr:9b36e11d-495c-42f5-b757-e80c4e88d793/en/gb15e.pdf
- ^ https://www.roche.com/dam/jcr:880b44a1-3fd6-4e66-bf10-f4af1e724d4d/en/gb14e.pdf
- ^ https://www.roche.com/dam/jcr:64fd6b2d-1a76-467f-badd-ab94b85b6d70/en/gb13e.pdf
- ^ https://www.roche.com/dam/jcr:3e048249-e3ce-4969-a77e-cc90d8f3fa73/en/gb12e.pdf
- ^ https://www.roche.com/dam/jcr:52174b39-feab-4210-82f6-9b8786a69ecf/en/gb11e.pdf
- ^ https://www.biospace.com/article/releases/pfizer-reports-fourth-quarter-and-full-year-2019-results/?s=72
- ^ https://s21.q4cdn.com/317678438/files/doc_financials/Quarterly/2018/q4/Q4-2018-PFE-Earnings-Release.pdf
- ^ https://s21.q4cdn.com/317678438/files/doc_financials/Quarterly/2017/Q4_2017_PFE_Earnings_Release.pdf
- ^ https://s21.q4cdn.com/317678438/files/doc_financials/Annual/2016/2016-financial-report.pdf
- ^ https://s21.q4cdn.com/317678438/files/doc_financials/Annual/2015/2015_Pfizer_Financial_Report.pdf
- ^ https://s21.q4cdn.com/317678438/files/doc_financials/Annual/2014/2014_Pfizer_Financial_Report.pdf
- ^ https://s21.q4cdn.com/317678438/files/doc_financials/Annual/2013/FinancialReport2013.pdf
- ^ https://s21.q4cdn.com/317678438/files/doc_financials/Annual/2012/financial2012.pdf
- ^ https://s21.q4cdn.com/317678438/files/doc_financials/Annual/2011/financial2011.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/q4-2019-media-release-en.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/q4-2018-media-release-en.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/novartis-annual-report-2017-en.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/novartis-annual-report-2016-en.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/novartis-annual-report-2015-en.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/novartis-annual-report-2014-en.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/novartis-annual-report-2013-en.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/novartis-annual-report-2012-en.pdf
- ^ https://www.novartis.com/sites/www.novartis.com/files/novartis-annual-report-2011-en.pdf
- ^ https://www.bayer.com/en/quarterly-reports.aspx
- ^ "Bayer's Annual Report 2018". www.annualreport2018.bayer.com.
- ^ http://www.annualreport2017.bayer.com/servicepages/downloads/files/bayer_ar17_entire.pdf
- ^ http://www.annualreport2016.bayer.com/servicepages/downloads/files/bayer_ar16_entire.pdf
- ^ http://www.annualreport2015.bayer.com/servicepages/downloads/files/entire_bayer_ar15.pdf
- ^ AG, Bayer. "Bayer – Global Home". www.bayer.com.
- ^ https://www.bayer.com/en/ar-2013.pdfx
- ^ https://www.bayer.com/en/ar-2012.pdfx
- ^ https://www.bayer.com/en/ar-2011.pdfx
- ^ https://www.gsk.com/en-gb/media/press-releases/gsk-delivers-sales-of-94-billion-plus16-aer-plus11-cer-pro-forma-plus6-cerstar/
- ^ "GSK delivers sales, earnings and cash flow growth in 2018 - GSK". www.gsk.com.
- ^ https://www.gsk.com/media/4629/fy-2017-results-announcement.pdf
- ^ https://www.gsk.com/media/3609/annual-report-2016.pdf
- ^ https://www.gsk.com/media/2718/gsk-annual-report-2016.pdf
- ^ https://www.gsk.com/media/2710/gsk-annual-report-2014-interactive.pdf
- ^ https://www.gsk.com/media/2701/annual-report-2013-interactive.pdf
- ^ https://www.gsk.com/media/2694/annual-report-2012.pdf
- ^ https://www.gsk.com/media/2696/annual-report-2011.pdf
- ^ https://www.biospace.com/article/releases/merck-announces-third-quarter-2019-financial-results/?s=72
- ^ "Merck Announces Fourth-Quarter and Full-Year 2018 Financial Results". BioSpace.
- ^ LaVito, Angelica (2 February 2018). "Merck posts mixed fourth-quarter results as Keytruda sales skyrocket".
- ^ http://s21.q4cdn.com/488056881/files/doc_financials/2017/Q4/merck-q4-10k.pdf
- ^ http://s21.q4cdn.com/488056881/files/doc_financials/2015/annual/MRK_2015_Form_10-K_FINAL_r879.pdf
- ^ http://s21.q4cdn.com/488056881/files/doc_financials/2014/annual/2014-Form-10-K_FINAL_022715.pdf
- ^ http://s21.q4cdn.com/488056881/files/doc_financials/2013/annual/MRK_2013_Form_10_K_FINAL_022714.pdf
- ^ http://s21.q4cdn.com/488056881/files/doc_financials/2012/annual/MRK_form_10_k_2012.pdf
- ^ http://s21.q4cdn.com/488056881/files/doc_financials/2011/annual/form-10-k-2011.pdf
- ^ https://www.sanofi.com/-/media/Project/One-Sanofi-Web/Websites/Global/Sanofi-COM/Home/en/investors/docs/Q3_2019_Results_Press_Release_EN.pdf?la=en&hash=8BF184008D241B7AB03515AE9F73CEB3
- ^ https://www.sanofi.com/-/media/Project/One-Sanofi-Web/Websites/Global/Sanofi-COM/Home/en/investors/docs/press-releases/Q42018results.pdf?la=en&hash=CDCE30350F0C658C000A909535AD9AF636A93560
- ^ https://www.sanofi.com/media/Project/One-Sanofi-Web/sanofi-com/en/investors/docs/press-releases/Press_release_Q4_FY_2017.pdf
- ^ https://en.sanofi.com/Images/49288_20-F_2016.pdf
- ^ https://en.sanofi.com/Images/45889_Sanofi_20-F_2015_V2.pdf
- ^ https://en.sanofi.com/Images/38473_Sanofi_20-F_2014.pdf
- ^ https://en.sanofi.com/Images/35795_20F_SANOFI_2013.pdf
- ^ https://en.sanofi.com/Images/31972_20-F_2012_V2.pdf
- ^ https://en.sanofi.com/Images/29804_20F_2011.pdf
- ^ https://investors.abbvie.com/news-releases/news-release-details/abbvie-reports-third-quarter-2019-financial-results
- ^ "AbbVie Reports Full-Year and Fourth-Quarter 2018 Financial Results - AbbVie News Center". news.abbvie.com.
- ^ "Financial Release - AbbVie". investors.abbvie.com.
- ^ "Financial Release - AbbVie". investors.abbvie.com.
- ^ "Financial Release - AbbVie". investors.abbvie.com.
- ^ "Financial Release - AbbVie". investors.abbvie.com.
- ^ "Financial Release - AbbVie". investors.abbvie.com.
- ^ https://www.biospace.com/article/releases/abbott-reports-fourth-quarter-2019-results-announces-strong-forecast-for-2020/?s=72
- ^ "Abbott Reports 2018 Results and Issues Strong Forecast for 2019". BioSpace.
- ^ Abbott. "Abbott Reports Fourth-Quarter 2017 Results". www.prnewswire.com.
- ^ Abbott. "Abbott Reports Fourth-Quarter 2016 Results". www.prnewswire.com.
- ^ "Abbott Reports Fourth-Quarter 2015 Results".
- ^ "Abbott Reports Fourth-Quarter 2014 Results".
- ^ Abbott. "Abbott Reports Fourth-Quarter and Full-Year 2013 Results". www.prnewswire.com.
- ^ "Abbott Reports Fourth-Quarter and Full-Year 2012 Results".
- ^ "Abbott Hosts Conference Call for Fourth-Quarter and Full-Year 2011 Earnings - FiercePharma". www.fiercepharma.com.
- ^ https://www.biospace.com/article/releases/thermo-fisher-scientific-reports-fourth-quarter-and-full-year-2019-results/?s=72
- ^ https://www.biospace.com/article/releases/thermo-fisher-scientific-reports-fourth-quarter-and-full-year-2019-results/?s=72
- ^ https://ir.thermofisher.com/investors/news-and-events/news-releases/news-release-details/2018/Thermo-Fisher-Scientific-Reports-Fourth-Quarter-and-Full-Year-2017-Results/default.aspx
- ^ https://ir.thermofisher.com/investors/news-and-events/news-releases/news-release-details/2017/Thermo-Fisher-Scientific-Reports-Fourth-Quarter-and-Full-Year-2016-Results/default.aspx
- ^ https://ir.thermofisher.com/investors/news-and-events/news-releases/news-release-details/2016/Thermo-Fisher-Scientific-Reports-Record-Fourth-Quarter-and-Full-Year-2015-Results/default.aspx
- ^ https://ir.thermofisher.com/investors/news-and-events/news-releases/news-release-details/2015/Thermo-Fisher-Scientific-Reports-Strong-Fourth-Quarter-and-Full-Year-2014-Results/default.aspx
- ^ https://ir.thermofisher.com/investors/news-and-events/news-releases/news-release-details/2015/Thermo-Fisher-Scientific-Reports-Strong-Fourth-Quarter-and-Full-Year-2014-Results/default.aspx
- ^ http://thermofisher.mediaroom.com/2013-01-31-Thermo-Fisher-Scientific-Reports-Fourth-Quarter-and-Full-Year-2012-Results
- ^ http://thermofisher.mediaroom.com/2013-01-31-Thermo-Fisher-Scientific-Reports-Fourth-Quarter-and-Full-Year-2012-Results
- ^ https://www.biospace.com/article/releases/lilly-reports-strong-fourth-quarter-and-full-year-2019-financial-results-updates-2020-guidance-for-pending-dermira-acquisition/?s=72
- ^ "Lilly Reports Strong Fourth-Quarter and Full-Year 2018 Financial Results, Lowers 2019 EPS Guidance to Reflect the Pending Acquisition of Loxo Oncology". BioSpace.
- ^ http://files.shareholder.com/downloads/LLY/5951368162x0x970018/15B962F7-AF5A-4FFA-BE13-42206D3A0820/Q4_2017_PressRelease.pdf
- ^ "Lilly Reports Fourth-Quarter and Full-Year 2016 Results (NYSE:LLY)". investor.lilly.com.
- ^ http://files.shareholder.com/downloads/LLY/5951368162x0x871993/5BE670A3-2B82-4876-8471-CA6BC3BD49F8/Lilly_Q4_2015_Press_Release.pdf
- ^ http://files.shareholder.com/downloads/LLY/5951368162x0x806120/8637C572-31C4-402E-A179-5E107A5366B2/Q414_Lilly_Sales_and_Earnings_Press_Release.pdf
- ^ http://files.shareholder.com/downloads/LLY/5951368162x0x721860/2DB60538-94FE-4E96-98D2-DA72CC301EA0/Q413%20Lilly%20Sales%20and%20Earnings%20Press%20Release.pdf
- ^ http://files.shareholder.com/downloads/LLY/5951368162x0x631117/85679233-E13C-4FE7-9431-E97EFFDA6D5D/Q412%20Lilly%20Sales%20and%20Earnings%20Press%20Release.pdf
- ^ http://files.shareholder.com/downloads/LLY/5951368162x0x538046/24A15621-7850-45EC-8E20-30535C3D9FC9/Q411_Lilly_Sales_and_Earnings_Press_Release.pdf
- ^ https://www.biospace.com/article/releases/amgen-reports-fourth-quarter-and-full-year-2019-financial-results/?s=72
- ^ "Amgen - Investors - Press Release". investors.amgen.com.
- ^ "Amgen Reports Fourth Quarter And Full Year 2017 Financial Results". www.amgen.com.
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NjY1NTQ1fENoaWxkSUQ9MzczMzk1fFR5cGU9MQ==&t=1
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NjI2OTYzfENoaWxkSUQ9MzI5ODc3fFR5cGU9MQ==&t=1
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NTc0NTMzfENoaWxkSUQ9Mjc3NjczfFR5cGU9MQ==&t=1
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NTM3Nzc3fENoaWxkSUQ9MjI2ODE2fFR5cGU9MQ==&t=1
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NDk5NjQxfENoaWxkSUQ9NTM5NDU4fFR5cGU9MQ==&t=1
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9MTM0MzEzfENoaWxkSUQ9LTF8VHlwZT0z&t=1
- ^ https://s21.q4cdn.com/104148044/files/doc_financials/quarterly_reports/2019/q3/Q32019-Earnings-Release.pdf
- ^ "Bristol-Myers Squibb Reports Fourth Quarter and Full Year Financial Results - BMS Newsroom". news.bms.com.
- ^ "Bristol-Myers Squibb Reports Fourth Quarter and Full Year Financial Results". investors.bms.com.
- ^ "Bristol-Myers Squibb Reports Fourth Quarter and Full Year 2016 Financial Results - BMS Newsroom". news.bms.com.
- ^ "Bristol-Myers Squibb Reports Fourth Quarter and Full Year 2015 Financial Results - BMS Newsroom". news.bms.com.
- ^ "Bristol-Myers Squibb Reports Fourth Quarter and Full Year 2014 Financial Results - BMS Newsroom". news.bms.com.
- ^ "Bristol-Myers Squibb Reports Fourth Quarter and Full Year 2013 Financial Results - BMS Newsroom". news.bms.com.
- ^ https://s21.q4cdn.com/104148044/files/doc_financials/annual_reports/Bristol-Myers-Squibb-2012AR-lr.pdf
- ^ https://s21.q4cdn.com/104148044/files/doc_financials/annual_reports/BristolMyersSquibb-2011-AnnualReport.pdf
- ^ https://www.biospace.com/article/releases/gilead-sciences-announces-third-quarter-2019-financial-results/?s=72
- ^ "Gilead Sciences Announces Fourth Quarter and Full Year 2018 Financial Results". BioSpace.
- ^ أ ب ت ث ج ح خ "Investor Overview". Gilead Sciences.
- ^ https://www.astrazeneca.com/content/dam/az/PDF/2019/q3/Year-to-date_and_Q3_2019_Results_announcement.pdf
- ^ https://www.astrazeneca.com/content/dam/az/PDF/2018/full-year/Full-Year_2018_Results_announcement.pdf
- ^ https://www.astrazeneca.com/content/dam/az/PDF/2017/Full-Year/Full-Year%202017%20Results%20announcement%20.pdf
- ^ https://www.astrazeneca.com/content/dam/az/PDF/Full_year_and_q4_2016_results/Full_Year_and_Q4_2016_Results_announcement.pdf
- ^ "Full-Year and Q4 2015 Results". www.astrazeneca.com.
- ^ "AstraZeneca PLC fourth quarter and full year results 2014". www.astrazeneca.com.
- ^ "AstraZeneca PLC fourth quarter and full year results 2013 - AstraZeneca". www.astrazeneca.com.
- ^ "AstraZeneca PLC Fourth quarter and full year results 2012". www.astrazeneca.com.
- ^ "AstraZeneca PLC Fourth quarter and full year results 2011". www.astrazeneca.com.
- ^ https://s22.q4cdn.com/366566841/files/doc_financials/2019/quarterly/Q1-2019-PR-tables.pdf
- ^ https://s24.q4cdn.com/720828402/files/doc_downloads/doc_financial/2018/q4/Teva-Form-10-K-2018.pdf
- ^ "Teva Reports 2017 Full Year and Fourth Quarter Financial Results".
- ^ http://www.tevapharm.com/news/teva_reports_full_year_and_fourth_quarter_2016_financial_results_02_17.aspx
- ^ http://www.tevapharm.com/news/teva_reports_full_year_2015_and_fourth_quarter_financial_results_02_16.aspx
- ^ "Teva Reports Fourth Quarter and Full Year 2014 Results". www.tevapharm.com.
- ^ http://www.tevapharm.com/news/teva_reports_fourth_quarter_and_full_year_2013_results_02_14.aspx
- ^ "Teva Reports Fourth Quarter and Full Year 2012 Results". tevapharm.com.
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9MTI2NDkwfENoaWxkSUQ9LTF8VHlwZT0z&t=1
- ^ http://annualreport.boehringer-ingelheim.com/fileadmin/Download-Center/BI_GB_18_en_ohne_Unterschriften.pdf
- ^ "Boehringer Ingelheim 2017 Annual Report" (PDF). www.boehringer-ingelheim.com.
- ^ أ ب ت ث ج ح "Boehringer Ingelheim total revenue 2007-2017 - Statistic". Statista.
- ^ https://www.takeda.com/newsroom/newsreleases/2019/takeda-reports-fy2018-full-year-results-and-issues-fy2019-guidance/
- ^ "Takeda reports FY2017 full year results and issues FY2018 guidance". www.takeda.com.
- ^ https://www.merckgroup.com/content/dam/web/corporate/non-images/investors/reports-and-financials/earnings-materials/2019-q2/en/2019-Q2-Press-Release-EN.pdf
- ^ "Q4/FY Results of 2018 - News - Merck KGaA, Darmstadt, Germany". www.emdgroup.com.
- ^ أ ب ت ث "404 page - EMD Group". www.emdgroup.com.
{{cite web}}: Cite uses generic title (help) - ^ http://ar2016.merckgroup.com/sites/default/files/downloads/en/merck_annual_report_2016.pdf
- ^ http://ar2015.emdgroup.com/sites/default/files/downloads/emd/Merck_GB2015_EN.pdf
- ^ http://ar2014.merckgroup.com/sites/default/files/downloads/en/Merck_GB2014_EN.pdf
- ^ https://www.novonordisk.com/content/dam/Denmark/HQ/investors/irmaterial/quarterly_financial_reports/2019/20191101_Financial%20statement%20Q3%202019.pdf
- ^ https://www.novonordisk.com/content/dam/Denmark/HQ/investors/irmaterial/quarterly_financial_reports/2019/20190201_Financial%20statement%20Q4%202018_UK.pdf
- ^ "News details". www.novonordisk.com.
- ^ https://www.novonordisk.com/content/dam/Denmark/HQ/investors/irmaterial/quarterly_financial_reports/2017/20170202_Financial%20statement_FY%202016_UK.pdf
- ^ Transcripts, SA (3 February 2016). "Novo Nordisk's (NVO) CEO Lars Rebien Sorensen on Q4 2015 Results - Earnings Call Transcript".
- ^ Transcripts, SA (30 January 2015). "Novo Nordisk's (NVO) CEO Lars Sorensen on Q4 2014 Results - Earnings Call Transcript".
- ^ Transcripts, SA (31 January 2014). "Novo Nordisk A/S Management Discusses Q4 2013 Results - Earnings Call Transcript".
- ^ Transcripts, SA (31 January 2013). "Novo Nordisk's CEO Discusses Q4 2012 Results - Earnings Call Transcript".
- ^ http://www.novonordisk.co.uk/content/dam/Denmark/HQ/Commons/documents/Novo-Nordisk-AR-2011-en.pdf
- ^ https://www.allergan.com/investors/quarterly-results
- ^ "Allergan Reports Fourth Quarter and Full-Year 2018 Financial Results". BioSpace.
- ^ أ ب ت https://www.allergan.com/news/news/thomson-reuters/allergan-reports-solid-finish-to-2017
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NTczMDc2fENoaWxkSUQ9Mjc1MzEzfFR5cGU9MQ==&t=1
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NTM5MDk2fENoaWxkSUQ9MjI4NjI0fFR5cGU9MQ==&t=1
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9MTc3MTM2fENoaWxkSUQ9LTF8VHlwZT0z&t=1
- ^ http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NDYwMzczfENoaWxkSUQ9NDg4Mzk1fFR5cGU9MQ==&t=1
- ^ https://www.biospace.com/article/releases/danaher-reports-third-quarter-2019-results/?s=72
- ^ http://investors.danaher.com/download/Danaher_Annual_Report_2018.pdf
- ^ http://investors.danaher.com/download/danaher_2017_annualreport.pdf
- ^ http://investors.danaher.com/download/Danaher_2016+Annual+Report.pdf
- ^ http://investors.danaher.com/download/2015+Danaher+Annual+Report.pdf
- ^ http://investors.danaher.com/download/DHR_AR_2014.pdf
- ^ http://investors.danaher.com/download/DHR_AR_2013.pdf
- ^ http://investors.danaher.com/download/DHR_AR_2012.pdf
- ^ http://investors.danaher.com/download/DHR_AR_2011.pdf
- ^ https://s22.q4cdn.com/728481125/files/doc_financials/2019/q3/2019-10-31-Q3-2019-earnings-deck_FINAL.pdf
- ^ "Celgene Reports Fourth Quarter and Full Year 2018 Operating and Financial Results". BioSpace.
- ^ https://investors.biogen.com/static-files/7863b554-d325-44e8-9c2d-ceace9698781
- ^ http://investors.biogen.com/static-files/c0d4fbe2-d4f2-404b-be17-19e770386d6e
- ^ "Biogen's Spinraza: Great Launch, Rough Ride". 25 January 2018 – via www.bloomberg.com.
- ^ http://investors.biogen.com/sites/biogen.investorhq.businesswire.com/files/doc_library/file/Biogen_Annual_Report_2016_on_Form_10K.pdf
- ^ http://investors.biogen.com/sites/biogen.investorhq.businesswire.com/files/doc_library/file/Biogen_Annual_Report_2015_on_Form_10K.pdf
- ^ http://investors.biogen.com/sites/biogen.investorhq.businesswire.com/files/doc_library/file/Biogen_2014_Annual_Report_Web.pdf
- ^ http://investors.biogen.com/sites/biogen.investorhq.businesswire.com/files/doc_library/file/BiogenIdec_AR_2013.pdf
- ^ http://investors.biogen.com/sites/biogen.investorhq.businesswire.com/files/doc_library/file/BiogenIdec_AR_2012.pdf
- ^ http://investors.biogen.com/sites/biogen.investorhq.businesswire.com/files/doc_library/file/2011ar.pdf
- ^ "Astellas Pharma Inc. Annual Report 2018" (PDF). www.astellas.com.
- ^ https://www.biospace.com/article/releases/labcorp-announces-2019-third-quarter-results-and-updates-2019-guidance/?s=72
- ^ أ ب ت ث ج http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9NDE2OTE0fENoaWxkSUQ9LTF8VHlwZT0z&t=1&cb=636873221632383468
- ^ أ ب ت http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9MjI4ODI1fENoaWxkSUQ9LTF8VHlwZT0z&t=1
- ^ https://s22.q4cdn.com/911189824/files/doc_presentations/2019/10/Q3-2019-BAX-PRELIMINARY-RESULTS-FINANCIAL-SCHEDULES-(FINAL).pdf
- ^ أ ب https://s22.q4cdn.com/911189824/files/doc_financials/quarterly/2018/q4/Q4-2018-BAX-FINANCIAL-SCHEDULES-(FINAL).pdf
- ^ https://s22.q4cdn.com/911189824/files/doc_financials/quarterly/2017/q4/Q4-2017-BAX-FINANCIAL-SCHEDULES-(FINAL).pdf
- ^ https://s22.q4cdn.com/911189824/files/doc_financials/quarterly/2016/q4/Q4-2016-Financial-Schedules.pdf
- ^ https://s22.q4cdn.com/911189824/files/doc_financials/quarterly/2015/q4/Q4-2015-Financial-Schedules.pdf
- ^ https://s22.q4cdn.com/911189824/files/doc_financials/quarterly/2014/q4/Q4-2014-FINAL-Financial-Schedules.pdf
- ^ أ ب https://s22.q4cdn.com/911189824/files/doc_downloads/financial_schedules/2012/Reclassified-Sales-Final.pdf
- ^ https://www.biospace.com/article/releases/mylan-reports-second-quarter-2019-results/?s=72
- ^ أ ب ت ث ج http://investor.mylan.com/static-files/ed066de0-8491-4327-a044-9bb136d5b8c3
- ^ أ ب ت http://investor.mylan.com/static-files/29cc2678-5735-461a-9972-6ac01dfce6c4
- ^ Goldacre, Ben (2014). Bad pharma : how drug companies mislead doctors and harm patients (First American Paperback ed.). ISBN 9780865478060.
- ^ Kaufman, Marc (2005-05-06). "Merck CEO Resigns as Drug Probe Continues". Washington Post. Retrieved 2007-05-23.
- ^ "Drug Lobby Second to None: How the pharmaceutical industry gets its way in Washington". publicintegrity.org. 2005-07-07. Retrieved 2007-05-23.
- ^ Moynihan, R. (29 May 2003). "Drug company sponsorship of education could be replaced at a fraction of its cost". BMJ. 326 (7400): 1163. doi:10.1136/bmj.326.7400.1163. PMC 1126044. PMID 12775595.
- ^ "Dr. No Free Lunch". Mother Jones. Retrieved 19 May 2016.
- ^ Moynihan, Ray; Cassels, Alan (2005). Selling sickness : how the drug companies are turning us all into patients. Crows Nest, N.S.W.: Allen & Unwin. ISBN 978-1-74114-579-3.
- ^ "A Collection of Articles on Disease Mongering". Public Library of Science. Archived from the original on 7 يونيو 2007. Retrieved 23 مايو 2007.
- ^ "Pharmaceutical Market Research, Trends And Analysis Reports". www.literated.com. Retrieved 17 January 2016.
- ^ "UK parliamentarians put the pharma industry under the spotlight". European Public Health Alliance. Retrieved 2007-05-23.
- ^ Buchkowsky, SS; Jewesson, PJ (Apr 2004). "Industry sponsorship and authorship of clinical trials over 20 years". Ann Pharmacother. 38 (4): 579–85. doi:10.1345/aph.1D267. PMID 14982982.
- ^ Perlis RH, Perlis CS, Wu Y, Hwang C, Joseph M, Nierenberg AA (October 2005). "Industry sponsorship and financial conflict of interest in the reporting of clinical trials in psychiatry". Am J Psychiatry. 162 (10): 1957–60. doi:10.1176/appi.ajp.162.10.1957. PMID 16199844.
- ^ Tungaraza, T; Poole, R (Jul 2007). "Influence of drug company authorship and sponsorship on drug trial outcomes". Br J Psychiatry. 191 (1): 82–3. doi:10.1192/bjp.bp.106.024547. PMID 17602130.
- ^ Healy, D (2006). "The Latest Mania: Selling Bipolar Disorder". PLoS Med. 3 (4): e185. doi:10.1371/journal.pmed.0030185. PMC 1434505. PMID 16597178.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Cosgrove, Lisa; Krimsky, Sheldon; Vijayaraghavan, Manisha; Schneider, Lisa (2006). "Financial Ties between DSM-IV Panel Members and the Pharmaceutical Industry". Psychotherapy and Psychosomatics. 75 (3): 154–160. doi:10.1159/000091772. PMID 16636630.
- ^ "Open Payments". February 2019.
- ^ Lipton, Eric; Thomas, Katie (2017-05-29). "Drug Lobbyists' Battle Cry Over Prices: Blame the Others". New York Times. Retrieved 2017-05-30.
- ^ أ ب Goldacre, Ben (2014). Bad pharma : how drug companies mislead doctors and harm patients (First American Paperback ed.). pp. 123–124. ISBN 9780865478060.
- ^ "www.whitehouse.gov" (PDF).
- ^ "Financial Crimes to the Public Report 2006". FBI. 2006.
- ^ "FBI-Health Care Fraud". FBI.
- ^ "Department of Justice". Department of Justice. 2015-03-19.
- ^ Duff Wilson (2 October 2010). "Side Effects May Include Lawsuits". New York Times.
- ^ "GlaxoSmithKline". BBC News. 4 July 2012.
- ^ "GlaxoSmithKline Agrees to Pay $3 Billion in U.S. Drug Settlement". Bloomberg. 2 July 2012.
- ^ Fred Mogul (2 يوليو 2012). "NY to Get Millions in GlaxoSmithKlein Settlement". WNYC. Archived from the original on 19 أبريل 2013. Retrieved 2 يوليو 2012.
- ^ "BBC News -GlaxoSmithKline to pay $3bn in US drug fraud scandal". BBC Online. 2012-07-02. Retrieved 2 July 2012.
- ^ Thomas, Katie; Schmidt, Michael S. (2 July 2012). "Glaxo Agrees to Pay $3 Billion in Fraud Settlement". The New York Times. Retrieved 3 July 2012.
{{cite news}}: Unknown parameter|lastauthoramp=ignored (|name-list-style=suggested) (help) - ^ "Rapidly Increasing Criminal and Civil Penalties Against the Pharmaceutical Industry: 1991-2010". www.citizen.org. Retrieved 19 May 2016.
- ^ Thomas, Katie; Schmidt, Michael S. (2012-07-02). "GlaxoSmithKline Agrees to Pay $3 Billion in Fraud Settlement". The New York Times.
- ^ "GlaxoSmithKline to Plead Guilty and Pay $3 Billion to Resolve Fraud Allegations and Failure to Report Safety Data". 2012-07-02.
- ^ "JUSTICE DEPARTMENT ANNOUNCES LARGEST HEALTH CARE FRAUD" (PDF). US department of Justice. Retrieved 19 May 2016.
- ^ "Abbott Labs to Pay $1.5 Billion to Resolve Criminal & Civil Investigations of Off-label Promotion of Depakote". 2012-05-07.
- ^ "#09-038: Eli Lilly and Company Agrees to Pay $1.415 Billion to Resolve Allegationsof Off-label Promotion of Zyprexa (2009-01-15)".
- ^ انظر على سبيل المثال: 'ر هوين ، إلين. "تريبس ، براءات الاختراع الدوائية ، والوصول إلى الأدوية الأساسية: طريق طويل من سياتل إلى الدوحة". Chicago Journal of International Law ، 27 (43)، 2002؛ موسونجو ، سيسول إف ، وسيسيليا أوه. "استخدام مواطن المرونة في اتفاق تريبس من جانب البلدان النامية: هل يمكنها إتاحة الوصول إلى الأدوية؟" لجنة حقوق الملكية الفكرية والابتكار والصحة العامة ، منظمة الصحة العالمية ، 2005.
- ^ "Declaration on the TRIPS agreement and public health". World Trade Organization. Retrieved 19 May 2016.
- ^ "GlaxoSmithKline to 'drop patents in poor countries for better drug access'". BBC News. Retrieved 19 May 2016.
- ^ "Bumper Year for Corporate Donations Reveals Profit Motives". www.corpwatch.org.
- ^ Pfizer Will Donate Fluconazole to South Africa
- ^ "Corporate Responsibility: Novartis". www.novartis.com. Retrieved 19 May 2016.
قالب:Pharmaceutical industry by country
خطأ استشهاد: وسوم <ref> موجودة لمجموعة اسمها "N"، ولكن لم يتم العثور على وسم <references group="N"/>
- CS1 errors: unsupported parameter
- CS1 maint: unflagged free DOI
- CS1 maint: DOI inactive as of يناير 2020
- CS1 errors: generic title
- جميع الصفحات التي تحتاج تنظيف
- مقالات بالمعرفة تحتاج توضيح from June 2015
- Articles with unsourced statements from November 2015
- Wikipedia articles in need of updating from July 2018
- All Wikipedia articles in need of updating
- Articles with unsourced statements from June 2015
- Articles with hatnote templates targeting a nonexistent page
- شركات مدرجة في بورصة نيويورك
- شركات مدرجة في بورصة فرانكفورت
- Companies listed on NASDAQ
- مقالات ذات منظور ثقافي جغرافي محدود
- Pages with empty portal template
- صناعات دوائية
- علم الأدوية
- Pharmacy