غلاف تكافؤ
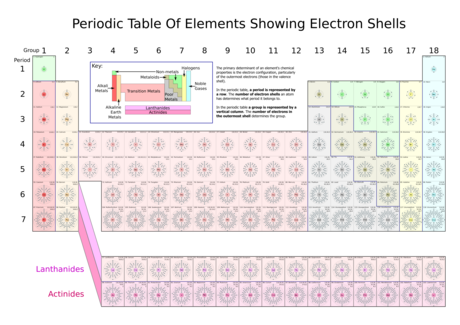
غلاف التكافؤ Electron shell هو الغلاف الأخير في الذرة ، والذى يحتوى على الإلكترونات التى تساهم في أى تفاعل تدخل فيه الذرة ، والتفاعلات التى تحدث بين الروابط بين الذرات . تسمى الإلكترونات التى توجد في غلاف التكافؤ بإلكترونات التكافؤ . وقد كان الكيميائي جيلبرت نيوتن لويس هو أول من حاول تطوير النظرية التى تفسر مشاركة إلكترونات غلاف التكافؤ في الروابط الكيميائية . وقد قام لينوس باولينج بتعميم وتمديد النظرية بعد ظهور ميكانيكا الكم.
تميل الغازات النبيلة لأن يكون بها 8 إلكترونات في الغلاف الخارجي ( فيما عدا الهيليوم ، والذى يملأ غلافه الخارجى 2 إلكترون ). وهذا يتماشى مع نظرية الثمانيات ( تسمى أيضا ثمانيات نيولاندز ) والتى يمكن أن تطبق على عناصر الدورة الثالثة والرابعة. ومن منطلق المدارات الذرية فإن الإلكترونات الثمانية الموجودة في غلاف التكافؤ موزعة في كلآتى 2 في المدار s ، و 2 في كل من مدارات p الثلاثة .
المركبات العضوية المعدنية التى تضم الفلزات الإنتقالية, يتكون غلاف التكافؤ من إلكترونات المدار s ، p ، والتى تبلغ 8 إلكترونات ، كما ان لها 10 إلكترونات موزعة 2 في كل من المدارات d الخمسة والتى تصبح 18 إلكترون والتى تكون غلاف مكتمل لهذه العناصر . والتى ترجع لنظرية الثمانية عشر .
الأغلفة الفرعية
| Subshell label | ℓ | Max electrons | Shells containing it | Historical name |
|---|---|---|---|---|
| s | 0 | 2 | Every shell | sharp |
| p | 1 | 6 | 2nd shell and higher | principal |
| d | 2 | 10 | 3rd shell and higher | diffuse |
| f | 3 | 14 | 4th shell and higher | fundamental |
| g | 4 | 18 | 5th shell and higher (theoretically) | (next in alphabet after f, excluding j)[1] |
عدد الإلكترونات في كل غلاف
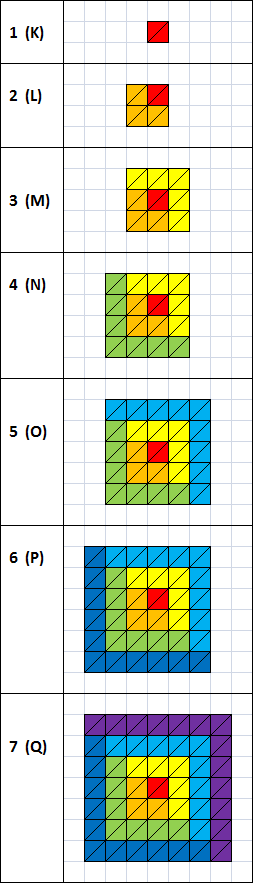
| Shell name |
Subshell name |
Subshell max electrons |
Shell max electrons |
|---|---|---|---|
| K | 1s | 2 | 2 |
| L | 2s | 2 | 2 + 6 = 8 |
| 2p | 6 | ||
| M | 3s | 2 | 2 + 6 + 10 = 18 |
| 3p | 6 | ||
| 3d | 10 | ||
| N | 4s | 2 | 2 + 6 + 10 + 14 = 32 |
| 4p | 6 | ||
| 4d | 10 | ||
| 4f | 14 | ||
| O | 5s | 2 | 2 + 6 + 10 + 14 + 18 = 50 |
| 5p | 6 | ||
| 5d | 10 | ||
| 5f | 14 | ||
| 5g | 18 |
Each subshell is constrained to hold 4ℓ + 2 electrons at most, namely:
- Each s subshell holds at most 2 electrons
- Each p subshell holds at most 6 electrons
- Each d subshell holds at most 10 electrons
- Each f subshell holds at most 14 electrons
- Each g subshell holds at most 18 electrons
غلاف التكافؤ
The valence shell is the outermost shell of an atom. Valence electrons in non-transition metal elements reside in this shell. Such elements with complete valence shells (noble gases) are the most chemically non-reactive, while those with only one electron in their valence shells (alkali metals) or just missing one electron from having a complete shell (halogens) are the most reactive.[2]
قائمة العناصر مع عدد الإلكترونات للغلاف
The list below gives the elements arranged by increasing atomic number and shows the number of electrons per shell. At a glance, one can see that subsets of the list show obvious patterns. In particular, the seven elements (in electric blue) before a noble gas (group 18, in yellow) higher than helium have the number of electrons in the valence shell in arithmetic progression. (However, this pattern may break down in the seventh period due to relativistic effects.)
Sorting the table by chemical group shows additional patterns, especially with respect to the last two outermost shells. (Elements 57 to 71 belong to the lanthanides, while 89 to 103 are the actinides.)
The list below is primarily consistent with the Aufbau principle. However, there are a number of exceptions to the rule; for example palladium (atomic number 46) has no electrons in the fifth shell, unlike other atoms with lower atomic number. Some entries in the table are uncertain, when experimental data is unavailable. (For example, the elements past 108 have such short half-lives that their electron configurations have not yet been measured.)
| Z | Element | No. of electrons/shell | Group |
|---|---|---|---|
| 1 | هيدروجين | 1 | 1 |
| 2 | Helium | 2 | 18 |
| 3 | Lithium | 2, 1 | 1 |
| 4 | Beryllium | 2, 2 | 2 |
| 5 | Boron | 2, 3 | 13 |
| 6 | Carbon | 2, 4 | 14 |
| 7 | Nitrogen | 2, 5 | 15 |
| 8 | Oxygen | 2, 6 | 16 |
| 9 | Fluorine | 2, 7 | 17 |
| 10 | Neon | 2, 8 | 18 |
| 11 | Sodium | 2, 8, 1 | 1 |
| 12 | Magnesium | 2, 8, 2 | 2 |
| 13 | Aluminium | 2, 8, 3 | 13 |
| 14 | Silicon | 2, 8, 4 | 14 |
| 15 | Phosphorus | 2, 8, 5 | 15 |
| 16 | Sulfur | 2, 8, 6 | 16 |
| 17 | Chlorine | 2, 8, 7 | 17 |
| 18 | Argon | 2, 8, 8 | 18 |
| 19 | Potassium | 2, 8, 8, 1 | 1 |
| 20 | Calcium | 2, 8, 8, 2 | 2 |
| 21 | Scandium | 2, 8, 9, 2 | 3 |
| 22 | Titanium | 2, 8, 10, 2 | 4 |
| 23 | Vanadium | 2, 8, 11, 2 | 5 |
| 24 | Chromium | 2, 8, 13, 1 | 6 |
| 25 | Manganese | 2, 8, 13, 2 | 7 |
| 26 | Iron | 2, 8, 14, 2 | 8 |
| 27 | Cobalt | 2, 8, 15, 2 | 9 |
| 28 | Nickel | 2, 8, 16, 2 | 10 |
| 29 | Copper | 2, 8, 18, 1 | 11 |
| 30 | Zinc | 2, 8, 18, 2 | 12 |
| 31 | Gallium | 2, 8, 18, 3 | 13 |
| 32 | Germanium | 2, 8, 18, 4 | 14 |
| 33 | Arsenic | 2, 8, 18, 5 | 15 |
| 34 | Selenium | 2, 8, 18, 6 | 16 |
| 35 | Bromine | 2, 8, 18, 7 | 17 |
| 36 | Krypton | 2, 8, 18, 8 | 18 |
| 37 | Rubidium | 2, 8, 18, 8, 1 | 1 |
| 38 | Strontium | 2, 8, 18, 8, 2 | 2 |
| 39 | Yttrium | 2, 8, 18, 9, 2 | 3 |
| 40 | Zirconium | 2, 8, 18, 10, 2 | 4 |
| 41 | Niobium | 2, 8, 18, 12, 1 | 5 |
| 42 | Molybdenum | 2, 8, 18, 13, 1 | 6 |
| 43 | Technetium | 2, 8, 18, 13, 2 | 7 |
| 44 | Ruthenium | 2, 8, 18, 15, 1 | 8 |
| 45 | Rhodium | 2, 8, 18, 16, 1 | 9 |
| 46 | Palladium | 2, 8, 18, 18 | 10 |
| 47 | Silver | 2, 8, 18, 18, 1 | 11 |
| 48 | Cadmium | 2, 8, 18, 18, 2 | 12 |
| 49 | Indium | 2, 8, 18, 18, 3 | 13 |
| 50 | Tin | 2, 8, 18, 18, 4 | 14 |
| 51 | Antimony | 2, 8, 18, 18, 5 | 15 |
| 52 | Tellurium | 2, 8, 18, 18, 6 | 16 |
| 53 | Iodine | 2, 8, 18, 18, 7 | 17 |
| 54 | Xenon | 2, 8, 18, 18, 8 | 18 |
| 55 | Caesium | 2, 8, 18, 18, 8, 1 | 1 |
| 56 | باريوم | 2, 8, 18, 18, 8, 2 | 2 |
| 57 | Lanthanum | 2, 8, 18, 18, 9, 2 | 3 |
| 58 | Cerium | 2, 8, 18, 19, 9, 2 | |
| 59 | Praseodymium | 2, 8, 18, 21, 8, 2 | |
| 60 | Neodymium | 2, 8, 18, 22, 8, 2 | |
| 61 | Promethium | 2, 8, 18, 23, 8, 2 | |
| 62 | Samarium | 2, 8, 18, 24, 8, 2 | |
| 63 | Europium | 2, 8, 18, 25, 8, 2 | |
| 64 | Gadolinium | 2, 8, 18, 25, 9, 2 | |
| 65 | Terbium | 2, 8, 18, 27, 8, 2 | |
| 66 | Dysprosium | 2, 8, 18, 28, 8, 2 | |
| 67 | Holmium | 2, 8, 18, 29, 8, 2 | |
| 68 | Erbium | 2, 8, 18, 30, 8, 2 | |
| 69 | Thulium | 2, 8, 18, 31, 8, 2 | |
| 70 | Ytterbium | 2, 8, 18, 32, 8, 2 | |
| 71 | Lutetium | 2, 8, 18, 32, 9, 2 | |
| 72 | Hafnium | 2, 8, 18, 32, 10, 2 | 4 |
| 73 | Tantalum | 2, 8, 18, 32, 11, 2 | 5 |
| 74 | Tungsten | 2, 8, 18, 32, 12, 2 | 6 |
| 75 | Rhenium | 2, 8, 18, 32, 13, 2 | 7 |
| 76 | Osmium | 2, 8, 18, 32, 14, 2 | 8 |
| 77 | Iridium | 2, 8, 18, 32, 15, 2 | 9 |
| 78 | Platinum | 2, 8, 18, 32, 17, 1 | 10 |
| 79 | Gold | 2, 8, 18, 32, 18, 1 | 11 |
| 80 | Mercury | 2, 8, 18, 32, 18, 2 | 12 |
| 81 | Thallium | 2, 8, 18, 32, 18, 3 | 13 |
| 82 | Lead | 2, 8, 18, 32, 18, 4 | 14 |
| 83 | Bismuth | 2, 8, 18, 32, 18, 5 | 15 |
| 84 | Polonium | 2, 8, 18, 32, 18, 6 | 16 |
| 85 | Astatine | 2, 8, 18, 32, 18, 7 | 17 |
| 86 | Radon | 2, 8, 18, 32, 18, 8 | 18 |
| 87 | Francium | 2, 8, 18, 32, 18, 8, 1 | 1 |
| 88 | Radium | 2, 8, 18, 32, 18, 8, 2 | 2 |
| 89 | Actinium | 2, 8, 18, 32, 18, 9, 2 | 3 |
| 90 | Thorium | 2, 8, 18, 32, 18, 10, 2 | |
| 91 | Protactinium | 2, 8, 18, 32, 20, 9, 2 | |
| 92 | Uranium | 2, 8, 18, 32, 21, 9, 2 | |
| 93 | Neptunium | 2, 8, 18, 32, 22, 9, 2 | |
| 94 | Plutonium | 2, 8, 18, 32, 24, 8, 2 | |
| 95 | Americium | 2, 8, 18, 32, 25, 8, 2 | |
| 96 | Curium | 2, 8, 18, 32, 25, 9, 2 | |
| 97 | Berkelium | 2, 8, 18, 32, 27, 8, 2 | |
| 98 | Californium | 2, 8, 18, 32, 28, 8, 2 | |
| 99 | Einsteinium | 2, 8, 18, 32, 29, 8, 2 | |
| 100 | Fermium | 2, 8, 18, 32, 30, 8, 2 | |
| 101 | Mendelevium | 2, 8, 18, 32, 31, 8, 2 | |
| 102 | Nobelium | 2, 8, 18, 32, 32, 8, 2 | |
| 103 | Lawrencium | 2, 8, 18, 32, 32, 8, 3 | |
| 104 | Rutherfordium | 2, 8, 18, 32, 32, 10, 2 | 4 |
| 105 | Dubnium | 2, 8, 18, 32, 32, 11, 2 | 5 |
| 106 | Seaborgium | 2, 8, 18, 32, 32, 12, 2 | 6 |
| 107 | Bohrium | 2, 8, 18, 32, 32, 13, 2 | 7 |
| 108 | Hassium | 2, 8, 18, 32, 32, 14, 2 | 8 |
| 109 | Meitnerium | 2, 8, 18, 32, 32, 15, 2 (?) | 9 |
| 110 | Darmstadtium | 2, 8, 18, 32, 32, 16, 2 (?) | 10 |
| 111 | Roentgenium | 2, 8, 18, 32, 32, 17, 2 (?) | 11 |
| 112 | Copernicium | 2, 8, 18, 32, 32, 18, 2 (?) | 12 |
| 113 | Nihonium | 2, 8, 18, 32, 32, 18, 3 (?) | 13 |
| 114 | Flerovium | 2, 8, 18, 32, 32, 18, 4 (?) | 14 |
| 115 | Moscovium | 2, 8, 18, 32, 32, 18, 5 (?) | 15 |
| 116 | Livermorium | 2, 8, 18, 32, 32, 18, 6 (?) | 16 |
| 117 | Tennessine | 2, 8, 18, 32, 32, 18, 7 (?) | 17 |
| 118 | Oganesson | 2, 8, 18, 32, 32, 18, 8 (?) | 18 |
انظر أيضاً
الهامش
- ^ Jue, T. (2009). "Quantum Mechanic Basic to Biophysical Methods". Fundamental Concepts in Biophysics. Berlin: Springer. p. 33. ISBN 1-58829-973-2.
{{cite book}}: External link in|chapterurl=|chapterurl=ignored (|chapter-url=suggested) (help) - ^ Chemical Reactions. Vision Learning (26 July 2011). Retrieved on 1 December 2011.
المصادر
- ويكيبيديا الإنجليزية.