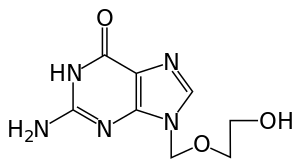
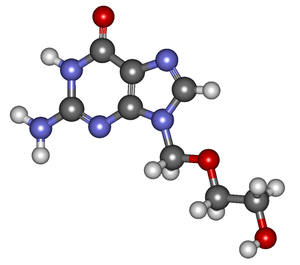
أسيكلوڤير
 | |
 | |
| البيانات السريرية | |
|---|---|
| الأسماء التجارية | زوڤيراكس |
| أسماء أخرى | acycloguanosine |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a681045 |
| License data | |
| فئة السلامة أثناء الحمل |
|
| مسارات الدواء | وريدي، فمي، موضعي |
| رمز ATC | |
| الحالة القانونية | |
| الحالة القانونية | |
| بيانات الحركية الدوائية | |
| التوافر الحيوي | 10–20% (فموي) |
| ارتباط الپروتين | 9–33% |
| الأيض | Viral thymidine kinase |
| Elimination half-life | 2.2–20 ساعة |
| الإخراج | عن طريق البول |
| المعرفات | |
| |
| رقم CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.056.059 |
| Chemical and physical data | |
| التركيب | C8H11N5O3 |
| الكتلة المولية | 225.21 g/mol |
| 3D model (JSmol) | |
| Melting point | 256.5 °C (493.7 °F) |
| |
| |
| (verify) | |
الأسيكلوڤير إنگليزية: aciclovir أو acyclovir ويرمز له بACV، هو أحد أكثر المضادات الڤيروسية شيوعاً، يستخدم بشكل خاص لعلاج عدوى فيروس الهربس البسيط وعلاج عدوى الهربس النطاقي. وللدواء عدد من الأسماء التجارية مثل سيسلوڤير وهرپكس وأسيڤير وأسيڤيراكس وزوڤيراكس وزوڤير.
واعتبر اكتشاف الأسيكلوڤير بداية عصر جديد في تصنيع المضادات الڤيروسية لكونه شديد الخصوصية،[1] وقد حصل مستكشف الدواء گرترود إليون جائزة نوبل في الطب لعام 1988.
الخواص الدوائية
عمل الدواء

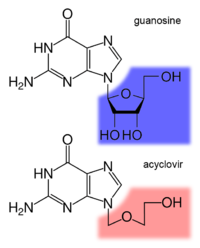
الأسيكلوڤير هو أحد أنواع مضاهئات النوكليوزيد التي تقوم بتعطيل عملية تكاثر الفيروس عن طريق تخريب عملية بناء الرنا للڤيروس. و تتم هذه العملية عندما يتم إضافة مجموعة الفوسفات إلى الأسيكلوڤير عن طريق أحد إنزيمات الڤيروس المعروف بثيميدين كيناز (الإنزيم يتم إنتاجه في الخلايا البشرية إلا إنه أضعف ب3000 مرة من الإنزيم الفيروسي)، و ينتج من هذه العملية الكيميائية أسيكلو-أحادي فسفات الگوانوزين (acyclo-GMP) وتستمر عملية الفسفرة من خلال مجموعة من إنزيمات الكيناز الخلوية ليتنج أسيكلو-ثلاثي فسفات الگوانوزين (acyclo-GTP). ويعتبر أسيكلو-ثلاثي فسفات الگوانوزين مثبط جيد لبوليميراز الرنا مع قدرة لتعطيل البوليميراز الڤيروسي تفوق ب100 مرة قدرته لتعطيل البوليميراز الخلوي.
وباختصار، يعتبر الأسيكلوڤير دواء مبدئي يتم تحويله لمنتج أكثر فاعلية بواسطة الإنزيمات الفيروسية ولبشرية داخل الخلية.
الأحياء الدقيقة
الأسيكلوڤير فعال ضد أغلب مجموعة ڤيروسات الهربس. ويمكن ترتيب فاعلية الڤيروس تنازلياً:[2]
- ڤيروس الهربس البسيط 1 (HSV-1)
- ڤيروس الهربس البسيط 2 (HSV-2)
- ڤيروس نطاقي حماقي (VZV)
- ڤيروس إبشتاين-بار (EBV)
- الڤيروس المضخم للخلايا (CMV) -- الأقل فاعلية
فعالية الدواء محدودة لكل من ڤيروس إبشتاين-بار والڤيروس المضخم للخلايا، كما إنه غير فعال للڤيروسات داخل العقد العصبية. ولم تسجل أي حالات مقاومة للدواء ذات قيمة إكلينيكية، وطرق مقاومة الدواء تشمل نقص إنزيم ثيميدين كيناز لدى الفيروس أو طفرة في إنزيم ثيميدين كيناز أو إنزيم بوليميراز الرنا.[3]
الحرائك الدوائية
الآسيكلوفير شحيح الذوبان في الماء، وقليل التوافر البيولوجي (10-20%) ولهذا يتم إعطاء الدواء من خلال الحقن الوريدية عند الحاجة لتركيز عالٍ من الدواء في الدم. عند أخذ الدواء عن طريق الفم، تصل قمة تركيزه في الدم بعد ساعة إلى ساعتين.
ويبلغ عمر النصف للدواء حوالي 3 ساعات، ويتخلص الجسم منه عن طريق الكلى عن طريق الترشيح الكبيبي والإخراج الأنبوبي.
يمكن تحسين التوافر البيولوجي عن طريق إعطاء المريض لدواء الفالسيكلوفير حيث يتحول في خلايا الكبد رلى أسيكلوڤير وبتوافر بيولوجي يقدر ب55%.
استخدامات الدواء
يستخدم الأسيكلوڤير في عدوى ڤيروس الهربس البسيط والژيروس النطاقي الحماقي، و تشمل على:[4]
- الهربس التناسلي (علاج ووقاية)
- الهربس الشفوي
- هربس نطاقي
- الحالات الحادة من جدري الماء في المرضى منقوصي المناعة
- التهاب الدماغ الهربسي البسيط
- التهابات الهربس البسيط التي تصيب المخاط الجلدي للمرضى منقوصي المناعة
- التهاب القرنية الهربسي البسيط
- التهاب الجفن الهربسي البسيط
- شلل بل
الجرعات الدوائية

أكثر أنواع الأسيكلوڤير شيوعاً هو الأقراص (200 مل و400 مج و800 مل و گارام) ودهان موضعي (5%) وحقن وريدية (25 مل/مل ل.) ومرهم للعين (3%). يستخدم الدهان الموضعي للهربس الشفوي بشكل خاص، بينما تستخدم الحقن الوريدية عند الحاجة لإعطاء كميات مركزة من الدواء.
الآثار الجانبية
كعلاج مجموعي
أكثر الأعراض الجانبية شيوعاً (≥1% من المرضى) والمرتبطة بالعلاج المجموعي للآسيكلوفير (عن طريق الفم أو الحقن الوريدية) تشمل على: غثيان وقيء وإسهال وصداع. وقد يسبب الدواء هلوسة عند الجرعات العالية. وتشمل الأعراض الأقل شيوعاً (0.1–1% من المرضى) على: هياج ودوار ودوخة وآلام المفاصل واحتقان البلعوم وإمساك وآلام البطن وطفح جلدي واستسقاء. وتشمل الأعراض نادرة الحدوث (<0.1% من المرضى) على: غيبوبة ونوبة صرعية وقلة الكريات البيض وقلة الشهية المرضية و التهاب الكبد ومتلازمة ستڤن-جونسون.[4]
كما قد تسبب الحقن الوريدية من الأسيكلوڤير (1% من المرضى) اعتلالاً دماغياً. وجرعات كبيرة من الدواء قد تسبب اعتلالات في وضائف الكلى نتيجة ترسب الدواء على هيئة بلورات في الكلى.[5][6]
كعلاج موضعي
دهان الأسيكلوڤير يسبب لدى أكثر من 1٪ من المرضى تقشر وجفاف في الجلد وإحساس بحرارة في موضع الدواء. كما قد يسبب إحمرار وحكة. كما أن الأعراض الجانبية الشائعة لمرهم الأسيكلوڤير للعين تشمل على إحساس لاسع في العين.[4]
السمية
يجب تجنب استخدام الدواء أثناء الحمل وذلك لتدخله في صنع الرنا، إلا لم تثبت أي حالة امساخ.
انظر أيضاً
المصادر
- ^ de Clercq, Erik; Field, Hugh J (5 October 2005), "Antiviral prodrugs — the development of successful prodrug strategies for antiviral chemotherapy", British Journal of Pharmacology (Wiley-Blackwell) 147 (1), January 2006, doi:, PMID 16284630
- ^ O'Brien JJ, Campoli-Richards DM. Aciclovir. An updated review of its antiviral activity, pharmacokinetic properties and therapeutic efficacy. Drugs 1989;37(3):233-309. PMID 2653790
- ^ Sweetman S, editor. Martindale: The complete drug reference. 34th ed. London: Pharmaceutical Press; 2004. ISBN 0-85369-550-4
- ^ أ ب ت Rossi S, editor. Australian Medicines Handbook 2006. Adelaide: Australian Medicines Handbook; 2006. ISBN 0-9757919-2-3
- ^ Brigden D, Rosling AE, Woods NC (1982). "Renal function after acyclovir intravenous injection". The American Journal of Medicine. 73 (1A): 182–5. PMID 6285711.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - ^ Sawyer MH, Webb DE, Balow JE, Straus SE (1988). "Acyclovir-induced renal failure. Clinical course and histology". The American Journal of Medicine. 84 (6): 1067–71. PMID 3376977.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link)
قراءات إضافة
- Harvey Stewart C. in Remington’s Pharmaceutical Sciences 18th edition: (ed. Gennard, Alfonso R.) Mack Publishing Company, 1990. ISBN 0-912734-04-3.
- Huovinen P., Valtonen V. in Kliininen Farmakologia (ed. Neuvonen et al.). Kandidaattikustannus Oy, 1994. ISBN 951-8951-09-8.
- Périgaud C., Gosselin G., Imbach J. -L.: Nucleoside analogues as chemotherapeutic agents: a review. Nucleosides and nucleotides 1992; 11(2–4)
- Rang H.P., Dale M.M., Ritter J.M.: Pharmacology, 3rd edition. Pearson Professional Ltd, 1995. 2003 (5th) edition ISBN 0-443-07145-4; 2001 (4th) edition ISBN 0-443-06574-8; 1990 edition ISBN 0-443-03407-9.
وصلات خارجية
- CS1 errors: unsupported parameter
- Template:drugs.com link with non-standard subpage
- ECHA InfoCard ID from Wikidata
- Infobox-drug molecular-weight unexpected-character
- Pages using infobox drug with unknown parameters
- Articles containing إنگليزية-language text
- Pages using Lang-xx templates
- منتجات گلاكسو سميث كلاين
- پيورينات
- الأدوية الأساسية حسب منظمة الصحة العالمية
- أدوية مضادة للڤيروسات