كبريتات الصوديوم

| |
| الأسماء | |
|---|---|
| أسماء أخرى | |
| المُعرِّفات | |
| رقم CAS | |
| ECHA InfoCard | 100.028.928 |
| E number | E514(i) (acidity regulators, ...) |
PubChem CID
|
|
| رقم RTECS |
|
CompTox Dashboard (EPA)
|
|
| الخصائص | |
| الصيغة الجزيئية | Na2SO4 |
| كتلة مولية | 142.04 g/mol (anhydrous) 322.20 g/mol (decahydrate) |
| المظهر | white crystalline solid hygroscopic |
| الكثافة | 2.664 g/cm3 (anhydrous) 1.464 g/cm3 (decahydrate) |
| نقطة الانصهار | |
| نقطة الغليان | |
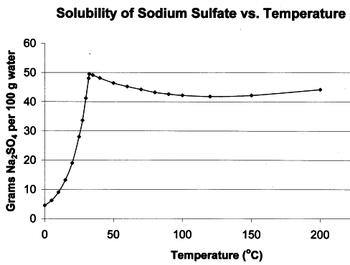
| قابلية الذوبان في الماء | 4.76 g/100 ml (0 °C) 42.7 g/100 ml (100 °C) |
| قابلية الذوبان | insoluble in ethanol |
| معامل الانكسار (nD) | 1.468 (anhydrous) 1.394 (decahydrate) |
| البنية | |
| البنية البلورية | orthorhombic or hexagonal (anhydrous) monoclinic (decahydrate) |
| المخاطر | |
| خطر رئيسي | Irritant |
| NFPA 704 (معيـَّن النار) | |
| نقطة الوميض | Non-flammable |
| مركبات ذا علاقة | |
أنيونات أخرى
|
سيلينات الصوديوم تيلوريت الصوديوم |
كاتيونات أخرى
|
كبريتات الليثيوم كبريتات البوتاسيوم كبريتات الروبيديوم كبريتات السيزيوم |
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |
| مراجع الجدول | |
كبريتات الصوديوم وهو مركب كيميائي له الصيغة Na2SO4، وهو الملح الصوديومي لحمض الكبريت. يمكن أن يتواجد بشكل لامائي ويدعى الشكل الخام منه أثناء إنتاجه بـكعكة الملح، أو متسانداً مع عشرة جزيئات ماء Na2SO4.10H2O ويدعى في هذه الحالة ملح غلاوبر. يتم الحصول على هذا الملح تقريباً بشكل متساوي إما من مصادر طبيعية أو من مصادر صناعية من المنتجات الثانوية لصناعة الرايون، الليثيوم، حمض كلور الماء ومركبات الكروم.
التحضير
من أهم المصادر الصناعية لكبريتات الصوديوم هي النواتج الثانوية لصناعة مركبات الكروم. تتم مفاعلة حمض الكبريت مع كلوريد الصوديوم حسب طريقة مانهايم، حيث يتشكل في البداية بيكبريتات الصوديوم ومن ثم الملح المطلوب وذلك حسب المعادلات التالية:
العملية تجرى بشكل متقطع (Batch process).
توجد طريقة أخرى لتحضير هذا الملح بدرجة أعلى وذلك حسب طريقة هاريغريفز :
تحضير ملح غلاوبر
يحضر ملح غلاوبر Na2SO4.10H2O وذلك بحل كعكة الملح بالمحلول الأم (mother liquor) وبإزالة الشوائب والتصفية ثم إعادة البلورة. يعالج المحلول بالكلس وأملاحه لتعديل الوسط، وبعد إزالة الشوائب الراسبة من أملاح الحديد، المغنسيوم، والكالسيوم يمرر المحلول إلى مبلورات حيث يتم الحصول على البلورات بعد إجراء عملية التثفيل.
الاستخدامات
- الاستهلاك الأعظمي من ملح كبريتات الصوديوم يكون في صناعة عجينة الورق (kraft pulp).
- يستخدم في صناعة المنظفات المنزلية.
- يستخدم في صناعة الزجاج وذلك لإزالة فقاعات الهواء الصغيرة من الزجاج المصهور.
- يستخدم في الصناعات النسيجية حيث يضاف أثناء الصباغة لتقليل الشحن السالبة على الألياف مما يسهل من انتشار الصباغ بشكل متساوي.
المصادر
- shreve´s chemical process industries, fifth edition, ISBN 0-07-057147-3
- [1]
وصلات خارجية
- Pages using Chembox with unknown parameters
- ECHA InfoCard ID from Wikidata
- E number from Wikidata
- Chemical articles with unknown parameter in Chembox
- Articles containing unverified chemical infoboxes
- Chembox image size set
- Short description is different from Wikidata
- كبريتات
- مركبات الصوديوم
- مجففات
- مواد خيميائية
- مقالات تحتوي مقاطع ڤيديو
- كيماويات فوتوغرافية