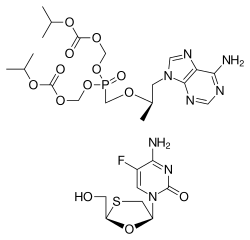
إمتريسيتابين/تنوفوڤير
 | |
 | |
| البيانات السريرية | |
|---|---|
| الأسماء التجارية | Truvada, Tenvir-EM, other |
| أسماء أخرى | Emtricitabine/tenofovir disoproxil fumarate |
| AHFS/Drugs.com | Professional Drug Facts |
| MedlinePlus | a612036 |
| License data | |
| فئة السلامة أثناء الحمل | |
| مسارات الدواء | by mouth |
| رمز ATC | |
| الحالة القانونية | |
| الحالة القانونية | |
| المعرفات | |
| PubChem CID | |
| NIAID ChemDB | |
| (verify) | |
إمتريسيتابين/تنوفوڤير، يُباع تحت الاسم التجاري تروڤادا Truvada، هو دواء يستخدم للعلاج والوقاية من متلازمة نقص المناعة المكتسبة (الإيدز).[2][3] وهو مزيج ذو جرعة ثابتة من اثنين من الأدوية المضادة للفيروسات الرجعية : تينوفوفير ديسوبروكسيل و إمتريسيتابين.[2] للعلاج ، يتم استخدامه إما بمفرده أو مع أدوية أخرى مضادة للفيروسات الرجعية ..[4][5] للوقاية قبل التعرض، في أولئك الذين هم في خطر كبير ، فمن المستحسن ممارسة الجنس الآمن.[4] يعالج متلازمة نقص المناعة المكتسبة / الإيدز.[2] يؤخذ إمتريسيتابين / تينوفوفير عن طريق الفم.[6]
تشمل الآثار الجانبية الشائعة الصداع والإرهاق ومشاكل النوم وآلام البطن وفقدان الوزن والطفح الجلدي.[2] قد تشمل الآثار الجانبية الخطيرة حماض لبني وتضخم الكبد ..[4] لا يبدو أن استخدام هذا الدواء أثناء الحمل يضر بالطفل ، ولكن لم يتم دراسته جيدًا..[1]
تمت الموافقة على إمتريسيتابين/تنوفوڤير للاستخدام الطبي في الولايات المتحدة في عام 2004.[2] هي مدرجة في قائمة الأدوية الأساسية لمنظمة الصحة العالمية ، وهي الأدوية الأكثر أمانًا والأكثر فعالية اللازمة في النظام الصحي.[7] في الولايات المتحدة ، إمتريسيتابين/تنوفوڤير تحت براءة االاختراع حتى عام 2020 ، ولكنه متاح كجنيس في بقية العالم.[8] بلغ التكلفة الجملة لعام 2015 في العالم النامي حوالي 6.06 دولار إلى 7.44 دولار في الشهر
.[6] في الولايات المتحدة ، اعتبارًا من عام 2019 ، تبلغ تكلفة الجملة حوالي 1،710.00 دولارًا أمريكيًا في الشهر
.[9] في أستراليا ، يكلف هذا المبلغ حوالي 8 دولارات أمريكية.[8]
الاستخدامات الطبية
يستخدم إمتريسيتابين/تنوفوڤير لعلاج ومنع متلازمة نقص المناعة المكتسبة / الإيدز.[2] هو قرص يؤخذ عن طريق الفم.[6] توصي معاهد الوطنية للصحة الأمريكية (NIH) بالعلاج المضاد للفيروسات الرجعية (ART) لجميع الأشخاص المصابين بمتلازمة نقص المناعة المكتسبة / الإيدز.[10]
الوقاية من الإيدز
توصي مراكز السيطرة على الأمراض والوقاية منها (CDC) باستخدام إمتريسيتابين/تنوفوڤير للوقاية قبل التعرض (PrEP) للأفراد غير المصابين بمتلازمة نقص المناعة المكتسبة -1 الذين قد يكونون معرضين لخطر الإصابة بمتلازمة نقص المناعة المكتسبة -1 .[11][12][13]وجدت مراجعة كوكرين أن كلا من تنوفوڤير وحده ، وكذلك تركيبة إمتريسيتابين/تنوفوڤير ، قللت من خطر الإصابة بمتلازمة نقص المناعة المكتسبة بنسبة 51 ٪..[14] تمت الموافقة على الوقاية قبل التعرض ضد الإصابة بمتلازمة نقص المناعة المكتسبة في الولايات المتحدة في عام 2012.[15]
توصي مراكز مكافحة الأمراض والوقاية منها (CDC) بالنظر في الوقاية قبل التعرض للمجموعات عالية المخاطر التالية::[16]
- الأفراد في علاقة جنسية مستمرة مع شريك إيجابي لمتلازمة نقص المناعة المكتسبة
- الرجال المثليون أو ثنائيو الجنس الذين مارسوا الجنس الشرجي بدون واقي أو تم تشخيص إصابتهم بأمراض منقولة جنسيًا في الأشهر الستة الماضية.
- الرجال أو النساء من جنسين مختلفين الذين لا يستخدمون الواقي الذكري بانتظام أثناء ممارسة الجنس مع شركاء غير معروفين حالتهم اذا كانوا مصابين بمتلازمة نقص المناعة المكتسبة والذين يشكلون خطرًا كبيرًا
- حقن الأدوية في الأشهر الستة الماضية بمشاركة الادوات
- الشركاء من جنسين مختلفين ومثليين في الجنس حيث يكون أحد الشريكين مصابًا بمتلازمة نقص المناعة المكتسبة والآخر سلبيًا لمتلازمة نقص المناعة المكتسبة
يتضمن النظر في استخدام إمتريسيتابين/تنوفوڤير كاستراتيجية اختزال مناقشة مع أخصائي صحي يمكنه مساعدة المريض في معرفة الفوائد والمخاطر. ينصح المرضى بمناقشة أي تاريخ من مشاكل العظام ، مشاكل الكلى ، من عدوي التهاب الكبد الڤيروسي ب مع مقدم الرعاية الصحية الخاص بهم.[17]
يرى الأشخاص الذين بدأوا في تناول إمتريسيتابين/تنوفوڤير فائدة الحد من متلازمة نقص المناعة المكتسبة حتى 72 ساعة بعد البدء ، ولكن يجب تناول الدواء لمدة ثلاثين يومًا بعد حدث جنسي عالي الخطورة لضمان خفض مستويات انتقال متلازمة نقص المناعة المكتسبة على النحو الأمثل .[18][19] تعتمد فعالية الوقاية قبل التعرض للوقاية من العدوى على قدرة الفرد على تناول الدواء باستمرار.[20]
تروڤادا كما الوقاية قبل التعرض لا ينبغي أن تستخدم للأفراد إيجابية لمتلازمة نقص المناعة المكتسبة -1. [21]
علاج الإيدز
تمت الموافقة على إمتريسيتابين/تنوفوڤير في الولايات المتحدة كجزء من العلاج المركب المضاد للفيروسات القهقهرية لعلاج متلازمة نقص المناعة المكتسبة -1.[4] يُقترح العلاج المركب كأحد الخيارات للبالغين الذين لم يتلقوا أي علاج مسبق لعدوى متلازمة نقص المناعة المكتسبة.[22]
التهاب الكبد الڤيروسي ب
يشار إلى كل من إمتريسيتابين/تنوفوڤير لعلاج التهاب الكبد الڤيروسي ب ، مع فائدة إضافية أنه يمكنهم استهداف متلازمة نقص المناعة المكتسبة لأولئك الذين يعانون من العدوى المشتركة.[23] مكن أيضًا تناول إمتريسيتابين/تنوفوڤير لبعض التهاب الكبد الڤيروسي ب المقاوم لمضاد للفيروسات.[24]
الحمل والرضاعة الطبيعية
في الولايات المتحدة ، يوصى بأن تبدأ جميع النساء الحوامل المصابات بمتلازمة نقص المناعة المكتسبة علاج بمضاد للفيروسات الرجعية (ART) في وقت مبكر من الحمل للحد من خطر انتقال العدوى. لا يزيد العلاج المضاد للفيروسات الرجعية بشكل عام من خطر العيوب الخلقية باستثناء دولوتگراڤير ، الذي لا يوصى به خلال الأشهر الثلاثة الأولى من الحمل فقط بسبب المخاطر المحتملة لعيوب الأنبوب العصبي.[25]
يفرز إمتريسيتابين/تنوفوڤير في حليب الثدي.[26] في البلدان المتقدمة ، يوصى بشكل عام الأمهات المصابات بمتلازمة نقص المناعة المكتسبة بعدم الرضاعة الطبيعية بسبب وجود خطر ضئيل لانتقال متلازمة نقص المناعة المكتسبة من الأم إلي الاطفال.[27][28] Iي البلدان النامية ، حيث قد لا يكون خيار الرضاعة الطبيعية خيارًا ، توصي منظمة الصحة العالمية بنظام دوائي ثلاثي منتنوفوڤير ، إيفافيرينز ، وإما لاميفودين أو إمتريسيتابين.[28]
الآثار الجانبية
إمتريسيتابين/تنوفوڤير جيد التحمل بشكل عام. تشمل بعض آثاره الجانبية ما يلي:[13]
- نادر: الحماض اللبني ، ضعف وظيفة الكبد ، تفاقم عدوى التهاب الكبد الڤيروسي ب
- شائع: الصداع ، آلام البطن ، نقص الوزن ، الغثيان ، الإسهال ، وانخفاض كثافة العظام
قد لوحظ إعادة توزيع الدهون وتراكمها ( الحثل الشحمي ) لدى الأشخاص الذين يتلقون العلاج المضاد للفيروسات الرجعية ، بما في ذلك تخفيض الدهون في الوجه والأطراف والأرداف وزيادة الدهون الحشوية في البطن والتراكم في الجزء العلوي من الظهر.[13] عند استخدامه كوقاية سابقة للتعرض (الوقاية قبل التعرض) ، قد لا يكون هذا التأثير موجودًا..[29] ومع ذلك فقد تم ربط تغيرات الوزن بالدواء.[30]
التداخلات الدوائية
| التداخلات الدوائية | التناول المشترك | |
|---|---|---|
| Tenofovir | دايدانوسين |
|
| Atazanavir |
| |
| Lopinavir/ritonavir, atazanavir coadministered with ritonavir & darunavir coadministered with ritonavir |
| |
| Ledipasvir/sofosbuvir |
| |
| Emtricitabine/tenofovir | P-glycoprotein and breast cancer resistance protein (BCRP) transporters inhibitors |
|
| Drugs may decrease renal function (e.g. adefovir, acyclovir, adefovir, dipivoxil, cidofovir, ganciclovir, valacyclovir, valganciclovir, aminoglycosides, etc.) |
| |
| High-dose or multiple NSAIDs |
| |
| Orlistat |
| |
Other drugs with adverse reactions include dabigatran etexilate, lamivudine, and vincristine. Dabigatran etexilate used with p-glycoprotein inducers require monitoring of decreased levels and effects of dabigatran. Lamivudine may increase the adverse or toxic effect of emtricitabine. Vincristine used with P-glycoprotein/ABCB1 inducers can decrease the serum concentration of vincristine.[32]
المجتمع والثقافة
التكلفة
اعتبارا من 2014[تحديث], the median cost per tablet, in Namibia and South Africa, was US$0٫20.[6] In Canada, emtricitabine/tenofovir cost between $800 - $1,100 per month in 2016.[33] Generic emtricitabine/tenofovir was approved by Health Canada in August 2017, with a wholesale cost of $400 per month.[34] The cost for emtricitabine/tenofovir PrEP in Ontario, Canada dropped significantly after approval in September 2017.[35]
In the United States, اعتبارا من 2016[تحديث], the wholesale cost is about US$1٬415٫00 per month.[36] This increased in 2019 to about US$1,710.00 per month.[9] The price of emtricitabine/tenofovir in the United States has been criticized by activists, who argued in a 2018 The New York Times opinion piece that the high cost keeps the drug out of reach for millions, thus harming efforts to reduce new HIV infections.[37] The Gilead CEO defended the high price at a U.S. House of Representatives committee hearing.[38] Generic emtricitabine/tenofovir was approved in the United States in 2018,[39] and it is scheduled to be released by Teva in September 2020.[40]
Emtricitabine/tenofovir can be dispensed by trained pharmacists in California, without a prescription, for a maximum of 60 days.[41][42][43]
براءة الاختراع
The patent for the drug combination is owned by Gilead Sciences in some regions. The European patent EP0915894B1[44] was due to expire in July 2017, however a case is due[when?] before the European Court of Justice seeking to extend the patent.[45][needs update] An Irish court rejected an injunction request to prevent the launch of generic Emtricitabine/tenofovir prior to the resolution of the case.[46]
In 2019, Gilead Sciences challenged patents held by the United States for the drug combination.[47][48][49]
المصادر
- ^ أ ب ت "Emtricitabine / tenofovir Pregnancy and Breastfeeding Warnings". Drugs.com. 1 August 2018. Archived from the original on 10 October 2019. Retrieved 10 October 2019.
- ^ أ ب ت ث ج ح "Truvada". Drugs.com. Archived from the original on 20 December 2016. Retrieved 12 December 2016.
- ^ "UK label Truvada film-coated tablets". Electronic Medicines Compendium. August 2016. Archived from the original on 2016-12-20.
- ^ أ ب ت ث "Truvada - FDA prescribing information, side effects and uses". www.drugs.com. April 2016. Archived from the original on 20 December 2016. Retrieved 12 December 2016.
- ^ World Health Organization (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). WHO Model Formulary 2008. World Health Organization. p. 160. hdl:10665/44053. ISBN 9789241547659.
- ^ أ ب ت ث "Tenofovir DF+Emtricitabine". International Drug Price Indicator Guide. Management Sciences for Health and World Health Organization. 2014. Retrieved 2015-08-01.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ أ ب "AOC asks pharma CEO why $2,000 HIV drug costs just $8 in Australia". The Independent (in الإنجليزية). 17 May 2019. Retrieved 15 November 2019.
- ^ أ ب "NADAC as of 2019-11-13 | Data.Medicaid.gov". Centers for Medicare and Medicaid Services (in الإنجليزية). Retrieved 15 November 2019.
- ^ "Guidelines for the Use of Antiretroviral Agents in Adults and Adolescents with HIV" (PDF). AIDSinfo Clinical Guidelines. July 2019. Retrieved October 30, 2019.
{{cite web}}: CS1 maint: url-status (link) - ^ "PrEP". Centers for Disease Control and Prevention (CDC). 17 October 2019. Archived from the original on 31 October 2019. Retrieved 31 October 2019.
 هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
- ^ "TRUVADA- emtricitabine and tenofovir disoproxil fumarate tablet, film coated label". DailyMed. 18 May 2018. Archived from the original on 31 October 2019. Retrieved 31 October 2019.
- ^ أ ب ت ث "US Truvada (emtricitabine/tenofovir disoproxil fumarate) label" (PDF). U.S. Food and Drug Administration (FDA). March 2016. Archived (PDF) from the original on 2016-12-21.
- ^ Okwundu CI, Uthman OA, Okoromah CA (2012). "Antiretroviral pre-exposure prophylaxis (PrEP) for preventing HIV in high-risk individuals". Cochrane Database Syst Rev. 7 (7): CD007189. doi:10.1002/14651858.CD007189.pub3. PMID 22786505.
- ^ Perrone, Matthew (16 July 2012). "FDA approves first pill to help prevent HIV". The Seattle Times. Associated Press. Archived from the original on 19 July 2012.
{{cite news}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ "Pre-Exposure Prophylaxis (PrEP)". Archived from the original on 5 June 2015. Retrieved 4 June 2015.
{{cite web}}: CS1 maint: unfit URL (link) هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
- ^ "Administration of pre-exposure prophylaxis against HIV infection". UpToDate. Retrieved 31 October 2019.
- ^ Panlilio AL, Cardo DM, Grohskopf LA, et al. (September 2005). "Updated U.S. Public Health Service guidelines for the management of occupational exposures to HIV and recommendations for postexposure prophylaxis" (PDF). MMWR Recomm Rep. 54 (RR-9): 1–17. PMID 16195697.
- ^ Kuhar DT, Henderson DK, Struble KA, et al. (September 2013). "Updated US Public Health Service guidelines for the management of occupational exposures to human immunodeficiency virus and recommendations for postexposure prophylaxis" (PDF). National Prevention Information Network. 20711.
 هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
- ^ "Pre-exposure prophylaxis of HIV in adults at high risk: Truvada (emtricitabine/tenofovir disoproxil)".
{{cite web}}: CS1 maint: url-status (link) - ^ "Truvada: HIGHLIGHTS OF PRESCRIBING INFORMATION" (PDF).
{{cite web}}: CS1 maint: url-status (link) - ^ "Guidelines for the Use of Antiretroviral Agents in Adults and Adolescents with HIV" (PDF).
{{cite web}}: CS1 maint: url-status (link) - ^ "Update on Prevention, Diagnosis, and Treatment of Chronic Hepatitis B: AASLD 2018 Hepatitis B Guidance" (PDF).
{{cite web}}: CS1 maint: url-status (link) - ^ "Emtricitabine and Tenofovir Disoproxil Fumarate (Professional Patient Advice)". Drugs.com. Retrieved 31 October 2019.
- ^ "Brief What's New in the Guidelines Perinatal". AIDSinfo. Retrieved 2019-10-23.
- ^ "Recommendations for use of antiretroviral drugs in pregnant HIV-1-infected women for maternal health and interventions to reduce perinatal HIV transmission in the United States" (PDF). National Institutes of Health (NIH). Archived (PDF) from the original on 12 April 2014. Retrieved 21 October 2014.
- ^ "Emtricitabine / tenofovir Use During Pregnancy". Drugs.com. Retrieved 23 October 2019.
- ^ أ ب "Tenofovir". Drugs and Lactation Database (LactMed). National Library of Medicine (US). 2006. Retrieved 23 October 2019.
- ^ "PrEP does not raise lipids or alter body fat, safety study finds". Retrieved 2018-02-16.
- ^ Glidden DV, Mulligan K, McMahan V, et al. (July 2018). "Metabolic Effects of Preexposure Prophylaxis With Coformulated Tenofovir Disoproxil Fumarate and Emtricitabine". Clin. Infect. Dis. 67 (3): 411–419. doi:10.1093/cid/ciy083. PMC 6051460. PMID 29415175.
{{cite journal}}: Unknown parameter|lay-url=ignored (help) - ^ "DailyMed - XENICAL- orlistat capsule". dailymed.nlm.nih.gov. Retrieved 2019-10-30.
- ^ Ramanathan S, Shen G, Cheng A, et al. (July 2007). "Pharmacokinetics of emtricitabine, tenofovir, and GS-9137 following coadministration of emtricitabine/tenofovir disoproxil fumarate and ritonavir-boosted GS-9137". J. Acquir. Immune Defic. Syndr. 45 (3): 274–9. doi:10.1097/QAI.0b013e318050d88c. PMID 17414929.
- ^ "Pre-Exposure Prophylaxis (PrEP) as a form of HIV prevention". AIDS Committee of Toronto. Archived from the original on 2016-11-04. Retrieved 2016-11-01.
- ^ "Generic tenofovir + FTC coming to Canada". www.catie.ca. Archived from the original on 30 August 2017. Retrieved 30 August 2017.
- ^ "PrEP in Ontario" (PDF). AIDS Committee of Toronto. 28 September 2017. Archived (PDF) from the original on 31 October 2019. Retrieved 31 October 2019.
- ^ "NADAC as of 2016-12-07". Centers for Medicare and Medicaid Services (CMS). Archived from the original on 21 December 2016. Retrieved 12 December 2016.
- ^ Krellenstein, James; Lord, Aaron; Staley, Peter (16 July 2018). "Why Don't More Americans Use PrEP?". The New York Times. Retrieved 30 July 2018.
{{cite news}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ Grover, Natalie (17 May 2019). "Under fire for Truvada US pricing at House hearing, Gilead chief O'Day touts R&D costs, asserts governments patents are void". Endpoints News. Retrieved 31 October 2019.
{{cite web}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ "2018 First Generic Drug Approvals". U.S. Food and Drug Administration (FDA). 2019-11-01. Archived from the original on 30 October 2019. Retrieved 29 October 2019.
 هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
- ^ "Gilead Sciences Form 10-Q Quarterly Filing". Gilead Sciences. 31 March 2019. Archived from the original on 30 October 2019. Retrieved 29 October 2019.
- ^ Metz, Sam (7 October 2019). "Newsom signs bill allowing California pharmacists to give PrEP and PEP for HIV prevention". The Desert Sun. Retrieved 9 October 2019.
{{cite web}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ Zraick, Karen; Garcia, Sandra E. (9 October 2019). "California Makes H.I.V.-Prevention Drugs Available Without a Prescription". The New York Times. Retrieved 9 October 2019.
{{cite news}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ "Senate Bill No. 159 HIV: preexposure and postexposure prophylaxis". California Legislative Information. 8 October 2019. Retrieved 9 October 2019.
- ^ "EP0915894B1 - NUCLEOTIDE ANALOGS". Espacenet. Retrieved 13 December 2017.
- ^ "Gilead in row with generics manufacturers over HIV drug in Ireland". The Irish Times. Retrieved 30 October 2017.
- ^ "Gilead loss of generic HIV drug battle a boost for gay community". The Irish Times. Retrieved 18 May 2018.
- ^ Rowland, Christopher (24 April 2019). "Gilead defied a government HIV patent. The Justice Department has opened a review". The Washington Post. Archived from the original on 31 October 2019. Retrieved 31 October 2019.
{{cite news}}:|archive-date=/|archive-url=timestamp mismatch; 1 نوفمبر 2019 suggested (help); Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ Rowland, Christopher (21 August 2019). "Gilead files challenge to government patents for HIV prevention pill". The Washington Post. Archived from the original on 31 October 2019. Retrieved 29 October 2019.
{{cite news}}:|archive-date=/|archive-url=timestamp mismatch; 1 نوفمبر 2019 suggested (help); Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help) - ^ "Petitions to US Patent and Trademark Office on HIV PrEP Patents". Gilead Sciences (Press release). 21 August 2019. Archived from the original on 30 October 2019. Retrieved 29 October 2019.
وصلات خارجية
- CS1 maint: url-status
- CS1 errors: unsupported parameter
- CS1 maint: unfit URL
- CS1 errors: archive-url
- Template:drugs.com link with non-standard subpage
- Pages using infobox drug with unknown parameters
- Chemical articles without CAS registry number
- Articles without EBI source
- Chemical pages without ChemSpiderID
- Chemical pages without DrugBank identifier
- Articles without KEGG source
- Articles without InChI source
- Articles without UNII source
- Infobox drug tracked parameters
- مقالات فيها عبارات متقادمة منذ 2014
- جميع المقالات التي فيها عبارات متقادمة
- مقالات فيها عبارات متقادمة منذ 2016
- Wikipedia articles in need of updating from August 2018
- All Wikipedia articles in need of updating
- Fixed dose combination (antiretroviral)
- گلعاد للعلوم
- ذيفانات الكبد
- Pre-exposure prophylaxis
- RTT
- الأدوية الأساسية حسب منظمة الصحة العالمية