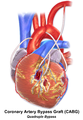
جراحة مجازة الشريان التاجي
| جراحة مجازة الشريان التاجي Coronary artery bypass surgery | |
|---|---|
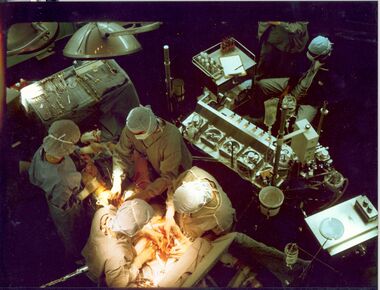 في وقت مبكر من العملية الجراحية لتجاوز الشريان التاجي ، أثناء حصاد الوريد من الساقين (يسار الصورة) وإنشاء مجرى القلب الرئوي عن طريق وضع الأورطي قنية (أسفل الصورة). يوجد [اختصاصي الإرواء] و الجهاز الرئوي للقلب في الجزء العلوي الأيمن. رأس المريض (غير مرئي) في الأسفل | |
| ICD-10-PCS | 021209W |
| ICD-9-CM | 36.1 |
| MeSH | D001026 |
| MedlinePlus | 002946 |
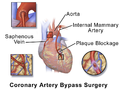
جراحة مجازة الشريان التاجي، أو اختصاراً مجازة القلب أو جراحة المجازة، هو إجراء جراحي لاستعادة تدفق الدم الطبيعي إلى الشريان التاجي المسدود. ينقل الشريان التاجي الطبيعي الدم من وإلى عضلة القلب نفسها ، وليس من خلال الدورة الدموية الرئيسية.
هناك طريقتان رئيسيتان. في أحدهما ، يتم تحويل الشريان الصدري الداخلي الأيسر ، LITA (يُسمى أيضًا الشريان الثديي الداخلي الأيسر ، LIMA) إلى الفرع النازل الأمامي الأيسر للشريان التاجي الأيسر. في هذه الطريقة ، يكون "الشريان" مختلقًا ، مما يعني أنه غير منفصل عن الأصل. في الجانب الآخر ، يتم إزالة الوريد الصافيني الكبير من الساق. يتم ربط أحد الطرفين بالشريان الأورطي أو أحد فروعه الرئيسية ، ويتم ربط الطرف الآخر بالشريان المسدود مباشرة بعد الانسداد لاستعادة تدفق الدم.
يتم إجراء تطعيم تجاوز الشريان التاجي لتخفيف الذبحة الصدرية التي يتم التحكم فيها بشكل غير مرضي عن طريق الحد الأقصى من الأدوية المضادة لنقص الدم الموضعي التي تتحملها ، ومنع أو تخفيف ضعف البطين الأيسر ، و / أو تقليل خطر الوفاة. تطعيم تجاوز الشريان التاجي لا يمنع احتشاء عضلة القلب (نوبة قلبية). عادة ما يتم إجراء هذه الجراحة مع توقف القلب ، مما يستلزم استخدام مجرى القلب الرئوي. ومع ذلك ، يتوفر أيضًا أسلوبان بديلان ، مما يسمح بإجراء تجاوز الشريان التاجي على القلب النابض إما دون استخدام مجرى القلب تجاوز الدورة القلبية الرئوية ، أو إجراء يشار إليه باسم جراحة "خارج المضخة" ، أو إجراء جراحة الضرب باستخدام مساعدة جزئية من مجرى القلب الرئوي ، الإجراء المشار إليه باسم جراحة "الضرب على المضخة". يوفر الإجراء الأخير مزايا إيقاف المضخة داخل المضخة وخارجها مع تقليل آثارها الجانبية.
تجاوز الشريان التاجي غالبًا ما يشار إليه عند انسداد الشرايين التاجية بنسبة 50 إلى 99 في المائة. العائق الذي يتم تجاوزه عادة ما يكون بسبب زيادة سمك الشرايين أو تصلب الشرايين أو كليهما. يتميز تصلب الشرايين بالسمك ، وفقدان المرونة ، وتكلس جدار الشرايين ، مما يؤدي في معظم الأحيان إلى تضييق عام في الشريان التاجي المتأثر. يتميز تصلب الشرايين بلوحات صفراء من الكوليسترول والدهون والحطام الخلوي المودعة في الطبقة الداخلية لجدار الشريان التاجي الكبير أو المتوسط الحجم ، مما يؤدي في معظم الأحيان إلى انسداد جزئي في الشريان المصاب. كلتا الحالتين يمكن أن تحد من تدفق الدم إذا تسببت في تضييق مقطعي بنسبة 50 في المائة على الأقل..
المصطلح
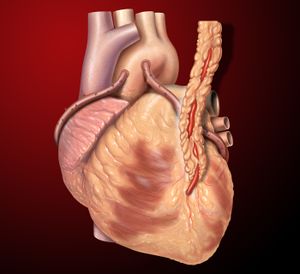
هناك العديد من الاختلافات في المصطلحات ، حيث يتم استبعاد واحد أو أكثر من "الشريان" أو "الالتفافية" أو "التجاوز". أكثر الاختصارات استخدامًا لهذا النوع من الجراحة هو CABG (ينطق "كاباج") ، بصيغة الجمع لـ CABGs (تنطق "كابجس"),[1] . في البداية ، استخدم مصطلح الالتفافية الأبهرية (ACB) بشكل أكثر شيوعًا لوصف هذا الإجراء. يجب عدم الخلط بين CAGS (جراحة الكسب غير المشروع الشريان التاجي ، عند نطقها صوتيا) مع تصوير الأوعية التاجية (CAG).[2]
عدد الشرايين المتجاوزة
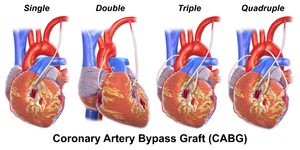
يشير المصطلح "تجاوز الفردي" ، "تجاوز مزدوج" ، "تجاوز ثلاثي" ، "تجاوز الرباعي" و "تجاوز الخماسي" إلى عدد الشرايين التاجية التي تم تجاوزها في الإجراء. بمعنى آخر ، يعني الالتفافية المزدوجة أنه يتم تجاوز شريانين تاجيين (على سبيل المثال ، الشريان التاجي النازل الأمامي الأيسر (LAD) والشريان التاجي الأيمن (RCA)) ؛ يعني الالتفافية الثلاثية تجاوزت ثلاث شرايين (مثل LAD و RCA وشريان محيطي الأيسر (LCX)) ؛ يعني تجاوز الرباعي أربع شرايين تم تجاوزها (مثل LAD و RCA و LCX والشريان القطري الأول للـ LAD) بينما تعني الالتفافية الخماسية خمسة شرايين تم تجاوزها. يتطلب انسداد الشريان التاجي الرئيسي الأيسر مسارين ، أحدهما إلى LAD والآخر إلى LCX
قد يكون الشريان التاجي غير مناسب للتطعيم الالتفافي إذا كان صغيرًا (أقل من 1 مم أو أقل من 1.5 مم)، أو متكلس بشدة، أو يقع داخل عضلة القلب بدلاً من السطح. ويرتبط انسداد واحد في الشريان التاجي الرئيسي الأيسر مع زيادة خطر الوفاة القلبية وعادة ما يتلقى ضعف الالتفافية.[citation needed]
يقوم الجراح بمراجعة تصوير الأوعية التاجية قبل الجراحة ويحدد عدد العوائق والنسب المئوية لكل منها ومدى ملائمة الشرايين مع العوائق كأهداف لاجراء العملية. يتم تحديد العدد المفترض للطعوم الالتفافية اللازمة وكذلك موضع تعلق الطعم بطريقة أولية قبل الجراحة ، ولكن يتم اتخاذ القرار النهائي بشأن العدد والموقع أثناء الجراحة عن طريق الفحص المباشر للقلب.
الفعالية
- تنص إرشادات الجامعة الامريكية للقلب \ جمعية القلب الأمريكية لعام 2004 على أن تطعيم تجاوز الشريان التاجي هو العلاج المفضل لما يلي:[3]
- مرض الشريان التاجي الرئيسي الأيسر (LMCA).
- مرض كل الشرايين التاجية الثلاثة (الايسر الامامي النازل, الفرع المنحني للشريان التاجي الايسر و الشريان التاجي الايمن).
- مرض منتشر غير قابل للعلاج باستخدام التدخل الشريان باستخدام القسطرة في الشريان عن طريق الجلد.
- تنص إرشادات الجامعة الامريكية للقلب/ جمعية القلب الأمريكية لعام 2005 أيضًا على أن التجاوز الشريان التاجي المطعم هو العلاج المفضل للمرضى الآخرين المعرضين لمخاطر عالية مثل المصابين بخلل وظيفي حاد في البطين (أي انخفاض نسبة الدم التي تضخ الي الجسم بواسطة القلب) أو مرض السكري.[3]
- يمكن لعملية الجراحة الالتفافية أن تريح الذبحة الصدرية عندما يمنع موقع العوائق الجزئية تحسين تدفق الدم مع الدعامات
- لا توجد فائدة للنجاة مع جراحة الالتفافية مقابل العلاج الطبي في مرضى الذبحة الصدرية مستقرة.[citation needed]
- جراحة الالتفافية لا تمنع احتشاء عضلة القلب في المستقبل.[4]
العمر في حد ذاته ليس عاملاً في تحديد المخاطر مقابل الاستفادة من تطعيم تجاوز الشريان التاجي.[5]
يعتمد التشخيص الذي يتبع تطعيم تجاوز الشريان التاجي على مجموعة متنوعة من العوامل ، وعادة ما تستمر الطعوم الناجحة ما بين 8-15 عامًا.[citation needed] بشكل عام ، يحسن تطعيم تجاوز الشريان التاجي من فرص البقاء على قيد الحياة للمرضى المعرضين لخطر كبير (بشكل عام ثلاثة أضعاف أو أعلى لعملية الالتفافية) ، على الرغم من انه إحصائيا بعد حوالي خمس سنوات الفرق في معدل البقاء على قيد الحياة بين أولئك الذين خضعوا لعملية جراحية والذين عولجوا بواسطة الادوية يقلل. يعد السن في وقت حدوث تطعيم التجاوز للشريان التاجي أمرًا مهمًا للتنبؤ ، حيث أن المرضى الأصغر سناً الذين لا توجد لديهم أمراض معقدة يؤدون بشكل أفضل ، في حين أن المرضى الأكبر سناً يتوقع عادةً المزيد من انسداد الشرايين التاجية.[6]
الأوردة التي يتم استخدامها إما أن صمامتها تم ازالتها أو تكون ملفوفة بحيث لا تسقط الصمامات الموجودة بها تدفق الدم في التطعيم. قد يتم وضع الدعم الخارجي على الوريد قبل التطعيم في الدورة التاجية القلبية للمريض. تعد طعوم الشريان الثديي الداخلي الايسر أطول مدة من طعوم الوريد ، لأن الشريان أقوى من الوريد ، ولأنه متصل بالفعل بشجرة الشرايين ، فإن طعم الشريان الثديي الداخلي الايسر يحتاج فقط إلى تطعيمه في نهاية واحدة. عادة ما يتم تطعيم الشريان الثديي الداخلي الايسر إلى الشريان التاجي الهابط الأمامي الأيسر (LAD) بسبب تحمله الطويل الأمد بالمقارنة مع تطعيم الوريد الصافني.[7][8]
النتائج مقارنة بوضع الدعامات
يشار إلى تطعيم التفافية الشريان التاجي او وضع الدعامة عندما يكون المعالجة الطبية - الأدوية المضادة للذبحة الصدرية ، الاستاتين ، خافضات الضغط ، الإقلاع عن التدخين ، و / أو التحكم في نسبة السكر في الدم بشكل صارم في مرضى السكر - لا تخفف الأعراض المرضية.
- التدخل الشرياني التاجي باستخدام تطعيم التفافية الشريان التاجي و القسطرة عن طريق الجلد أكثر فعالية من المعالجة الطبية في تخفيف الأعراض ، (مثل الذبحة الصدرية وضيق التنفس والتعب).[9]
- CABG تطعيم التفافية الشريان التاجي متفوقة على التدخل الشرياني التاجي باستخدام القسطرة عن طريق الجلد لبعض المرضى الذين يعانون من امراض الشريان التاجي في اوعية متعددة[10][11]
- كانت تجربة الجراحة أو الدعامات (SoS) تجربة عشوائية محكومة قارنت تطعيم التفافية الشريان التاجي مع التدخل الشرياني التاجي باستخدام القسطرة عن طريق الجلد مع الدعامات المعدنية العارية. أثبتت تجربة دعامة او جراحة أن تطعيم التفافية الشريان التاجي متفوق على التدخل الشرياني التاجي باستخدام القسطرة عن طريق الجلد في مرض الشريان التاجي متعدد الأوعية.[10]
- كانت تجربة SYNTAX تجربة عشوائية محكومة من 1800 مريض يعانون من مرض الشريان التاجي متعدد الاوعية ، مقارنة تطعيم التفافية الشريان التاجي مقابل التدخل في الشرياني التاجي باستخدام القسطرة عن طريق الجلد باستخدام الدعامةالمغطاة بالدواء(DES). وجدت الدراسة أن معدلات الجوانب القلبية أو الدماغية الضارة الرئيسية في 12 شهرًا كانت أعلى بكثير في مجموعة DES (17.8 ٪ مقابل 12.4 ٪ ل تطعيم التفافية الشريان التاجي ؛ P = 0.002).[11] كان هذا مدفوعًا بشكل أساسي بالحاجة المرتفعة لإجراءات إعادة تكوين الأوعية المتكررة في مجموعة التدخل في الشرياني التاجي باستخدام القسطرة عن طريق الجلد دون أي فرق في تكرار الاحتشاءات أو النجاة . شوهدت معدلات أعلى من السكتات الدماغية في المجموعة تطعيم التفافية الشريان التاجي.
- ستقوم تجربة FREEDOM (تقييم إعادة تكوين الاوعية المستقبلية في المرضى الذين يعانون من داء السكري – التعامل الامثل للأمراض متعدد الاوعية ) بمقارنة تطعيم تجاوز الشريان التاجي و الدعامة المغطاة بالدواء في المرضى الذين يعانون من مرض السكري. قد توفر سجلات المرضى الغير العشوائية الذين تم فحصهم لهذه التجارب قدرًا كبيرًا من البيانات المتعلقة بنتائج إعادة تكوين الاوعية مثل التحليل العشوائي.[12]
- اظهرت دراسة مقارنة نتائج جميع المرضى في ولاية نيويورك الذين تعالجوا بواسطة تطعيم تجاوز الشريان التاجي أو التدخل التاجي عن طريق الجلد (PCI) تطعيم تجاوز الشريان التاجي كان متفوقا على التدخل الشرياني التاجي باستخدام القسطرة عن طريق الجلد مع الدعامة المغطاة بالدواء في الاوعية المتعددة (أكثر من واحد شريان مصاب) مرض الشريان التاجي (CAD). كان المرضى الذين عولجوا بـ تطعيم تجاوز الشريان التاجي لديهم معدلات أقل للوفاة والموت أو احتشاء عضلة القلب من العلاج مع الدعامة التاجية. المرضى الذين يخضعون لـ تطعيم تجاوز الشريان التاجي لديهم أيضًا معدلات أقل لإعادة تكرار تكوين الاوعية.[13] شمل سجل ولاية نيويورك جميع المرضى الذين يخضعون لإعادة تكوين الاوعية لمرض الشريان التاجي ، ولكن لم تكن تجربة عشوائية ، وبالتالي قد يكون انعكس عوامل أخرى إلى جانب طريقة إعادة تكوين الاوعية التاجية.
- Aأظهر التحليل الاحصائي مع أكثر من 6000 مريض أن تجاوز الشريان التاجي ارتبط بانخفاض خطر حدوث اعراض قلبية سلبية كبيرة مقارنة بالدعامات التي تغطي بالدواء. ومع ذلك ، كان المرضى أكثر عرضة لأحداث السكتة الدماغية.[14]
وجد التحليل الاحصائي لعام 2018 مع أكثر من 4000 حالة مريض إعادة تكوين الاوعية المهجنة (توصيل الشريان الثديي الايسر الداخلي إلى الشريان الامامي الهابط جنبًا إلى جنب مع الدعامات عن طريق الجلد في مواقع تصلب الشرايين الأخرى) لتكون لها مزايا كبيرة مقارنة مع طريقة تجاوز الشريان التاجي التقليدية. تم الإبلاغ عن انخفاض حالات نقل الدم وتقليل مدة الإقامة في المستشفى وتقليل مدة تركيب الانبوب الطبي. في المقابل ، وجد أن إعادة تكوين الاوعية المهجنة أغلى بكثير مقارنة بـ تطعيم تجاوز الشريان التاجي.[15]
المضاعفات
المتعلقة بمجازة الشريان التاجي
- متلازمة مابعد التروية ، وهي ضعف عصبي مؤقت يرتبط بتجاوز الدورة القلبية. تظهر بعض الأبحاث أن معدل الإصابة انخفض في البداية عن طريق تجاوز الشريان التاجي بدون ضخ من القلب ، ولكن دون فرق بعد ثلاثة أشهر من الجراحة. لقد ظهر انخفاض التحكم العصبي مع مرور الوقت لدى الأشخاص المصابين بمرض الشريان التاجي بغض النظر عن العلاج (تجاوز الشريان التاجي بدون ضخ من القلب ، تطعيم تجاوز الشريان التاجي التقليدي أو االتعامل الطبي). ومع ذلك ، تشير دراسة بحثية أجريت عام 2009 إلى أن الضعف العصبي على المدى الطويل (أكثر من 5 سنوات) لا ينجم عن تطعيم تجاوز الشريان التاجي بل هو نتيجة للأمراض الوعائية الخاصة بالشرايين.[16] فقدان الوظيفة العقلية هو أحد مضاعفات الجراحة الالتفافية لدى كبار السن ، وقد يؤثر على التكلفة لاجراء العملية.[17] قد تساهم عدة عوامل في التراجع العقلي الفوري. نظام الدورة الدموية في القلب والرئة والجراحة نفسها تطلق مجموعة متنوعة من الانسجة الميتة ، بما في ذلك أجزاء من خلايا الدم والاوعية والطبقات. على سبيل المثال ، عندما يقوم الجراحون بربط وتوصيل الشريان الأبهر بالأنابيب ، ينتج عنه انسداد تدفق الدم ويسبب جلطات صغيرة. قد تكون عوامل جراحة القلب الأخرى المرتبطة بالأضرار العقلية هي حالات نقص الأكسجين وارتفاع درجة حرارة الجسم أو انخفاضها وضغط الدم غير الطبيعي وضربات القلب غير المنتظمة والحمى بعد الجراحة.[18]
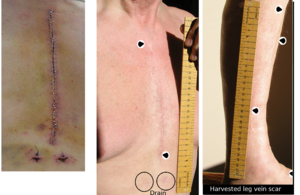
- عظمة القص الغير مكتملة الالتصاق. يزيد حصاد الشريان الصدري الداخلي من خطر عدم توصيل الدم لعظمةالقص.[19]
- احتشاء عضلة القلب بسبب الانسداد ، نقص تدفق الدم ، أو فشل التطعيم.
- التضييق المتأخر الناتج عن التطعيم ، خاصةً من تطعيم الوريد الصافني بسبب تصلب الشرايين الذي يسبب الذبحة الصدرية المتكررة أو احتشاء عضلة القلب.[20]
- الفشل الكلوي الحاد بسبب الانسداد أو نقص تدفق الدم.[21][22]
- السكتة الدماغية ، التابعة للانسداد أو نقص تدفق الدم.[23]
- متلازمة الشلل الوعائي ، ألتابعة لتجاوز القلب وقلة حرارة الجسم
- فشل التطعيم: تستمر الطعوم بين 8-15 عامًا ، ومن ثم يجب استبدالها.
- استرواح الصدر: مجموعة هواء حول الرئة تضغط على الرئة
- الدم في الصدر : الدم في الفضاء حول الرئتين
- سدادات التامور: جمع الدم حول القلب الذي يضغط القلب ويسبب قلة التروية للجسم والدماغ. يتم وضع أنابيب الصدر حول القلب والرئة لمنع هذا. في حالة انسداد أنابيب الصدر في فترة ما بعد الجراحة المبكرة عندما يكون النزيف مستمرًا ، فقد يؤدي ذلك إلى سداد التامور أو استرواح الصدر أو تجمع الدم في الصدر
- الانصباب الجنبي: السائل في الفراغ حول الرئتين. هذا يمكن أن يؤدي إلى نقص الأكسجين والتي يمكن أن تبطئ التعافي
- التهاب اغشية القلب
- الوذمة السفلية الطرفية ، التسرب خارج الاوعية ، الالتهاب ، واالكدمات الناتجة عن حصاد الوريد ؛ يعتبر انحباس السوائل بحد أقصى 9 أرطال (4.1 كجم) في أقصى الاطراف أمرًا شائعًا. يتم التعامل مع هذا من خلال شراب ضاغط بطول الفخذ ، رفع مستوي الطرف السفلي ، والمشي البطيء والمتكرر في وقت مبكر ؛ وكذلك تجنب الوقوف في مكانه ، والجلوس ، وثني الساق من الركبة بأكثر من بضع درجات.
المتعلقة بجراحة القلب المفتوح
- الرجفان الأذيني بعد العملية والرفرفة الأذينية.[24]
- فقر الدم - التابع لفقدان الدم ، بالإضافة إلى فقر الدم الناجم عن الالتهاب ، والالتهاب أمر لا مفر منه مع فتح الصدر بالإضافة إلى حصاد وريد الساق لتطعيمه. هبوط في الهيموغلوبين من مستويات ما قبل الجراحة الطبيعية (على سبيل المثال 15) إلى مستويات ما بعد الجراحة من 6 إلى 10 أمر لا مفر منه. لا يوجد أي فائدة من عمليات نقل الدم حتى يقل الهيموغلوبين عن 7.5.[25] يجب على المؤسسات إنشاء بروتوكولات لضمان عدم نقل الدم ما لم يقل الهيموغلوبين عن 7.5 دون وجود أسباب إضافية.[26]
- تأخر التئام أو انكسار القص - ينقسم القص بشكل طولي (شق عظمة القص المتوسط) وتتقلص للوصول إلى القلب. عدم اتباع "الاحتياطات لعظمةالقص" بعد الجراحة يمكن أن يؤدي إلى تأخر التئام أو انكسار عظمة القص الذي يتم خياطة عند إغلاق جرح الصدر:
- امسك وسادة على الصدر كلما تحركت من الكرسي أو السرير او ذهبت اليه؛ أو السعال أو العطس أو النفخ أو الضحك ، من أجل معارضة القوة الخارجية داخل الصدر الناتجة عن هذه الأنشطة على التئام عظمةالقص.
- تجنب استخدام العضلات الصدرية ، مثل الضغط على ذراع الكرسي لمساعدة المرء على الخروج من الكرسي ، أو باستخدام الذراعين للمساعدة في الجلوس. تتمثل تقنية الوقوف المناسبة في الاهتزاز ثلاث مرات على الكرسي ومن ثم الوقوف لتوفير قوة دفع لنقل مركز الثقل من الجلوس إلى وضع الوقوف. تتمثل تقنية الجلوس المناسبة في خفض الجزء السفلي ببطء نحو مقعد الكرسي باستخدام عضلات الفخذ وعضلات الفخذ ("الأرجل فقط") دون الإمساك بأذرع الكرسي. ثانياً ، يجب على المرضى تجنب رفع الأجسام التي تستخدم العضلات الصدرية: حمل الأشياء الخفيفة ذات الذراعين الممتدين على الجانبين ، ورفع الأجسام الخفيفة مع المرفقين المضغوطين على الصدر واستخدام العضلة ذات الرأسين ، أمر مقبول. أيضا تجنب استخدام الذراعين حول الراس.
- تجنب الجلوس في المقعد الأمامي للسيارة (بدون قيادة) لمدة أربعة أسابيع على الأقل: يمكن أن يؤدي انفجار الوسادة الهوائية إلى كسر الاتحاد لعظمة القص.
المتعلقة بالجراحة العامة
- Infection at incision sites
- Sepsis
- Deep vein thrombosis
- Anesthetic complications such as malignant hyperthermia
- Keloid scarring
- Chronic pain at incision sites
- Chronic stress related illnesses
الجراحة

- The patient is brought to the operating room and moved onto the operating table.
- An anaesthetist or anesthesiologist places intravenous and arterial lines and injects an analgesic, usually fentanyl, intravenously, followed within minutes by an induction agent (usually propofol or etomidate) to render the patient unconscious.
- An endotracheal tube is inserted and secured by the anaesthetist and mechanical ventilation is started. General anaesthesia is maintained with an inhaled volatile anesthetic agent such as isoflurane.
- The chest is opened via a median sternotomy and the heart is examined by the surgeon.
- The bypass grafts are harvested – frequent vessels are the internal thoracic arteries, radial arteries and saphenous veins. When harvesting is done, the patient is given heparin to inhibit blood clotting.
- In the case of "off-pump" surgery, the surgeon places devices to stabilize the heart.
- In the case of "on-pump" surgery, the surgeon sutures cannulae into the heart and instructs the perfusionist to start cardiopulmonary bypass (CPB) normally instructing the perfusionist to "Go on pump". Once CPB is established, there are two technical approaches: either the surgeon places the aortic cross-clamp across the aorta and instructs the perfusionist to deliver cardioplegia with a cooled potassium mixture to stop the heart and slow its metabolism or performing bypasses on beating state (on-pump beating).
- One end of each vein graft is sewn on to the coronary arteries beyond the obstruction and the other end is attached to the aorta or one of its branches. For the internal thoracic artery, the artery is severed and the proximal intact artery is sewn to the LAD beyond the obstruction. Aside the latter classical approach, there are emerging techniques for construction of composite grafts as to avoiding connecting grafts on the ascending aorta (Un-Aortic) in view of decreasing neurologic complications.
- The heart is restarted by removing the aortic cross clamp; or in "off-pump" surgery, the stabilizing devices are removed. In cases where the aorta is partially occluded by a C-shaped clamp, the heart is restarted and suturing of the grafts to the aorta is done in this partially occluded section of the aorta while the heart is beating.
- Once the grafts are completed distally and proximally, the patient is rewarmed to a normal temperature and the heart and other pressures are normal to support coming off the bypass machine, weaning off the bypass machine begins.
- The perfusionist makes sure they have enough volume to come off bypass, confirms that anesthesia is ventilating the patient, confirms that vacuum assist is off (if used), and vocalizes each step in the weaning process to the surgeon and anesthesia. Volume can be given to the patient through the arterial line of the bypass machine while the aortic cannula is still in.
- Protamine is given to reverse the effects of heparin.
- Chest tubes are placed in the mediastinal and pleural space to drain blood from around the heart and lungs.
- The sternum is wired together and the incisions are sutured closed.
- The patient is moved to an intensive care unit (ICU) or cardiac universal bed (CUB) to recover. Nurses in the ICU monitor blood pressure, urine output, respiratory status, and chest tubes for excessive or no drainage.
- After awakening and stabilizing in the ICU for 18 to 24 hours, the person is transferred to the cardiac surgery ward. If the patient is in a CUB, equipment and nursing is "stepped down" appropriate to the patient's progress without having to move the patient. Vital sign monitoring, remote rhythm monitoring, early ambulation with assistance, breathing exercises, pain control, blood sugar monitoring with intravenous insulin administration by protocol, and anti-platelet agents are all standards of care.
- The patient without complications is discharged in four or five days.
تقنية التوغل الطفيف
Alternate methods of minimally invasive coronary artery bypass surgery have been developed. Off-pump coronary artery bypass (OPCAB) is a technique of performing bypass surgery without the use of cardiopulmonary bypass (the heart-lung machine).[27] Avoidance of aortic manipulation may be achieved through the "anaortic" or no-touch OPCAB technique, which has been shown to reduce stroke and mortality compared to on-pump CABG.[28] Further refinements to OPCAB have resulted in minimally invasive direct coronary artery bypass surgery (MIDCAB), a technique of performing bypass surgery through a 5 to 10 cm incision.[29]
Hybrid Coronary Revascualrisation, where the LIMA-to-LAD anastomosis is combined with percutaneous stents in other atherosclerotic sites, has been shown to have significant advantages compared to conventional CABG, including a decrease in the incidence of blood transfusion, and a reduced intubation time. A 2018 meta-analysis has however demonstrated a greater financial cost when compared to conventional CABG.[30]
اختيار مصدر الطعوم
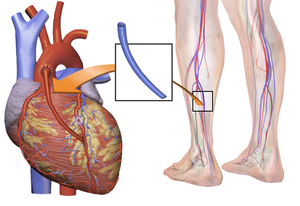
The choice of vessel(s) is highly dependent upon the particular surgeon and institution. Typically, the left internal thoracic artery (LITA) (previously referred to as left internal mammary artery or LIMA) is grafted to the left anterior descending artery and a combination of other arteries and veins is used for other coronary arteries.[31] The great saphenous vein from the leg is used approximately in 80% of all grafts for CABG.[32] The right internal thoracic (mammary) artery (RITA or RIMA) and the radial artery from the forearm are frequently used as well; in the U.S., these vessels are usually harvested either endoscopically, using a technique known as endoscopic vessel harvesting (EVH), or with the open-bridging technique, employing two or three small incisions. The right gastroepiploic artery from the stomach is infrequently used given the difficult mobilization from the abdomen.
المتابعة
- Acute - patients without complications are typically seen 3–4 weeks post operatively, at which time driving may be resumed and formal cardiac rehabilitation begun to increase aerobic endurance and muscular strength.
- Chronic -
- a cardiac stress test at five years is recommended, even in the absence of cardiac symptoms.[33][34]
- an intensive medical regimen including statins, aspirin, and aerobic exercise is essential to delaying the progression of plaque formation in both the native and grafted vessels.
-
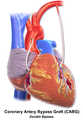
Illustration depicting coronary artery bypass surgery (double bypass)
-
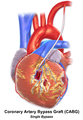
Illustration of Single bypass
-
Illustration of Double bypass
-
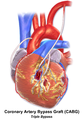
Illustration of Triple bypass
-
Illustration of Quadruple bypass
الانتشار
CABG is one of the most common procedures performed during U.S. hospital stays; it accounted for 1.4% of all operating room procedures performed in 2011.[35] Between 2001 and 2011, however, its volume decreased by 46%, from 395,000 operating procedures performed in 2001 to 213,700 procedures in 2011.[36]
Between 2000 and 2012, the number of CABG procedures carried out decreased across the majority of OECD countries. However, there remained substantial variation in the rate of procedures, with the U.S. carrying out four times as many CABG operations per 100,000 people as Spain.[37] These differences do not appear to be closely related to the incidence of heart disease, but may be due to variation in financial resources, capacity, treatment protocols and reporting methods.[38]
التاريخ
- The first coronary artery bypass surgery was performed in the United States on May 2, 1960, at the Albert Einstein College of Medicine-Bronx Municipal Hospital Center by a team led by Robert H. Goetz and the thoracic surgeon, Michael Rohman with the assistance of Jordan Haller and Ronald Dee.[39][40] In this technique the vessels are held together with circumferential ligatures over an inserted metal ring. The internal mammary artery was used as the donor vessel and was anastomosed to the right coronary artery. The actual anastomosis with the Rosenbach ring took fifteen seconds and did not require cardiopulmonary bypass. The disadvantage of using the internal mammary artery was that, at autopsy nine months later, the anastomosis was open, but an atheromatous plaque had occluded the origin of the internal mammary that was used for the bypass.[citation needed] [التحقق مطلوب]
- Soviet cardiac surgeon, Vasilii Kolesov, performed the first successful internal mammary artery–coronary artery anastomosis in 1964.[41][42] However, Goetz has been cited by others, including Kolesov,[43] as the first successful human coronary artery bypass.[44][45][46][47][48][49] Goetz's case has frequently been overlooked. Confusion has persisted for over 40 years and seems to be due to the absence of a full report and to misunderstanding about the type of anastomosis that was created. The anastomosis was intima-to-intima, with the vessels held together with circumferential ligatures over a specially designed metal ring. Kolesov did the first successful coronary bypass using a standard suture technique in 1964, and over the next five years he performed 33 sutured and mechanically stapled anastomoses in Leningrad (now St. Petersburg), USSR.[50][51]
- René Favaloro, an Argentine surgeon, achieved a physiologic approach in the surgical management of coronary artery disease—the bypass grafting procedure—at the Cleveland Clinic in May 1967.[42][52] His new technique used a saphenous vein autograft to replace a stenotic segment of the right coronary artery. Later, he successfully used the saphenous vein as a bypassing channel, which has become the typical bypass graft technique we know today; in the U.S., this vessel is typically harvested endoscopically, using a technique known as endoscopic vessel harvesting (EVH).
- Soon Dudley Johnson extended the bypass to include left coronary arterial systems.[42]
- In 1968, doctors Charles Bailey, Teruo Hirose and George Green used the internal mammary artery instead of the saphenous vein for the grafting.[42]
التكلفة
According to the CDC, the average cost of hospitalization (only) associated with a coronary bypass operation in the United States in 2013 was $38,707, for an aggregate hospitalization cost of $6.4 billion.[53] The International Federation of Healthcare Plans[54] has estimated the average cost of hospitalization and physician fees for a coronary bypass operation in various countries as shown in the Table below.[55]
| البلد | التكلفة |
|---|---|
| United States | $75.345 |
| Australia | $42.130 |
| New Zealand | $40.368 |
| Switzerland | $36.509 |
| Argentina | $16.492 |
| Spain | $16.247 |
| Netherlands | $15.742 |
| India | $1,583[56] |
انظر أيضاً
- Angioplasty
- Cardiothoracic surgery
- Dressler's syndrome
- Hybrid coronary revascularization
- Totally endoscopic coronary artery bypass surgery
- Chest tube
المصادر
- ^ "Bypass Surgery, Coronary Artery". American Heart Association. Retrieved March 26, 2010.
- ^ "Results for "aortocoronary bypass,coronary artery bypass graft" between 1960 and 2008". Google Ngram Viewer. Retrieved 8 January 2015.
- ^ أ ب Eagle, KA; Guyton RA; Davidoff R; et al. (October 5, 2004). "ACC/AHA 2004 guideline update for coronary artery bypass graft surgery: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Update the 1999 Guidelines for Coronary Artery Bypass Graft Surgery)". Circulation. 110 (14): e340–437. doi:10.1161/01.CIR.0000138790.14877.7D. PMID 15466654.
- ^ Kolata, Gina. "New Heart Studies Question the Value Of Opening Arteries" The New York Times, March 21, 2004. Retrieved January 14, 2011.
- ^ Ohki, S; Kaneko T; Satoh Y; et al. (2002). "[Coronary artery bypass grafting in octogenarian]". Kyobu Geka (in Japanese). 55 (10): 829–33, discussion 833–6. PMID 12233100.
{{cite journal}}: CS1 maint: unrecognized language (link) - ^ Weintraub, W. S. (17 February 2003). "Twenty-Year Survival After Coronary Artery Surgery: An Institutional Perspective From Emory University". Circulation. 107 (9): 1271–1277. doi:10.1161/01.CIR.0000053642.34528.D9. PMID 12628947.
- ^ Kitamura, S; Kawachi K; Kawata T; et al. (March 1996). "[Ten-year survival and cardiac event-free rates in Japanese patients with the left anterior descending artery revascularized with internal thoracic artery or saphenous vein graft: a comparative study]". Nippon Geka Gakkai Zasshi (in Japanese). 97 (3): 202–9. PMID 8649330.
{{cite journal}}: CS1 maint: unrecognized language (link) - ^ Arima, M; Kanoh T; Suzuki T; et al. (August 2005). "Serial angiographic follow-up beyond 10 years after coronary artery bypass grafting". Circ. J. 69 (8): 896–902. doi:10.1253/circj.69.896. PMID 16041156. Archived from the original (PDF) on 2006-03-18. Retrieved 2005-12-25.
- ^ Rihal C, Raco D, Gersh B, Yusuf S (2003). "Indications for coronary artery bypass surgery and percutaneous coronary intervention in chronic stable angina: review of the evidence and methodological considerations". Circulation. 108 (20): 2439–45. doi:10.1161/01.CIR.0000094405.21583.7C. PMID 14623791.
- ^ أ ب SoS Investigators (September 28, 2002). "Coronary artery bypass surgery versus percutaneous coronary intervention with stent implantation in patients with multivessel coronary artery disease (the Stent or Surgery trial): a randomised controlled trial". Lancet. 360 (9338): 965–70. doi:10.1016/S0140-6736(02)11078-6. PMID 12383664.
- ^ أ ب Serruys, P.W.; Morice M.-C.; Kappetein A.P.; et al. (March 5, 2009). "Percutaneous Coronary Intervention versus Coronary-Artery Bypass Grafting for Severe Coronary Artery Disease". N Engl J Med. 360 (10): 961–72. doi:10.1056/NEJMoa0804626. hdl:2437/95138. PMID 19228612.
- ^ Desai ND (January 2008). "Pitfalls assessing the role of drug-eluting stents in multivessel coronary disease". Ann Thorac Surg. 85 (1): 25–7. doi:10.1016/j.athoracsur.2007.08.063. PMID 18154771.
- ^ Hannan, EL; Wu C; Walford G; et al. (January 24, 2008). "Drug-eluting stents vs. coronary-artery bypass grafting in multivessel coronary disease". N. Engl. J. Med. 358 (4): 331–41. doi:10.1056/NEJMoa071804. PMID 18216353.
- ^ Li, X; Kong, M; Jiang, D; Dong, A (Dec 16, 2013). "Comparing coronary artery bypass grafting with drug-eluting stenting in patients with diabetes mellitus and multivessel coronary artery disease: a meta-analysis". Interactive Cardiovascular and Thoracic Surgery. 18 (3): 347–54. doi:10.1093/icvts/ivt509. PMC 3930218. PMID 24345688.
- ^ Reynolds Reynolds, AC; King, N. (August 2018). "Hybrid coronary revascularization versus conventional coronary artery bypass grafting: Systematic review and meta-analysis". Medicine. 97 (33): e11941. doi:10.1097/MD.0000000000011941. PMC 6112891. PMID 30113498.
- ^ Harmon, Katherine (August 6, 2009). "Heart-Lung Machine May Not Be the Culprit in Post-Op "Pump Head" Syndrome". ScientificAmerican.com. Retrieved February 2, 2010.
- ^ Selnes OA, Gottesman RF, Grega MA, Baumgartner WA, Zeger SL, McKhann GM (January 2012). "Cognitive and neurologic outcomes after coronary-artery bypass surgery". N. Engl. J. Med. 366 (3): 250–7. doi:10.1056/NEJMra1100109. PMID 22256807.
- ^ Stutz, Bruce "Pumphead: Does the heart-lung machine have a dark side?" Scientific American, January 9, 2009.
- ^ Li, Arthur E.; Fishman, Elliot K. (2003). "Evaluation of Complications After Sternotomy Using Single- and Multidetector CT with Three-Dimensional Volume Rendering". American Journal of Roentgenology. 181 (4): 1065–1070. doi:10.2214/ajr.181.4.1811065. PMID 14500232.
- ^ Force, T; Hibberd, P; Weeks, G; Kemper, AJ; Bloomfield, P; Tow, D; Josa, M; Khuri, S; Parisi, AF (1990). "Perioperative myocardial infarction after coronary artery bypass surgery. Clinical significance and approach to risk stratification". Circulation. 82 (3): 903–12. doi:10.1161/01.CIR.82.3.903. PMID 2394010.
- ^ Bucerius, J; Gummert, Jan F; Walther, Thomas; Schmitt, Dierk V; Doll, Nicolas; Falk, Volkmar; Mohr, Friedrich W (2004). "On-pump versus off-pump coronary artery bypass grafting: impact on postoperative renal failure requiring renal replacement therapy". The Annals of Thoracic Surgery. 77 (4): 1250–6. doi:10.1016/S0003-4975(03)01346-8. PMID 15063246.
- ^ Silber, JH; Rosenbaum, PR; Schwartz, JS; Ross, RN; Williams, SV (1995). "Evaluation of the Complication Rate as a Measure of Quality of Care in Coronary Artery Bypass Graft Surgery". JAMA. 274 (4): 317–23. doi:10.1001/jama.1995.03530040045039. PMID 7609261.
- ^ Selnes, OA; Gottesman, Rebecca F.; Grega, Maura A.; Baumgartner, William A.; Zeger, Scott L.; McKhann, Guy M. (2012). "Cognitive and neurologic outcomes after coronary-artery bypass surgery". NEJM. 366 (3): 250–7. doi:10.1056/NEJMra1100109. PMID 22256807.
- ^ Leitch, JW; Thomson, D; Baird, DK; Harris, PJ (1990). "The importance of age as a predictor of atrial fibrillation and flutter after coronary artery bypass grafting". The Journal of Thoracic and Cardiovascular Surgery. 100 (3): 338–42. PMID 2391970.
- ^ Murphy, GJ.; Pike, K; Rogers, C. A.; Wordsworth, S.; Stokes, E. a.; Angelini, G. D.; Reeves, B. C. (March 12, 2015). "Liberal or restrictive transfusion after cardiac surgery". New England Journal of Medicine. 372 (11): 997–1008. doi:10.1056/NEJMoa1403612. hdl:2381/36005. PMID 25760354.
- ^ Spertus, J. (March 12, 2015). ""TITRe"ing the Approach to Transfusions after Cardiac Surgery". New England Journal of Medicine. 372 (11): 1069–1070. doi:10.1056/NEJMe1415394. PMID 25760360.
- ^ Sabik, Joseph (2010). "Off Pump Bypass Surgery: Improving outcomes for coronary artery bypass surgery". Clevelandclinic.com. Retrieved February 28, 2011.
- ^ Zhao, Dong Fang (February 28, 2017). "Coronary Artery Bypass Grafting With and Without Manipulation of the Ascending Aorta: A Network Meta-Analysis". Journal of the American College of Cardiology. 69 (8): 924–936. doi:10.1016/j.jacc.2016.11.071. PMID 28231944.
- ^ Sabik, Joseph (2010). "Minimally Invasive Bypass Surgery". Clevelandclinic.com. Retrieved February 28, 2011.
- ^ Reynolds, AC; King, N (2018). "Hybrid coronary revascularization versus conventional coronary artery bypass grafting: Systematic review and meta-analysis". Medicine (Baltimore). 97 (33): e11941. doi:10.1097/MD.0000000000011941. PMID 30113498.
- ^ Head, Stuart J.; Milojevic, Milan; Taggart, David P.; Puskas, John D. (2 October 2017). "Current Practice of State-of-the-Art Surgical Coronary Revascularization". Circulation. 136 (14): 1331–1345. doi:10.1161/CIRCULATIONAHA.116.022572. PMID 28972063.
- ^ Mawhinney, Jamie A; Mounsey, Craig A; Taggart, David P (8 December 2017). "The potential role of external venous supports in coronary artery bypass graft surgery†". European Journal of Cardio-Thoracic Surgery. 53 (6): 1127–1134. doi:10.1093/ejcts/ezx432. PMID 29228235.
- ^ American College of Cardiology. "Five Things Physicians and Patients Should Question" (PDF). Choosing Wisely: An Initiative of the ABIM Foundation. Archived from the original (PDF) on June 24, 2012. Retrieved August 17, 2012.
- ^ Douglas, P. S.; Garcia, M. J.; Haines, D. E.; Lai, W. W.; Manning, W. J.; Patel, A. R.; Picard, M. H.; Polk, D. M.; Ragosta, M.; Ward, R. P.; Douglas, R. B.; Weiner, R. B.; Society for Cardiovascular Angiography Interventions; Society of Critical Care Medicine; American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Failure Society of America; Society for Cardiovascular Magnetic Resonance; Society of Cardiovascular Computed Tomography; American Heart Association; Heart Rhythm Society (2011). "ACCF/ASE/AHA/ASNC/HFSA/HRS/SCAI/SCCM/SCCT/SCMR 2011 Appropriate Use Criteria for Echocardiography". Journal of the American College of Cardiology. 57 (9): 1126–1166. doi:10.1016/j.jacc.2010.11.002. PMID 21349406.
- ^ Weiss AJ, Elixhauser A, Andrews RM (February 2014). "Characteristics of Operating Room Procedures in U.S. Hospitals, 2011". HCUP Statistical Brief #170. Rockville, MD: Agency for Healthcare Research and Quality.
- ^ Weiss AJ, Elixhauser A (March 2014). "Trends in Operating Room Procedures in U.S. Hospitals, 2001—2011". HCUP Statistical Brief #171. Rockville, MD: Agency for Healthcare Research and Quality.
- ^ "Indicator: International comparisons of surgical procedures". QualityWatch. Nuffield Trust & Health Foundation. Retrieved 5 May 2015.
- ^ Lafortune, Gaetan. "Comparing activities and performance of the hospital sector in Europe: how many surgical procedures performed as inpatient and day cases?" (PDF). OECD. OECD. Retrieved 5 May 2015.
- ^ Dee, R (2003). "Who Assisted Whom?". Tex Heart Inst J. 30 (1): 90. PMC 152850. PMID 12638685.
- ^ Haller, JD; Olearchyk, AS (2002). "Cardiology's 10 Greatest Discoveries". Tex Heart Inst J. 29 (4): 342–4. PMC 140304. PMID 12484626.
- ^ Kolessov, VI (October 1967). "Mammary artery-coronary artery anastomosis as method of treatment for angina pectoris". J Thorac Cardiovasc Surg. 54 (4): 535–44. PMID 6051440.
- ^ أ ب ت ث Mehta, NJ; Khan, IA (2002). "Cardiology's 10 Greatest Discoveries of the 20th Century". Tex Heart Inst J. 29 (3): 164–71. PMC 124754. PMID 12224718.
- ^ Kolesov, VI; Potashov, LV (1965). "Surgery of coronary arteries". Eksp Khir Anesteziol (in Russian). 10 (2): 3–8. PMID 5851057.
{{cite journal}}: CS1 maint: unrecognized language (link) - ^ Olearchyk, AS (1988). "Coronary revascularization: past, present and future". J Ukr Med Assoc North Am. 1 (117): 3–34.
- ^ Olearchyk, AS; Olearchyk, RM (January 1999). "Reminiscences of Vasilii I. Kolesov". Ann Thorac Surg. 67 (1): 273–6. doi:10.1016/S0003-4975(98)01225-9. PMID 10086577.
- ^ Glenn, WW (April 1972). "Some reflections on the coronary bypass operation". Circulation. 45 (4): 869–77. doi:10.1161/01.CIR.45.4.869. PMID 5016019.
- ^ Ochsner JL, Mills NL (1978). Coronary artery surgery. Philadelphia: Lea & Febiger.
- ^ Cushing, WJ; Magovern, GJ; Olearchyk, AS (November 1986). "Internal mammary artery graft: retrospective report with 17 years' survival". J Thorac Cardiovasc Surg. 92 (5): 963–4. PMID 3773554.
- ^ Konstantinov, IE (June 2000). "Robert H. Goetz: the surgeon who performed the first successful clinical coronary artery bypass operation". Ann Thorac Surg. 69 (6): 1966–72. doi:10.1016/S0003-4975(00)01264-9. PMID 10892969.
- ^ Kolesov, VI; Kolesov, EV (February 1991). "Twenty years' results with internal thoracic artery-coronary artery anastomosis". J Thorac Cardiovasc Surg. 101 (2): 360–1. PMID 1992247.
- ^ Haller, JD; Olearchyk, AS (2002). "Cardiology's 10 Greatest Discoveries". Tex Heart Inst J. 29 (4): 342–4. PMC 140304. PMID 12484626.
Reference 4
{{cite journal}}: External link in|quote= - ^ Favaloro, RG; Effler, DB; Cheanvechai, C; Quint, RA; Sones Jr, FM (November 1971). "Acute coronary insufficiency (impending myocardial infarction and myocardial infarction): surgical treatment by the saphenous vein graft technique". Am J Cardiol. 28 (5): 598–607. doi:10.1016/0002-9149(71)90104-4. PMID 5116978.
- ^ "www.cdc.gov" (PDF).
- ^ "About IFHP — IFHP".
- ^ "static.squarespace.com" (PDF).
- ^ Gokhale, Ketaki (July 28, 2013). "Heart Surgery in India for ,583 Costs $106,385 in U.S". Bloomberg.
وصلات خارجية
- Articles with unsourced statements from February 2007
- Articles with unsourced statements from January 2019
- Articles with unsourced statements from March 2015
- المقالات needing additional references from December 2010
- كل المقالات needing additional references
- Articles with unsourced statements from June 2010
- مقالات بالمعرفة تحتاج تمحيص الحقائق from June 2010
- جميع الصفحات التي تحتاج تمحيص حقائق
- جراحة القلب