نيرماترلڤير
 | |
| البيانات السريرية | |
|---|---|
| أسماء أخرى | PF-07321332 |
| رمز ATC |
|
| الحالة القانونية | |
| الحالة القانونية | |
| المعرفات | |
| |
| رقم CAS | |
| PubChem CID | |
| UNII | |
| KEGG | |
| ChEBI | |
| Chemical and physical data | |
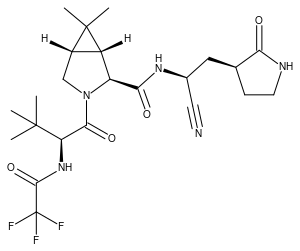
| التركيب | C23H32F3N5O4 |
| الكتلة المولية | 499٫54 g·mol−1 |
| 3D model (JSmol) | |
| Melting point | 192.9 °C (379.2 °F) [2] |
| |
| |
نيرماترلڤير (إنگليزية: Nirmatrelvir)، هو مضاد ڤيروسات فموي، طوّر من قبل شركة فايزر-بيونتيك. يعمل الدواء كمثبط لإنزيم 3CL پروتياز. الدواء عبارة عن مزيج لدواء نيرماترلڤير (المضاد الڤيروسي) مع دواء ريتوناڤير (مثبط CYP3A4)، المسمى تجارياً بپاكسلوڤيد Paxlovid.
ولقد أعلنت وكالة الغذاء والدواء الأمريكية FDA ترخيصها للاستخدام الطارىء لهذا المزيج لمعالجة مرض ڤيروس كورونا COVID-19 في 21 ديسمبر 2021.
لا يعتبر الدواء واقياً ومانعاً للإصابة بعدوى ڤيروس كورونا، حيث أنه لا يستخدم لمنع تطوير العدوى بعد التعرض، وكذلك لا يمنع الإصابة ولا يمنح وقاية قبل التعرض.
كما أنه غير مرخص لعلاج الإصابات الشديدة الخطيرة التي تتطلب رقود المريض وعلاجه في المستشفى.
الاستخدامات الطبية
يوصف پاكسلوڤيد Paxlovid لعلاج الحالات المعتدلة والمتوسطة الشدة لمرض ڤيروس كورونا، للأعمار من 12 عاماً فما فوق والمعرضين لخطر تطوير إصابة شديدة مضاعفة تتطلب العلاج في المشفى أو ربما الموت.
لا يعتبر الدواء واقياً ومانعاً للإصابة بعدوى ڤيروس كورونا، حيث أنه لا يستخدم لمنع تطوير العدوى بعد التعرض، وكذلك لا يمنع الإصابة ولا يمنح وقاية قبل التعرض.
كما أنه غير مرخص لعلاج الإصابات الشديدة الخطيرة التي تتطلب رقود المريض وعلاجه في المستشفى.
التطوير
الدوائي
يشق البروتياز الڤيروسي التاجي مواقع متعددة في الپروتين المتعدد الڤيروسي، عادةً بعد بقايا الجلوتامين. أظهر العمل المبكر على ڤيروسات الأنف البشرية ذات الصلة، أن السلسلة الجانبية المرنة للجلوتامين يمكن استبدالها بالبيروليدون الصلب. تم تطوير هذه الأدوية بشكل أكبر قبل جائحة السارس CoV2 للأمراض الأخرى بما في ذلك السارس. وتم توضيح فائدة استهداف البروتياز 3CL في بيئة العالم الحقيقي لأول مرة في عام 2018 عندما تم استخدام GC376 (دواء أولي من GC373) لعلاج مرض ڤيروس كورونا القاتل بنسبة 100٪ سابقاً، والتهاب الصفاق المعدي، الناجم عن ڤيروس كورونا في القطط.
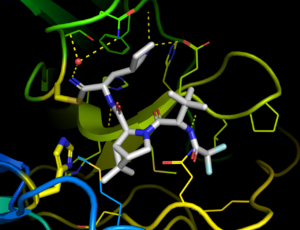
Nirmatrelvir هو نظير لـ GC373، حيث تم استبدال متقبل السيستين التساهمي للألدهيد بالنتريل.
تم تطوير Nirmatrelvir عن طريق تعديل المرشح السريري السابق. lufotrelvir وهو أيضاً مثبط بروتياز 3CL التساهمي ولكن غطائه الرأسي عبارة عن عقار أولي من الفوسفات لهيدروكسي كيتون. يحتاج Lufotrelvir إلى أن يُعطى عن طريق الوريد ليقتصر استخدامه على المستشفى. أدى التعديل التدريجي لمحاكاة البروتين ثلاثي الببتيد إلى nirmatrelvir، وهو مناسب للإعطاء عن طريق الفم.
تشمل التغييرات الرئيسية تقليل عدد مانح الرابطة الهيدروجينية، وعدد الروابط القابلة للدوران عن طريق إدخال حمض أميني ثنائي الحلقات صلب، والذي يحاكي بقايا الليوسين الموجودة في المثبطات السابقة. كانت هذه البقايا قد استخدمت سابقاً في تخليق بوسبريفير.
السريري
في أبريل 2021، بدأت شركة فايزر تجارب المرحلة الأولى. وفي سبتمبر 2021، بدأت الشركة المرحلتين الثانية والثالثة من التجربة.
وفي تشرين الثاني 2021، أعلنت شركة فايزر عن انخفاض بنسبة 89٪ في دخول المستشفى للمرضى ذوي الخطورة العالية الذين تمت دراستهم عند إعطائهم في غضون ثلاثة أيام بعد ظهور الأعراض.
في 14 ديسمبر 2021، أعلنت شركة فايزر أن الجمع بين nirmatrelvir و ritonavir، عند إعطائه في غضون ثلاثة أيام من ظهور الأعراض، يقلل من خطر الاستشفاء أو الوفاة بنسبة 89٪ مقارنةً بالدواء الوهمي في 2246 مشاركاً عالي الخطورة تمت دراستهم.
الكيمياء وعلم الأدوية
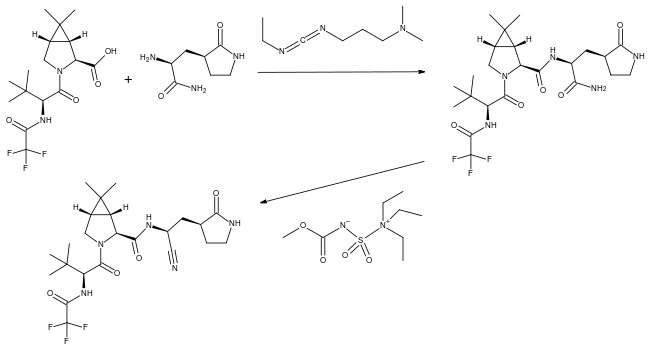
تم نشر التفاصيل الكاملة لتصنيع دواء نيرماترلڤير nirmatrelvir لأول مرة بواسطة علماء من شركة فايزر.
في الخطوة قبل الأخيرة، يقترن حمض أميني متماثل اصطناعي مع أميد أميني متجانس باستخدام كربوديميد EDCI القابل للذوبان في الماء كعامل اقتران. يتم بعد ذلك معالجة المادة الوسيطة الناتجة باستخدام كاشف بورغيس، الذي يجفف مجموعة الأميد إلى نيتريل المنتج.
نيرماتريلفير مثبط تساهمي، يرتبط مباشرة ببقايا السيستين (Cys145) من إنزيم البروتياز السيستين.
في الدواء المعبأ بشكل مشترك، يعمل ريتوناڤير على إبطاء عملية التمثيل الغذائي للنيرماتريلفڤير بواسطة إنزيمات السيتوكروم للحفاظ على تراكيز أعلى للدواء الرئيسي.
المجتمع والثقافة
الاقتصاد
قدمت المملكة المتحدة طلباً للحصول على 250.000 دورة تدريبية في أكتوبر 2021، وطلبت أستراليا مسبقاً 500000 دورة من الدواء.
الترخيص
في نوفمبر 2021، وقعت شركة فايزر اتفاقية ترخيص مع مجموعة براءات اختراع الأدوية المدعومة من الأمم المتحدة للسماح بتصنيع وبيع nirmatrelvir في 95 دولة. وذكرت فايزر أن الاتفاقية ستسمح لمصنعي الأدوية المحليين بإنتاج حبوب منع الحمل "بهدف تسهيل وصول أكبر إلى سكان العالم". ومع ذلك، فإن الصفقة تستثني العديد من البلدان التي بها تفشي كبير لـ COVID-19 بما في ذلك البرازيل والصين وروسيا والأرجنتين وتايلاند.
في 22 ديسمبر 2021، أقرت إدارة الغذاء والدواء الأمريكية، أول دواء ضد ڤيروس كورونا المستجد، من إنتاج شركة فايزر، يؤخذ عن طريق الفم. وذكر بيان هيئة الدواء الأمريكية: "أصدرت إدارة الغذاء والدواء الأمريكية، اليوم تصريح استخدام طارئ، لدواء باكسلوفيد من شركة فايزر (أقراص نيرماترلڤير، وأقراص ريتوناڤير، المعبأة للاستخدام عن طريق الفم)، لعلاج مرض ڤيروس كورونا الخفيف إلى المتوسط، لدى البالغون والأطفال المرضى (12 سنة وما فوق ويزنون 40 كيلو جرام على الأقل أو حوالي 88 رطلا)". وأشارت إلى أن الاختبارات على الدواء أظهرت نتائج إيجابية؛ لاسيما لدى الذين أكثر عرضة للتطور إلى إصابة شديدة بالڤيروس، موضحة أن العقار يتم تقديمه بوصفة طبية فقط.[3]
الوضع القانوني
في 16 نوڤمبر 2021، قدمت شركة فايزر طلباً إلى إدارة الغذاء والدواء الأمريكية (FDA) للحصول على تصريح استخدام طارئ لنيرماتريلڤير بالاشتراك مع ريتونافير. تم منح التفويض في 22 ديسمبر 2021 أصدرت وكالة الأدوية الأوروبية (EMA) إرشادات حول استخدام پاكسلوفيد لعلاج COVID-19 في الاتحاد الأوروبي في 16 ديسمبر 2021.
المقارنة المضللة مع الريتوناڤير
في بعض الأحيان، يُزعم خطأً أن الجمع بين نيرماتريلڤير وريتوناڤير هو نسخة "معاد تعبئتها" من عقار إيفرمكتين المضاد للطفيليات، والذي تم الترويج له بشكل مشكوك فيه باعتباره أحد علاجات COVID-19. تعتمد مثل هذه الادعاءات، التي تستخدم أحياناً لقب فايزرمكتين على أوجه التشابه السطحية بين الحرائك الدوائية لكلا العقاقير والادعاء بأن شركة فايزر تحد من فوائد الإيفرمكتين.
المصادر
- ^ "FDA Authorizes First Oral Antiviral for Treatment of COVID-19". U.S. Food and Drug Administration (FDA) (Press release). 22 December 2021. Retrieved 22 December 2021.
 هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
هذا المقال يضم نصاً من هذا المصدر، الذي هو مشاع.
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةOwen - ^ "إقرار أول دواء ضد فيروس كورونا عن طريق الفم في أمريكا". جريدة الشروق المصرية. 2021-12-22. Retrieved 2021-12-23.
وصلات خارجية
- "PF-07321332". Drug Information Portal. U.S. National Library of Medicine.
- "Early Data Suggest Pfizer Pill May Prevent Severe COVID-19". National Institutes of Health. 16 November 2021.
- Short description is different from Wikidata
- Drugs not assigned an ATC code
- Infobox drug articles with non-default infobox title
- Chemical pages without ChemSpiderID
- Chemical pages without DrugBank identifier
- Articles containing unverified chemical infoboxes
- Articles containing إنگليزية-language text
- Pages using Lang-xx templates
- Portal-inline template with redlinked portals
- Pages with empty portal template
- Amides
- Antiviral drugs
- COVID-19 drug development
- Cyclopropanes
- Nitriles
- Pfizer products
- Pyrrolidones
- Trifluoromethyl compounds