الورم الأرومي الدبقي
| الورم الأرومي الدبقي Glioblastoma | |
|---|---|
| الأسماء الأخرى | الورم الأرومي الدبقي متعدد الأشكال، ورم نجمي من الدرجة الرابعة |
 | |
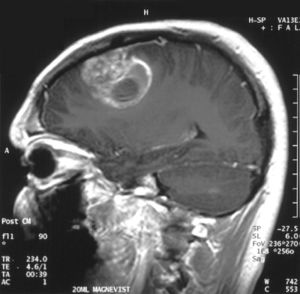
| تصوير بالرنين المغناطيسي للمنطقة التاجية يظهر الورم الأرومي الدبقي في ذكر في الخامسة عشر من عمره. | |
| التخصص | علم الأورام، جراحة الأعصاب |
| الأعراض | غير محددة في البداية، صداع، تغيرات في الشخصية، غثيان، أعراض شبيهة بأعراض الصدمة[1] |
| البداية المعتادة | ~ 64 سنة وأكثر[2][3] |
| المسببات | غير واضحة عادة[2] |
| عوامل الخطر | الأمراض الوراثية (الورم الليفي العصبي، متلازمة لي-فرومني)، الخضوع لعلاج إشعاعي سابق[2][3] |
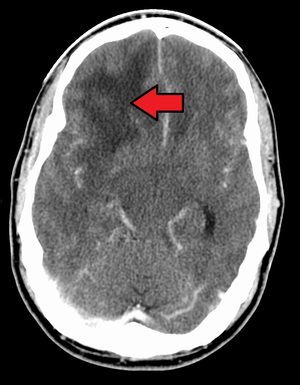
| الطريقة التشخيصية | الأشعة المقطعية، الرنين المغناطسي، الخزعة[1] |
| الوقاية | غير معروفة[3] |
| العلاج | الجراحة، العلاج الكيميائي، العلاج الإشعاعي[3] |
| الدواء | تموزولوميد، السترويديات[1][4] |
| Prognosis | العمر المتوقع ~ 14 شهر مع العلاج[2][3] |
| التردد | 3 من بين 100.000 شخص سنويأً[3] |
الورم الأرومي الدبقي Glioblastoma، يُعرف أيضاً بالورم الأرومي الدبقي متعدد الأشكال glioblastoma multiforme (اختصاراً GBM)، هو واحداً من أكثر السرطانات شراسة ويبدأ في المخ.[5] في البداية، تكون أعراض وعلامات الورم الأرومي الدبقي غير محددة.[1] قد يتظهر أعراضه على شكل نوبات صداع، تغيرات في الشخصية، غثيان، وأعراض شبيهة بأعراض الصدمة.[1] عادة ما تسوء الأعراض بشكل سريع.[2] وقد تتطور إلى فقدان الوعي.[2]
في معظم الحالات الأسباب غير معروفة.[2] ومن عوامل الخطر الشائعة الأمراض الوراثية مثل الورم الليفي العصبي، متلازمة لي-فرومني الخضوع لعلاج إشعاعي سابق.[2][3] يمثل الورم الأرومي الدبقي 15% من أورام المخ.[1] قد يبدأ المرض من خلايا المخ الطبيعية أو يتطور من الإصابة بورم نجمي ليفي.[6] عادة ما يتم التشخيص عن طريق التصوير بالأشعة المقطعية، التصوير بالرنين المغناطيسي والخزعة.[1]
لا توجد منهجية واضحة للوقاية من المرض.[3] عادة ما يتضمن العلاج الجراحة، بعدها يخضع المريض للعلاج الكيميائي والإشعاعي.[3] يستخدم عقار التولوزوميد كجزء من العلاج الإشعاعي.[3][7][4] قد تستخدم جرعات عالية من الأدوية الستيرويدية للمساعدة في تقليل انتشار الورم والأعراض.[1] لا يعرف ما إذا كان من الأفضل إزالة الورم أو معظمه.[8]
على الرغم من العلاج، إلا أن السرطان عادة ما يعاود الظهور.[3] مع العلاج، قد يعيش المريض بعد التشخيص من 12 إلى 15 شهر، وقد يعيش حوالي 3-5% من الأشخاص لمدة تزيد عن خمس سنوات.[2][3] بدون علاج، لا يعيش المريض سوى ثلاثة أشهر.[9] ويعتبر الورم الأرومي الدبقي من أكثر سرطانات المخ شيوعاً وثاني أكثر أورام المخ شيوعاً بعد الورم السحائي.[5][10] يصاب بالمرض ما حوالي 3 من بين 100.000 شخص سنوياً.[3] عادة ما يصيب المرض الأشخاص في عمر 64 سنة ويشيع بين الذكور عن الإناث.[2][3] حالياً يجرى دراسة العلاج المناعي.[11]
الأورام الدبقية هي واحدة من الأنواع الأكثر شيوعًا من أورام الدماغ الأولية. يساعد نوع الورم الذي يعاني منه المريض في تحديد علاجه وتوقعات سير المرض. بشكل عام، تشمل خيارات علاج الورم الدبقي كل من، الجراحة، والعلاج الإشعاعي، والعلاج الكيميائي، والعلاج الموجه والتجارب السريرية التجريبية.
الأنواع
الورم الدبقي هو نوع من الأورام يحدث في الدماغ والحبل الشوكي. تبدأ الأورام الدبقية في الخلايا الداعمة الدبقية (الخلايا الدبقية) التي تحيط بالخلايا العصبية وتساعدها على العمل.[12]
يوجد ثلاثة أنواع من الخلايا الدبقية يمكن أن تنتج الأورام. وتصنف الأورام الدبقية وفقًا لنوع الخلايا الدبقية الموجودة في الورم.
أنواع الورم الدبقي تشمل:
- الأورام النجمية، بما في ذلك الورم النجمي، والورم النجمي الكشمي والورم الأرومي الدبقي
- الأورام البطانية العصبية، بما في ذلك الورم البطاني العصبي الكشمي، والورم البطاني العصبي المخاطي الحليمي وورم البطانة العصبية وتحتها
- أورام الدبقيات قليلة التغصُّن، بما في ذلك الورم الدبقي قليل التغصُّن، والورم الدبقي قليل التغصُّن الكشمي والورم الدبقي قليل التغصُّن النجمي الكشمي
يمكن للأورام الدبقية أن تؤثر على وظيفة الدماغ وتصبح مهددة للحياة اعتمادًا على موقعها ومعدل نموها.
الأعراض والعلامات
تختلف أعراض الورم الدبقي على حسب نوع الورم وكذلك حجمه وموقعه ومعدل نموه.
وتتضمن العلامات والأعراض الشائعة للورم الدبقي ما يلي:
- الصداع
- الغثيان أو القيء
- اختلال أو انخفاض في وظيفة المخ
- فقدان الذاكرة
- تغيُّرات في الشخصية أو سرعة الغضب
- صعوبة في الاتزان
- سلس البول
- مشاكل بالرؤية، مثل عدم وضوح الرؤية أو الرؤية المزدوجة أو فقدان الرؤية المحيطة
- صعوبات في الكلام
- نوبات، وخاصة لدى الأشخاص الذين ليس لديهم تاريخ من الإصابة بنوبات
الأسباب
مثل معظم أورام المخ الأولية، لا يعد سبب الأورام الدبقية معروفًا بالضبط. لكن يوجد بعض العوامل التي قد تزيد من خطر الإصابة بورم في المخ.
عوامل الخطر
تشمل عوامل الخطر:
- العمر: ازدياد خطر الإصابة بورم في المخ مع تقدم العمر. الأورام الدبقية هي الأكثر شيوعًا في البالغين الذين تتراوح أعمارهم بين 60 و80 سنة. ومع ذلك، يمكن أن يحدث ورم الدماغ في أي عمر. وهناك أنواع معينة من الأورام الدبقية، مثل الأورام البطانية العصبية والأورام النجمية شعريّة الخلايا، هي الأكثر شيوعًا لدى الأطفال والشباب.
- التعرض للإشعاع. الأشخاص الذين تعرضوا لنوع من الإشعاع يسمى الإشعاع المؤين أكثر عرضة للإصابة بورم في المخ. وتشمل أمثلة الإشعاع المؤين، العلاج الإشعاعي المستخدم لعلاج السرطان والتعرض للإشعاع الناجم عن القنابل الذرية.
- لم تظهر أشكال أكثر شيوعًا للإشعاع، مثل المجالات الكهرومغناطيسية من خطوط الكهرباء وإشعاع ترددات موجات الراديو من الهواتف المحمولة وأفران الميكروويف، زيادة في خطر الإصابة بالورم الدبقي.
- وجود تاريخ عائلي للإصابة بالورم الدبقي. من النادر أن يظهر الورم في الأسر. ولكن وجود تاريخ عائلي من الورم الدبقي يمكن أن يضاعف من خطر الإصابة به. بعض الجينات ترتبط ارتباطًا ضعيفًا بالورم الدبقي، ولكن هناك حاجة إلى مزيد من الدراسة لتأكيد الصلة بين هذه الاختلافات الجينية وأورام الدماغ.
التشخيص
إذا اشتبه طبيب الرعاية الأولية في إصابة الحالة بورم في المخ، فقد يتم تحويله إلى أخصائي متخصص في علاج اضطرابات المخ والجهاز العصبي (الأعصاب). قد يوصي الطبيب بعدد من الاختبارات والإجراءات، وتشمل:
- الفحص العصبي: خلال الفحص العصبي، قد يتحقق طبيبك من رؤيتك وسمعك وتوازنك وقدرتك التنسيقية وقوتك وردود أفعال جسمك. وجود مشكلات في واحدة أو أكثر من هذه المناطق قد يوفر دلائل حول الجزء من الدماغ الذي يمكن أن يكون قد تأثر بورم في الدماغ.
- اختبارات التصوير: وغالبًا ما يستخدم التصوير بالرنين المغناطيسي للمساعدة في تشخيص أورام الدماغ. في بعض الحالات، قد يتم حقن صبغة (مواد تباين) خلال وريد في ذراع المريض أثناء دراسة التصوير بالرنين المغناطيسي للمساعدة في إظهار الاختلافات في أنسجة الدماغ.
قد يساعد عدد من مكونات التصوير بالرنين المغناطيسي المتخصصة — بما في ذلك التصوير بالرنين المغناطيسي الوظيفي، وتصوير التروية بالرنين المغناطيسي وتنظير الطيف بالرنين المغناطيسي — في تقييم الطبيب للورم وخطة العلاج.
ويمكن أن تشمل الاختبارات، التصوير المقطعي المحوسب والتصوير المقطعي بالإصدار البوزيتروني.
- اختبارات للكشف عن وجود السرطان في أجزاء أخرى من الجسم: لاستبعاد أنواع أخرى من أورام المخ قد تكون انتشرت من أجزاء أخرى من الجسم، قد يوصي الطبيب بفحوص وإجراءات لتحديد المكان الذي نشأ فيه السرطان. تنشأ الأورام الدبقية داخل الدماغ وليست نتيجة السرطان الذي انتشر (انتقل) من مكان آخر.
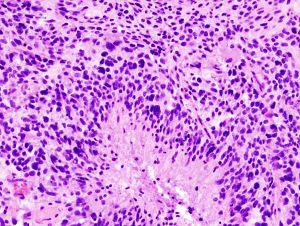
- جمع واختبار عينة من الأنسجة غير الطبيعية (خزعة): اعتمادًا على موقع الورم الدبقي، قد يتم إجراء خزعة باستخدام إبرة قبل العلاج أو كجزء من عملية لإزالة ورم الدماغ.
قد يتم إجراء خزعة باستخدام إبرة بالتوضيع التجسيمي للأورام الدبقية في المناطق التي يصعب الوصول إليها أو المناطق الحساسة جدًا داخل الدماغ التي قد تتضرر من أي عملية أكثر توسعًا. خلال خزعة إبرة التوضيع التجسيمي، يحفر جراح الأعصاب ثقبًا صغيرًا في الجمجمة. ثم يتم إدخال إبرة رفيعة من خلال ثقب. تتم إزالة الأنسجة من خلال الإبرة، والتي كثيرًا ما يتم توجيهها باستخدام التصوير المقطعي المحوسب أو المسح الضوئي بالتصوير بالرنين المغناطيسي. ثم يتم تحليل عينة الخزعة تحت المجهر لتحديد ما إذا كانت سرطانية أو حميدة.
تعد الخزعة هي الطريقة الوحيدة لتشخيص ورم الدماغ بشكل نهائي وإمدادك بتشخيص لتوجيه قرارات العلاج. واستنادًا إلى هذه المعلومات، يمكن لطبيب الأمراض تحديد درجة الورم في الدماغ أو مرحلته.
وتنقسم الأورام إلى أربع درجات حيث تكون أورام الدرجة الأولى الأبطأ نموًا وأكثرها خلايا حميدة وتحتوي أورام الدرجة الرابعة على أكثر الخلايا السرطانية شذوذًا وعنفًا.
العلاج
يعتمد علاج الورم الدبقي على نوع الورم وحجمه وشدته ومكانه، فضلاً عن العمر والحالة الصحية بشكل عام وتفضيلات المريض.
علاج الأعراض
وبالإضافة إلى الإجراءات اللازمة لإزالة الورم نفسه، قد يتطلب علاج الورم الدبقي أيضًا استخدام العقاقير للحد من علامات الورم وأعراضه. قد يصف الطبيب الستيرويد للحد من التورم وتخفيف الضغط على المناطق المتضررة من الدماغ. يمكن استخدام العقاقير المضادة للصرع للسيطرة على النوبات الصرعية.
الجراحة
عادة ما يكون إجراء الجراحة لإزالة أكبر قدر ممكن من الورم هو الخطوة الأولى في علاج معظم أنواع الأورام الدبقية.
في بعض الحالات، تكون الأورام الدبقية صغيرة وسهلة الفصل من الأنسجة الصحية المحيطة في الدماغ ، مما يجعل الإزالة الجراحية الكاملة ممكنة. في حالات أخرى، لا يمكن فصل الأورام عن الأنسجة المحيطة بها، أو تكون واقعة بالقرب من المناطق الحساسة في الدماغ وتجعل العملية الجراحية محفوفة بالمخاطر. في هذه الحالات، يزيل الطبيب قدرًا كبيرًا من الورم طالما الأمر آمن.
مجرد إزالة جزء من الورم قد يساعد في تقليل علاماتك وأعراضك.
وفي بعض الحالات، قد يقوم أخصائيو علم الأمراض العصبية بتحليل عينات الأنسجة التي يزيلها الجراح ويبلغون بالنتائج أثناء العملية الجراحية. هذه المعلومات تساعد الجراح في تحديد حجم الأنسجة التي يجب إزالتها.
ويمكن استخدام مجموعة متنوعة من التقنيات والأساليب الجراحية لمساعدة جراح الأعصاب في حماية أكبر قدر ممكن من أنسجة المخ السليمة أثناء إزالة الورم، بما في ذلك جراحة الدماغ بمساعدة الحاسوب، وجراحة الدماغ مع اليقظة والتصوير بالرنين المغناطيسي أثناء العملية. على سبيل المثال، أثناء جراحة الدماغ مع اليقظة، قد يطلب منك تحريك طرف أو إخبار قصة أثناء الجراحة للتأكد من عدم تلف مناطق الدماغ المسيطرة على تلك الوظائف.
وتنطوي جراحة إزالة الأورام الدبقية على بعض المخاطر، مثل العدوى والنزف. وتتوقف المخاطر الأخرى علي المنطقة التي يقع فيها الورم في الدماغ. فعلى سبيل المثال، تنطوي جراحات الأورام القريبة من الأعصاب المتصلة بالعينين على خطر فقدان الرؤية.
العلاج الإشعاعي
عادةً ما يتبع العلاج الإشعاعي الجراحة في علاج الأورام الدبقية، وخصوصًا الأورام الدبقية ذات الدرجة العالية. ويستخدم العلاج الإشعاعي حزمة من الأشعة عالية الطاقة، مثل الأشعة السينية أو البروتونات، لقتل الخلايا السرطانية.
يصدر العلاج الإشعاعي للورم الدبقي من جهاز خارج الجسم (حزمة الإشعاع الخارجي).
وهناك عدة أنواع من حزم الإشعاع الخارجية المستخدمة حاليًا وقيد الدراسة لعلاج للورم الدبقي. ويؤخذ في الاعتبار نوع الورم الدبقي ودرجته وعوامل تشخيصية أخرى لتحديد توقيت ونوع العلاج بالإشعاعي.
وتشمل خيارات العلاج الإشعاعي استخدام أجهزة الكمبيوتر لاستهداف ورم الدماغ (العلاج الإشعاعي منظم الشدة) واستخدام البروتونات بدلاً من الأشعة السينية كمصدر للإشعاع (العلاج الإشعاعي بالبروتونات) والعلاج الإشعاعي التجسيمي (الجراحة الإشعاعية).
العلاج الكيميائي
يستخدم العلاج الكيميائي الأدوية لقتل خلايا الورم. يمكن تناول أدوية العلاج الكيميائي في صورة أقراص (فمويًا) أو بالحقن في الوريد (وريديًا).
عادةً ما يُستخدم العلاج الكيميائي بالتزامن مع العلاج الإشعاعي لعلاج الأورام الدبقية.
إن دواء العلاج الكيميائي المستخدم في معظم الأحيان في علاج الأورام الدبقية هو تيموزولوميد (تيمودار)، حيث يؤخذ في صورة قرص.
تعتمد الآثار الجانبية للعلاج الكيميائي على نوع وجرعة الإشعاع التي تتلقاها. وتشمل الآثار الجانبية الشائعة الغثيان والقيء والصداع وفقدان الشعر والحمى والضعف. يمكن إدارة بعض الآثار الجانبية بالأدوية.
العلاج الدوائي الموجه
تركز العلاجات الموجهة على تشوهات محددة موجودة داخل الخلايا السرطانية. ومن خلال حجب هذه التشوهات، يمكن للعلاجات الدوائية الموجهة أن تسبب موت الخلايا السرطانية.
يعد بيفاسيزوماب (أفاستين) أحد العلاجات الدوائية الموجهة المستخدمة لعلاج نوع من سرطان دماغ يُطلق عليه الورم الدبقي. يُعطى هذا الدواء من خلال وريد (الحقن الوريدي)، ويُوقف تكوين الأوعية الدموية الجديدة، ويمنع تدفق الدم إلى الورم ويقتل الخلايا السرطانية.
إعادة التأهيل
نظرًا إلى أن أورام الدماغ يمكن أن تنمو في أجزاء الدماغ المسؤولة عن المهارات الحركية والتخاطب والرؤية والتفكير، فقد تمثل إعادة التأهيل جزءًا ضروريًا في مرحلة التعافي. يمكن للطبيب أن يُحيلك إلى الخدمات التي يمكن أن تساعدك، مثل:
- العلاج الطبيعي يمكن أن يساعدك في استعادة قوة العضلات أو مهارات الحركة المفقودة
- العلاج المهني يمكن أن يساعدك في العودة لممارسة الأنشطة اليومية العادية، بما في ذلك أنشطة العمل، بعد إزالة ورم الدماغ أو علاج مرض آخر
- علاج التخاطب بالتعاون مع أخصائيين في مجال صعوبات التخاطب (أخصائيي علم أمراض التخاطب)، يمكن أن يساعدك إذا كنت تعاني صعوبة في الكلام
- التدريس لأطفال في سن المدرسة يمكن أن يساعد الأطفال على التكيف مع التغييرات التي تطرأ على الذاكرة والتفكير لديهم بعد علاج أورام الدماغ
الطب البديل
تم عمل أبحاث صغيرة عن علاجات أورام الدماغ المكملة أو البديلة. لم يتم إثبات وجود أي علاجات بديلة لعلاج الأورام الدبقية. ومع ذلك، يمكن أن تساعدك العلاجات المكملة في التعايش مع ورم الدماغ المصاب به وعلاجه. تحدث إلى طبيبك بشأن خياراتك.
وتشمل بعض العلاجات المكملة التي يمكنها مساعدتك في التعايش ما يلي:
- العلاج بالوخز بالإبر
- التنويم المغناطيسي
- التأمل
- العلاج عن طريق الموسيقى
- تمارين الاسترخاء
التأقلم والدعم
قد يستحوذ تشخيص الإصابة بورم الدماغ على تفكيرنا ويصيبنا بالهلع والخوف. فقد يجعلك تشعر بقلة سيطرتك على صحتك. ولكن يمكنك اتخاذ بعض الخطوات للتغلب على الحزن والصدمة التي قد تأتي بعد تشخيص إصابتك. ضع فى الاعتبار تجربة:
- تعرف على معلومات كافية عن الأورام الدبقية لاتخاذ قرارات بشأن رعايتك الطبية. اسأل طبيبك حول نوع الورم الدماغي الذي تعانيه، بما في ذلك خيارات العلاج المتاحة لك، وإذا ما كنت ترغب في معرفة توقعات سير المرض. فكلما عرفت المزيد عن أورام الدماغ، قد تصبح أكثر ثقة في اتخاذ قرارات العلاج.
- اجعل أصدقاءك وعائلتك بقربك. كما أن الحفاظ على قوة علاقاتك الوثيقة سيساعدك على التعامل مع الورم الدماغي. يمكن للأصدقاء والعائلة تقديم الدعم العملي الذي ستحتاج إليه، مثل المساعدة في الاهتمام بمنزلك إذا كنت في المستشفى. ويمكن أن يمثلوا دعمًا عاطفيًا حينما يرهقك السرطان.
- اعثر على شخص ما للتحدث معه. العثور على مستمع جيد لديه الرغبة فى الاستماع لحديثك عن آمالك ومخاوفك. قد يكون صديقًا أو فردًا من العائلة. قد يكون من المفيد أيضًا الحصول على الاهتمام والتفهم من مستشار أو الأخصائي الطبي الاجتماعي أو عضو من رجال الدين أو مجموعة دعم السرطان.
- اسأل طبيبك عن مجموعات الدعم في منطقتك. أو راجع دليل هاتفك، أو المكتبة أو إحدى منظمات السرطان، مثل المعهد الوطني للسرطان (National Cancer Institute) أو جمعية السرطان الأمريكية (American Cancer Society).
مسار المرض
| Recursive partitioning analysis (RPA) class |
التعريف | متوسط البقاء التاريخي | البقاء التاريخ لسنة واحدة | البقاء التاريخ لثلاث سنوات | البقاء التاريخي لخمس سنوات |
|---|---|---|---|---|---|
| III | العمر < 50، KPS ≥ 90 | 17.1 شهر | 70% | 20% | 14% |
| IV | العمر< 50، KPS < 90 | 11.2 شهر | 46% | 7% | 4% |
| العمر ≥ 50، KPS ≥ 70، إزالة جراحية للورم مع وظائف عصبية جيدة | |||||
| V + VI | العمر≥ 50، KPS ≥ 70، إزالة جراحية للورم مع وظائف عصبية ضعيفة | 7.5 شهر | 28% | 1% | 0% |
| العمر ≥ 50، KPS ≥ 70، لا يمكن إزالة الورم جراحياً | |||||
| العمر ≥ 50، KPS < 70 |
الانتشار
يصايب بالمرض 3 من بين 100.00 شخص سنوياً.[3] عادة ما يبدأ المرض في الظهور لدى الأشخاص في عمر 65 سنة ويشيع بين الذكور عن الإناث.[2][3] ويعتبر ثاني سرطانات الجهاز العصبي المركزي شيوعاً بعد الورم السحائي.[10]
التاريخ
طُرح مصطلح الورم الأرومي الدبقي متعدد الأشكال عام 1926 بواسطة پرسيڤال بيلي وهارڤي كوشينگ، استناداً إلى فكرة أن الورم ينشأ من الطلائع الرئيسية للخلايا الدبقية، ويتمتع بمظهر شديد التغير بسبب النخر والنزف والخراجات (متعدد الأشكال).[13]
الأبحاث
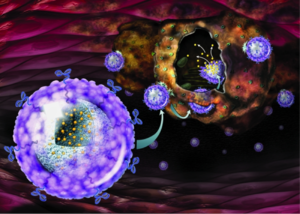
في 17 يناير 2019، اكتشف علماء من جامعة تورين للتكنولوجيا تقنية جديدة تستخدم الجسيمات النانوية الكهربائية للقضاء على الخلايا السرطانية.
حسب علماء من جامعة تورين للتكنولوجيا، من الممكن للجسيمات النانوية بعد ضغطها بالموجات فوق الصوتية، في تقنية تسمى التقنية الكهروضغطية، أن تطلق شحنات كهربائية لمهاجمة الخلايا السرطانية والقضاء عليها. كما طور الفريق آلية هامة للاستهداف، فالجزيئات النانوية يجب أن تُصمم بحيث تلتصق بالخلايا المسرطنة مع تجاهلها للخلايا السليمة، وقد أنجز فريق جامعة تورين للتكنولوجيا هذه المهمة عن طريق تغليف جسيمات النانو بپوليمر لدن، ثم وضع هذا المركب داخل أجسام مضادة تلتصق بمستقبلات موجودة في نوع بعينة من الخلايا السرطانية.[14]
أجرى الفريق تجاربهم على أحد أشرس أنواع سرطان المخ، المسمى بالورم الأرومي الدبقي متعدد الأشكال glioblastoma multiforme، وفي أغشية مستقبلات التراسنفيرين، على النقيض من أغلب الخلايا السليمة، لذا، قام العلماء بتغليف جزيئات النانو بغشاء من أجسام الترانسفيريني المضادة، التي تلتصق بمستقبلات الترانسفيرين على الخلايا المسرطنة، ويؤدي هذا إلى تحويل الجزيئات النانوية إلى ما يشبه الصواريخ الموجهة التي لا تستهدف إلا الخلايا السرطانية، ويجب أن تمر الجزئيات النانوية أيضاً عبر عائق خلايا دم المخ، وهو عامل مهم في علاج سرطان المخ، يمكن للجزيئات النانوية إنجاز هذا الأمر إذا كانت بصغيرة بالقدر الكافي، لذا إختار الفريق جزيئات يبلغ نصف قطرها 300 نانو-متر، وهو الحجم القادر على تجاوز هذا العائق.
انظر أيضاً
المصادر
- ^ أ ب ت ث ج ح خ د Young, RM; Jamshidi, A; Davis, G; Sherman, JH (June 2015). "Current trends in the surgical management and treatment of adult glioblastoma". Annals of Translational Medicine. 3 (9): 121. doi:10.3978/j.issn.2305-5839.2015.05.10. PMC 4481356. PMID 26207249.
- ^ أ ب ت ث ج ح خ د ذ ر ز "Chapter 5.16". World Cancer Report 2014. World Health Organization. 2014. ISBN 978-9283204299.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط Gallego, O (August 2015). "Nonsurgical treatment of recurrent glioblastoma". Current Oncology (Toronto, Ont.). 22 (4): e273–81. doi:10.3747/co.22.2436. PMC 4530825. PMID 26300678.
- ^ أ ب Hart, MG; Garside, R; Rogers, G; Stein, K; Grant, R (30 April 2013). "Temozolomide for high grade glioma". The Cochrane Database of Systematic Reviews. 4 (4): CD007415. doi:10.1002/14651858.CD007415.pub2. PMID 23633341.
- ^ أ ب Bleeker, Fonnet E.; Molenaar, Remco J.; Leenstra, Sieger (2012). "Recent advances in the molecular understanding of glioblastoma". Journal of Neuro-Oncology. 108 (1): 11–27. doi:10.1007/s11060-011-0793-0. PMC 3337398. PMID 22270850.
- ^ "Chapter 3.8". World Cancer Report 2014. World Health Organization. 2014. ISBN 978-9283204299.
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةRTG1 - ^ Van Meir, E. G.; Hadjipanayis, C. G.; Norden, A. D.; Shu, H. K.; Wen, P. Y.; Olson, J. J. (2010). "Exciting New Advances in Neuro-Oncology: The Avenue to a Cure for Malignant Glioma". CA: A Cancer Journal for Clinicians. 60 (3): 166–93. doi:10.3322/caac.20069. PMC 2888474. PMID 20445000.
- ^ Schapira, Anthony H.V. (2007). Neurology and clinical neuroscience. Philadelphia: Mosby Elsevier. p. 1336. ISBN 9780323070539. Archived from the original on 2017-07-29.
{{cite book}}: Unknown parameter|deadurl=ignored (|url-status=suggested) (help) - ^ أ ب McNeill, Katharine A. (2016). "Epidemiology of Brain Tumors". Neurologic Clinics. 34 (4): 981–98. doi:10.1016/j.ncl.2016.06.014. PMID 27720005.
- ^ "With Immunotherapy, Glimmers of Progress against Glioblastoma". National Cancer Institute. 9 December 2015. Archived from the original on 24 December 2015. Retrieved 23 December 2015.
{{cite web}}: Unknown parameter|deadurl=ignored (|url-status=suggested) (help) - ^ الورم الدبقي، مايو كلينيك
- ^ Bailey & Cushing: Tumors of the Glioma Group. JB Lippincott, Philadelphia, 1926.[صفحة مطلوبة]
- ^ "جزئيات النانو الكهربائية قادرة على استهداف الخلايا السرطانية وقتلها". إم آي تي تكنولوجي رڤيو. 2019-01-17. Retrieved 2019-01-20.
وصلات خارجية
| Classification | |
|---|---|
| External resources |
- Information about Glioblastoma Multiforme (GBM) from the American Brain Tumor Association
- AFIP Course Syllabus – Astrocytoma WHO Grading Lecture Handout
- Image Database – MR & CT of Glioblastoma