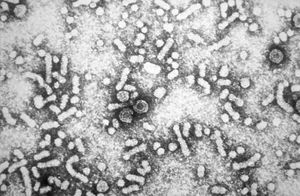
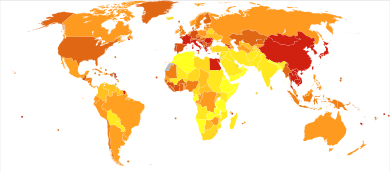
سرطان الكبد
| سرطان الكبد | |
|---|---|
| الأسماء الأخرى | السرطان الكبدي، الخباثة الكبدية الأولية، سرطان الكبد الأولي |
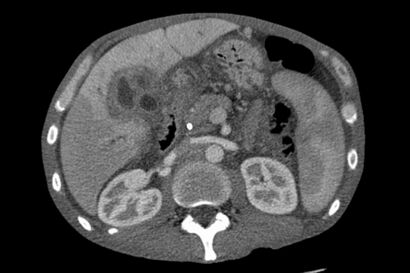 | |
| تصوير مقطعي للكبد مصاب بسرطان الأوعية الصفراوية | |
| التخصص | طب الجهاز الهضمي، طب الكبد، علم الأورام |
| الأعراض | تكتل أو ألم في الجانب الأيمن أسفل القفص الصدري، تورم البطن، اصفرار الجلد، الكدمات، فقدان الوزن، الضعف[1] |
| البداية المعتادة | 55 إلى 65 سنة [2] |
| المسببات | التهاب الكبد الڤيروسي ب، التهاب الكبد الڤيروسي ج، المشروبات الكحولية، السموم الفطرية، مرض الكبد الدهني اللاكحولي، مثقبيات الكبدs[3][4] |
| الطريقة التشخيصية | تحاليل الدم، التصوير الطبي، الخزعة النسيجية[1] |
| الوقاية | التطعيم ضد التهاب الكبد الڤيروسي ب، اختبار الإصابة بالتهاب الكبد الڤيروسي ج ود[3] تقليل التعرض للسموم الفطرية، وتقليل المستويات العالية من استهلاك الكحول |
| العلاج | الجراحة، العلاج المستهدف، العلاج الإشعاعي[1] |
| Prognosis | معدل البقاء لخمس سنوات ~18% (الولايات المتحدة)؛[2] 40% (اليابان)[5] |
| التردد | 618.700 (وقت ما عام 2015)[6] |
| الوفيات | 782.000 (2018)[7] |
سرطان الكبد (إنگليزية: Liver cancer، يُعرف أيضاً باسم السرطان الكبدي، سرطان الكبد الأولي، أو خباثة الكبد الأولية)، هو سرطان يبدأ تكونه في الكبد.[1] قد يكون سرطان الكبد سرطاناً أولياً (يبدأ في الكبد) أو ثانوياً (أي السرطان الذي انتشر للكبد من مكان آخر، والذي يُعرف باسم سرطان الكبد النقيلي). سرطان الكبد النقيلي أكثر شيوعاً عن ذلك الذي يبدأ في الكبد.[3] هناك تزايد في معدل الإصابة بسرطان الكبد حول العالم.[8][9]
سرطان الكبد الأولي هو سادس أكثر أنواع السرطانات شيوعًا ورابع السرطانات المسببة للوفاة.[7][10] عام 2018، أصيب 841.000 شخص بسرطان الكبد وأسفر عن 782.000 حالة وفاة على مستوى العالم.[7]
ترتفع معدلات الإصابة بسرطان الكبد في الأماكن التي ينتشر فيها التهاب الكبد الڤيروسي ب وج، بما في ذلك آسيا وأفريقيا جنوب الصحراء.[3] الذكور أكثر إصابة بسرطانة الخلية الكبدية عن الإناث (HCC).[3] التشخيص أكثر شيوعًا بين أولئك الذين تتراوح أعمارهم بين 55 و65 عامًا.[2]
السبب الرئيسي لسرطان الكبد هو تليف الكبد بسبب التهاب الكبد الڤيروسي ب، التهاب الكبد الڤيروسي ج أو المشروبات الكحولية.[4] تشمل الأسباب الأخرى السموم الفطرية، مرض الكبد الدهني اللاكحولي ومثقبيات الكبد.[3] النوع الأكثر شيوعاً هو سرطان الخلايا الكبدية، إذ يشكل أكثر من 80% من الحالات وسرطان الأوعية الصفراوية.[3] قد يُدعم التشخيص بتحاليل الدم والتصوير الطبي، مع التأكد بإجراء خزعة نسيجية.[1]
نظرًا لوجود العديد من الأسباب المختلفة لسرطان الكبد، فهناك العديد من الأساليب للوقاية من سرطان الكبد. تشمل هذه الجهود التطعيم ضد التهاب الكبد الڤيروسي ب،[3] علاج التهاب الكبد الڤيروسي ب، علاج التهاب الكبد الڤيروسي ج، التقليل من احتساء المشروبات الكحولية[8] التقليل من التعرض للسموم الفطرية في الزراعة، علاج البدانة وضبط السكري.[9] يوصى بفحص المصابين بمرض الكبد المزمن.[3] على سبيل المثال ، يوصى بفحص الأشخاص المصابين بأمراض الكبد المزمنة والمعرضين لخطر سرطان الخلايا الكبدية كل 6 أشهر باستخدام التصوير بالموجات فوق الصوتية.[8]
نظرًا لأن سرطان الكبد هو مصطلح شامل للعديد من أنواع السرطان، فإن الأعراض والعلامات تعتمد على نوع السرطان الموجود. يمكن أن تكون الأعراض غامضة وواسعة النطاق. يرتبط سرطان الأوعية الصفراوية بالتعرق واليرقان وألم البطن وفقدان الوزن وتضخم الكبد.[11] يرتبط سرطان الخلاي الكبدية بزيادة كتلة البطن، ألم البطن، القيء، فقر الدم، آلام الظهر، اليرقان، الحكة، فقدان الوزن والحمى.[12]
تتضمن خيارات العلاج الجراحة، العلاج المستهدف والعلاج الإشعاعي.[1] في بعض الحالات قد يستخدم العلاج بالاستئصال، بالعلاج بالإنسداد، أو زراعة الكبد.[1]
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
التصنيف
يمكن أن يأتي سرطان الكبد من نسيج الكبد الأرضي وكذلك التكوينات الأخرى داخل الكبد مثل القناة الصفراوية والأوعية الدموية والخلايا المناعية. هناك العديد من الأنواع الفرعية لسرطان الكبد، وأكثرها شيوعًا موصوفة أدناه.
سرطان الخلايا الكبدية
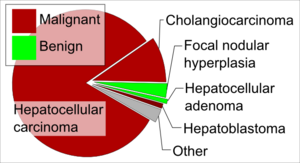
سرطان الكبد الأكثر شيوعًا، والذي يمثل حوالي 75٪ من جميع سرطانات الكبد الأولية، هو سرطان الخلايا الكبدية (HCC).[14] يتكون سرطان الخلايا الكبدية داخل خلايا الكبد، المعروفة باسم الخلايا الكبدية، التي تصبح خبيثة. من حيث وفيات لاسرطان، يعتبر سرطان الخلايا الكبدية السبب الثالث الأكثر شيوعًا لوفيات السرطان.[15]
من حيث التشخيص، يوصى الأشخاص المعروض للخطر (يشمل هذا المصابون بأمراض الكبد المزمنة، التليف الكبدي، وغيرها) إجراء التصوير بالموجات فوق الصوتية. إذا أظهرت الموجات فوق الصوتية منطقة بؤرية أكبر من واحد سنتيمتر، يجب على المرضى الحصول على تصوير ثلاثي الطور معزز بالتصوير المقطعي المحوسب أو التصوير بالرنين المغناطيسي.[16] بعد ذلك يمكن تشخيص سرطان الخلايا الكبدية إشعاعيًا باستخدام نظام بيانات وتقارير تصوير الكبد (LI-RADS).[17] هناك أيضاً أنواع مختلفة من سرطان الخلايا الكبدية التي تتألف من كلاً من سرطان الخلايا الكبدية وسرطان الأوعية الصفراوية .[18]
سرطان الأوعية الصفراوية
يشكل سرطان الأوعية الصفراوية (cholangiocarcinoma والسرطان الغدي الكيسي cystadenocarcinoma حوالي 6% من سرطانات الكبد الأولية.[19] سرطان الأوعية الصفراوية داخل الكبد إنگليزية: Intrahepatic cholangiocarcinoma (CCA) هو سرطان طلائي لأفرع الشجيرات الصفراوية داخل الكبد.[20] سرطان الأوعية الصفراوية داخل الكبد هو ثاني الأسباب المؤدية لسرطان الكبد الأولي.[20] وهو أكثر شيوعًا لدى الرجال وعادة ما يتم تشخيصه عند الأشخاص الذين تتراوح أعمارهم بين 60 و70 عامًا.[20] تشمل عوامل الخطر لتطور سرطان الأوعية الصفراوية داخل الكبد عدوى متأخر الخصية الزبادي Opisthorchis viverrini، متفرع الخصية الصيني Clonorchis sinensis، التهاب الأوعية الصفراوية المصلب، كيسات القناة الصفراوية، العمليات السابقة في الشجيرة الصفراوية، التعرض للثوروتراست والديوكسينات وتليف الكبد.[20] عادة ما يكون هذا السرطان بدون أعراض حتى يتقدم المرض. تشمل الأعراض آلام البطن والتعرق الليلي ونقص الوزن والإرهاق[20] علامات الكبد التي قد ترتفع مع الإصابة بسرطان الأوعية الصفراوية داخل الكبد هي المستضد السرطاني المضغي Carcinoembryonic antigen "CEA"، CA19-9، وCA-125.[20]
الغرن الكبدي الوعائي والغرن الوعائي
تعتبر هذه من سرطانات الكبد النادرة والخطيرة، ومع ذلك فهي ثالث أكثر أنواع سرطانات الكبد الأولية شيوعًا وتشكل 0.1-2.0٪ من سرطان الكبد الأولي.[21] يأتي الغرن الوعائي الكبدي Angiosarcoma والغرن الوعائي hemangiosarcoma في الكبد من الطبقة المبطنة للأوعية الدموية. نتائج علاج هذه الأورام سيئة لأنها سريعة النمو وسهلة الانتقال. كما أنه من الصعب تشخيصها لكنها عادة ما تكتشف عن طريق التصوير الطبقي المحوسب والتصوير بالرنين المغناطيسي الذي يظهر آفات بؤرية بكميات متفاوتة من الصدى (تحتوي هذه الأورام على كميات كبيرة من النزيف والأنسجة الميتة (النخر).[22] ينتج التشخيص النهائي عن طريق الخزعة مع تقييم الأنسجة المرضية.[21] في حين لا يتم تحديد السبب في كثير من الأحيان (75% تكون مجهولة السبب)، فهي مرتبطة بالتعرض لمواد مثل كلوريد الڤاينيل، الزرنيخ، الثوروتراست (على سبيل المثال التعرض المهني). يمثل الإشعاع أيضاً عامل خطر.[21] بين البالغين، هذه السرطانات أكثر شيوعاً بين الذكور؛ إلا أنه في الأطفال تكون أكثر شيوعاً بين الإناث.[21]
حتى مع الجراحة فغن مآل المرض يكون سيئاً حيث لا يعيش معظم المصابين أكثر من ستة أشهر بعد التشخيص. 3٪ فقط من الحالات فقط تعيش لأكثر من عامين.[21]
الورم الأرومي الكبدي
هناك نوع آخر من السرطانات التي تشكلها خلايا الكبد هو الورم الأرومي الكبدي hepatoblastoma، والذي يتكون تحديدًا من خلايا الكبد غير الناضجة.[19] وهو ورم خبيث نادر يتطور بشكل أساسي عند الأطفال، ويمثل ما يقرب من 1٪ من جميع السرطانات عند الأطفال و79٪ من جميع سرطانات الكبد الأولية تحت 15 سنة.[23][24] تتكون معظم الأورام الأرومية الكبدية في الفص الأيمن من الكبد.[25]
السرطانات المنتقلة إلى الكبد
العديد من السرطانات الموجودة في الكبد ليست سرطانات حقيقية للكبد لكنها سرطانات من أماكن أخرى في الجسم انتشرت إلى الكبد (المعروفة باسم النقائل). في كثير من الأحيان، يكون موقع المنشأ هو الجهاز الهضمي، نظرًا لأن الكبد قريب من العديد من هذه الأعضاء النشطة الأيضية والغنية بالدم بالقرب من الأوعية الدموية والعقد الليمفاوية (مثل سرطان الپنكرياس، سرطان المعدة، سرطان القولون والأورام السرطانية بشكل رئيسي من الزائدة الدودية)، لكن السرطانات تنتقل للكبد أيضاً من الثدي، المبيض، الرئة، الكلى، والپروستاتا.
الأطفال
طورت مجموعة علم أورام الأطفال (COG) بروتوكولًا للمساعدة في تشخيص أورام الكبد في مرحلة الطفولة وإدارتها.[26]
الأسباب
العدوى الڤيروسية
تعد العدوى الڤيروسية بفيروس التهاب الكبد الڤيروسي ج (HCV) أو ڤيروس التهاب الكبد الڤيروسي ب (HBV) السبب الرئيسي لسرطان الكبد في العالم اليوم، حيث يمثل 80٪ من حالات سرطان الكبد.[27][28][29] الرجال المصابون بڤيروس التهاب الكبد الڤيروسي ج أو التهاب الكبد الڤيروسي ب أكثر عرضة للإصابة بسرطان الكبد مقارنة بالنساء المصابات بڤيروس التهاب الكبد ج أو HBV المزمن؛ ومع ذلك، فإن أسباب هذا الاختلاف بين الجنسين غير معروفة. ترتبط عدوى ڤيروس التهاب الكبد الڤيروسي ب أيضًا بسرطان الأوعية الصفراوية.[30] دور الفيروسات الأخرى غير HCV أو HBV في سرطان الكبد أقل وضوحًا ، على الرغم من وجود بعض الأدلة على أن الإصابة المشتركة بڤيروس HBV والتهاب الكبد الڤيروسي د قد تزيد من خطر الإصابة بسرطان الكبد.[31]
قد يؤدي التهاب الكبد الڤيروسي ب والتهاب الكبد الڤيروسي ج إلى الإصابة بسرطان الكبد، لأن هذه العدوى الڤيروسية تسبب التهاب هائل، تليف، وفي النهاية يحدث تليف داخل الكبد.[32] بالإضافة إلى ذلك، تتشكل العديد من التغيرات الوراثية واللاجينية في خلايا الكبد أثناء الإصابة بڤيروس التهاب الكبد الڤيروسي ج والتهاب الكبد الڤيروسي ب، وهو عامل رئيسي في تكون أورام الكبد. تحفز الڤيروسات تغيرات خبيثة في الخلايا عن طريق تغيير مثيلة الجين، والتأثير على التعبير الجيني، وتعزيز أو قمع مسار تحويل الإشارة الخلوي. من خلال القيام بذلك، يمكن للڤيروسات منع الخلايا من الخضوع لشكل مبرمج من موت الخلايا (موت الخلايا المبرمج) وتعزيز تكاثر الڤيروس واستمراره.[27][33]
كما يحفظ التهاب الكبد الڤيروسي ب وج إحداث تغييرات خبيثة عن طريق التسبب في تلف الحمض النووي وعدم الاستقرار الجيني. يتم ذلك عن طريق تكوين أنواع الأكسجين التفاعلية، والپروتينات السريعة التي تتداخل مع إنزيمات إصلاح الحمض النووي، ويؤدي التهاب الكبد الڤيروسي إلى تنشيط التنشيط الناجم عن إنزيم السيتيدين.[34][35]
التليف الكبدي

بالإضافة إلى تليف الكبد المرتبط بالڤيروسات الموصوفة أعلاه، يمكن أن تؤدي الأسباب الأخرى لتليف الكبد إلى الإصابة بسرطان الكبد. يرتبط تناول الكحول بخطر الإصابة بسرطان الكبد، والخطر أكبر بكثير لدى الأفراد المصابين بتليف الكبد الناجم عن الكحول.[36] هناك عدد قليل من الاضطرابات المعروفة بأنها تسبب تليف الكبد وتؤدي إلى السرطان، بما في ذلك فرط حمل الحديد hemochromatosis وتليف الكبد الصفراوي الأولي primary biliary cirrhosis.[37]
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
السموم الفطرية
قد يؤدي التعرض للسموم الفطرية إلى الإصابة بسرطان الخلايا الكبدية.[38] السموم الفطرية هي مجموعة من المواد الكيميائية التي تنتجها فطريات "Aspergillus flavus". يؤدي تلوث الطعام بالفطريات إلى ابتلاع مواد كيميائية شديدة السمية للكبد. الأطعمة الشائعة الملوثة بالسموم هي الحبوب والفول السوداني والخضروات الأخرى. الكمية (الجرعة) والمدة التي يتعرض فيها الشخص للسموم الفطرية مرتبطة بسرطان الكبد.[38] يعد تلوث الطعام شائعًا في أفريقيا وجنوب شرق آسيا والصين. الآلية التي تسبب بها السموم الفطرية السرطان هي من خلال الطفرات والتغيرات الجينية. تحفز السموم الفطرية مجموعة من الطفرات،[39][40] بما في ذلك جين p53 الكابت للورم، وهو طفرة تظهر في أنواع كثيرة من السرطانات.[39] الطفرة في الجين p53، يفترض أنه، بالاقتران مع الطفرات الأخرى التي يسببها السموم الفطرية والتغيرات اللاجينية،[41] من المحتمل أن يكون سببًا شائعًا للتسرطن الناجم عن السموم الفطرية.
التهاب الكبد الدهني اللاكحولي (NASH) والكبد الدهني اللاكحولي (NAFL)
يعتبر التهاب الكبد الدهني اللاكحولي (NASH) والكبد الدهني اللاكحولي (NAFL) عامل خطر لسرطان الكبد، خاصة سرطان الخلايا الكبدية.[42] في السنوات الأخيرة، كانت هناك زيادة ملحوظة في عمليات زرع الكبد لسرطان الخلايا الكبدية والتي تُعزى إلى التهاب الكبد الدهني اللاكحولي.[38] هناك المزيد من الأبحاث المطلوبة حول التهاب الكبد الدهني اللاكحولي والكبد الدهني اللاكحولي.[42]
عوامل خطر أخرى لدى البالغين
- عقيدات خلل التنسج عالية الدرجة هي آفات سرطانية في الكبد. في غضون عامين، تبلغ نسبة خطر الإصابة بالسرطان الناتج عن هذه العقيدات 30-40٪.[43]
- تعتبر البدانة والمتلازمة الأيضية كعامل خطر هام، حيث يمكن أن تؤدي إلى التهاب الكبد الدهني.[29][44]
- يزيد داء السكري من خطر الإصابة بسرطان الخلايا الكبدية.[44][38]
- يزيد التدخين من خطر الإصابة بسرطان الخلايا الكبدية مقارنة بغير المدخنين أو المدخنين السابقين.[44]
- هناك حوالي 5-10٪ خطر على مدى العمر للإصابة بسرطان الأوعية الصفراوية لدى الأشخاص المصابين بالتهاب القنوات الصفراوية المصلب الأولي.[45]
- تزيد مثقبيات الكبد من خطر الإصابة بسرطان الأوعية الصفراوية، ولهذا تزداد معدلات انتشار هذا النوع من السرطان في تايلند بصفة خاصة.[46]
- ترتبط كيسات القناة الصفراوية ومرض كارولي والتليف الكبدي الخلقي بتطور سرطان الأوعية الصفراوية.[47]
- الحالات الوراثية: الاصطباغ الدموي الوراثي الغير معالج، نتيجة نقص ألفا-1 مضاد الترپبسين، داء اختزان الگليكوجن، البرفيرية الجلدية الآجلة، داء ولسون، فرط تايروسين الدم ترتبط جميعها بسرطان الخلايا الكبدية.[38][42]
- حبوب منع الحمل الفموية: لا توجد أدلة كافية لوصف حبوب منع الحمل الفموية كعامل خطر. ومع ذلك، فقد وجدت الدراسات الحديثة أن تناول حبوب منع الحمل الفموية لمدة تزيد عن 5 سنوات يرتبط بسرطان الكبد.[38]
الأطفال
سرطان الكبد شائع لدى الأطفال.[26] الأنواع الفرعية لسرطان الكبد الأكثر شيوعًا بين الأطفال هي الورم الأرومي الكبدي، سرطان الخلايا الكبدية، الساركوما الجنينية الكبدية، سرطان الكبد المشيمي الطفلي، والساركوما العضلية المخططة الصفراوية.[26] يمكن أن يكون سبب زيادة خطر الإصابة بسرطان الكبد لدى الأطفال هو متلازمة بيكوث-ڤيدمان (المرتبطة بالورم الأرومي الكبدي)،[48][49] داء السلائل الورمي الغدي العائلي (المرتبط بالورم الأرومي الكبدي المرتبط)،[49] انخفاض الوزن عند الولادة (المرتبط بالورم الأرومي الكبدي)،[25] الركود الصفراوي الكبدي العائلي المتقدم (المرتبط بسرطان الخلايا الكبدية)[50] والصبغي 18 (المرتبطة بالورم الأرومي الكبدي).[49]
التشخيص
تُستخدم العديد من طرق التصوير الطبي للمساعدة في تشخيص سرطان الكبد. بالنسبة لسرطان الكبد، تتضمن هذه الطرق الموجات فوق الصوتية الطبية، التصوير المقطعي المحوسب والتصوير بالرنين المغناطيسي. عند تصوير الكبد بالموجات فوق الصوتية، من المحتمل أن تكون الآفات الكبيرة لسرطان الكبد (على سبيل المثال، كتلة أكبر من 2 سم لديها فرصة أكثر من 95٪ لكونها سرطان كبد). سيكون أكثر وضوحًا عندما يتدفق التباين عبر شرايين الكبد (وتسمى أيضًا المرحلة الشريانية) وليس عندما يتدفق التباين عبر الأوردة (وتسمى أيضًا المرحلة الوريدية).[16] في بعض الأحيان، يطلب الأطباء خزعة من الكبد، إذا كانوا قلقين بشأن سرطان الكبد ولم يكن لدراسات التصوير (التصوير المقطعي المحوسب أو التصوير بالرنين المغناطيسي) نتائج واضحة.[16] تحدث غالبية سرطانات الأوعية الصفراوية في منطقة الكبد، وغالبًا ما تظهر على شكل انسداد في القناة الصفراوية. في حالة الاشتباه في أن سبب الانسداد خبيث، يُجرى تصوير الپنكرياس والأوعية الصفراوية بالتنظير الباطني (ERCP) والموجات فوق الصوتية والتصوير المقطعي المحوسب والتصوير بالرنين المغناطيسي وتصوير الپنكرياس والأوعية الصفراوية بالرنين المغناطيسي (MRCP).[51]
علامة الورم، وهي مواد كيميائية توجد أحيانًا في دم المصابين بالسرطان، يمكن أن تكون مفيدة في تشخيص ومراقبة مسار سرطان الكبد. يمكن العثور على مستويات عالية من فپروتين ألفا (AFP) في الدم في العديد من حالات سرطان الكبد الوبائي وسرطان الأوعية الصفراوية داخل الكبد.[16] وتجدر الإشارة إلى أن الـ AFP هو الأكثر فائدة لرصد ما إذا كانت سرطانات الكبد تعود بعد العلاج وليس للتشخيص الأولي.[16] يمكن الكشف عن سرطان الأوعية الصفراوية باستخدام علامات الورم الشائعة الاستخدام: مستضد الكربوهيدرات 19-9 (CA 19-9)، مستضد السرطانات المضغية (CEA) ومستضد السرطان 125 (CA125). توجد علامات الورم هذه في سرطانات الكبد الأولية، وكذلك في سرطانات أخرى وبعض الاضطرابات الأخرى.[52][53]
الوقاية
يمكن تقسيم الوقاية من السرطانات إلى الوقاية الأولية والثانوية والثالثية. تقلل الوقاية الأولية بشكل استباقي من التعرض لعامل خطر للإصابة بسرطان الكبد. أحد أكثر وسائل الوقاية الأولية من سرطان الكبد نجاحًا هو التطعيم ضد التهاب الكبد الڤيروسي ب.[42] التلقيح ضد ڤيروس التهاب الكبد الڤيروسي ج غير متوفر حالياً.[54] تهدف الأشكال الأخرى للوقاية الأولية إلى الحد من انتقال هذه الڤيروسات من خلال تعزيز ممارسات الحقن الآمنة، وفحص منتجات التبرع بالدم، وفحص الأشخاص المعرضين لمخاطر عالية بدون أعراض.[54] يمكن تجنب التعرض للسموم الفطرية عن طريق تدخل ما بعد الحصاد لتثبيط العفن، والذي كان فعالاً في غرب أفريقيا. كما أن تقليل تناول الكحوليات وعلاج البدانة وضبط داء السكري من شأنه أن يقلل أيضًا من معدلات الإصابة بسرطان الكبد. التحكم في النظام الغذائي في داء ترسب الأصبغة الدموية يمكن أن يقلل من خطر الحديد الزائد، مما يقلل من خطر الإصابة بالسرطان.[55]
تشمل الوقاية الثانوية كلاً من علاج العامل المشارك في تكوين السرطان (التسرطن) والوقاية من التسرطن إذا لم يكن ذلك ممكنًا. لا يمكن علاج الأفراد المصابين بالڤيروس، ولكن العلاج بالعقاقير المضادة للڤيروسات يمكن أن يقلل من خطر الإصابة بسرطان الكبد. قد يكون للكلوروفيلين إمكانية الحد من تأثيرات السموم الفطرية.[55]
تشمل الوقاية من الدرجة الثالثة علاجات لمنع تكرار الإصابة بسرطان الكبد. وتشمل هذه استخدام التدخلات الجراحية وأدوية العلاج الكيميائي والأدوية المضادة للڤيروسات.[55]
العلاج
اعتبارات عامة
مثل العديد من أنواع السرطان، يعتمد علاج سرطان الكبد على النوع المحدد للسرطان بالإضافة إلى مرحلة المرض. الطريقة الرئيسية التي يتم بها إدارة السرطان تعتمد على أنظمة مراحل TMN. هناك أيضًا أنظمة تصنيف محددة لسرطان الكبد، ولكل منها خيارات علاجية قد تؤدي إلى عدم عودة السرطان أو العلاج.[56][57] [58] (انظر الاستئصال بالتردد الراديوي) على سبيل المثال، في حالة سرطان الخلايا الكبدية يشيع استخدام نظام الكبد السريري-برلشونة لمراحل السرطان.[38]
تشمل العلاجات الجراحة والأدوية وطرق الاستئصال الموضحة في الأقسام أدناه. هناك العديد من أدوية العلاج الكيميائي المعتمدة لسرطان الكبد بما في ذلك: أتزوليزوماب، نيڤولوماب، كايترودا، ستيڤارگا، وغيرها.[59] على نحو متزايد، تستخدم عوامل العلاج المناعي (وتسمى أيضًا علاجات السرطان المستهدفة أو الطب الدقيق) لعلاج سرطان الكبد الصفراوي.[60]
سرطان الخلايا الكبدية
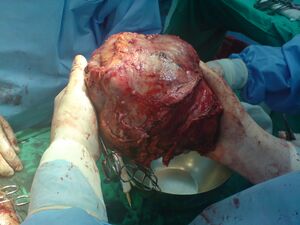
الاستئصال الجراحي هو العلاج الموصى به لسرطان الخلايا الكبدية (HCC) عندما تكون معدلات وظائف الكبد لدى المرضى مناسبة.[38] تحسنت معدلات البقاء لخمس سنوات بشكل كبير خلال العقود القليلة الماضية ويمكن أن تتراوح الآن من 41 إلى 74٪.[38] ومع ذلك، يمكن أن تتجاوز معدلات الانتكاس بعد الاستئصال 70٪، سواء كان ذلك بسبب انتشار الورم الأولي أو تكوين أورام جديدة.[61] يمكن أيضاً اعتبار زرع الكبد خياراً لعلاج سرطان الخلايا الكبدية حيث يمكن تحمل هذا النوع من العلاج والورم يلائم معايير محددة (مثل معايير ميلانو). بشكل عام، بالنسبة لزراعة الكبد، فيوصى بها للمرضى الذين يعانون من آفات كبدية متعددة، أو خلل وظيفي حاد في الكبد، أو كليهما.
الاستئصال عن طريق الجلد هو العلاج الوحيد غير الجراحي الذي يمكن أن يوفر علاجاً. هناك العديد من أشكال الاستئصال عن طريق الجلد، والتي تتكون إما من حقن مواد كيميائية في الكبد (الإيثانول أو حمض الأسيتيك) أو إنتاج درجات حرارة قصوى باستخدام الاستئصال بالتردد الراديوي، الميكروويڤ، الليزر أو العلاج بالتبريد. من بين هؤلاء، يتمتع الاستئصال بالترددات الراديوية بأحد أفضل السمعة في سرطان الكبد، ولكن القيود تشمل عدم القدرة على علاج الأورام القريبة من الأعضاء والأوعية الدموية الأخرى بسبب توليد الحرارة وتأثير المشتت الحراري، على التوالي.[62][63]
بالإضافة إلى ذلك لم تدرس جيدًا نتائج إجراءات الاستئصال عن طريق الجلد لمرض سرطان الكبد على المدى الطويل. بشكل عام، الجراحة هي طريقة العلاج المفضلة عندما يكون ذلك ممكنًا.
لا يستخدم العلاج الكيميائي بشكل روتيني لعلاج سرطان الكبد، على الرغم من أنه يمكن استخدام العلاج الكيميائي الموضعي في إجراء يعرف باسم الانصمام الكيميائي عبر الشرايين (TACE). في هذا الإجراء، تستخدم الأدوية التي تقتل الخلايا السرطانية وتقطع تدفق الدم على الورم. نظرًا لأن معظم الأدوية الجهازية ليس لها فعالية في علاج سرطان الكبد، فإن البحث في المسارات الجزيئية المتضمنة في إنتاج سرطان الكبد أسفر عن استخدام السورافنيب، وهو علاج موجه يمنع تكاثر الخلايا ونمو خلايا الدم. حصل السورافنيب على موافقة إدارة الغذاء والدواء الأمريكية (FDA) لعلاج سرطان الخلايا الكبدية المتقدم في نوفمبر 2007.[64] يوفر هذا الدواء زيادة في معدل البقاء على قيد الحياة لمرضى سرطان الخلايا الكبدية المتقدم.[63]
يعتبر الانصمام الإشعاعي عبر الشرايين (TRACE) خيارًا آخر لعلاج سرطان الخلايا الكبدية.[38] في هذا الإجراء، يستهدف العلاج الإشعاعي الورم. لا يزال TRACE يعتبر إضافة على العلاج وليس الخيار الأول لعلاج سرطان الخلايا الكبدية،[38] نظرًا لأن العلاجات المزدوجة من العلاج الإشعاعي بالإضافة إلى الانصمام الكيميائي أو العلاج الكيميائي الموضعي أو العلاج الكيميائي الجهازي أو أدوية العلاج الموجه قد تظهر فائدة على العلاج الإشعاعي وحده.[65]
طرق الاجتثاث (مثل الاجتثاث بالترددات الراديوية أو الاجتثاث بالموجات الدقيقة) هي أيضًا خيار لعلاج سرطان الكبد.[38][66] يوصى بهذه الطريقة لأورام الكبد الصغيرة الموضعية حيث يوصى بأن تكون المنطقة المعالجة بالترددات الراديوية 2 سم أو أقل.[66]

. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
سرطان الأوعية الصفراوية داخل الكبد
الاستئصال هو أحد خيارات علاج سرطان الأوعية الصفراوية، لكن أقل من 30٪ من حالات سرطان الأوعية الصفراوية يمكن استئصالها عند التشخيص. السبب في أن غالبية أورام الأوعية الصفراوية داخل الكبد لا يمكن إزالتها جراحيًا هو أنه غالبًا ما يكون هناك أورام بؤرية متعددة داخل الكبد.[67] بعد الجراحة، تصل معدلات عودة المرض إلى 60٪.[68][69] يمكن استخدام زراعة الكبد عندما لا يكون الاستئصال الجزئي خيارًا، وقد يفيد العلاج الكيميائي المساعد في بعض الحالات.[45]
يتكون 60٪ من أورام الأوعية الصفراوية في منطقة محيط نقي ويمكن استخدام العلاج الضوئي لتحسين جودة الحياة ومعدل البقاء على قيد الحياة في الحالات غير القابلة للاستئصال.[47] العلاج الضوئي هو علاج جديد يستخدم الجزيئات المنشطة بالضوء لعلاج الورم. يتم تنشيط المركبات في منطقة الورم بواسطة ضوء الليزر، مما يتسبب في إطلاق أنواع الأكسجين التفاعلية السامة، مما يؤدي إلى قتل الخلايا السرطانية.[68][70]
تُستخدم العلاجات الكيميائية الجهازية مثل الجمسيتابين والسيسپلاتين أحيانًا في حالات سرطان الأوعية الصفراوية الغير قابلة للعلاج الجراحي.[45]
الاجتثاث بالترددات الراديوية، الانصمام الكيميائي عبر الشرايين والعلاج الإشعاعي الداخلي (المعالجة القريبة) جميعها علاجات مبشرة لسرطان الأوعية الصفراوية[69] ويمكنها أحياناً تحسين تدفق الصفراء، مما يقلل من ألأعراض التي يعاني منها المريض.[67]
يمكن استخدام العلاج الإشعاعي في الإعداد المساعد أو العلاج الملطف لسرطان الأوعية الصفراوية.[71]
الورم الأرومي الكبدي
لعلاج الورم الأرومي الكبدي يمكن إزالة الورم إما بالاستئصال الجراحي أو زرع الكبد. في بعض الحالات يمكن أن تقدم الجراحة علاجًا. يمكن استخدام العلاج الكيميائي قبل وبعد الجراحة والزرع.[72]
العلاج الكيميائي للورم الأرومي الكبدي، يشمل السيسپلاتين، الڤينكريستين، السيكلوفوسفاميد، الدوكسوروبيسين. من بين هذه الأدوية، يبدو أن السيسپلاتين هو الأكثر فعالية.[73]
الغرن الكبدي الوعائي والغرن الوعائي
ينتهي المطاف بالعديد من هذه الأورام بأنها غير قابلة للعلاج الجراحي.[22] تشمل خيارات العلاج الاستئصال الجراحي لأجزاء الكبد المصابة.[21] زراعة الكبد والعلاج الكيميائي غير فعال للغرن الكبدي الوعائي والغرن الوعائي.[21]
علم الأوبئة
عالمياً، يعتبر سرطان الكبد منتشرًا ومتزايدًا.[10] تقترح معظم البيانات الوبائية الحديثة إلى أن سرطان الكبد من بين السرطان العشرة الأولى من حيث الانتشار والوفيات (يُشار إلى أنه السبب الرئيسي السادس للسرطان ورابع أكثر أسباب الوفاة شيوعًا).[42] وجد الصندوق العالمي لتعاون عبء مرضى سرطان الكبد أنه من عام 1990 حتى 2015، زادت الحالات الجديدة لسرطان الكبد سنويًا بنسبة 75٪.[10] تشير التقديرات المستندة لأحدث البيانات إلى أن هناك 841.000 تشخيص جديد لسرطان الكبد سنوياً و782.000 حالة وفاة في جميع أنحاء العالم.[54] سرطان الكبد هو أكثر أنواع السرطانات شيوعًا في مصر وگامبيا وغينيا ومنغوليا وكمبوديا وڤيتنام.[54] من حيث تفصيل النوع، فإن سرطان الكبد على مستوى العالم أكثر شيوعًا بين الرجال منه بين النساء.[42][54]
بالنظر إلى أن سرطان الخلايا الكبدية هو النوع الأكثر شيوعًا من سرطان الكبد، فإن المناطق حول العالم التي يوجد بها أكثر حالات سرطان الكبد الجديدة كل عام هي شمال وغرب أفريقيا بالإضافة إلى شرق وجنوب شرق آسيا..[42] يوجد في الصين 50٪ من حالات سرطان الخلايا الكبدية على مستوى العالم، وأكثر من 80٪ من إجمالي الحالات تحدث في أفريقيا جنوب الصحراء أو في شرق آسيا بسبب ڤيروس التهاب الكبد الڤيروسي ب.[46][74] في هذه المناطق ذات العبء المرضي المرتفع، تشير الدلائل إلى أن غالبية حالات العدوى بڤيروس التهاب الكبد الڤيروسي ب وج تحدث عن طريق الانتقال في الفترة المحيطة بالولادة (يُسمى أيضًا انتقال العدوى من الأم إلى الطفل).[42]
ومع ذلك، من المهم ملاحظة أن عوامل الخطر الخاصة بسرطان الكبد تختلف باختلاف المنطقة الجغرافية. على سبيل المثال، في الصين العدوى المزمنة بالتهاب الكبد الڤيروسي ب والسموم الفطرية هما أكبر عوامل الخطر؛ في حين أنه في منغوليا مزيج من التهاب الكبد الوبائي والتهاب الكبد الڤيروسي المشترك ومستويات عالية من احتساء الكحول التي تؤدي إلى ارتفاع مستويات سرطان الخلايا الكبدية.[54]
فيما يتعلق بسرطان الأوعية الصفراوية داخل الكبد، لا توجد حاليًا بيانات وبائية كافية لأنه سرطان نادر. وفقًا للمعهد الوطني للسرطان بالولايات المتحدة، فإن الإصابة بسرطان الأوعية الصفراوية غير معروفة. يتميز سرطان الأوعية الصفراوية أيضًا بتوزيع جغرافي كبير، حيث تظهر تايلاند أعلى المعدلات في جميع أنحاء العالم بسبب وجود مثقبيات الكبد.[46][75]
في الولايات المتحدة، كان هناك 42.810 حالة جديدة من سرطان الكبد والقناة الصفراوية داخل الكبد عام 2020، وهو ما يمثل 2.4٪ من جميع حالات السرطان الجديدة في الولايات المتحدة.[76] هناك حوالي 89.950 شخصًا مصابين بسرطان الكبد وسرطان الأوعية الصفراوية داخل الكبد في الولايات المتحدة.[76] من حيث الوفيات، فإن معدل البقاء على قيد الحياة لمدة 5 سنوات لسرطان الكبد وسرطان الأوعية الصفراوية داخل الكبد في الولايات المتحدة هو 19.6٪.[76] في الولايات المتحدة، هناك احتمال بنسبة 1٪ للإصابة بسرطان الكبد طوال العمر، مما يجعل هذا السرطان نادرًا نسبيًا.[76] على الرغم من قلة عدد الحالات، إلا أنه أحد الأسباب الرئيسية للوفيات بالسرطان.[42]
المصادر
- ^ أ ب ت ث ج ح خ "Adult Primary Liver Cancer Treatment (PDQ®)–Patient Version". NCI. 6 July 2016. Archived from the original on 2 October 2016. Retrieved 29 September 2016.
- ^ أ ب ت "SEER Stat Fact Sheets: Liver and Intrahepatic Bile Duct Cancer". NCI. Archived from the original on 2017-07-28.
- ^ أ ب ت ث ج ح خ د ذ World Cancer Report 2014. World Health Organization. 2014. pp. Chapter 5.6. ISBN 978-9283204299.
- ^ أ ب GBD 2013 Mortality Causes of Death Collaborators (January 2015). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013". Lancet. 385 (9963): 117–171. doi:10.1016/S0140-6736(14)61682-2. PMC 4340604. PMID 25530442.
{{cite journal}}:|author1=has generic name (help)CS1 maint: numeric names: authors list (link) - ^ "がん診療連携拠点病院等院内がん登録生存率集計:[国立がん研究センター がん登録・統計]". ganjoho.jp. Retrieved 2 February 2020.
- ^ Vos, Theo; et al. (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
- ^ أ ب ت Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A (November 2018). "Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries". CA. 68 (6): 394–424. doi:10.3322/caac.21492. PMID 30207593. S2CID 52188256.
- ^ أ ب ت Bruix J, Han KH, Gores G, Llovet JM, Mazzaferro V (April 2015). "Liver cancer: Approaching a personalized care". Journal of Hepatology. 62 (1 Suppl): S144–S156. doi:10.1016/j.jhep.2015.02.007. PMC 4520430. PMID 25920083.
- ^ أ ب Mantovani A, Targher G (July 2017). "Type 2 diabetes mellitus and risk of hepatocellular carcinoma: spotlight on nonalcoholic fatty liver disease". Annals of Translational Medicine. 5 (13): 270. doi:10.21037/atm.2017.04.41. PMC 5515814. PMID 28758096.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ أ ب ت Akinyemiju T, Abera S, Ahmed M, Alam N, Alemayohu MA, Allen C, et al. (December 2017). "The Burden of Primary Liver Cancer and Underlying Etiologies From 1990 to 2015 at the Global, Regional, and National Level: Results From the Global Burden of Disease Study 2015". JAMA Oncology. 3 (12): 1683–1691. doi:10.1001/jamaoncol.2017.3055. hdl:10037/11672. PMC 5824275. PMID 28983565.
- ^ Cholangiocarcinoma at eMedicine
- ^ "Liver tumors in Children". Boston Children's Hospital. Archived from the original on 2011-06-04.
- ^ Table 37.2 in: Sternberg S (2012). Sternberg's diagnostic surgical pathology. Place of publication not identified: LWW. ISBN 978-1-4511-5289-0. OCLC 953861627.
- ^ Yang JD, Hainaut P, Gores GJ, Amadou A, Plymoth A, Roberts LR (October 2019). "A global view of hepatocellular carcinoma: trends, risk, prevention and management". Nature Reviews. Gastroenterology & Hepatology. 16 (10): 589–604. doi:10.1038/s41575-019-0186-y. PMC 6813818. PMID 31439937.
- ^ Mokdad AA, Singal AG, Yopp AC (2015-12-22). "JAMA PATIENT PAGE. Liver Cancer". JAMA. 314 (24): 2701. doi:10.1001/jama.2015.15425. PMID 26720038.
- ^ أ ب ت ث ج "Adult Primary Liver Cancer Treatment (PDQ®)–Health Professional Version - National Cancer Institute". www.cancer.gov (in الإنجليزية). 2021-01-15. Retrieved 2021-02-25.
- ^ Mitchell DG, Bruix J, Sherman M, Sirlin CB (March 2015). "LI-RADS (Liver Imaging Reporting and Data System): summary, discussion, and consensus of the LI-RADS Management Working Group and future directions". Hepatology. 61 (3): 1056–1065. doi:10.1002/hep.27304. PMID 25041904. S2CID 205894014.
- ^ Khan SA, Davidson BR, Goldin RD, Heaton N, Karani J, Pereira SP, et al. (December 2012). "Guidelines for the diagnosis and treatment of cholangiocarcinoma: an update". Gut. 61 (12): 1657–1669. doi:10.1136/gutjnl-2011-301748. PMID 22895392.
- ^ أ ب Ahmed I, Lobo DN (January 2009). "Malignant tumours of the liver". Surgery. Oxford. 27 (1): 30–37. doi:10.1016/j.mpsur.2008.12.005.
- ^ أ ب ت ث ج ح Dooley JS, Lok AS, Garcia-Tsao G, Pinzani M (8 June 2018). Sherlock's Diseases of the Liver and Biliary System. pp. 705–729. ISBN 978-1-119-23764-8. OCLC 1187411089.
- ^ أ ب ت ث ج ح خ Kumar A, Sharma B, Samant H (2021). "Liver Angiosarcoma". StatPearls. Treasure Island (FL): StatPearls Publishing. PMID 30855812. Retrieved 2021-02-25.
- ^ أ ب "Editor's Pick: Primary Hepatic Angiosarcoma: A Brief Review of the Literature". European Medical Journal (in الإنجليزية البريطانية). 2018-05-31. Retrieved 2021-02-25.
- ^ PDQ Pediatric Treatment Editorial Board (2002), Childhood Liver Cancer Treatment (PDQ®): Health Professional Version, Bethesda (MD): National Cancer Institute (US), PMID 26389232, http://www.ncbi.nlm.nih.gov/books/NBK65790/, retrieved on 2021-02-25
- ^ Khanna R, Verma SK (September 2018). "Pediatric hepatocellular carcinoma". World Journal of Gastroenterology. 24 (35): 3980–3999. doi:10.3748/wjg.v24.i35.3980. PMC 6148423. PMID 30254403.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ أ ب Emre S, McKenna GJ (December 2004). "Liver tumors in children". Pediatric Transplantation. 8 (6): 632–638. doi:10.1111/j.1399-3046.2004.00268.x. PMID 15598339. S2CID 35883310.
- ^ أ ب ت "Childhood Liver Cancer Treatment (PDQ®)–Health Professional Version - National Cancer Institute". www.cancer.gov (in الإنجليزية). 2020-11-27. Retrieved 2021-02-25.
- ^ أ ب Arzumanyan A, Reis HM, Feitelson MA (February 2013). "Pathogenic mechanisms in HBV- and HCV-associated hepatocellular carcinoma". Nature Reviews. Cancer. 13 (2): 123–135. doi:10.1038/nrc3449. PMID 23344543. S2CID 29447705.
- ^ Rosen HR (June 2011). "Clinical practice. Chronic hepatitis C infection". The New England Journal of Medicine. 364 (25): 2429–2438. doi:10.1056/NEJMcp1006613. PMID 21696309. S2CID 19755395.
- ^ أ ب "General Information About Adult Primary Liver Cancer". National Cancer Instituteb. 1980-01-01. Archived from the original on 2 January 2013. Retrieved 13 January 2013.
- ^ Ralphs S, Khan SA (May 2013). "The role of the hepatitis viruses in cholangiocarcinoma". Journal of Viral Hepatitis. 20 (5): 297–305. doi:10.1111/jvh.12093. PMID 23565610. S2CID 44318080.
- ^ Kew MC (March 2013). "Hepatitis viruses (other than hepatitis B and C viruses) as causes of hepatocellular carcinoma: an update". Journal of Viral Hepatitis. 20 (3): 149–157. doi:10.1111/jvh.12043. PMID 23383653. S2CID 206164005.
- ^ Dooley JS, Lok AS, Garcia-Tsao G, Pinzani M (8 June 2018). Dooley JS, Lok AS, Garcia-Tsao G, Pinzani M (eds.). Sherlock's diseases of the liver and biliary system. ISBN 978-1-119-23756-3. OCLC 1019837000.
- ^ Jeong SW, Jang JY, Chung RT (December 2012). "Hepatitis C virus and hepatocarcinogenesis". Clinical and Molecular Hepatology. 18 (4): 347–356. doi:10.3350/cmh.2012.18.4.347. PMC 3540370. PMID 23323249.
- ^ Takeda H, Takai A, Inuzuka T, Marusawa H (January 2017). "Genetic basis of hepatitis virus-associated hepatocellular carcinoma: linkage between infection, inflammation, and tumorigenesis". Journal of Gastroenterology. 52 (1): 26–38. doi:10.1007/s00535-016-1273-2. PMID 27714455.
- ^ Yang SF, Chang CW, Wei RJ, Shiue YL, Wang SN, Yeh YT (2014). "Involvement of DNA damage response pathways in hepatocellular carcinoma". BioMed Research International. 2014: 153867. doi:10.1155/2014/153867. PMC 4022277. PMID 24877058.
- ^ Du X, Hidayat K, Shi BM (June 2017). "Abdominal obesity and gastroesophageal cancer risk: systematic review and meta-analysis of prospective studies". Bioscience Reports. 37 (3): BSR20160474. doi:10.1042/BSR20160474. PMC 5426287. PMID 28336766.
- ^ Fattovich G, Stroffolini T, Zagni I, Donato F (November 2004). "Hepatocellular carcinoma in cirrhosis: incidence and risk factors". Gastroenterology. 127 (5 Suppl 1): S35–S50. doi:10.1053/j.gastro.2004.09.014. PMID 15508101.
- ^ أ ب ت ث ج ح خ د ذ ر ز س Balogh J, Victor D, Asham EH, Burroughs SG, Boktour M, Saharia A, et al. (October 2016). "Hepatocellular carcinoma: a review". Journal of Hepatocellular Carcinoma. 3: 41–53. doi:10.2147/JHC.S61146. PMC 5063561. PMID 27785449.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ أ ب Smela ME, Currier SS, Bailey EA, Essigmann JM (April 2001). "The chemistry and biology of aflatoxin B(1): from mutational spectrometry to carcinogenesis". Carcinogenesis. 22 (4): 535–545. doi:10.1093/carcin/22.4.535. PMID 11285186.
- ^ Perduca V, Omichessan H, Baglietto L, Severi G (January 2018). "Mutational and epigenetic signatures in cancer tissue linked to environmental exposures and lifestyle". Current Opinion in Oncology. 30 (1): 61–67. doi:10.1097/CCO.0000000000000418. PMID 29076965. S2CID 20842446.
- ^ Dai Y, Huang K, Zhang B, Zhu L, Xu W (November 2017). "Aflatoxin B1-induced epigenetic alterations: An overview". Food and Chemical Toxicology. 109 (Pt 1): 683–689. doi:10.1016/j.fct.2017.06.034. PMID 28645871.
- ^ أ ب ت ث ج ح خ د ذ "Liver (Hepatocellular) Cancer Prevention (PDQ®)–Health Professional Version - National Cancer Institute". www.cancer.gov (in الإنجليزية). 2005-05-23. Retrieved 2021-02-23.
- ^ Di Tommaso L, Sangiovanni A, Borzio M, Park YN, Farinati F, Roncalli M (April 2013). "Advanced precancerous lesions in the liver". Best Practice & Research. Clinical Gastroenterology. 27 (2): 269–284. doi:10.1016/j.bpg.2013.03.015. PMID 23809245.
- ^ أ ب ت Chuang SC, La Vecchia C, Boffetta P (December 2009). "Liver cancer: descriptive epidemiology and risk factors other than HBV and HCV infection". Cancer Letters. 286 (1): 9–14. doi:10.1016/j.canlet.2008.10.040. hdl:11585/682618. PMID 19091458.
- ^ أ ب ت Razumilava N, Gores GJ (January 2013). "Classification, diagnosis, and management of cholangiocarcinoma". Clinical Gastroenterology and Hepatology. 11 (1): 13–21.e1, quiz e3–4. doi:10.1016/j.cgh.2012.09.009. PMC 3596004. PMID 22982100.
- ^ أ ب ت Jemal A, Bray F, Center MM, Ferlay J, Ward E, Forman D (Mar–Apr 2011). "Global cancer statistics". CA. 61 (2): 69–90. doi:10.3322/caac.20107. PMID 21296855. S2CID 30500384.
- ^ أ ب Patel T (April 2011). "Cholangiocarcinoma--controversies and challenges". Nature Reviews. Gastroenterology & Hepatology. 8 (4): 189–200. doi:10.1038/nrgastro.2011.20. PMC 3888819. PMID 21460876.
- ^ DeBaun MR, Tucker MA (March 1998). "Risk of cancer during the first four years of life in children from The Beckwith-Wiedemann Syndrome Registry". The Journal of Pediatrics. 132 (3 Pt 1): 398–400. doi:10.1016/S0022-3476(98)70008-3. PMID 9544889.
- ^ أ ب ت Spector LG, Birch J (November 2012). "The epidemiology of hepatoblastoma". Pediatric Blood & Cancer. 59 (5): 776–779. doi:10.1002/pbc.24215. PMID 22692949. S2CID 65545.
- ^ Davit-Spraul A, Gonzales E, Baussan C, Jacquemin E (January 2009). "Progressive familial intrahepatic cholestasis". Orphanet Journal of Rare Diseases. 4: 1. doi:10.1186/1750-1172-4-1. PMC 2647530. PMID 19133130.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Ariff B, Lloyd CR, Khan S, Shariff M, Thillainayagam AV, Bansi DS, et al. (March 2009). "Imaging of liver cancer". World Journal of Gastroenterology. 15 (11): 1289–1300. doi:10.3748/wjg.15.1289. PMC 2658841. PMID 19294758.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Malaguarnera G, Paladina I, Giordano M, Malaguarnera M, Bertino G, Berretta M (2013). "Serum markers of intrahepatic cholangiocarcinoma". Disease Markers. 34 (4): 219–228. doi:10.1155/2013/196412. PMC 3809974. PMID 23396291.
- ^ Zhao YJ, Ju Q, Li GC (July 2013). "Tumor markers for hepatocellular carcinoma". Molecular and Clinical Oncology. 1 (4): 593–598. doi:10.3892/mco.2013.119. PMC 3915636. PMID 24649215.
- ^ أ ب ت ث ج ح Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A (November 2018). "Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries". CA. 68 (6): 394–424. doi:10.3322/caac.21492. PMID 30207593.
- ^ أ ب ت Hoshida Y, Fuchs BC, Tanabe KK (November 2012). "Prevention of hepatocellular carcinoma: potential targets, experimental models, and clinical challenges". Current Cancer Drug Targets. 12 (9): 1129–1159. doi:10.2174/156800912803987977. PMC 3776581. PMID 22873223.
- ^ Yen YH, Cheng YF, Wang JH, Lin CC, Chen YY, Yong CC, et al. (2020-03-12). "Real world clinical practice in treating advanced hepatocellular carcinoma: When East meets West". PLOS ONE. 15 (3): e0230005. Bibcode:2020PLoSO..1530005Y. doi:10.1371/journal.pone.0230005. PMC 7067409. PMID 32163475.
- ^ Bruix J, Sherman M (March 2011). "Management of hepatocellular carcinoma: an update". Hepatology. 53 (3): 1020–1022. doi:10.1002/hep.24199. PMC 3084991. PMID 21374666.
- ^ Chen CH (2016-12-01). "Percutaneous radiofrequency ablation for hepatocellular carcinoma: Shortened duration does not comprise its efficacy". Advances in Digestive Medicine (in الإنجليزية). 3 (4): 149–150. doi:10.1016/j.aidm.2016.10.001. S2CID 44047011.
- ^ "Drugs Approved for Liver Cancer - National Cancer Institute". www.cancer.gov (in الإنجليزية). 2011-10-04. Retrieved 2021-02-25.
- ^ "Targeted Cancer Therapies Fact Sheet - National Cancer Institute". www.cancer.gov (in الإنجليزية). 2021-01-25. Retrieved 2021-02-25.
- ^ Bruix J, Sherman M (March 2011). "Management of hepatocellular carcinoma: an update". Hepatology. 53 (3): 1020–1022. doi:10.1002/hep.24199. PMC 3084991. PMID 21374666.
- ^ Wang Z, Zhang G, Wu J, Jia M (August 2013). "Adjuvant therapy for hepatocellular carcinoma: current situation and prospect". Drug Discoveries & Therapeutics. 7 (4): 137–143. doi:10.5582/ddt.2013.v7.4.137. PMID 24071575.
- ^ أ ب de Lope CR, Tremosini S, Forner A, Reig M, Bruix J (2012). "Management of HCC". Journal of Hepatology. 56 (Suppl 1): S75–S87. doi:10.1016/S0168-8278(12)60009-9. PMID 22300468.
- ^ Keating GM, Santoro A (2009). "Sorafenib: a review of its use in advanced hepatocellular carcinoma". Drugs. 69 (2): 223–240. doi:10.2165/00003495-200969020-00006. PMID 19228077.
- ^ Feng M, Ben-Josef E (October 2011). "Radiation therapy for hepatocellular carcinoma". Seminars in Radiation Oncology. 21 (4): 271–277. doi:10.1016/j.semradonc.2011.05.002. PMID 21939856.
- ^ أ ب Tarasik A, Jaroszewicz J, Januszkiewicz M (March 2017). "Surgical treatment of liver tumors - own experience and literature review". Clinical and Experimental Hepatology. 3 (1): 1–8. doi:10.5114/ceh.2017.65498. PMC 5497454. PMID 28856283.
- ^ أ ب "Bile Duct Cancer (Cholangiocarcinoma) Treatment (PDQ®)–Health Professional Version - National Cancer Institute". www.cancer.gov (in الإنجليزية). 2021-02-19. Retrieved 2021-02-25.
- ^ أ ب Ulstrup T, Pedersen FM (February 2013). "[Photodynamic therapy of cholangiocarcinomas]". Ugeskrift for Laeger. 175 (9): 579–582. PMID 23608009.
- ^ أ ب Kuhlmann JB, Blum HE (May 2013). "Locoregional therapy for cholangiocarcinoma". Current Opinion in Gastroenterology. 29 (3): 324–328. doi:10.1097/MOG.0b013e32835d9dea. PMID 23337933. S2CID 37403999.
- ^ Ortner MA (September 2011). "Photodynamic therapy for cholangiocarcinoma". Lasers in Surgery and Medicine. 43 (7): 776–780. doi:10.1002/lsm.21106. PMID 22057505. S2CID 36852386.
- ^ Valero V, Cosgrove D, Herman JM, Pawlik TM (August 2012). "Management of perihilar cholangiocarcinoma in the era of multimodal therapy". Expert Review of Gastroenterology & Hepatology. 6 (4): 481–495. doi:10.1586/egh.12.20. PMC 3538366. PMID 22928900.
- ^ Meyers RL, Czauderna P, Otte JB (November 2012). "Surgical treatment of hepatoblastoma". Pediatric Blood & Cancer. 59 (5): 800–808. doi:10.1002/pbc.24220. PMID 22887704. S2CID 27329163.
- ^ Perilongo G, Malogolowkin M, Feusner J (November 2012). "Hepatoblastoma clinical research: lessons learned and future challenges". Pediatric Blood & Cancer. 59 (5): 818–821. doi:10.1002/pbc.24217. PMID 22678761. S2CID 19059413.
- ^ El-Serag HB, Rudolph KL (June 2007). "Hepatocellular carcinoma: epidemiology and molecular carcinogenesis". Gastroenterology. 132 (7): 2557–2576. doi:10.1053/j.gastro.2007.04.061. PMID 17570226.
- ^ Khan SA, Toledano MB, Taylor-Robinson SD (2008). "Epidemiology, risk factors, and pathogenesis of cholangiocarcinoma". HPB. 10 (2): 77–82. doi:10.1080/13651820801992641. PMC 2504381. PMID 18773060.
- ^ أ ب ت ث "Cancer of the Liver and Intrahepatic Bile Duct - Cancer Stat Facts". SEER (in الإنجليزية). Retrieved 2021-02-23.
وصلات خارجية
| Classification | |
|---|---|
| External resources |
- CS1 errors: generic name
- CS1 maint: numeric names: authors list
- CS1 maint: unflagged free DOI
- CS1 الإنجليزية البريطانية-language sources (en-gb)
- الصفحات بخصائص غير محلولة
- Articles containing إنگليزية-language text
- Articles with hatnote templates targeting a nonexistent page
- أورام الجهاز الهضمي
- أمراض الكبد
- طب الكبد