فقر دم
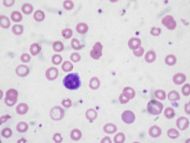
| Peripheral blood smear microscopy of a patient with iron-deficiency anemia. | |
| ICD-10 | D50.-D64. |
| ICD-9 | 280-285 |
| DiseasesDB | 663 |
| MedlinePlus | 000560 |
| eMedicine | med/132 emerg/808 emerg/734 |
| MeSH | D000740 |
فقر الدم أو الأنيميا من الاغريقية القديمة Ἀναιμία anaîmia, وتعني بدون دم") ، وهي عبارة عن نقص كمي أو نوعي في نسبة الهيموجلوبين, جزيء عثر عليه داخل خلايا الدم الحمراء (RBCs). حيث أن الهيموجلوبين يحمل الأكسجين من الرئتين إلى الأنسجة, فتؤدي الأنيميا إلى نقص الأكسجة (نقص الأكسجين في الأعضاء). حيث أن كل الخلايا البشري تعتمد على الأكسجين لحياتها, فإن الإصابة بدرجات متفاوتة من فقر الدم يمكن أن يؤدي إلى أعراض سريرية عديدة. ويمكن أن يرجع فقر الدم أيضا إلى نقص الحديد في الدم.
يوجد ثلاث درجات لفقر الدم وتشمل فقدان الدم المفرط (مثل النزيف أو النزيف المزمن حسب حجم الدم المفقود), تدمير خلايا الدم المفرط hemolysis أو خلل إنتاج خلايا الدم الحمراء hematopoiesis الغير فعالة.
ويعتبر فقر الدم من أكثر أمراض الدم شيوعا. يوجد عدة أنواع من فقر الدم, وذلك لتنوع الأسباب الكامنة وراء الإصابة به. ويمكن أن يصنف فقر الدم بطرق متنوعة, تقوم على الشكل الخارجي لخلايا الدم الحمراء, underlying etiologic mechanisms, and discernible clinical spectra, to mention a fe.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
تعريف
حالة ينخفض فيها عدد كريَّات الدم الحمراء الصحية إلى ما تحت الحالة العادية، وتسمى أيضًا الأنيميا. تأخذ كريات الدم الحمراء الأكسجين من الرئتين، وتنقله إلى الأنسجة في سائر الجسم. وهناك يُدمج الأكسجين مع الغذاء من أجل إنتاج الطاقة. أما الشخص المصاب بفقر الدم، فلا يستطيع دمه نقل الأكسجين الكافي للأنسجة. وبذلك يحس بالضعف والإرهاق والغثيان وآلام الرأس، والبشرة الشاحبة والباردة، والنبض السريع للقلب، وقصر النفس. وفقر الدم ليس مرضًا بحد ذاته، بل حالة تسببها مجموعة مختلفة من الأمراض والاعتلالات الجسدية. والأسباب الرئيسية لفقر الدم هي: 1- الانتاج غير الكافي للكريات الحمراء في الدم. 2- فقدان الدم. 3- التحطيم المفرط لكريات الدم الحمراء.
العلامات والأعراض
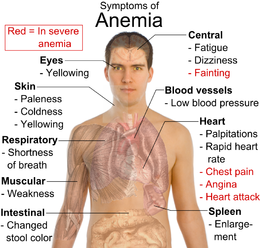
يمكن لفقر الدم أن يبقى غير مكتشفاً، وتكون الأعراض غير واضحة. والأكثر شيوعا, أن تظهر أعراض الأنيميا على الأشخاص بالإحساس بالضعف بصفة عامة أو أثناء القيام بمجهود, الضيق العام وأحيانا ضعف التركيز. ويعاني المصابون بالأنيميا الحادة عادة من dyspnea (ضيق التنفس). ويؤدي فقر الدم الشديد إلى دفع القلب لزيادة cardiac output, مما يؤدي إلى الخفقان وزيادة مقدار العرق, و heart failure.
وتختلف أعراض فقر الدم تبعا لنوع فقر الدم، والأسباب الكامنة للإصابة بها و المشاكل الصحية الخاصة بالمصاب. فقر الدم قد يترافق مع مشاكل طبية اخرى مثل النزف ، والقرح ، مشاكل الحيض أو حتى السرطان، مما قد يؤدي إلى ظهور أعراض لتلك المشاكل الصحية أولا. يجب ملاحظة أن للجسم البشري قدرة على التعامل في وقت مبكر لتعويض فقر الدم. فإذا كانت الإصابة بسيطة أو تطورت على مدى فترة زمنية طويلة من الوقت، فقد لا يتم ملاحظ أي عرض.
أعراض مشتركة لمعظم أنواع فقر الدم
- اإرهاق سريع وفقدان للطاقة.
- سرعة دقات القلب بشكل غير عادي ، لا سيما مع ممارسة الرياضة
- ضيق في التنفس و الصداع ، وخاصة أثناء التمارين.
- صعوبة التركيز.
- الدوخة.
- شحوب الجلد.
- تشنجات في الساق.
- الأرق.
الأعراض الأخرى المصاحبة لأشكال مختلفة من الأنيميا.
فقر الدم الناجم عن نقص الحديد
- تطور حالة يطلق عليها Pica و هي الإحساس بالجوع ناحية مواد غريبة مثل الورق ، والجليد ، أو الأوساخ.
- انحناء الأظافر إلى الأعلى ويشار إلى هذه الحالة باسم koilonychias.
- التقرح في الفم مع تشققات في الزوايا.
فقر الدم الناجم عن نقص فيتامين بي12
- إحساس بالتوخز، "وخز دبابيس وإبر" في اليدين أو القدمين.
- فقدان الاحساس باللمس.
- صعوبة المشي.
- التصرف بصورة خرقة وتصلب الأذرع و الساقين.
- الخرف.
- الهلوسه ، والذعر والفصام.
فقر الدم المزمن الناجم عن التسمم بالرصاص
فقر الدم المزمن الناجم عن تدمير خلايا الدم الحمراء
يسبب انحلال الدم تحطيم (تكسر) كريات الدم الحمراء القديمة في الكبد والطُّحال. وإذا حدث هذا الانحلال بشكل أسرع من عملية إنتاج الكريات الحمراء الجديدة في نقي العظم، يحدث فقر الدم. وقد يحدث فقر الدم الانحلالي هذا نتيجة للنقص الوراثي في كريات الدم الحمراء، كما يمكن أن يكون مكتسبًا. وتتضمّن الأسباب الوراثية لفقر الدم الانحلالي، فقر الدم المنجلي وفقر الدم الوراثي اللذين يؤثران في الجزء الهيموجلوبيني من كريات الدم الحمراء. والهيموجلوبين هو الجزيء الذي يجعل كريات الدم الحمراء قادرة على نقل الأكسجين. ويمكن أن تشمل بعض النواقص الوراثية غشاء الخلايا (الغطاء الذي يحيط بخلية الدم الحمراء) أو الأنزيمات في خلية الدم الحمراء. وكل هذه الأمراض والاعتلالات تنتج كريات الدم الحمراء الشاذة، وهي كريات يمكن تدميرها بشكل أسرع من الكريات العادية. يحدث فقر الدم الانحلالي المكتسب إذا تم تحطيم كريات الدم الحمراء بوساطة الحروق البليغة أو البرودة القاسية. ويمكن أن يحدث أيضًا بعد التلوث. ويجعل التلوث أو العدوَى الجسم قادرًا ـ عادة ـ على إنتاج الأجسام المضادة التي تهاجم الجراثيم التي تدخل الجسم. وفي بعض الأحيان يفرز الجسم أجسامًا مضادة غير عادية تُسَمَّى الأجسام المضادة الذاتية وهي تهاجم كريات الدم الحمراء في جسم الإنسان نفسه. وتختلف معالجة فقر الدم الانحلالي، حسب السبب والدرجة، وتجاوب بعض الحالات مع العقاقير أو حالات نقل الدم. ويمكن للحالات الأخرى أن تتم السيطرة عليها بإزالة طحال المريض؛ وهذه تسمى بعملية استئصال الطحال.
أنيميا الخلايا المنجلية
- اعياء
- القابلية للإصابة بالعدوى بسرعة.
- تأخر النمو والتطور لدى الأطفال.
- نوبات ألم شديد، وخاصة في المفاصل، البطن والأطراف.
فقر الدم الناجم عن تدمر خلايا الدم الحمراء المفاجئ
- آلام البطن
- اليرقان في الجلد.
- بول بني أو أحمر.
- ظهور كدمات صغيرة تحت الجلد.
- نوبات صرع.
- أعراض الفشل الكلوي. [2]
التشخيص
| المجموعة العمرية والجنس | Hb threshold (g/dl) | Hb threshold (mmol/l) |
|---|---|---|
| أطفال (0.5–5.0 عاماً) | 11.0 | 6.8 |
| أطفال (5–12 عاماً) | 11.5 | 7.1 |
| أطفال (12–15 عاماً) | 12.0 | 7.4 |
| نساء، غير حوامل (>15 عاماً) | 12.0 | 7.4 |
| نساء حوامل | 11.0 | 6.8 |
| رجال (>15 عاماً) | 13.0 | 8.1 |
التصنيف
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الإنتاج مقابل التدمير أو النقص
The "kinetic" approach to anemia yields what many argue is the most clinically relevant classification of anemia. This classification depends on evaluation of several hematological parameters, particularly the blood reticulocyte (precursor of mature RBCs) count. This then yields the classification of defects by decreased RBC production versus increased RBC destruction and/or loss. Clinical signs of loss or destruction include abnormal peripheral blood smear with signs of hemolysis; elevated LDH suggesting cell destruction; or clinical signs of bleeding, such as guiaic-positive stool, radiographic findings, or frank bleeding.
The following is a simplified schematic of this approach:
| Anemia | |||||||||||||||||||||||||||||||||||
| Reticulocyte production index shows inadequate production response to anemia. | Reticulocyte production index shows appropriate response to anemia = ongoing hemolysis or blood loss without RBC production problem. | ||||||||||||||||||||||||||||||||||
| No clinical findings consistent with hemolysis or blood loss: pure disorder of production. | Clinical findings and abnormal MCV: hemolysis or loss and chronic disorder of production*. | Clinical findings and normal MCV= acute hemolysis or loss without adequate time for bone marrow production to compensate**. | |||||||||||||||||||||||||||||||||
| Macrocytic anemia (MCV>100) | Normocytic anemia (80<MCV<100) | Microcytic anemia (MCV<80) | |||||||||||||||||||||||||||||||||
* For instance, sickle cell anemia with superimposed iron deficiency; chronic gastric bleeding with B12 and folate deficiency; and other instances of anemia with more than one cause.
** Confirm by repeating reticulocyte count: ongoing combination of low reticulocyte production index, normal MCV and hemolysis or loss may be seen in bone marrow failure or anemia of chronic disease, with superimposed or related hemolysis or blood loss.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
حجم خلايا الدم الحمراء
In the morphological approach, anemia is classified by the size of red blood cells; this is either done automatically or on microscopic examination of a peripheral blood smear. The size is reflected in the mean corpuscular volume (MCV). If the cells are smaller than normal (under 80 fl), the anemia is said to be microcytic; if they are normal size (80-100 fl), normocytic; and if they are larger than normal (over 100 fl), the anemia is classified as macrocytic. This scheme quickly exposes some of the most common causes of anemia; for instance, a microcytic anemia is often the result of iron deficiency. In clinical workup, the MCV will be one of the first pieces of information available; so even among clinicians who consider the "kinetic" approach more useful philosophically, morphology will remain an important element of classification and diagnosis.
Here is a schematic representation of how to consider anemia with MCV as the starting point:
| Anemia | |||||||||||||||||||||||||||||||||||||||||||||
| Macrocytic anemia (MCV>100) | Normocytic anemia (80<MCV<100) | Microcytic anemia (MCV<80) | |||||||||||||||||||||||||||||||||||||||||||
| High reticulocyte count | Low reticulocyte count | ||||||||||||||||||||||||||||||||||||||||||||
Other characteristics visible on the peripheral smear may provide valuable clues about a more specific diagnosis; for example, abnormal white blood cells may point to a cause in the bone marrow.
Microcytic anemia
Microcytic anemia is primarily a result of hemoglobin synthesis failure/insufficiency, which could be caused by several etiologies:
- Heme synthesis defect
- Iron deficiency anemia
- Anemia of chronic disease (more commonly presenting as normocytic anemia)
- Globin synthesis defect
- alpha-, and beta-thalassemia
- HbE syndrome
- HbC syndrome
- and various other unstable hemoglobin diseases
- Sideroblastic defect
- Hereditary sideroblastic anemia
- Acquired sideroblastic anemia, including lead toxicity
- Reversible sideroblastic anemia
Iron deficiency anemia is the most common type of anemia overall and it has many causes. RBCs often appear hypochromic (paler than usual) and microcytic (smaller than usual) when viewed with a microscope.
- Iron deficiency anemia is caused by insufficient dietary intake or absorption of iron to replace losses from menstruation or losses due to diseases.[4] Iron is an essential part of hemoglobin, and low iron levels result in decreased incorporation of hemoglobin into red blood cells. In the United States, 20% of all women of childbearing age have iron deficiency anemia, compared with only 2% of adult men. The principal cause of iron deficiency anemia in premenopausal women is blood lost during menses. Studies[من؟] have shown that iron deficiency without anemia causes poor school performance and lower IQ in teenage girls. Iron deficiency is the most prevalent deficiency state on a worldwide basis. Iron deficiency is sometimes the cause of abnormal fissuring of the angular (corner) sections of the lips (angular stomatitis).
- Iron deficiency anemia can also be due to bleeding lesions of the gastrointestinal tract. Fecal occult blood testing, upper endoscopy and lower endoscopy should be performed to identify bleeding lesions. In men and post-menopausal women the chances are higher that bleeding from the gastrointestinal tract could be due to colon polyp or colorectal cancer.
- Worldwide, the most common cause of iron deficiency anemia is parasitic infestation (hookworm, amebiasis, schistosomiasis and whipworm).[5]
Macrocytic anemia
- Megaloblastic anemia, the most common cause of macrocytic anemia, is due to a deficiency of either vitamin B12, folic acid (or both). Deficiency in folate and/or vitamin B12 can be due either to inadequate intake or insufficient absorption. Folate deficiency normally does not produce neurological symptoms, while B12 deficiency does.
- Pernicious anemia is caused by a lack of intrinsic factor. Intrinsic factor is required to absorb vitamin B12 from food. A lack of intrinsic factor may arise from an autoimmune condition targeting the parietal cells (atrophic gastritis) that produce intrinsic factor or against intrinsic factor itself. These lead to poor absorption of vitamin B12.
- Macrocytic anemia can also be caused by removal of the functional portion of the stomach, such as during gastric bypass surgery, leading to reduced vit B12/folate absorption. Therefore one must always be aware of anemia following this procedure.
- Hypothyroidism
- Alcoholism commonly causes a macrocytosis, although not specifically anemia. Other types of Liver Disease can also cause macrocytosis.
- Methotrexate, zidovudine, and other drugs that inhibit DNA replication.
Macrocytic anemia can be further divided into "megaloblastic anemia" or "non-megaloblastic macrocytic anemia". The cause of megaloblastic anemia is primarily a failure of DNA synthesis with preserved RNA synthesis, which result in restricted cell division of the progenitor cells. The megaloblastic anemias often present with neutrophil hypersegmentation (6-10 lobes). The non-megaloblastic macrocytic anemias have different etiologies (i.e. there is unimpaired DNA globin synthesis,) which occur, for example in alcoholism.
In addition to the non-specific symptoms of anemia, specific features of vitamin B12 deficiency include peripheral neuropathy and subacute combined degeneration of the cord with resulting balance difficulties from posterior column spinal cord pathology.[6] Other features may include a smooth, red tongue and glossitis.
The treatment for vitamin B12-deficient anemia was first devised by William Murphy who bled dogs to make them anemic and then fed them various substances to see what (if anything) would make them healthy again. He discovered that ingesting large amounts of liver seemed to cure the disease. George Minot and George Whipple then set about to chemically isolate the curative substance and ultimately were able to isolate the vitamin B12 from the liver. All three shared the 1934 Nobel Prize in Medicine.[7]
Normocytic anemia
Normocytic anaemia occurs when the overall hemoglobin levels are always decreased, but the red blood cell size (Mean corpuscular volume) remains normal. Causes include:
- Acute blood loss
- Anemia of chronic disease
- Aplastic anemia (bone marrow failure)
- Hemolytic anemia
Dimorphic anemia
When two causes of anemia act simultaneously, e.g., macrocytic hypochromic, due to hookworm infestation leading to deficiency of both iron and vitamin B12 or folic acid [8] or following a blood transfusion more than one abnormality of red cell indices may be seen. Evidence for multiple causes appears with an elevated RBC distribution width (RDW), which suggests a wider-than-normal range of red cell sizes.
Heinz body anemia
Heinz bodies form in the cytoplasm of RBCs and appear like small dark dots under the microscope. There are many causes of Heinz body anaemia, and some forms can be drug induced. It is triggered in cats by eating onions[9] or acetaminophen (Tylenol). It can be triggered in dogs by ingesting onions or zinc, and in horses by ingesting dry red maple leaves.
الأنيميا خلال الحمل
تعاني كثير من الحوامل يعانين من فقر الدم بسبب زيادة الطلب على عنصر الحديد والفيتامينات الأخرى خلال الحمل . نظرا لحاجة الجنين للعناصر الغذائية الهامة والتي منها الحديد والفيتامينات فإن إنتاج الكريات الحمراء أثناء الحمل يزيد لتوفير العناصر الغذائية اللازمة للجنين. إن حجم الدم في الأم الحامل يزيد بنسبة 50 % عن الأمهات الغير حوامل وهذا لزيادة إحتياج الجنين والمشيمة والتغييرات التي تحدث أثناء الحمل . هذه الزيادة تسبب بدورها إلى تخفيف الدم ويصبح تركيز الهيموغلوبين في الدم قليل خاصة بين الأسبوع الخامس والعشرين والثلاثين من الحمل . وبسبب هذه التغيرات فإن الأم الحامل تحتاج إلى التزود بالحديد والفيتامينات أثناء الحمل لمنع حدوث مرض فقر الدم .
أعراض فقر الدم أثناء الحمل
إذا كانت الأم الحامل بصحة جيدة فقليل أن تعاني من أعراض لفقر الدم إلا إذا كان تركيز الهيموجلوبين في الدم أقل من 8 جرام لكل ديسيليتر.
أول أعراض فقر الدم الشعور بالتعب والإرهاق وشحوب الجسم. ومن الأعراض الأخرى زيادة خفقان القلب والصعوبة في التنفس والشعور بالدوخة . إذا كان مرض فقر الدم شديداً - أقل من 6 جرام لكل ديسيليتر - فإن المريض قد يعاني من آلام بالصدر وصداع شديد. [10]
مسببات المرض
بعض أشكال فقر الدم هي وراثيه ويمكن أن تُأثر في الاطفال من لحظة الولادة. النساء بعد البلوغ يتعرضن لشكل من أشكال فقر الدم يسمى انيميا نقص الحديد بسبب فقدان الدم مع الحيض، كما يمكن أن تتطور الحالة مع زيادة الطلب من قبل الجنين على المعادن من الدم أثناء الحمل. كبار السن قد يكونوا عرضة للإصابة بصورة أكبر بفقر الدم بسبب سوء التغذيه وغيرها من الظروف الطبية.
يوجد أنواع عديدة من الأنيميا. وجميعها تختلف بصورة ضخمة سواء من ناحية مسبباتها أو وسائل علاجها. فانيميا نقص الحديد، النوع الأكثر شيوعا، سهل العلاج وذلك من خلال تعديل النظام الغذائي وتناول مكملات الحديد. بعض أشكال فقر الدم—مثل فقر الدم أثناء الحمل—يعتبر أمرا طبيعيا ولا يحتاج للقلق. ومع ذلك، هنالك أنواع من فقر الدم قد تسبب مشاكل صحية مدى الحياة.
هناك أكثر من 400 نوع من أنواع فقر الدم، هذه الأنواع تقسم إلى 3 مجموعات :
- فقر الدم الناجم عن فقدان الدم.
- فقر الدم الناجم عن نقص أو عيوب في إنتاج خلايا الدم الحمراء.
- فقر الدم الناجم عن تدمير خلايا الدم الحمراء.
فقر الدم الناجم عن فقدان الدم
يستجيب الجسم للفقدان المفرط للدم بالحفاظ على الماء ليعوض الجزء السائل في الدم. ونتيجة لذلك، تتناقص النسبة المئوية للكريات الحمراء في الدم، ويحصل مرض فقر الدم. ويمكن أن يكون فقدان الدم سريعًا كما في حالات الجروح أو بطيئًا كما في حالة القرحة الدامية في المعدة. وتتطلب المعالجة إيقاف النزف الدموي وعند الضرورة إجراء عملية نقل الدم. خلايا الدم الحمراء تفقد خلال النزيف، مثل هذه العملية يمكن أن تحدث ببطء على مدى فترة طويلة من الزمن، وكثيرا ما يمكن أن تحدث دون أن تكتشف. هذا النوع من النزيف المزمن ينتج بسبب:
- حالات مرضية ضمن المعدة والأمعاء مثل القرحة، البواسير، التهاب المعدة والسرطان
- استخدام العقاقير المضاده للالتهابات اللاستيروئيدية (NSAIDS) مثل الأسبرين أو Motrin Nonsteroidal
- الحيض والولادة لدى النساء، وخاصة إذا كان نزيف الحيض كثيفا جدا، أو في التكرار المستمر للحمل.
فقر الدم الناجم عن نقص ا أو عيب في إنتاج خلايا الدم الحمراء
قد ينتج الجسم عددا قليلا جدا من خلايا الدم أو قد لا تعمل الخلايا المنتجة بالشكل السليم. وفي كلتا الحالتين، يمكن أن تظهر أعراض فقر الدم. خلايا الدم الحمراء قد تكون مشوهة بسبب بناءها بشكل غير طبيعي، أو بسبب نقصي المعادن والفيتامينات اللازمة لعملها بشكل صحيح. الحالات المرتبطه بهذه الأنيميا تشمل ما يلي :
الإنتاج غير الكافي لكريات الدم الحمراء
تموت كل يوم حوالي 8% من الكريات الحمراء في دم الإنسان. وإذا لم يستطع الجسم تعويض هذه الخلايا الدموية بالقدر نفسه، فسينتج فقر الدم حتمًا. ويتم إنتاج الكريات الحمراء الدموية في نقي العظم، وهو نسيج يوجد في مراكز العظام. وتتطلب هذه العملية توافر المعادن المختلفة والفيتامينات التي يتزود بها الجسم عن طريق الغذاء. فقر الدم العوزي يحدث في حالة عدم احتواء الدم على كميات كافية من الحديد، أو فيتامين ب¢¡، أو حمض الفوليك، حيث تعتبر هذه المواد المغذية جوهرية لإنتاج كريات الدم الحمراء. ويحدث فقر الدم العوزي أيضًا إذا لم يستطع الجسم امتصاص هذه المواد الغذائية جيدًا. فمثلاً يحدث فقر الدم الخبيث عندما يتعذر امتصاص الفيتامين ب¢¡. ويعالج الأطباء المرضى الذين يعانون من فقر الدم العوزي بإضافة المواد المغذية المفقودة إلى الغذاء أو بالمعالجة عن طريق الحُقَن أو الأقراص الطبية. فقر الدم اللاتنسجي يحدث إذا فقد نقي العظم قدرته على إنتاج كريات الدم الحمراء. وتحدث بعض الحالات بسبب الأمراض التي تؤثر على نقي العظم مثل ابيضاض الدم في مراحله الأولى. وتحصل الحالات الأخرى نتيجة التعرض للمواد الكيميائية أو الإشعاعية. ولكن هناك حالات كثيرة، ليس لها سبب واضح. ويتلقى المصابون بفقر الدم اللاتنسجي، المعالجة عن طريق عمليات نقل الدم المنظم، حتى يبدأ نقي العظم عندهم بالعمل جيدًا، والقيام بوظيفته المطلوبة. ولكن في حالات كثيرة لا يستطيع نقي العظم استعادة قدرته على القيام بدوره أبدًا، ولذلك يموت المريض.
فقر الدم المنجلي
فقر الدم المنجلي هو خلل وراثي يصيب بشكل خاص الأمريكيين من أصل أفريقي، حيث تأخذ خلايا الدم الحمراء شكل الهلال بسبب عيب وراثي. تتحطم هذ الخلايا بسرعة أكبر من الخلايا الطبيعية، مما لا يعطي فرصة لوصول الأكسجين إلى أعضاء الجسم بالكميات اللازمة، وبالتالي يصاب الشخص بفقر دم. أيضا هذه الخلايا (التي هي على شكل هلال) تعلق بسهولة ضمن الأوعية الدموية الدقيقة مما يسبب الالم.
فقر الدم بعوز الحديد
 مقالة مفصلة: فقر الدم بعوز الحديد
مقالة مفصلة: فقر الدم بعوز الحديد
فقر الدم بعوز الحديد تحدث بسبب نقص معدن الحديد في الجسم. نخاع العظم في وسط العظام يحتاج إلى الحديد لإنتاج خضاب الدم، وهو المادة ضمن خلايا الدم الحمراء التي تنقل الأكسجين إلى أجهزة الجسم. بدون وجود ما يكفي من الحديد لا يمكن للجسم أن ينتج ما يكفي من الهيموغلوبين لخلايا الدم الحمراء. والنتيجة هي فقر الدم بعوز الحديد. فقر الدم بسبب نقص الحديد يمكن أن تسببه العوامل التالية:
انيميا نقص الفيتامين
أنيميا نقص الفيتامين قد تحدث عندما حدوث نقص في فيتامين بي12 وحامض الفوليك. هذان الفيتامينان ضروريان لإنتاج خلايا الدم الحمراء. الظروف التي تؤدي إلى فقر الدم الناجم عن نقص الفيتامينات تشمل ما يلي :
- فقر الدم الوبيل: وهو أحد أمراض مناعة ذاتية حيث تحارب خلايا المناعية خلايا فرز البروتين المسؤول عن تسهيل امتصاص فيتامين بي12
- فقر الدم ضخم الأرومات: نقصان فيتامين بي12 أو حامض الفوليك أو كلاهما معا.
- فقر الدم الخبيث : أمتصاص سيء في الجهاز الهضمي لفيتامين ب - 12 بسبب ظروف مثل داء كرون والعدوى الطفيليه، الالتهابات، والجراحة التي تشمل إزالة جزء من المعده أو الإمعاء، أو الإصابة بفيروس نقص المناعة البشرية (الأيدز).
- سوء التغذية : عدم أكل اللحوم أو تناول كميات قليلة منها يسبب نقص فيتامين بي 12، في حين أن التمادي في طهي و/أو قلة أكل الخضروات قد يتسبب في حدوث نقص حامض الفوليك.
- اسباب أخرى لنقص الفيتامينات : الحمل، وبعض الأدوية، الكحول، والأمراض المعوية.
يجب الانتباه إلى أنه أثناء فترات الحمل المبكرة، الحصول على ما يكفي من حمض الفوليك يمكن أن يحمي الجنين من عيوب الأنبوب العصبي مثل spina bifida
فقر الدم الناجم عن مشاكل نخاع العظم
هنالك مشاكل في نخاع العظم والخلايا الجذاعيه قد تمنع الجسم من إنتاج ما يكفي من خلايا الدم الحمراء. بعض من الخلايا الجذعيه الموجودة في نخاع العظم تتطور إلى خلايا الدم الحمراء. إذا كانت الخلايا الجذعية قليلة جدا، مصابة بعيوب، أو يتم استبدالها بخلايا أخرى (مثل خلايا السرطان)، فقد يؤدي ذلك إلى فقر الدم. فقر الدم الناجم عن مشاكل نخاع العظم أو الخلايا الجذعيه تشمل ما يلي :
- فقر الدم اللاتنسجي وتحدث عندما يكون هناك انخفاض ملحوظ في عدد الخلايا الجذعية أو حالة عدم وجود هذه الخلايا. يمكن للإصابة أن تكون وراثية ويمكن أن تحدث دون سبب واضح، يمكن أيضا أن تحدث عند حدوث إصابة في نخاع العظام بسبب الأدوية، الإشعاع، العلاج الكيميائي، أو الالتهابات.
- . الثلاسيميا هي حالة عدم قدرة خلايا الدم الحمراء على النضج والنمو بشكل صحيح. وهي مرض وراثي يؤثر على الأفراد في منطقة البحر الأبيض المتوسط، أفريقيا، الشرق الأوسط، وجنوب شرق آسيا. تتراوح خطورة هذه الإصابة في شدتها بين خفيفة إلى مهدده للحياة ؛ اقسي شكل لها يسمى Cooley's anemia.
- التعرض للرصاص، فالرصاص سام لنخاع العظم، وهو يؤدي إلى خفض عدد خلايا الدم الحمراء. التسمم بالرصاص يصيب البالغين بسبب ظروف العمل الذي يفرض على البالغ مثلا التعرض لهذه المادة. أما مع الأطفال فيكون السبب في العادة هو آكل رقائق الدهان. الفخار المزجج بصورة سيئة يمكن أن يلوث الاغذيه والسوائل بالرصاص.
فقر الدم المرتبط بمشاكل أخرى
فقر الدم المرتبط بمشاكل أخرى، عادة ما يحدث ذلك عندما عدم وجود ما يكفي من الهرمونات الضروريه لإنتاج خلايا الدم الحمراء. أسباب حدوث مثل هذا النوع من الأنيميا تشمل ما يلي :
- أمراض الكلى في حالاتها المتقدمة.
- قصور الدرقية.
- أمراض مزمنه أخرى.. وتشمل السرطان، الالتهابات، وأمراض جهاز المناعة مثل الذئبة أو التهاب المفاصل الرثواني
فقر الدم الناجم عن تدمير خلايا الدم الحمراء
عندما تكون خلايا الدم الحمراء هشوهه ولا يمكنها الصمود ضد الإجهاد الروتيني الناتج عن الدورة الدمويه، فقد تتمزق قبل الأوان، مما يسبب فقر دم انحلالي. فقر الدم الإنحلالي يمكن أن ينشأ عند الولادة أو يمكن أن يتطور في وقت لاحق. قد يحدث أن يتم ذلك بدون سبب معروف (العفويه). بشكل عام، الأسباب المعروفة لفقر الدم الإنحلالي قد تشتمل على أي من التالي :
- الحالات الوراثية، مثل خلية الدم المنجلية والثلاسيميا.
- الاجهاد والالتهابات، والأدوية، أو السموم مثل سم العنكبوت والثعابين، أو بعض الأطعمة.
- السموم الناتجة في الجسم بسبب الأمراض المزمنة المتقدمة في الكلى والكبد.
- هجوم خاطئ من قبل جهاز المناعة (والذي يسمى انحلال الوليد عندما يصيب الجنين أثناء الحمل).
- ترقيع الاوعيه الدمويه، صمامات القلب الاصطناعيه، والأورام، الحروق الخطيرة، والتعرض للمواد الكيميائية، وارتفاع ضغط الدم الشديد، واضطرابات التخثر.
- وفى حالات نادرة، يمكن أن لطحال متضخم أن يصطاد خلايا الدم الحمراء ويدمرها قبل أن يأتي وقت التخلص منها...
علاج فقر الدم
يوجد أدوية مختلفة لعلاج فقر الدم ويعتمد العلاج على شدة المرض وسببه.
Iron deficiency from nutritional causes is rare in non-menstruating adults (men and post-menopausal women). The diagnosis of iron deficiency mandates a search for potential sources of loss such as gastrointestinal bleeding from ulcers or colon cancer. Mild to moderate iron deficiency anemia is treated by iron supplementation with ferrous sulfate or ferrous gluconate. Vitamin C may aid in the body's ability to absorb iron.
تعطى جرعات من الفيتامين عن طريق الفم (حمض الفوليك) أو تعطى جرعات من فيتامين ب12 عن طريق الحقن.
In anemia of chronic disease, anemia associated with chemotherapy, or anemia associated with renal disease, some clinicians prescribe recombinant erythropoietin, epoetin alfa, to stimulate red cell production.
في حالات فقر الدم الشديدة, أو في حالة فقدان الدم عن طريق النزف, فإن نقل الدم يعتبر ضروريا.
نقل الدم للأنيميا
Doctors attempt to avoid blood transfusion in general, since multiple lines of evidence point to increased adverse patient clinical outcomes with more intensive transfusion strategies. The physiological principle that reduction of oxygen delivery associated with anemia leads to adverse clinical outcomes is balanced by the finding that transfusion does not necessarily mitigate these adverse clinical outcomes.
In severe, acute bleeding, transfusions of donated blood are often lifesaving. Improvements in battlefield casualty survival is attributable, at least in part, to the recent improvements in blood banking and transfusion techniques.[بحاجة لمصدر]
Transfusion of the stable but anemic hospitalized patient has been the subject of numerous clinical trials, and transfusion is emerging as a deleterious intervention.
Four randomized controlled clinical trials have been conducted to evaluate aggressive versus conservative transfusion strategies in critically ill patients. All four of these studies failed to find a benefit with more aggressive transfusion strategies.[11][12][13][14]
In addition, at least two retrospective studies have shown increases in adverse clinical outcomes with more aggressive transfusion strategies.[15][16]
Hyperbaric oxygenation
Treatment of exceptional blood loss (anemia) is recognized as an indication for hyperbaric oxygen (HBO) by the Undersea and Hyperbaric Medical Society.[17][18] The use of HBO is indicated when oxygen delivery to tissue is not sufficient in patients who cannot be transfused for medical or religious reasons. HBO may be used for medical reasons when threat of blood product incompatibility or concern for transmissible disease are factors.[17] The beliefs of some religions (ex: Jehovah's Witnesses) may prohibit the receipt of transfused blood products.[17]
In 2002, Van Meter reviewed the publications surrounding the use of HBO in severe anemia and found that all publications report a positive result.[19]
عن طريق الأغذية
- تناول الغذاء المنوع والمفيد:
فيجب المحافظة على التغذية الملائمة و الكافية، و الغنية بالسعرات الحرارية و البروتين و الحديد، و خصوصا تناول الخضار الخضراء، و اللحوم الحمراء و الكبد، و من الأطعمة المناسبة أيضا، السمك و المأكولات البحرية و الدجـاج، و البقوليات مثل الفاصوليا، و الفول السوداني.
- إذا كنتم تخططون تخطط للحمل فأستشيرو الطبيب عن نوعية الغذاء الضرورية التي يجب تناولها أثناء الحمل .
- تناول الكبد واللحوم الحمراء والبيض والفواكه .
- أكثر من الأغذية التي تحتوي على كمية وفيرة من فيتامين سي والذي يوجد في الخضروات الطازجة والليمون والبرتقال والبطاطس .
- أكثر من الأغذية التي تحتوي على حمض الفوليك مثب الفطر والكبد والبقوليات وغيرها .
- التفاح:إما بأكله طازجاً بقشوره او شرب العصير الطازج المحضر منه والطريقة ان يشرب كوباً من عصير التفاح الطازج مرة في الصباح واخرى في المساء
- الفراولة:فهي غنية بالمعادن والفيتامينات وهي تستخدم في تنقية الدم والجسم من السموم وذلك بتناول ثمار الفراولة الطازجة وغير المفرزنة بمعدل ربع كيلو جرام يومياً.
- الحلبة:فهي تحتوي على مركب الدايزوجنين فهي علاوة على انها مقوية ومخفضة للسكر في الدم وجيدة لمشاكل القولون والتشققات الجلدية إلا ان فوائدها عظيمة في فقر الدم والطريقة ان يؤخذ ملء ملعقة من مسحوق الحلبة الناعم وتخلط بالعسل النقي وتؤخذ يومياً مرة قبل الغذاء بربع ساعة واخرى قبل العشاء بربع ساعة.
- إستعمل هذه الخلطة للعلاج:تخلط كميات متساوية من الزعتر والنعناع وازهار البابونج ثم يؤخذ ملء ملعقة من المزيج وتغمر في كوب ماء مغلي وتترك لمدة 5الى 10دقائق ثم تصفى وتشرب قبل الغداء وقبل العشاء.
- الجرجير:فيعتبر الجرجير من الخضار المفيدة لعلاج فقر الدم حيث يؤخذ ملء ملعقة كبيرة من عصير الجرجير الطازج 2الى 3مرات في اليوم مع الماء او الحليب الطازج، كما ان تناول حزمة كاملة من الجرجير الطازج المغسول جيداً وبالأخص في فصل الشتاء حيث انه هو فصل الجرجير تؤدي نفس الغرض والجرجير جيد لتنقية الدم.
- الشعير مع اللبن:حيث يؤخذ حوالي 100الى 150جراماً من دقيق الشعير ويخلط مع نصف لتر من اللبن المخيض "الرائب" ويضاف للخليط ذرات من الملح ثم يحرك جيداً ويوضع على نار هادئة ويترك على النار لمدة عشر دقائق ويحرك بين وقت وآخر وعند الانتهاء يضاف له قشدة او عسل النحل النقي كما يضاف اليه قليل من الزبيب بدون بذر ثم يؤكل مع ملاحظة أن هذه الوصفة لا تعطى للمصابين بمرض السكر.
- الحلاوة الطحينية: وهي متميزة لفقر الدم فهي تحتوي على زيت السمسم وعرق الحلاوة والطحينة البيضاء المغذية وهذه الوصفة مقوية ومسمنة ولكن يجب عدم استعمالها من قبل مرضى السكر.
- الليمون:يعتبر الليمون من المواد الغنية بفيتامين ج وهو يقوي جهاز المناعة ويؤخذ ملء كوب من عصير الليمون بعد الغداء مباشرة وآخر بعد وجبة العشاء مباشرة.
- جلوكونات الحديد:وهذا موجود على هيئة مستحضر يباع لدى محلات الاغذية التكميلية وهوافضل المستحضرات امتصاصاً.
- الكلوروفيل:وهو مسحوق اخضر مستخلص من الخضر وهو غني بالحديد وبعض الفيتامينات
الهامة ويوجد منه مستحضر في محلات الاغذية التكميلية ويستعمل لعلاج فقر الدم
- الجنسنج البرازيلي:وهو جذور لنبات الجنسنج ويحتوي على مواد صابونية
وهو مقوٍ جيد ويفيد في حالات فقر الدم ويوجد منه عدة مستحضرات في الصيدليات حيث يوجد منه شراب وكبسولات واقراص والجذور نفسها كما هي.
- حمض الفوليك:وهو مستحضر يمنع فقر الدم ويقوي الشهية و يخفض الكوليسترول.
- زيادة ساعات النوم و معدلات الراحة بما في ذلك النوم أثناء النهار.
- زيادة معدلات تروية الجسم والإكثار من تناول السوائل المختلفة
- تجنب القهوة و مركبات الكافيين و الأكلات الدسمة الثقيلة أثناء الليل
- تجنب النشاطات المرهقة.
انظر أيضا
- Hematology
- أيض الحديد البشري
- الهيم
- هيموجلوبين
- خلية منجلية.
- فقر دم بعوز الحديد.
- فقر الدم ومشاكل الحمل.
- نزيف دموي.
- فقر الدم المتوسطي (الثلاسيميا).
وصلات خارجية
- National Anemia Action Council (الولايات المتحدة)
المصادر
- ^ eMedicineHealth > anemia article Author: Saimak T. Nabili, MD, MPH. Editor: Melissa Conrad Stöppler, MD. Last Editorial Review: 12/9/2008. Retrieved on 4 April 2009
- ^ ويكيبديا
- ^ World Health Organization (2008). Worldwide prevalence of anaemia 1993–2005 (PDF). Geneva: World Health Organization. ISBN 9789241596657. Retrieved 2009-03-25.
- ^ Recommendations to Prevent and Control Iron Deficiency in the United States MMWR 1998;47 (No. RR-3) p. 5
- ^ Iron Deficiency Anaemia: Assessment, Prevention, and Control: A guide for programme managers
- ^ eMedicine - Vitamin B-12 Associated Neurological Diseases : Article by Niranjan N Singh, MD, DM, DNB July 18, 2006
- ^ Physiology or Medicine 1934 - Presentation Speech
- ^ Dorlands Medical Dictionary
- ^ Onions are Toxic to Cats
- ^ طبيبي
- ^ Hébert PC, Wells G, Blajchman MA; et al. (1999). "A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care. Transfusion Requirements in Critical Care Investigators, Canadian Critical Care Trials Group". N. Engl. J. Med. 340 (6): 409–17. PMID 9971864.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ^ Bush RL, Pevec WC, Holcroft JW (1997). "A prospective, randomized trial limiting perioperative red blood cell transfusions in vascular patients". Am. J. Surg. 174 (2): 143–8. doi:10.1016/S0002-9610(97)00073-1. PMID 9293831.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ^ Bracey AW, Radovancevic R, Riggs SA; et al. (1999). "Lowering the hemoglobin threshold for transfusion in coronary artery bypass procedures: effect on patient outcome". Transfusion. 39 (10): 1070–7. doi:10.1046/j.1537-2995.1999.39101070.x. PMID 10532600.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ^ McIntyre LA, Fergusson DA, Hutchison JS; et al. (2006). "Effect of a liberal versus restrictive transfusion strategy on mortality in patients with moderate to severe head injury". Neurocritical care. 5 (1): 4–9. doi:10.1385/NCC:5:1:4. PMID 16960287.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ^ Corwin HL, Gettinger A, Pearl RG; et al. (2004). "The CRIT Study: Anemia and blood transfusion in the critically ill--current clinical practice in the United States". Crit. Care Med. 32 (1): 39–52. doi:10.1097/01.CCM.0000104112.34142.79. PMID 14707558.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ^ Vincent JL, Baron JF, Reinhart K; et al. (2002). "Anemia and blood transfusion in critically ill patients". JAMA. 288 (12): 1499–507. doi:10.1001/jama.288.12.1499. PMID 12243637.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: multiple names: authors list (link) - ^ أ ب ت Undersea and Hyperbaric Medical Society. "Exceptional Blood Loss - Anemia". Retrieved 2008-05-19.
- ^ Hart GB, Lennon PA, Strauss MB. (1987). "Hyperbaric oxygen in exceptional acute blood-loss anemia". J. Hyperbaric Med. 2 (4): 205–210. Retrieved 2008-05-19.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ^ Van Meter KW (2005). "A systematic review of the application of hyperbaric oxygen in the treatment of severe anemia: an evidence-based approach". Undersea Hyperb Med. 32 (1): 61–83. PMID 15796315. Retrieved 2008-05-19.
- Articles containing Ancient Greek (to 1453)-language text
- Articles with unsourced statements from March 2009
- Articles with hatnote templates targeting a nonexistent page
- جميع المقالات الحاوية على عبارات مبهمة
- جميع المقالات الحاوية على عبارات مبهمة from January 2008
- مقالات ذات عبارات بحاجة لمصادر
- اضطرابات الدم
- علم الدم
- أنيميات