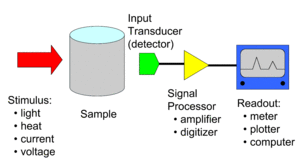
كيمياء تحليلية

الكيمياء التحليلية Analytical chemistry، هي فرع من علم الكيمياء يهتم بالتقدير الكمي والنوعي للعناصر او المركبات المكونة للماده المراد تحليلها. وينقسم هذا الفرع إلى عدة طرق واساليب يمكن استخدامها ولكل منها استخداماته وأهميته منها: التحليل الحجمي والتحليل الوزني والتحليل الحراري والتحليل النوعي والتحليل الطيفي والتحليل الآلي والتحليل الكهربائي. ويمكن لبعض هذه الطرق أن تكتشف وجود المركبات او العناضر وبحساسية عاليه قد تصل إلى تركيز جزء من مليون مليار جرام باللتر.
التاريخ
لقد كان لجابر بن حيان إنجازات كبيرة في مجال الكيمياء التحليلية، حيث قام بتحضير الفولاذ وتنقية المعادن، ثم بدأت الكيمياء التحليلية كفرع مستقل منذ عام 1907، وتطورت منذ ذلك الحين فزادت قائمة الكواشف الكيميائية وطـرق التحليل للمواد اللاعضوية والعضوية وحدث توسع في استخدام طرق التحليل الفيزيائية والكيميائية الآلية والكيميائية الكهربية والكرومـاتوجرافية وطـرق التحليل الإشعـاعي وطرق التحليل الطيفي.
تطور التحليل الكيميائي كتفاً إلى كتف مع تطور التقانات الحديثة. ففي العهود الأولى للتحليل الكمي في نهاية القرن التاسع عشر، أعطى التحليل الكيميائي أسساً مهمة لتطور الكيمياء. فمثلاً أعتمدت دراسات الاحتراق التي أجراها لافوازييه La Voisier والنظرية الذرية التي افترضها دالتون Dalton على نتائج التحليل الكيميائي الكمي. وفي الوقت الحاضر فإنه لا يمكن تطوير الترانزستورات بدون إجراء تحاليل كيميائية كمية دقيقة وحساسة، وبالمقابل كلما تحسن أداء الترانزستورات سمح ذلك ببناء أجهزة تحليلية أعلى حساسية ودقة ووسَّع مجال استخدامها، وفيما يلي بعض أهم مجالات استخدام التحليل الكيميائي:[1]
ـ الأبحاث الأساسية: أول خطوات البحوث العلمية هو تحديد مكونات المنظومات المجهولة بالتحليل الكيميائي النوعي، يلي ذلك إجراء الاستقصاءات البنيوية والقياسات الكمية ومثال ذلك كشف وتخليق الأدوية الجديدة.
ـ تطوير المنتجات: غالباً ما يتعلق تصميم وتطوير منتجات جديدة بالربط بين تركيبها الكيميائي وخواصها الفيزيائية أو أدائها، ومثال ذلك تطوير السبائك، أو البوليمرات الجديدة التركيب.
ـ ضبط جودة المنتجات: تتطلب أغلب الصناعات ثبات جودة المنتج. وللتأكد من الوصول إلى هذا المتطلب، يتم إخضاع كلٍّ من المواد الأولية والمنتجات النهائية إلى تحاليل كيميائية موسعة. من ناحية أخرى يجب المحافظة على المكونات اللازمة للإنتاج ضمن مستويات مثالية، في حين يجب المحافظة على الشوائب الأخرى، مثل المواد السمية في الأغذية، بمستويات أخفض من الحدود العليا التي تسمح بها المواصفات القياسية المعتمدة.
ـ متابعة وضبط المُلوِّثات: أشهر مشكلات التلوث هي المشكلات الناجمة عن المعادن الثقيلة والمبيدات العضوية المكلورة. فهناك حاجة ملحة لإجراء تحاليل حساسة ودقيقة دورياً للتمكن من تحديد مدى انتشار المُلوِّثات في البيئة ومستويات التلوث بها من أجل ضبط المخلَّفات الصناعية.
ـ طرائق الاختيار: تتعلق قيمة الخام المتداول تجارياً بمحتواه من المعدن كما في حال تداول الخامات الثمينة. غالباً ما يؤدي الاختلاف الطفيف في تركيز المكون المطلوب دوراً حاسماً حين الاختيار بين المواد الأولية المعروضة، وقد يكون لهذا الاختلاف شأن ملحوظ تجارياً. لذلك من الجوهري هنا إجراء تحليل كيميائي دقيق وموثوق.
ـ الدراسات الطبية والسريرية: يظهر مستوى الاختلال الحيوي للكائن عبر مستوى مختلف العناصر والمركبات في سوائل جسمه، فمثلاً يُشار إلى حالة داء السكري عبر كشف الارتفاع الحاد في تركيز السكر ضمن البول الذي يعني ارتفاعه ضمن الدم.
أهمية الكيمياء التحليلية
وتقوم الكيمياء التحليلية في كثير من العلوم بدور مهم ، وكذلك فهي لاغنى عنها أساسًا في علم الحياة ، إذ يستفاد من التقنية التحليلية في دراسة المواد الحية وعمليات التمثيل الغذائي وغيرها ، ولا يستطيع الأطباء تشخيص الامراض دون الاستناد إلى نتائج التحليلات اللازمة لذلك . كما نجد أن تقسيم المعادن جاء بعد معرفة تامة بالمكونات الكيميائية له . ولا يستطيع الفيزيائيون تشخيص نواتج تصادم الدقائق ذات الطاقة العالية بدون استخدام التقنية التحليلية في الصناعة الحديثة . إن قيمة المواد الخام ومدى نقاوة منتج صناعي وملاءمته للاستعمال والسيطرة على العمليات الصناعية في مرحلة أو أكثر نحتاج إلى معرفة الكيمياء التحليلية للتأكد من جودة الإنتاج الصناعي .
أنواع الكيمياء التحليلية

| نوع الطريقة المتبعة | الخاصة المقيسة |
|---|---|
| القياس الوزني gravimetric | وزن المادة النقية المراد تحليلها أو وزن مركب متناسب بنيوياً يحويها. |
| القياس الحجمي volumetric | حجم محلول كاشف معياري يتفاعل مع المادة المراد تحليلها. |
| القياس الطيفي spectrometric | كثافة الشعاع الكهرمغناطيسي الصادر عن المادة المراد تحليلها أو الممتص من قبلها. |
| الكهركيمياوي electrochemical | الخواص الكهربائية لمحلول المادة المراد تحليلها. |
| الإشعاعي radiometric | كثافة الإشعاعات النووية الصادرة عن المادة المراد تحليلها. |
| القياس الطيفي الكتلي mass spectro metric | غزارة الشظايا الجزيئية المشتقة من المادة المراد تحليلها. |
| الاستشرابي (الكروماتوغرافي) chromatographic | الخواص الفيزياكيمياوية لكل مادة من المواد المراد تحليلها بعد تفريقها. |
| الحراري thermometric | الخواص الفيزياكيمياوية للعينة عند تسخينها أو تبريدها. |
من الشائع تصنيف الطرائق التحليلية إلى طرائق تقليدية تعتمد خواص كيميائية بحتة وأخرى آلية instrumental analysis تعتمد بعض الخواص الفيزيائية والكيميائية، حيث يعبِّر التصنيف الأول عن الطرائق التحليلية الرطبة كالتحليل الوزني والتحليل الحجمي. وقد تم التوصل إلى هذا التصنيف تاريخياً، لكنه فَقَدَ أهميته لعدم وجود فارق جوهري بين طرائق كلا الصنفين، حيث تدور كل الطرائق حول إقامة علاقة بين الخاصة الفيزيائية المقيسة وبين تركيز المادة المراد تحليلها. وهناك عدد قليل جداً من الطرائق التحليلية تامة الأتمتة، إذ تحتاج أغلب الطرائق الأخرى لمعالجة كيميائية متخصصة قبل إجراء القياس الآلي. يوضح الجدول التالي تصنيفاً عاماً أكثر وضوحاً يعتمد الخاصة الفيزيائية المقيسة. وأخيراً تصنف طرائق التحليل أحياناً في طرائق تحليل عضوي، ولاعضوي.
يعتمد القياس الطيفي اختيار طول موجي أو أكثر محدِدِّ ومميِّز للمادة المطلوب تحليلها ثم قياس شدته ومعايرته. وقد يكون في مجال الأشعة تحت الحمراء أو مجال الأشعة السينية.
وقد فصل في تقنية التحليل الكهركيميائي لوجود خواص كهربائية عديدة يمكن اعتمادها.
أولا: التحليل النوعي أو الوصفي
هو مجموعة العمليات التي يتم فيها الكشف عن تركيب المواد أو المركبات أو العناصر الداخلة في تركيب مادة معينة أو خليط من المواد سواء أكان في الحالة الصلبة أو محلول في مذيب معين ولايتعرض هذا التحليل إطلاقًا إلى كميات هذه المكونات .
ثانيًا: التحليل الكمي
ويبحث في تقدير كميات المكونات أو العناصر الداخلة في تركيب المركب الكيميائي أو الخليط، ويتبين من هذا أن التحليل النوعي لمادة مجهولة التركيب يسبق عادة التحليل الكمي لها؛ لأنه لا يجوز تقدير مادة معينة تقديرًا كميًا ما لم يتأكد من وجودها وصفيًا. ويشمل التحليل الكمي على :
التحليل الكيميائي
التحليل الوزني
ويتم التحليل الكمي بالوزن بترسيب المادة وتقديرها كميًا في هيئة عنصر منفرد أو مشتق معين معروف التركيب يفصل عن المحلول بالترسيب أو الطرد المركزي ثم غسله وتجفيفه ووزنه، فيحسب وزن المادة المراد تقديرها من معرفتنا لوزن الراسب وتركيبه بدقة. فمثلا يمكن تعيين نسبة الكلور في ملح الطعام مثلا بإذابة وزن معين من الملح في الماء ثم إضافة محلول نترات الفضة إليه فيترسب على شكل كلوريد الفضة، ثم يرشح الراسب ويغسل ويجفف ثم يوزن لمعرفة كمية الكلور ونسبته في الملح، ويضم التحليل الوزني الطرق التي يتم فيها تقدير أوزان المواد أو بعض مكوناتها بطريقتين هما :
- الطريقة المباشرة :
وفيها يتم تحديد قياسات الأوزان لنواتج العملية التحليلية المعروفة التركيب .
- الطريقة غير المباشرة :
إذ تحدد بواسطتها قياسات الأوزان المفقودة أو الناقصة في الوزن بوصفها نتيجة لخاصية التطاير بالعينة .
طرق التحليل الحجمي
تستعمل في هذه الحالة طرق مباشرة وغير مباشرة لتعيين أوزان المواد أو بعض مكوناتها وتشمل هذه الطرق ما يلي :
- طريقة المعايرة :
وتتضمن استعمال محاليل ذات تراكيز معلومة وقياس حجوم مثل هذه المحاليل التي تتفاعل كميًا مع محلول المادة المراد تقديرها لحد نقطة معينة تسمى نقطة التكافؤ أو نقطة انتهاء التفاعل التي يمكن الكشف عنها بواسطة الأدلة التي تتضمن تغيرًا حادًا في خواص المحلول كاللون أو التعكير الذي تلحظهما بالعين المجردة أو تقاس بالطرق الكيميائية الفيزيائية كقياس فرق الجهد أو التوصيل الكهربائي . ويسمى المحلول المعلوم التركيز بالمحلول القياسي وهو المحلول الذي يحتوي حجم معين منه على وزن معلوم من المادة المذابة . أما عملية إضافة المحلول القياسي من السحاحة إلى حجم معين من محلول المادة المجهولة التركيز في الدورق المخروطي أو العكس حتى يتم التفاعل فتسمى بعملية المعايرة. ومن قوانين التكافؤ الكيميائي وتحديد حجم المحلول القياسي المستعمل في المعايرة نستطيع أن نعين وزن المادة المجهولة أو النسب الوزنية لما فيها من مكونات سواء أكان بطرق مباشرة أو غير مباشرة.
- التحليل الغازي:
وتقاس بهذه الطريقة كمية الغازات المستهلكة وفيه تقدر المادة بتقدير حجم الغاز الذي قد يكون هو المادة المراد تقديرها أو ناتجًا عن تفاعل تلك المادة مع مواد أخرى بحيث تعطي غازًا يمكن تقديره. ويجب أن لا يفهم بأن عمليات التحليل الكمي والنوعي لا يمكن أن تتم إلا عن طريق التفاعلات الكيميائية. وعمليات الفصل بالطرق الطبيعية لها أثرها الواضح في بناء أكثر مراحل التحليل الكروماتوجرا في لمكونات الخليط ثم يلي ذلك التمييز بطرق كيميائية. ومع أن طرق التحليل الحجمي تتطلب توفر شروط وخبرة لتجاوز الأخطاء أو العيوب فأنها تفضل في التطبيق العملي والاستعمال على طرق التحليل الوزني؛ على الرغم من دقة النتائج التي يمكن الحصول عليها عند استعمالها لكنها بطيئة وتستغرق وقتًا طويلا ً لإتمام التحليل، قد يتجاوز الإنتظار للحصول على نتائجها عدة ساعات أو أيام، وهو ما لا يتفق والحاجة العملية خاصة في السيطرة الكيميائية على العمليات الصناعية لتوجيه التفاعلات إلى الوجهة الصحيحة للحصول على نتائج ذات مواصفات عالية الجودة.
ثالثا: طرق التحليل الآلي
تقدر المادة بقياس بعض من خواصها الفيزيائية أو الكيميائية مثل الكثافة واللون ومعامل الإنكسار والتوصيلة الكهربائية والتغيرلت الحرارية والكهربائية .....الخ. وتعتمد هذه الطرق أساسًا على القياسات الآتية :
انبعاث الطاقة الضوئية
يتضمن هذا القياس إثارة المادة إلى مستويات عالية من الطاقة بالطاقة الضوئية أو الكهربائية ثم رجوعها إلى مستوى طاقة منخفض فينبعث منها من الطاقة الممتصة وتكون مقياسًا لكمية المادة وذلك بواسطة الطرق الآتية :
- طرق تسجيل الطيف الانبعاثي، حيث تثار المادة باستخدام القوس الكهربائي.
- المطياف الفوتومتري باللهب، حيث تثار المادة باستخدام أنواع مختلفة من اللهب وبعد رجوع المادة إلى حافة طاقة منخفضة تقاس كمية الضوء المنبعثة.
- وميض الأشعة السينية حيث تثار المادة بأشعة سينية ذات طول موجي معين وبعد رجوعها إلى حالة طاقة منخفضة تقاس الأشعة المنبعثة وهي التي تقوم بتمييز العنصر .
امتصاص الطاقة الضوئية
ويتضمن قياس كمية الطاقة الضوئية عند طول موجه معينة تمتصها المادة المراد تحليلها، ولهذا يمكن استخدام مايلي:
أ - الطرق الطيفية اللونية.
ب - الطرق الطيفية في المنطقة فوق البنفسجية.
جـ- الطرق الطيفية في المنطقة تحت الحمراء.
د - طريقة الأشعة السينية.
هـ- الرنين النووي المغناطيسي: تتضمن هذه الطريقة التفاعل بين موجات الراديو وأنوية الذرات التي تكون في مجال مغناطيسي.
الطرق الكهربائية
أ - التحليل بطريقة التوصيل الكهربائي حيث يقاس التغير في معامل التوصيل الكهربائي لمحلول النموذج.
ب - التحليل بقياس فرق الجهد حيث يقاس الجهد الكهربائي المتغير في أثناء التفاعل عند وضع القطب في المحلول ويمكن معرفة انتهاء التفاعل ومن ثم يمكن حساب تركيز المواد المتفاعلة.
جـ- التحليل بقياس الكمية الكهربائية حيث تقاس الكمية الكهريائية بالكولوم اللازمة لإكمال التفاعل الكهروكيميائي.
د - البولاروجرافيا حيث تقاس قيمة التيار الكهريائي حيث تتناسب مع تركيز المادة التي تختزل أو تتأكسد في تفاعل كهروكيميائي عند القطب المايكروني.
يعتمد التحليل الكهركيميائي electrochemical analysis الذي هو إحدى طرائق التحليل الكيميائي على الخواص الكهربائية للمادة. وترتكز هذه الخواص على عاملين أساسين هما: الطاقة اللازمة لاقتلاع الإلكترونات من المادة (أكسدتها) أو إدخالها إلى المادة (إرجاعها) وهذا ما يعبر عنه بكمون بداية الأكسدة أو كمون بداية الإرجاع، ويستعاض عنه عادة بكمون نصف الموجة(E1/2) half-wave potential وبما أن هذا العامل مرتبط بالبنية الذرية أو الجزيئية للمادة ؛ لذلك فإنه يستخدم للدلالة على النوعية. أما العامل الثاني فهو يتعلق بعدد الإلكترونات الناتجة عن عملية الأكسدة أو الإرجاع. فإذا حُسِبت كمية الإلكترونات الكلية، وعُرِف عدد الإلكترونات n الذي تعطيه كل ذرة أو جزيء من المادة تُعرَف كمية المادة الكلية. و تحسب الكمية الكلية للإلكترونات التي هي كمية الكهرباء Q (بالكولون) بدلالة شدة التيار i (بالأمبير) والزمن t (بالثانية) بالعلاقة: Q = i.t
لذلك فإن كمية الكهرباء تدل على كمية المادة. وقد ربط بينهما العالم فاراداي بعلاقته المشهورة التالية (والمسماة بعلاقة فاراداي):
m=Q/F
حيث: Q كمية الكهرباء وF ثابت فاراداي = 96500 وm كمية المادة بالمعادل الگرامي أو المكافيء الگرامي (Gram-equivale) g-eq والذي يعادل كمية من المادة تساوي وزنها الجزيئي (أو الذري) مقسوماً على n عدد الإلكترونات المتبادلة في التفاعل الكهركيميائي الحاصل لكل جزيئة (أو ذرة). وترتبط كثافة الإلكترونات التي تحصل نتيجة عمليات الأكسدة أو الإرجاع للمادة بتركيزها وبالتالي نجد:
i = K.C
حيث K ثابت وC تركيز المادة.
وبناء على ذلك يمكن استخدام كمية الكهرباء أو [[التيار الكهربائي]ي للدلالة على كمية المادة أو تركيزها أي للتحديد الكمي.
يقسم التحليل الكهركيميائي إلى قسمين رئيسين:
ـ التحليل الكهركيميائي المباشر direct electrochemical analysis
ـ المعايرات الكهركيميائية electrochemical titrations
1ـ التحليل الكهركيميائي المباشر
يعتمد هذا التحليل على تحديد المواد اعتماداً على خواصها الكهركيميائية مباشرة، ويشتمل على الطرائق الرئيسة التالية:
أ ـ التحليل بقياس كمية الكهرباء: يعتمد هذا التحليل على قياس كمية الكهرباء (المقدرة بالكولون ومنها جاءت التسمية) من أجل تحديد المادة، ويمكن أن يجرى هذا التحليل في كمون ثابت أو في تيار ثابت. كما يمكن أن يتم بصورة عكسية وذلك بأن ترسب المادة المراد تحليلها بتفاعل كهركيميائي مناسب ثم يزال الراسب بتفاعل كهركيميائي آخر وتحسب كمية الكهرباء اللازمة. ومن المنحني العياري Q=f(C) تحسب التراكيز للمادة المحددة.
ب ـ التحليل الفولط أمبيرومتري:
يعتمد التحليل الفولط أمبيرومتري volt-amperometric analysis على رسم المنحنيات الفولط أميبرومترية أي منحنيات تابعية التيار للكمون I=f(E) لأكسدة (أو إرجاع) المادة. تحدد النوعية من معرفة كمون بداية الأكسدة (أو الإرجاع) أو كمون نصف الموجة (E1/2). وتحدد الكمية عن طريق معرفة قيمة التيار (تيار النفوذ الإشباعي diffusion current saturated) الذي يتناسب مع تركيز المادة. ويمتاز هذا التحليل بإمكانية تحديد أكثر من مادة بتجربة واحدة. كما يمكن استخدام الطريقة العكسية أيضا.
ج ـ التحليل الاستقطابي (البولاروجرافي):
يعتمد التحليل الاستقطابي (البولاروجرافي) polarographic analysis على رسسم المنحنيات الفولط أمبيرومترية باستخدام مسرى من الزئبق وخصوصاً مسرى الزئبق القطََََََََََََََََََََََََََََّار، وتسمى هذه المنحنيات بالموجات الاستقطابية polarographic waves. ويمتاز مسرى الزئبق القطّار من غيره من المساري بأن كمون إرجاع البروتون عليه كبير جداً بالقيمة السالبة مما يتيح إرجاع عدد كبير من الشرجبات المعدنية. وتحدد النوعية في التحليل الاستقطابي عن طريق معرفة كمون نصف الموجة E1/2، وتحدد الكمية عن طريق معرفة تيار النفوذ الإشباعي id (المتناسب مع التركيز).
ويشتمل التحليل الاستقطابي على عدد كبير جداً من الطرائق تختلف باختلاف طريقة التحديد المستخدمه.
د ـ التحليل الكهروجرافي: يعتمد التحليل الكهروغرافي electrographic analysis على وضع القطعة المعدنية المراد تحليلها على مصعد anode الجهاز، وتغطيتها بورقة ترشيح مبللة بكهرليت مناسب، ثم إغلاق الدارة بالمهبط cathode، ويطبق فرق في الكمون مناسب خلال زمن قصير جداً؛ مما يؤدي إلى أكسدة جزء صغير للغاية من هذه القطعة وانتقاله إلى ورقة الترشيح؛ حيث يتم الكشف عن الشوارد المعدنية المختلفة المنتقلة إلى ورقة الترشيح بكواشف مناسبة. وتمتاز هذه الطريقة بإمكانية تحليل السبائك والقطع المعدنية من دون أن يتأثر شكلها أو وزنها بشكل محسوس مما يجعلها مهمة وملائمة لتحليل قطع الحلي والقطع الأثرية وما شابهها.
2ـ المعايرات الكهركيميائية تعتمد المعايرات الكهركيميائية electrochemical titrations على إجراء المعايرات الكيميائية الحجمية المعروفة وتحديد نقطة نهايتها بطريقة كهركيميائية. والمعايرات الكيميائية هي التالية: معايرات الأكسدة والإرجاع، ومعايرات التعديل حمض ـ أساس، ومعايرات تشكيل المعقدات، ومعايرات الترسيب.
تصنف المعايرات الكهركيميائية كما يلي:
أ ـ المعايرة الكمونية: تستخدم المعايرة الكمونية titration potentiometric في مختلف المعايرات الكيميائية إلا أنها تشترط أن تكون المادة المحددة والمادة الكاشفة (التي نعاير بها titrant) خاضعتين للنظام العكوس reversible system أو النظام المختلط mixed system وذلك حتى يكون كمون التوازن مستقراً. وتحصل عند نهاية المعايرة قفزة في الكمون ومنها يُعرَف الحجم اللازم لنقطة نهاية المعايرة Veq (من الحجم المقابل لمنتصف القفزة الكمونية) ومن ثم يحدد التركيز المجهول.
ب ـ المعايرة الـ pH مترية: تستخدم المعايرة الـ pH مترية (بقياس pH المحلول) pH-metric titration لمعايرات التعديل فقط. وتعتمد على قياس قيم pH المحلول في مختلف مراحل المعايرة حيث تحصل قفزة في الـ pH عند نقطة نهاية المعايرة. ويعرف Veq من الحجم المقابل لمنتصف القفزة. ويحدد التركيز المجهول للحمض أو للأساس كما في المعايرة السابقة.
جــ المعايرة بقياس الناقلية الكهربائية: تعتمد المعايرة بقياس الناقلية الكهربائية conductometric titration على قياس تغيرات ناقلية المحلول في مختلف مراحل المعايرة. ونظراً لتغير نوعية الشوارد وتركيزها أثناء المعايرة فان الناقلية الكهربائية تزداد أو تنقص. وتحدد نقطة نهاية المعايرة بالاعتماد على الاختلاف بين قيم الناقلية الكهربائية قبل نقطة نهاية المعايرة و بعدها، والذي يؤدي إلى حصول انحناء في منحني المعايرة العام. ويعرف Veq من الحجم المقابل لنقطة الانحناء المذكورة في منحني المعايرة. ويحدد تركيز المادة المدروسة كما في المعايرة الكمونية.
د ـ المعايرة عالية التواتر: تعتمد المعايرة عالية التواتر high frequency titration على تطبيق حقل كهربائي عالي التواتر (25-30 ميغا هرتز) على المحلول المدروس من خارج وعاء التحليل أو من داخله ولكن بشكل معزول عن المحلول بعازل زجاجي أو بلاستيكي. إن التواترات العالية للحقل الكهربائي تؤدي إلى اهتزاز الشوارد حول وضع التوازن، ويحصل ما يسمى بالاستقطاب الانحرافي distoration polarization أو الاستقطاب التوجيهي orientation polarization للجزيئات، وهذا يؤدي إلى تغيرات في الناقلية الكهربائية والعازلية الكهربائية بتغير تواتر الحقل وبتغير نوعية وتركيز الشوارد والجزيئات. مما يجعل شدة تواتر الحقل ثابتة وبالتالي تظهر تغيرات واضحة في الناقلية تحصل عند نقطة نهاية المعايرة، ومن معرفة الحجم المقابل لنقطة الانكسار في منحني المعايرة يعرف Veq، ويحدد تركيز المادة المحددة كما في المعايرة الكمونية.
تمتاز المعايرة عالية التواتر عن المعايرة بقياس الناقلية الكهربائية بأنها تصلح لكثير من الحالات التي لا تصلح لها المعايرة بقياس الناقلية الكهربائية، كأن تكون ناقلية المحلول ضعيفة أو أن المحاليل غروية أو أن المساري تؤثر بشكل واضح في التفاعل المدروس.
هــ المعايرة الأمبيرومترية: تستخدم المعايرة الأمبيرومترية amperometric titration لمختلف المعايرات الكيميائية شريطة وجود مادة فعالة كهركيميائياً، حيث يطبق كمون يوافق هذه المادة ويقاس تيار النفوذ الموافق لها في مختلف مراحل المعايرة، ومن الانكسار في منحني المعايرة تحدد نقطة نهايتها. ويعرف Veq من الحجم الموافق لنقطة الانكسار المذكورة، ومن ثم يحدد تركيز المادة المدروسة كما هو مبين في المعايرة الكمونية.
و ـ المعايرة البي أمبيرومترية: تعتمد المعايرة البي أمبيرومترية pi-amperometric titration على تطبيق فرق في الكمون على مسريين كاشفين موجودين في المحلول المدروس وقياس التيار الكهربائي المار بينهما.
ز ـ المعايرة الكولونومترية: تختلف المعايرة الكولونومترية coulometric titration عن كل المعايرات السابقة، فهي في الحقيقة توليد المادة الكاشفة (التي نعاير بها) كهركيميائياً (أو كولونومترياً) باستخدام تيار كهربائي للتوليد (موجب أو سالب) مُحدَّد الشدة تماماً (I)، ومن معرفة الزمن اللازم لنهاية المعايرة (teq)، تُحسَب كمية الكهرباء اللازمة (Q) من العلاقة:
Q = i.teq
ومن معرفة Q تُحسَب كمية المادة بالمعادل الگرامي أو المكافئ الگرامي (g-eq). وتُستخدَم هذه الطريقة في مختلف المعايرات الكيميائية، وهي ذات دقة وحساسية عاليتين وقابلة للمكننة التامة، إلا أنها تتطلب معرفة دقيقة للمردود التياري للتوليد.[2]
التحليل الكروماتوجرافي
يعتمد هذا النوع من التحليل على اختلاف المواد بعضها عن بعض في ميلها للأمتزاز أو التجزئة أو التبادل خلال سطح مغلف بمذيب مناسب أو خلال مادة كيميائية ومن ثم يمكن أن تنفصل تلك المواد ، وتنقسم طرق التحليل الكروماتوجرافي إلى :
- كروماتوجرافيا الادمصاص: ويقصد به التحليل الكروماتوجرافي عن طريق الأدمصاص على السطح.
- كروماتوجرافيا التبادل الأيوني : ويقصد به التحليل الكروماتوجرافي عن طريق تبادل الأيونات بين مادة التقدير وبين أيونات السطح الذي يحدث عملية التبادل وهي مادة كيميائية راتنجية.
- كروماتوجرافيا التجزئة: ويقصد به التحليل الكروماتوجرافي عن طريق الفصل التجزيئي لمخلوط من عدة مواد وتنقسم هذه الطريقة إلى كروماتوجرافيا العمود بالتجزئة ويتم فيها التحليل على عمود معبأ بمادة معينة.
- كروماتوجرافيا الطبقة الرقيقة: وفيه يتم التحليل الكروماتوجرافي بالادمصاص أو التوزيع على ألواح زجاجية تنثر عليها مادة مسامية يجرى عليها الفصل والتحليل.
- كروماتوجرافيا الغاز: ويتضمن هذا التحليل الكروماتوجرافي باستخدام غاز ناقل يقوم بحمل أبخرة المواد المحللة فيتم اتصال أبخرة هذه المواد تبعًا لدرجات غليانها أي تظهر أولا ً المواد ذات درجات الغليان المنخفضة يتبعها المواد ذات درجات الغليان العالية وتخرج هذه الأبخرة لتنضم إلى الغاز الناقل ومن ثم يمكن فصل هذه المواد عن بعضها وتعينها ويمكن أيضًا بطريقة كروماتوجرافيا الغاز إجراء التقدير الكمي لهذه المواد المنفصلة.
الفصل

طرق مختلفة
- التحليل باستخدام البولاروميتر: يقاس مقدار الانحراف الناتج عند مرور الضوء المستقطب خلال المحلول.
- التحليل بقياس انكسار الضوء: يقاس معامل الانكسار الذي يقوم بتعيين التركيب الكيميائي للخليط.
- مطياف الكتلة: يمكن بهذه الطريقة قياس النسبة بين شحنة كتلة أيونات مختلفة ناتجة من تكسير جزيئات كبيرة ومنه يمكن إيجاد الوزن الجزيئي والتركيز .
- التوصيل الحراري: وفيه يقاس التوصيل الحراري ويستدل منه على تركيب المادة.
- طرق تحليل المواد المشعة: وفيه تشع المادة المادة لتصبح ذات نشاط إشعاعي ثم تعد الأشعة أو الجسيمات المتدفقة منها لغرض تقديرها كميًا.
منهجية التحليل
تأخذ حلول كل المشاكل التحليلية أكانت نوعية أم كمية المنهجية ذاتها، وتتلخص هذه المنهجية باتباع التسلسل التالي:
ـ اختيار الطريقة: يُعد اختيار طريقة إجراء التحليل الخطوة الحيوية في حل المشكلة التحليلية. لا يتم الاختيار حتى يتم تعريف مجمل المشكلة. وعند اختيار الطريقة لا بد من إجراء مقارنة بين الحساسية والوثوقية والدقة المطلوبة للنتائج وبين التكاليف الواجب إنفاقها. فمثلاً، قد تزودنا مطيافية الفلورة بالأشعة السينية بنتائج سريعة لمشكلة آثار العناصر لكنها غير دقيقة كمياً. كمثال آخر، تزودنا مطيافية الامتصاص الذري بنتائج أكثر دقة، لكن على حساب العمل اليدوي الكيميائي المستهلِك للوقت.
ـ الاعتيان: الاعتيان الصحيح هو حجر الزاوية في الحصول على نتائج موثوقة، إذ من الضروري تحديد كيف ومتى وأين يجب أخذ العينة بحيث تُمثل بصدق المعطى الذي يجب قياسه.
ـ المعالجة المبدئية للعينة: عند التحليل الكمي يجب أخذ جزء من العينة يُمثلها، ويجبقياسه إما ككتلة أو كحجم، ففي حال تحليل عينة متجانسة يمكن تجزئتها بدون أي معالجة مسبقة، أما عند التعامل مع العديد من المواد الصلبة فإن الأمر يحتاج إلى معالجة مسبقة كالطحن والمزج. غالباً ما تحتاج العينة معالجة إضافية من أجل التحليل كالتجفيف والترميد والإذابة وقد تكون مثل هذه المعالجة كافية في بعض الأحيان وهو ما يعرف بالتحليل المباشر.
ـ الاستخلاص: تخضع نسبة مرتفعة من القياسات التحليلية للتأثير الناجم عن مكونات العينة الأخرى. تستفيد الطرائق الأكثر حداثة باطراد من التقانات الآلية للتمييز ما بين إشارة المادة المراد تحديدها وإشارات المواد المعيقة الأخرى. ومع ذلك، فإن هذا التمييز لا يحصل دوماً، وأحياناً يتم إجراء تفاعل كيميائي انتقائي لحجب المواد المعيقة. يجب استخلاص المادة المراد تحليلها من المكونات المعيقة عندما لا يمكن التوصل إلى حجب إعاقتها للتحليل. إذا كان الهدف إجراء تحديد كمي فيجب أن تكون عمليات الاستخلاص كمية أو معروفة نسبة استخلاص المادة المراد تحديدها.
ـ القياس النهائي: وهي الخطوة الأسرع والأسهل من الخطوات السبع الأخرى، ويجب أن تكون موثوقة بقدر الخطوات الأخرى. الأمر الأساسي الذي يجب معرفته هو التناسب ما بين مقدار القياس وكمية المادة المراد تحديدها.
ـ طريقة التحقق: لا معنى من إجراء التحليل بدون معرفة أن النتائج التي سيتم الحصول عليها لها معنى واضح معلوم. لا يتم التأكد من هذا الأمر إلا بعد تأمين طريقة لائقة للتحقق من الطريقة قبل إجرائها وإظهار فاعلية أدائها لاحقاً. أفضل أساليب التحقق هو تحليل معايير مقياسية (كواشف مرجعية) يجري اختبارها دورياً.
ـ تقييم النتائج: يجب تقييم النتائج التحليلية بطرائق إحصائية مناسبة والأخذ بمضامينها في ضوء المشكلة الأصلية.
التوجهات المستقبلية للطرائق والإجراءات التحليلية
هناك تطوير وتغيير مستمر في تقنيات وطرائق التحليل الكيميائي. يسمح التصميم الأفضل للأجهزة والمعرفة الأعمق لآليات العمليات التحليلية بالتطوير المستمر من أجل رفع سوية الحساسية والدقة والموثوقية تسهم هذه التغيرات في التوصل إلى طرائق تحليلية أكثر اقتصادية تقود بشكل متكرر إلى إلغاء خطوات الاستخلاص المستهلكة للوقت. التطوير والغاية النهائية وفق هذا الاتجاه هو التوصل إلى طريقة لا تحطم العينات ولا توفر الوقت فقط بل تترك العينة بعد تحليلها دون أي تغيير فيها من أجل استقصاءات أو عمليات أخرى.
تصاعدت أهمية أتمتة العمليات التحليلية، التي قد تكون أحياناً بوساطة الإنسالات (الروبوتات) التحليلية، إذ يمكنها إجراء سلسلة من العمليات المخبرية التحليلية على نحو أسرع وأكثر كفاية، وبموثوقية أعلى، وفي حالات أخرى يمكن استمرار متابعة إظهار نتائج تحليل مادة معينة في أثناء العمليات الإنتاجية الصناعية.
في العقد الأخير من القرن الماضي حصل تطوران مهمان أولهما إدخال عمليات الضبط عبر المعالِجات المنمنَمة (ميكروبروسيسور) ضمن الأجهزة التحليلية وثانيهما إظهار معطياتها باستخدام الحواسيب الدقيقة والصغيرة، والذي تحوَّل في بدء هذا القرن نحو استخدام الحواسيب الشخصية والمحمولة. أدى استخدام المعالِجات المنمنَمة إلى تحسين ضبط الجهاز وأدائه وسهولة إجراء صيانته الدورية وذلك عبر وجود إمكانية إظهار حالة الأجزاء المكونة للجهاز. من الممكن تشغيل هذه الأجهزة بوساطة يد عاملة غير خبيرة نسبياً عبر المحاورة من خلال لوحة مفاتيح بسيطة تتضمن حفظ وإعادة طلب الطرائق المعيارية، وتشكيل تقرير، وإجراء اختبارات فحص لحالة الجهاز. أفادت الحواسيب التي تعالج المعطيات بحنكة وبرامج الرسومات البيانية بشكل مشابهٍ في التوصل إلى جمع البيانات التحليلية وحفظها ومعالجتها وتحسينها وتفسيرها. كما تم التوصل إلى الحالة المثالية للتحليل الكيميائي ورفع سوية المعلومة الناتجة عبر أنظمة إدارة المعلومة المخبرية التي تسمح بالمناقشة الآلية لعدد كبير من العينات والقياسات الكيميائية التي نتجت حاسوبياً وأيضاً عبر إجراء معالجة إحصائية محنكة للنتائج، وكذلك عبر أنظمة الخبرة التي تستطيع أن تقوم بالقيادة الحاسوبية الذكية وتساعد في حل المشاكل التحليلية.
تتابع ظهور المشاكل التحليلية ضمن قوالب جديدة، إذ تزايد الطلب على التحليل ضمن مجال واسع بوساطة الأجهزة المحمولة التي تحتاجها دراسات مجسات الفضاء الخارجي وأعماق المحيطات. أما في المجالات الأخرى، كالدراسات البيئية والسريرية، فقد تزايدت أهمية التحديد الدقيق للشكل الكيميائي لعنصر ما ضمن العينة أكثر من أهمية تركيزه الموجود فيها. المثالان الأكثر تداولاً هما شدة ارتفاع سمية المركبات العضوية للزئبق أو للرصاص مقارنة مع مركباتهما غير العضوية المشابهة. يُمثل تحديد وقياس العنصر ضمن شكل كيميائي محدد من أصعب المشكلات التي تواجه المحللين الكيميائيين في الوقت الحاضر.
انظر أيضا
- AutoAnalyzer
- قائمة طرق الكيمياء التحليلية
- Important publications in analytical chemistry
- Measurement Science and Technology - journal
- Sensory analysis - in the field of Food science
- Virtual instrumentation
- تحليل كيمياء المياه
- Working range
- علم القياس
- Measurement uncertainty
- Microanalysis
المراجع
- كتاب الكيمياء التحليلية. د. صلاح أحمد محمد. Pr. A. j. Pr. B.d.
- M.Qintin, Electro chimic (P.U.F 1940).
- G.Milazr, Det coll. Electrochimic (Dunod 1969).
المصادر
- ^ محمود أبو دان. "التحليل الكيميائي". الموسوعة العربية. Retrieved 2011-09-29.
- ^ عبد العزيز رمضان. "التحليل الكهركيميائي". الموسوعة العربية.
- ^ Schermelleh, L.; Carlton, P. M.; Haase, S.; Shao, L.; Winoto, L.; Kner, P.; Burke, B.; Cardoso, M. C.; Agard, D. A. (2008). "Subdiffraction Multicolor Imaging of the Nuclear Periphery with 3D Structured Illumination Microscopy". Science. 320 (5881): 1332. doi:10.1126/science.1156947. PMC 2916659. PMID 18535242.