پروستاگلاندين
پروستاگلاندين Prostaglandin هو أي عضو في مجموعة مركبات الدهون المشتقة إنزيمياً من الأحماض الدهنية وتؤدي وظائف هامة في جسم الحيوان. ويحتوي كل پروستاگلاندين على 20 ذرة كربون، بما فيهم حلقة من 5 ذرات كربون. وهم وسطاء ولهم تشكيلة متنوعة من التأثيرات الفيزيولوجية القوية؛ بالرغم من أنهم، تقنياً، هرمونات، إلا أنهم نادراً ما يصنفوا كذلك.
الپروستاگلاندينات معاً مع الثرومبوكسانات thromboxane والپروستاسيكلينات prostacyclin يشكلوا رتبة prostanoid من مشتقات الأحماض الدهنية؛ ورتبة prostanoid هي رتبة جزئية من eicosanoids.
التاريخ والاسم

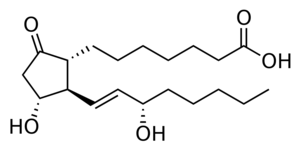
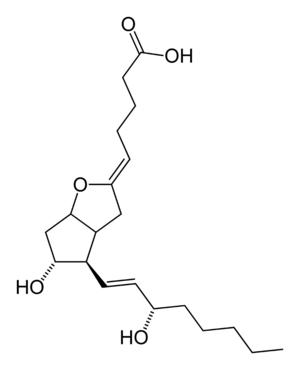
كشف الطبيب المشرح الأمريكي غولدبلات H.Goldblatt والفيزيولوجي السويدي فون أولير U.S.Von Euler البروستاغلاندينات كل منهما على حدة في بداية الثلاثينات. وحديثاً درس الباحثون شأن البروستاغلاندينات الفيزيولوجي والمرضي في الإنسان والحيوان. تصنيفها جميع البروستاغلاندينات حموض دهنية ذات 20 ذرة من الفحم، وفيها حلقة خماسية cyclopentane وسلسلتان جانبيتان وجذر هدروكسي أو أكثر.
تركيبها في الجسم
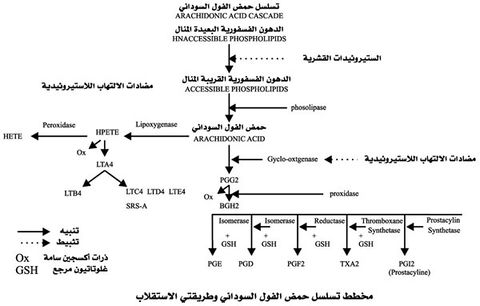
البروستاغلاندينات نواتج أكسدة الحموض الدهنية الأساسية اللامشبعة، وأهمها وأكثرها غزارة في الجسم حمض الفول السوداني arachidonic acid وهو سلف الزمرة 2. ويستقلب حمض الفول السوداني بعد تحرره بأحد طريقين: طريق خميرة السيكلوأكسيجيناز cyclo-oxygenase الذي ينتهي بتكوين البروستاغلاندينات، وطريق خميرة الليبوكسيجيناز lipoxygenase الذي ينتهي بتكوين اللوكوتريئين (LT) leukotrienes ومواد أخرى. شكل مخطط تسلسل حمض الفول السوداني وطريقتي الاستقلاب
آلية عملها الفيزيولوجي
أظهر الطبيب الدوائي الأمريكي سوذرلاند E.W.Sutherland. وجماعته أن التأثيرات الحيوية للهرمونات تتم عن طريق الرسول الثاني وهو cyclic adenosine monophosphate (cAMP) الذي يتشكل في غشاء الخلية بوساطة خميرة adenylate cyclase، ولوحظ أن معظم الهرمونات التي تزيد تركيز cAMP في الخلايا تزيد أيضاً تركيز البروستاغلاندين في الأنسجة. والبروستاغلاندينات مفعّلات قوية لخميرة adenylate cyclase ويبدو أن تأثير هذه المواد في كثير من الخلايا يتم عن طريق cAMP وفي قليل منها عن طريق (cyclic guanosine monophosphate) cGMP وبذلك تكون البروستاغلاندينات هي الرسول الثاني وcAMP الرسول الثالث لتأثير الهرمونات في الخلايا. لذلك عُدّت البروستاغلاندينات طبقة جديدة من الهرمونات الموضعية. ويمكن للبروستاغلاندين الواحد أن ينبه cAMP في أنسجة ما ويثبطها في أنسجة أخرى. مثال ذلك PGE1 ينبه cAMP في القلب والرئة والكريات البيض وقشر الكظر، ويثبطها في أنابيب الكلية والمعدة ولب الكظر.
وتقوم البروستاغلاندينات بأحد عملين: فإما أن تحدث استجابات خلوية معينة أو تنظم الاستجابات الخلوية لعوامل أخرى. ففي الحالة الأولى تعمل عمل الشادّات agonists المدرسية (كالإستيل كولين مثلاً) فتنشط خلية مهدوفاً إليها قادرة على الاستجابة. مثال: تأثير البروستاغلاندين المباشر المقبض للعضلات الملس في أنبوب الهضم. أما في الحالة الثانية فهي تعدل إنتاج مواد أخرى شادة أو تعدل فاعليتها. مثال: PGE2 يزيد نتح البروتين من البلاسما بتأثير البراديكينين. وقد تنظم البروستاغلاندينات إفراز الوسائط mediators، ومثال ذلك تثبيط PGE2 لإفراز الحمض في المعدة والهستامين من الخلايا البدينة mastocytes وانطلاق الإستيل كولين من نهايات الأعصاب الودية.
عمل البروستاغلاندينات وLT في الالتهاب
لوحظ عمل البروستاغلاندين في حالات الالتهاب عندما كشف الطبيب الدوائي الإنكليزي فان J.B.Vane. وجماعته أن قدرة مضادات الالتهاب اللاستيروئيدية (الأسبرين والإندوميتاسين وغيرهما) على قمع الالتهاب تتناسب وقدرتها على تثبيط السيكلوأكسيجيناز ومِن ثَمَّ تثبيط تركيب البروستاغلاندين. ولم تكن البروستاغلاندينات معدودة من الوسائط المهمة في الالتهاب قبل هذا الكشف. وحار الباحثون في هذا التناقض الظاهري إلى أن عُرف العمل الحقيقي لهذه المواد في الالتهاب. فهي مثلاً قلّما تحدث الألم بذاتها إلا أنها تزيد من شدة الألم المحدث بالبراديكينين bradykinin والهستامين histamine ومدته. ولسلسة PGE فعل مماثل في زيادة النفوذية الوعائية الناجمة عن هذين العاملين. وتوجد البروستاغلاندينات بتركيز عال في الانصبابات الالتهابية كالسائل الزليلي للمفاصل الملتهبة. وتشترك خلايا النسيج الضام والعضلات الملس وبطانة الأوعية بإنتاج PGE2 وPGI2 في الالتهاب. ويبدو أن البروستاغلاندينات عامة وPGE2 وPGI2 خاصة من وسائط الالتهاب الحاد إذ يتجلى الألم وتوسُّع الأوعية والوذمة. أما في الالتهاب المزمن، فأثر البروستاغلاندينات أقل وضوحاً، لأن الفعل الرئيس هنا للمفوكينات (وهي نواتج تفعيل اللمفيات) هو الجذب الكيمياوي للمعتدلات والوحيدات والبالعات الكبيرة، وفي تفعيل اللمفيات الأخرى وارتشاف العظم وإحداث السمية الخلوية. ويقتصر أثر البروستاغلاندينات هنا على تنظيم الوسائط الأخرى مثال: PGE2 مثبط فعال لتفعيل اللمفيات وما يرافقه من إفراز اللمفوكينات. ويعتقد أن له أثراً في التلقيم الراجع feed-back السلبي لمدى تفعيل اللمفيات ومدته. ويستنتج مما سبق أن للبروستاغلاندينات عملين متعاكسين في الالتهاب: هما تنبيه وتثبيط. وفي حالات عوز الحموض الدهنية السالفة للبروستاغلاندين تزداد فوعة الالتهابات المزمنة الاختبارية كمرض فئران NZB الشبيه بالذأب الحُمامي lupus erythematosus. وبالعكس إن استعمال الحموض الدهنية هذه أو البروستاغلاندينات يخفف من وطأة هذه الأمراض. ولهذا يخشى، نظرياً، من استعمال مضادات الالتهاب اللاستيروئيدية في الالتهابات المزمنة. لكن في الواقع يكون تأثيرها متوازناً بين فائدتها في تخفيف الألم وتوسع الأوعية والوذمة من جهة، وتفعيلها لإفراز وسائط الالتهاب من جهة أخرى. وقد يفسر هذا الأمر عدم جدوى مضادات الالتهاب اللاستيروئيدية في الالتهابات المزمنة عدا المفصليّة منها.
واستمر البحث لإيجاد مواد تثبط استقلاب حمض الفول السوداني، لعلاج الأمراض الالتهابية، ورُكِّبت مواد تثبط السيكلوأكسجيناز هي مضادات الالتهاب اللاستيروئيدية، ومنها اليوم العشرات في السوق الدوائية تنتمي إلى عدة أسر.
البروستاغلاندينات وجهاز الهضم
لهذه المواد أثر في حركة جهاز الهضم وإفرازه، فمنها PGE1 وPGE2 يرخيان مصرة الفؤاد وPGF يقبضها. وهي، عامة، ترخي مصرة البواب وتحافظ على حركة الأمعاء ولاسيما القولون فتزداد كميتها في الأمراض التي يرافقها الإسهال. ويثبط PGE1 وPGE2 وPGA1 إفراز الحمض في المعدة بتأثير مباشر على الخلايا الجدارية. وتنقص البروستاغلاندينات حجم مفرزات المعدة ومحتواها من الببسين على نحو متناسب، في حين تثبط إفراز الحمض بدرجة تفوق تثبيطها لحجم العصارة. أما في الأمعاء فينبه PGE إفراز الماء والالكتروليتات من الصائم بما يشبه فعل ذيفان الكوليرا. وتبين أن الذيفانات الداخلية (الإندوتوكسينات) تنبه إفراز البروستاغلاندينات فتكون هذه مسؤولة عن الإسهال وعن التبدلات الهيموديناميكية في الصدمة السمية.
لما سبق تطبيقات مهمة. فلمضادات الالتهاب اللاستيروئيدية تأثير مقرِّح معروف يعزى إلى زيادة إفراز الحمض وضعف مقاومة المخاطية نتيجة تثبيط بروستاغلاندينات أنبوب الهضم. ولا يستفاد من إعطاء البروستاغلاندينات عن طريق الفم للوقاية لأنها تستقلب في أنبوب الهضم ويتحول ما امتص منها إلى أشكال غير فعالة في الرئة والكبد. ولكن تمّ تركيب مضاهيات للبروستاغلاندينات تعطى عن طريق الفم للوقاية من التأثير المقرّح لمضادات الالتهاب اللاستيروئيدية منها (16.16 dimethyl-PGE2) DM-PGE2 والميزوبروستول misoprostol.
البروستاغلاندينات والولادة والإجهاض
للبروستاغلاندينات تأثيرات عدة في جهاز المرأة التناسلي تشمل علاقتها بهرمونات الوطاء أو تحت المهاد hypothalamus والنخامى وتأثيرها في المبيض والجسم الأصفر والرحم.
يزداد إفراز منتحيات المناسل بتأثير البروستاغلاندينات في ما تحت المهاد والنخامى. أما في المبيض فقد يكون لهذه المواد أثر في انبثاق الجريِّب لأن مضادات الالتهاب اللاستيروئيدية تثبط الإباضة. كما أن إحداث الإباضة بفعل الهرمون الملوتن يعتمد على البروستاغلاندينات وعلى cAMP وcGMP. ويفرز الرحم PGF2a (الذي يقوم بعمل هرمون منظم لدورة المبيض مسبباً غؤور الجسم الأصفر وتوقف إنتاج البروجسترون بتأثير مباشر، على الأقل في الحيوان). أما في الإنسان، فحقن PGF2a في الجسم الأصفر يؤدي إلى تراجع البروجسترون وحدوث حيض مبكر. وبالعكس، إن استئصال الرحم أو إعطاء مضادات الالتهاب اللاستيروئيدية يطيل عمر الجسم الأصفر ولايتم فعل الإستروجين في انحلال الجسم الأصفر بوجود هذه الأدوية مما يشير إلى أن هذا الفعل يعتمد على البروستاغلاندينات.
وتنبه البروستاغلاندينات تقلص العضلات الملس وتوجد بمقادير كبيرة جداً في دم الحيض. وهناك تناسب بين كمية البروستاغلاندينات وعسر الطمث. وتفرز بطانة الرحم هذه المواد بمقادير ونوعية تختلف باختلاف مرحلة الدورة الشهرية. فيكثر مثلاً PGF2a في نهاية المرحلة اللوتيئينية luteinic. وينظم كل من الإستروجين والبروجسترون مقدار البروستاغلاندينات المفرزة في الرحم ونسبها. فالإستروجين يزيدها والبروجسترون ينقصها ويعدل نسبة ويقلل من حساسية الرحم للبروستاغلاندين.
ويزداد إفراز البروستاغلاندينات من بطانة الرحم بوجود اللولب مما يفسر جزئياً العقم الناتج عن استخدامه. وإعطاء هذه المواد في أي مرحلة من مراحل الحمل ينبه المخاض، ويعد الطريقة المثلى للإجهاض في الثلث الثاني من الحمل. وتطيل مضادات الالتهاب اللاستيروئيدية مدة الحمل. ويهبط إنتاج البروجسترون في المشيمة في الأربع وعشرين ساعة السابقة للمخاض، فتزداد حساسية الرحم للبروستاغلاندين وتبدأ التقلصات الدورية. كما تقوم البروستاغلاندينات بدور وسيط للأوكسيتوسين في الرحم وقد يكون لها أثر في تنظيم دوران الدم فيها: ففي الحمل يزداد صبيب الدم في الرحم وتصبح أوعيتها مقاومة للهرمونات المقبضة.
ولما سبق تطبيقات عملية مهمة مثل: إحداث الإجهاض بإعطاء البروستاغلاندين بطريق المهبل أو بطريق الوريد، ومعالجة عسر الطمث بمضادات الالتهاب اللاستيروئيدية.
عمل البروستاغلاندينات في الكلية وتنظيم الماء والالكتروليتات
لهذه المواد عملها في تنظيم توعية الكلية وإدرار الصوديوم والماء. فإن PGE2 وPGI2 وPGA2 وPGD2 موسعة للأوعية. وتفرز الكبب الكلوية وأوعيتها الواردة PGE2 وPGI2 اللذين يعملان على زيادة الصبيب الدموي في الكلية وإعادة توزيعه بتوجيهه نحو باطن القشر. وتبطل مضادات الالتهاب اللاستيروئيدية هذا التأثير. ولا يتضح أثر البروستاغلاندينات في تنظيم دوران الكلية في الحالة السوية بل في اضطراب الدوران الكلوي أو قصوره إذ يزداد إفرازها. وتتدخل البروستاغلاندينات في إفراز الرينين من الخلايا المجاورة للكبب. فتحث البروستاغلاندينات الموسعة للأوعية على إفراز الرينين renin بتأثيرها في مستقبلات الضغط baroreceptors كما تفعل الموسعات الأخرى كالإستيل كولين والبراديكينين. وتبطل مضادات الالتهاب اللاستيروئيدية تلك التأثيرات. والمدرُّ المعروف furosemide يوسع الأوعية ويطلق الرينين بفعلٍ تعاكِسُه هذه الأدوية، ولهذا الأمر أهمية لدى إشراك مدر مع مضاد التهاب.
والبروستاغلاندينات مدرة للصوديوم كموسعات الأوعية الأخرى. وهي تتوسط استجابة البقعة الكثيفة macula densa للصوديوم. وبذلك يتضح أن إفراز الرينين يعتمد على البروستاغلاندين سواء بطريق مستقبلات الضغط أو البقعة الكثيفة. وإن كلا من PGE1 وPGE2 وPGA1 وPGA2 يزيد الصبيب الدموي في الكلية وحجم البول وطرح الصوديوم. وليس واضحاً إذا كان طرح الصوديوم مستقلاً عن التأثير الموسع للأوعية وبالتالي المدر. فقد بُرهن أن PGE2 ينقص عودة امتصاص الصوديوم في القسم الصاعد من عروة هنلة Henle. ويقلل الإندوميتاسين من طرح الصوديوم مؤقتاً لكنه لا يؤثر في طرحه في أثناء حقن السوائل الملحية. وبوجه عام، إن مضادات الالتهاب اللاستيروئيدية قد تسبب الوذمات وتنقص من وظيفة الكلية بمعاكستها البروستاغلاندينات الموسعة للأوعية والمدرة للصوديوم.
أما الماء فتتبع عودة امتصاصه في الكلية هرمون الفازوبريسين الذي يزيد نفوذية الأنبوب الجامع للماء. ويفعِّل هذا الهرمون الفسفوليباز فيزداد PGE2 في الخلايا الخلالية. ويثبط PGE2 نفوذية الأغشية للماء ومِن ثَمَّ ينقص الاستجابة للفازوبريسين. ولكن الفازوبريسين، من جهة أخرى، يحث على تركيب cAMP الذي يزيد نفوذية الأغشية. وهكذا فإن الهرمون نفسه ينبه إنتاج مادتين لهما تأثيران متضاربان، وهذا التناقض الظاهري هو في الواقع عملية تنظيم متوازن لطرح الماء. ونجح استعمال مواد مثبطة لتركيب PGE2 تزيد من حساسية الكلية للفازوبريسين في معالجة البيلة التفهة، هي مشتقات sulfonylurea.
عمل البروستاغلاندينات وLT في الرئة
تُركَّب البروستاغلاندينات بسهولة في الرئة لغناها بالركيزة substrate أي بالمادة التي يؤثر فيها إنظيم فيسهل تحولها الكيمياوي؛ وتتخرب أيضاً بسهولة فيها بخميرةprostaglandin dehydrogenase (PGDH) وإن استجابة أوعية الرئة وطرقها الهوائية للبروستاغلاندين أعظم من استجابتها لأي مادة أخرى ذات فاعلية وعائية. وأهم بروستاغلاندينات الرئة PGI2 بسبب غناها بالخلايا الوعائية البطانية. ولا يكاد PGI2 يتخرب في الرئة بعكس غيره، وهو البروستاغلاندين الوحيد القادر على توسيع أوعية الرئة الناضجة. ولا يتضح ذلك في الحالات السوية إذ تكون أوعية الرئة متسعة أصلاً، إلا أن عمله جلي في حالات فرط التوتر الرئوي فهو يوسع الأوعية والطرق الهوائية ويمنع تكدس الصفيحات. ويليه أهمية TxA2 وهو مقبض للأوعية وللطرق الهوائية ومكدس قوي للصفيحات، وله أثر في الصدمة السمية وأعراضها الرئوية. وأخيراً PGF2a مقبض فعال للقصبات ولأوعية الرئة دون غيرها، ويستقلب بمرور واحد في الرئة. أما PGE2 فيختلف أثره في الرئة بحسب النوع الحيواني وتبدو أهميته في الحفاظ على انفتاح القناة الشريانية في الجنين بالتعاضد مع PGI2. ولما كانت مضادات الالتهاب اللاستيروئيدية تعبر المشيمة فإن تناولها في الحمل قد يؤدي إلى انغلاق القناة الشريانية ومِن ثُمَّ إلى فرط التوتر الرئوي لدى الجنين. وبالعكس يستفاد من هذا الأمر في حالات عدم انغلاق القناة الشريانية بعد الولادة بإعطاء الوليد مضاد التهاب لاستيروئيدي في الأسبوعين الأولين، إذ تتناقص استجابة القناة لهذه الأدوية مع العمر. وتدعى هذه المعالجة «الربط الكيمياوي للقناة». وبروستاغلاندينات الزمرة 1 نادرة في الإنسان وتأثيراتها الرئوية مختلفة عن تأثيرات الزمرة 2. فمثلاً PGE1 موسع وعائي فعال وPGE2 مقبض ضعيف. ونجح استعمال PGE1 في معالجة فرط التوتر الرئوي العنيد عقب جراحة تشوهات القلب الولادية.
إن مشتقات طريق الليبوكسيجيناز وسائط مهمة للمكونات الخلطية والخلوية لحادثة الأرج. ولها خصائص مقبضة للأوعية والقصبات تؤثر في فرط التحسس. وتثبط مضادات الالتهاب اللاستيروئيدية السيكلوأكسيجيناز دون الليبوكسيجيناز. وقد يفسر ذلك حدوث الربو لدى المستعدين حين تناول هذه الأدوية، ويدعى ذلك بالربو الحساس للأسبرين.
البروستاغلاندينات في الأوعية الدموية والصفيحات: «حادثة التخثر»
تحتوي الصفيحات خميرة الفسفوليباز C التي تحرر حمض الفول السوداني فيها وتهيئه للتحول إلى بروستاغلاندين. وتقوم مواد كثيرة بتفعيل هذه الخميرة منها الترومبين والغراء والإيبينفرين و(ADP) (adenosine diphosphate) وdivalent ion ionophore وتركب الصفيحات عدة بروستاغلاندينات أكثرها كمّاً TxA2، وهو مقبض وعائي يضاهي الانجيوتنسين2، كما أنه أقوى مادة مكدسة للصفيحات عُرفت. وفي جدر الأوعية تركب الخلايا البطانية والعضلية الملس والفيبروبلاست PGI2 بالدرجة الأولى وأقل منه PGE2 وTxA2. وإن PGI2 موسع لمعظم شبكات الأوعية، وهو أقوى مضاد لتكدس الصفيحات عرف حتى اليوم. ويعمل عن طريق تنبيه cAMP وهو بعكس PGE2 لا يستقلب في الرئة إلا قليلاً، فيبقى مستوياه في الدم الشرياني والوريدي متساويين.
ويكمن أثر البروستاغلاندين في التخثر بالتوازن بين ما تفرزه جدر الأوعية من PGI2 وما تفرزه الصفيحات من TxA2 والتأثيرات المتضاربة لهاتين المادتين. ومضادات الالتهاب اللاستيروئيدية تثبط تركيب البروستاغلاندين عامة من دون انتقاء مطلق، لذلك صَعُب إيجاد عامل معين لتثبيط بروستاغلاندين معين لفائدة علاجية. لكن وُجد أن الأسبرين وحده يثبط سيكلوأكسيجيناز الصفيحات على نحو غير عكوس بالأستلة وفي دقائق. ولما كانت الصفيحات الناضجة لا تركب خميرة جديدة، كان تأثير الأسبرين يدوم دوام حياة الصفيحة في الدوران أي من 9 إلى 12 يوماً. ويكفي مقدار ضئيل من الأسبرين (350ملغ أي قرص واحد) لتعطيل 95% من الخميرة ومِن ثُمَّ من تركيب TxA2. وهذا المقدار غير كاف لمنع تركيب PGI2 من جدر الأوعية. لذلك يفيد إعطاء الأسبرين بمقدار ضئيل كل يومين في الوقاية من التخثر.
أنواعه
| النوع | Receptor | الوظيفة |
|---|---|---|
| PGI2 | IP | |
| PGE2 | EP1 |
|
| EP2 |
| |
| EP3 |
| |
| Unspecified | ||
| PGF2α | FP |
|