مولد إلكترونات خارجية
مولد الإلكترونات الخارجية exoelectrogen، مصطلح يشير إلى العضية الدقيقة التي تتمتع بالقدرة على نقل الإلكترونات خارج الخلية. رغم أن مصطلح مولد الإلكترونات الخارجية هو الاسم السائد، إلا أن هناك أسماء أخرى مستخدمة: البكتريا النشطة إلكترو-مكانيكياً، البكتريا المتنفسة أنودياً، ومولد الإلكترونات.[1] الإلكترونات المولدة خارجياً في هذه التقنية تُنتج في أعقاب إنتاج ثلاثي فوسفات الأدنوسين باستخدام سلسلة نقل الإلكترون أثناء الفسفرة التأكسدية. يتطلب التنفس الخلوي التقليدي مستقبل نهائي للإلكترون لاستقبال هذه الإلكترونات. الخلايا التي تستخدم الأكسجين الجزيئي (O2) كمستقبل نهائي للإلكترون توصف بأنها تستخدم التنفس الهوائي، بينما الخلايا التي تستخدم المركبات الأخرى القابلة للذوبان كمستقبل نهائيل للإلكترون توصف بأنها تستخدم التنفس اللاهوائي.[2] ومع ذلك، فإن المستقبل النهائي للإلكترون لمولد الإلكترونات الخارجية يوجد خارج الخلية وقد يكون عامل أكسدة قوي في المحلول المائي أو موصل صلب/مستقبل إلكترون. المستقبلين المرصودين الشائعين هما مركبات الحديد (خاصة أكاسيد الحديد الثلاثية) ومركبات المنجنيز (خاصة أكاسيد الحديد الثنائية والثلاثية).[3][4][5] وبما أن الأكسجين مؤكسد قوي، فإن الخلايا قادرة على القيام بذلك بدقة في غياب الأكسجين.[6]
في الوقت الحالي، استخدام مولد الإلكترونات الخارجية قيد البحث في مجال تطوير خلايا الوقود الدقيقة MFCs، والتي لديها القدرة على توليد المواد العضوية مثل الحمأة المنشطة الناتجة من معالجة مياه الصرف الصحي إلى إيثانول، غاز الهيدروجين، وتيار كهربائي.[1][7]
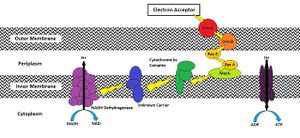
في حين أن العملية الدقيقة التي ستُختزل فيها المستقبل الخارجي تختلف من نوع لآخر، فقد تبين أن الطرق التي تتضمن استخدام مسار انزيم الأكسدة-الاختزال oxidoreductase الذي ينقل الإلكترونات إلى غشاء الخلية يكون معرض للبيئة الخارجية.[3] ينفصل هذا المسار عن مسار سلسلة نقل الإلكترون بعد أكسدة cytochrome bc1 complex (Complex III) بواسطة c-type cytochromes المصمم لنقل الإلكترونات نحو الوجه الخلوي الخارجي من الغشاء الخارجي بدلاً من سيتوكروم سي أكسيداز cytochrome c oxidase. MtrC وOmcA هما مثالين على السيتوكروم سي أكسيداز الذي يتواجد ذاتياً في الغشاء الخارجي لـ Shewanella oneidensis MR-1 مثقبات گاما، على الرغم من وجود العديد من الاختلافات الأخرى (شكل 1).[3][4][5][7][8]
بصرف النظر عن إطلاق الإلكترونات إلى المستقبل النهائي للإلكترون المؤكسد، قد يخدم نقل الإلكترون الخارجي في أغراض أخرى. أولاً، قد تنقل الخلايا الإلكترونات مباشرة لبعضها البعض دون الحاجة لمادة وسيطة. لوحظ أن Pelotomaculum thermopropioncum ترتبط بـ Methanothermobacter thermautotrophicus عن طريق الأشعار البكتيرية (بنى خارج خلوية تستخدم في الاقتران والالتصاق) that was determined to be electrically conductive. ثانياً، قد تؤدي الإلكترونات خارج الخلية دوراً في الاتصالات كإشارة نصاب في البيوفيلم.[1]
آلية نقل الإلكترونات الخارجية
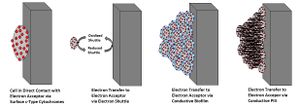
تبين أن انزيمات الأكسدة-الاختزال المختزلة عند الغشاء الخارجي للخلية تستخدم الطرق التالية لنقل إلكتروناتها إلى المستقبل النهائي للإلكترونات: المتصل النهائي، التنقل عبر مواد وسيطة مفرزة، عوامل استخلاب الحديد،[9] عبر البيوفيلم الموصل، وعبر الأشعار الموصلة (شكل 2). ومع ذلك، فإن هناك احتمالات بأن هذه الطرق غير تبادلية،[8] وقد تعتمد الطريقة المستخدمة على الظروف البيئية. في ظل الكثافة المنخفضة للبكتريا، قد يكون استخدام نواقل الإلكترون وعوامل الاستخلاب المخلقة بواسطة مولدات الإلكترونات الخارجية كلفة للغاية بسبب التركيزات الغير كافية لهذه الجزيئات المطلوبة للاسترداد واعادة الاستخدام.[9] في ظل هذه الظروف، قد يفضل النقل المباشر؛ ومع ذلك، سوف تفوق فوائد الطاقة على متطلبات الطاقة عندما يكون مجتمع البكتريا ذا حجم كاف.
يحدث الاختزال المباشر للمستقبل المؤكد عن طريق الاتصال بين انزيم الأكسدة-الاختزال داخل الخلية ومستقبل الإلكترون الطرفي (أي، القطب الكهربي أو المركب الفلزي الخارجي). على الرغم من تنوع هذه الپروتينات (مع أخذ كل من membrane-bound أو الأغشية القابلة للذوبان) ، فإن مواقعها الشائعة في الغشاء الخارجي أو الجبلة المحيطة في البكتريا سالبة-الگرام والبكتريا موجبة-الگرام توفر اتصالاً لصيقاً لنقل الإلكترونات.[10]
بالإضافة إلى ذلك، فوجود جزيئات نقل الإلكترونات تزيد معدل النقل المباشر بشكل كبير لأكثر من 80%.[4] على سبيل المثال، في Shewanella oneidensis MR-1، يتميز النقل من خلال سلسلة من الپروتينات المؤكسدة والهيكلية[11] الممتدة من الغشاء السيتوپلازمي إلى السطح الخارجي للخلية (كما في شكل 1). يعقد أن الفلاڤينات المفرزة تعمل لسد "الفجوة" بين پروتين/ات سطح الخلية والفلز الخارجي، مما قد يخفف من الحاجة إلى الاتصال المباشر ويسهل النقل عن بعد.[9] علاوة على ذلك، بما أن السيتوكرومات تعرف عمومًا الأسطح المحددة على المعدن الركيزي،[10] فقد تعمل الفلاڤينات القابلة للذوبان كجسر عام يسمح بالتبرع الإلكتروني لمجموعة متنوعة من الفلزات المختلفة فيالشكل والحجم،[4] التي قد تكون مفيدة في تطبقات خلايا الوقود الدقيقة. ويفترض أيضاً أن الفلاڤينات تعمل على ربط پروتينات الناقل الطرفي للإلكترونات كعامل مساعد لزيادة معدلات الأكسدة.[11]
في 11 يناير 2019 ابتكر علماء في معهد مساتشوستس للتكنولوجيا تقنية انتقال الإلكترونيات خارج الخلية Extracellular electron transport لانتقاء البكتريا المولدة للكهرباء مثل البكتريا الأرضية. تلك البكتريا تعيش في ظروف قاسية داخل فوهات البراكين أو في أعماق سحيقة بقاع المحيط أو داخل الأمعاء، ولذلك تولِّد إلكترونات لاستخلاص الأكسجين لتتنفسه. العلماء يبحثون استخدام تلك البكتريا وحثها لهضم المواد الملوثة للبيئة.[12]
المصادر
- ^ أ ب ت Logan B. (May 2009). "Exoelectrogenic bacteria that power microbial fuel cells". Nature Reviews Microbiology. 7: 375–383. doi:10.1038/nrmicro2113.
- ^ Willey J.; et al. (2011). Prescott's Microbiology. McGraw Hill. pp. 228–245. ISBN 978-0-07-337526-7.
- ^ أ ب ت Hartshorne R.; et al. (Dec 2009). "Characterization of an electron conduit between bacteria and the extracellular environment" (PDF). Proceedings of the National Academy of Sciences. 106: 22169–22174. doi:10.1073/pnas.0900086106.
- ^ أ ب ت ث Baron D. (Oct 2009). "Electrochemical Measurement of Electron Transfer Kinetics by Shewanella oneidensis MR-1". The Journal of Biological Chemistry. 284 (42): 28865–28873. doi:10.1074/jbc.M109.043455. PMC 2781432. PMID 19661057.
- ^ أ ب Shi L.; et al. (2006). "Isolation of a High-Affinity Functional Protein Complex between OmcA and MtrC: Two Outer Membrane Decaheme c-Type Cytochromes of Shewanella oneidensis MR-1". Journal of Bacteriology. 188 (13): 4705–4714. doi:10.1128/JB.01966-05. PMC 1483021. PMID 16788180.
- ^ Logan B. (2008). Microbial Fuel Cells. John Wiley & Sons Inc. pp. 4–6. ISBN 978-0470239483.
- ^ أ ب Flynn J.; et al. (2010). "Enabling Unbalanced Fermentations by Using Engineered Electrode-Interfaced Bacteria". mBio, American Society of Microbiology. 1 (5): 1–8. doi:10.1128/mBio.00190-10.
- ^ أ ب Lovley D. (2008). "The microbe electric: conversion of organic matter to electricity". Current Opinion in Biotechnology. 19: 1–8. doi:10.1016/j.copbio.2008.10.005.
- ^ أ ب ت Nevin, Kelly P.; Lovley, Derek R. (March 2002). "Mechanisms for Fe(III) Oxide Reduction in Sedimentary Environments". Geomicrobiology Journal. 19 (2): 141–159. doi:10.1080/01490450252864253.
- ^ أ ب Gralnick, Jeffrey A.; Newman, Dianne K. (July 2007). "Extracellular respiration". Molecular Microbiology. 65 (1): 1–11. doi:10.1111/j.1365-2958.2007.05778.x. PMC 2804852.
- ^ أ ب Shi, Liang; Dong, Hailiang; Reguera, Gemma; Beyenal, Haluk; Lu, Anhuai; Liu, Juan; Yu, Han-Qing; Fredrickson, James K. (30 August 2016). "Extracellular electron transfer mechanisms between microorganisms and minerals". Nature Reviews Microbiology. 14 (10): 651–662. doi:10.1038/nrmicro.2016.93.
- ^ Jennifer Chu (2019-01-11). "Technique identifies electricity-producing bacteria". MIT News.