أكسجين
 Liquid oxygen boiling (O2) | |||||||||||||||
| أكسجين | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| التآصلات | O2, O3 (أوزون) والمزيد (انظر تآصلات الأكسجين) | ||||||||||||||
| المظهر | غاز: عديم اللون سائل وصلب: أزرق شاحب | ||||||||||||||
| الوزن الذري العياري Ar°(O) | |||||||||||||||
| أكسجين في الجدول الدوري | |||||||||||||||
| |||||||||||||||
| الرقم الذري (Z) | 8 | ||||||||||||||
| المجموعة | 16 | ||||||||||||||
| الدورة | period 2 | ||||||||||||||
| المستوى الفرعي | p-block | ||||||||||||||
| التوزيع الإلكتروني | [He] 2s2 2p4 | ||||||||||||||
| الإلكترونات بالغلاف | 2, 6 | ||||||||||||||
| الخصائص الطبيعية | |||||||||||||||
| الطور at د.ح.ض.ق | gas | ||||||||||||||
| نقطة الانصهار | 54.36 K (−218.79 °س، −361.82 °F) | ||||||||||||||
| نقطة الغليان | 90.188 K (−182.962 °س، −297.332 °ف) | ||||||||||||||
| الكثافة (at STP) | 1.429 g/L | ||||||||||||||
| حين يكون سائلاً (عند ن.غ.) | 1.141 ج/سم³ | ||||||||||||||
| النقطة الثلاثية | 54.361 K, 0.1463 kPa | ||||||||||||||
| النقطة الحرجة | 154.581 K, 5.043 MPa | ||||||||||||||
| حرارة الانصهار | (O2) 0.444 kJ/mol | ||||||||||||||
| حرارة التبخر | (O2) 6.82 kJ/mol | ||||||||||||||
| السعة الحرارية المولية | (O2) 29.378 J/(mol·K) | ||||||||||||||
ضغط البخار
| |||||||||||||||
| الخصائص الذرية | |||||||||||||||
| حالات الأكسدة | 2، 1, −1، −2 | ||||||||||||||
| الكهرسلبية | مقياس پاولنگ: 3.44 | ||||||||||||||
| طاقات التأين |
| ||||||||||||||
| نصف قطر التكافؤ | 66±2 pm | ||||||||||||||
| نصف قطر ڤان در ڤالز | 152 pm | ||||||||||||||
| خصائص أخرى | |||||||||||||||
| التواجد الطبيعي | primordial | ||||||||||||||
| البنية البلورية | cubic | ||||||||||||||
| سرعة الصوت | 330 م/ث (غاز، عند 27 °س) | ||||||||||||||
| قضيب رفيع | 26.58×10−3 W/(m·K) | ||||||||||||||
| الترتيب المغناطيسي | مغناطيسي مساير | ||||||||||||||
| القابلية المغناطيسية | +3449.0·10−6 cm3/mol (293 K)[1] | ||||||||||||||
| رقم كاس | 7782-44-7 | ||||||||||||||
| التاريخ | |||||||||||||||
| الاكتشاف | كارل ڤلهلم شيله (1771) | ||||||||||||||
| سمّاه | أنطوان لاڤوازييه (1777) | ||||||||||||||
| نظائر الأكسجين | |||||||||||||||
| قالب:جدول نظائر أكسجين غير موجود | |||||||||||||||
الأكسجين هو أحد العناصر الكيميائية الموجودة في المجموعة السادسة في الجدول الدوري (جدول مندلييف)، وله الرمز O ورقم ذري 8, وزنه الذري 15.9994 بالنسبة إلى الكربون 12C، غازي عديم اللون والرائحة والطعم, وهذا العنصر شائع للغاية، ولا يوجد فقط على الأرض ولكن في كل الكون، وغالبا يكون مرتبطا مع عناصر أخرى. الأكسجين غير المرتبط (وغالبا ما يطلق عليه الأكسجين الجزيئي, O2) يوجد في أول الأمر على سطح الأرض كناتج لعمليات التأيض للبكتريا ثم تواجد الأكسجين الحر في الغلاف الجوي بعد ذلك في العصر الجيولوجي وحتى الآن ينتج بوفرة من النبات، والتى تنتج الأكسجين خلال عمليات البناء الضوئي. والأكسجين ضروري للتنفس وللحياة ولا ينافسه في القيمة والأهمية أي عنصر آخر على كوكبنا.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الخواص المميزة
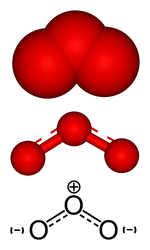
فى ظروف الحرارة والضغط القياسية ، يتواجد الأكسجين في الحالة الغازية يتكون الأكسجين من جزيئات ثنائية الذرة لها الشكل O2 . ويكون O2 له شكلان حسب الطاقة : الشكل ذو الطاقة الأقل ، غالبا ما يكون أحاى الرابطة راديكال ثنائي أكسجين ثلاثي ، والشكل ذو الطاقة الأعلى ، يكون جزيء ثنائي الرابطة أحادى الأكسجين . وهذه الطبيعة للراديكال الثنائي يعزى إليها التغير في الطبيعة الكيميائية .
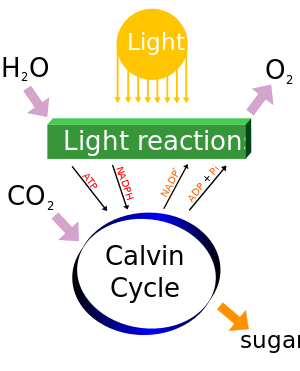
الأكسجين مركب أساسي للهواء ، يتكون من النباتات خلال عمليات البناء الضوئي، وهو مهم للتنفس في الكائنات الحية التى تعتمد على الهواء في تنفسها. الكلمة أكسجين تم إشتقاقها من كلمتين يونانيتين أكسى وتعنى حمض ، جينوماى متسبب . وتك إختيار هذا الإسم نظرا في القرن الثامن عشر نظرا لأنه كان يعتقد أن كل الأحماض تحتوى على أكسجين . تعريف الحمض تم تغيره بعد ذلك إلى أنه لا يجب احتواء الحمض على أكسجين في تركيبه الجزيئى .
الأكسجين السائل والصلب لهما لون أزرق فاتح وكلاهما مغناطيسي مساير (بارا مغناطيسي) قوى . يتم الحصول على الأكسجين السائل غالبا من التقطير الجزئي للهواء المسال . وكل من الأوزون O3 الصلب والسائل له لون أزرق غامق .
تم إكتشاف شكل اخر متأصل للأكسجين وهو الأكسجين الرباعي (O4), وهو مادة صلبة ذات لون أحمر غامق ويتم الحصول عليه بتأثير الضغط على الأكسجين O2 بمقدار 20 GPa . وتم دراسته ليتم إستخدامه في وقود الصواريخ والتطبيقات المشابهه ، وهو مادة مؤكسدة أقوى من O2 أو O3.
إستخداماته
يتم إستخدام الأكسجين بكثرة كمادة مؤكسده ، ولا يوجد عنصر أعلى منه في السالبية الكهربية سوى الفلور . ويتم إستخدام الأكسجين السائل كمادة مؤكسدة في دفع الصواريخ .كما أن الأكسجين أساسي في عمليات التنفس ، ولذا فإن له دور أساسي في الطب . كما أن متسلقى الجبال ومن يقومون بإستخدام الطائرات يكون لديهم إمدادات إضافية من الأكسجين . ويستخدم الأكسجين أيضا في اللحام . وفى صناعة كل من الصلب وميثانول .
الأكسجين من العناصر التى تثير ابهجة ، ولذا فإنه يتم إستخدامه في المنتجعات حتى الأوقات الحديثة . كما يلاحظ وجود أعمدة الأكسجين حتى الأن في الحفلات . في القرن التاسع عشر كان يتم خلطه مع أكسيد النيتروز لعمل نوع من أنوع المسكنات ، ويتم إستخدام نوعية من هذه المسكنات إلى الآن .
تاريخ الأكسجين
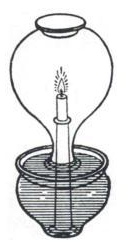
أحد أول التجارب المعروفة عن العلاقة بين الاحتراق والهواء أجراها في القرن الثاني ق.م. الكاتب اليوناني في علم الميكانيكا، فيلو من بيزنطيوم. ففي كتابه Pneumatica, لاحظ فيلو أن قلب وعاء فوق شمعة مشتعلة واحاطة عنق الوعاء بالماء ينتج عنه ارتفاع بعض الماء إلى العنق.[2] وقد أخطأ فيلو في استنتاج أن أجزاء الهواء في الوعاء تحولت إلى العنصر الكلاسيكي نار وبذلك تمكنت من الهروب عبر مسام الزجاج. وبعد عدة قرون لاحقاً، بنى ليوناردو دا ڤنشي على عمل فيلو بملاحظة أن جزءاً من الهواء يـُستهلك أثناء الاحتراق والتنفس.[3]
واكتشف الأكسجين عالم الصيدلة السويدي كارل وليام شيلى تقريبا قبل عام 1773، ولم يتم نشر اكتشافه قبل الاكتشاف المستقل للعالم جوزيف بريستلي في الأول من أغسطس عام 1774 والذي أطلق على الغاز اسم معاكس الفلوجستون (شاهد الفلوجستون. وقام بريستلى بنشر اعماله عام 1775 وشيلى عام 1777، وعادة ما يأخذ بريستلى الاهتمام لأنه قام بالنشر أولا.
و أطلق أنطوان لاڤوازييه على الغاز اسم أوكسجين في عام 1778 م. وكما ذكر أعلاه الاسم مشتق من كلمتين إغريقيتين وهما أوكسى بمعنى حامض الطعم أو مَضِر وجين ومعناها ما يَنتُج عن الشئ (متسسب ) وأيضا ما يُنتِج الشئ (مسبب). وقد اختار لافوازييه هذه الاشتقاق اللغوى نظرا للإعتقاد السائد آنذاك (خاصة بعد اكتشافات بريستلي عام 1775) بأن جميع الأحماض تحتوى على الأكسجين، وقد صحح هذا الإعتقاد بعد عدة إعادات لتعريف المواد الحمضية.
التواجد
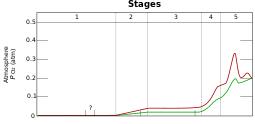
الأكسجين هو ثانى أكبر مكون للغلاف الجوي ( 20.947 % بالحجم ), وهو أكثر العناصر الكيمياوية وفرة في القشرة الأرضية (47% كتلة) وهو يكوّن 89% من كتلة المحيطات، و23% من كتلة الهواء؛ علماً بأن المادة الحية تحوي نحو 65% من الماء، ويتدخل الأكسجين أيضاً في الأوساط البروتينية وفي الشحميات والسكريات. وما الصخور إلا أكسجين اتحد بالسيليسيوم والمعادن (ولاسيما الألمنيوم والحديد والكالسيوم والصوديوم والبوتاسيوم والمغنسيوم).
ذرته
الأكسجين هو العنصر ذو العدد الذري 8= Z الواقع في رأس العمود السادس، وتوافق بنيته الإلكترونية الأساسية التشكيل 1S2, 2S2 , 2P2. وتبلغ طاقات التشارد (التأين) المتتالية فيه ما يأتي: 13.61 إ - ف (إلكترون فلط)؛ 35.1 إ - ف؛ 54.8 إ - ف؛ 114.1 إ - ف؛ 137.8 إ- ف؛ 73704 إ -ف؛ 839.5 إ -ف. ويبلغ نصف قطر الذرة 0.74 ْA (أنغستروم =10-10متر)، ونصف قطر الصاعدة O2- (anion) 1.40 ْA وتساوي الألفة الإلكترونية الموافقة لتكوّن 52- المقدار -7.28 إ - ف، مع أن الأكسجين يأخذ الشكل 52- في عدد من الأكاسيد المعدني المصهورة، وهذا يوافق أيضاً واقع كهرلة electrolysis الألومين Al2O3 المصهور في حوض من الكريوليت NA3AlF6 والفلورين CaF2، وانطلاق الأكسجين عند المصعد نتيجة لتفرُّغ شحنة الشوارد 52- على هذا المصعد.
الجسم البسيط
يتكون الأكسجين في جميع الحالات الفيزيائية من جزيئات صيغتها O2، وبإمكان الذرات أن توجد حرة بفعل الانفراغ الكهربائي أو بفعل إشعاع ما فوق البنفسجي يقل طوله الموجي عن 1900 ْA. وبفعل الدفق الكهربائي تحصل جزيئات صيغتها O3 تُعدُّ أنها تنتمي إلى نوع كيمياوي آخر يدعى الأوزون.
والأكسجين مكوّن مهم للهواء حيث يكون ممزوجاً مع الآزوت، وهو يحضَّر اليوم صناعياً بتسييل الهواء ثم تقطيره تقطيراً تجزيئياً. يغلي الأكسجين في الدرجة -183.0ْس وينصهر في الدرجة -218.9ْس. وهو قليل الانحلال جداً في الماء عندما يكون في حالته الغازية في الشروط العادية من درجة الحرارة والضغط، إلا أن قابلية انحلاله الضعيفة هذه تكفي لإتاحة بعض الظواهر كتنفس الأسماك أو الائتكال المعدني.
يتفاعل الأكسجين مع أغلب الأجسام البسيطة ومع كثير جداً من المركبات، ويحتاج عدد كبير من هذه التفاعلات إلى إزكاء بالتسخين إلى درجة حرارة كافية، وتكون هذه التفاعلات غالباً ناشرة للحرارة، وهي تتتابع بالحفاظ على درجة حرارتها مرتفعة (الاحتراق الشديد). ويأتي الجزء الأعظم من الطاقة، التي تستعملها الصناعة اليوم من الحرارة المنطلقة من احتراق ضروب الوقود الطبيعية (النفط أو الفحم أو الغازات الطبيعية المكونة أساساً من الميتان).
تعطي الأجسام البسيطة باتحادها مع الأكسجين أكاسيد، وتعطي المعادن القلوية مزيجاً من أكسيد وفوق أكسيد. ويُعطي كثير من العناصر عدة أكاسيد. ولتفاعلات أكسدة المعادن أهمية كبيرة، ذلك أنها تَحْدُث بدءاً من درجة الحرارة العادية، ويتيح بطؤها في هذه الدرجة من الحرارة انطلاق الحرارة من دون ارتفاع في درجتها. ويبدأ تأثر الجسم الصلب بالغاز (كما في تأثر قطعة معدنية بأكسجين الهواء) بتَكَوّن منتجات التفاعل على سطح المعدن، وبالفعل يتغطى المعدن (باستثناء الذهب والبلاتين) بطبقة رقيقة من أكسيد عند تعرضه لفعل أكسجين الهواء. وعلى العموم يتوقف التفاعل بسرعة عند تكوّن طبقة متصلة، إلا في المعادن القلوية أو القلوية الترابية التي تكوّن أكسيداً ذا حجم أصغر من حجم المعدن الذي وَلَّدَهُ.
فبوجود بخار الماء وغاز الكربون يتكوّن المنتج السطحي من هدروكسيدات وهدروكسي كربونات هشة قابلة للتفتت، قليلة الالتصاق بالمعدن تتيح تتابع التأثير وتخرب القطعة المعدنية تخرباً بطيئاً (صدأ الحديد، زنجار النحاس)؛ ومن هنا نشأت الفائدة من إلباس بعض المعادن القابلة للتأثر بطبقة مستمرة من معدن آخر يقاوم فعل الجو (رقاقة نيكل).
ويستعمل في عدد من الأكسدات وسيط كالبلاتين مثلاً في التفاعل المستعمل في الصناعة للحصول على حمض الآزوت:
إذ يتحول التيار الغازي من النشادر وأكسجين الهواء بوجود شبكة من البلاتين إلى أحادي أكسيد الآزوت بنسبة لاتقل عن 98%، ثم يتحول أحادي أكسيد الآزوت، بتفاعله مع أكسجين الهواء في الدرجة العادية من الحرارة، إلى ثنائي أكسيد الآزوت NO2 الذي يتحول بوجود الماء إلى حمض الآزوت.
وتتم الأكسدة الصناعية لثنائي أكسيد الكبريت SO2 إلى ثلاثي أكسيد الكبريت بأكسجين الهواء نحو الدرجة 400ْ -450ْس بوجود وسيط أساسه V2O5 ويحصل حمض الكبريت بإماهة ثلاثي الأكسيد. كما تحصل أكسدات صناعية شتى للمنتجات العضوية (البنزن إلى بلا ماء المالئيك مثلاً) باستعمال أكسجين الهواء بوجود وسيط.
ويزداد في الصناعة استعمال الغازات التي يزيد محتواها من الأكسجين على ما يوجد عادة في الهواء، ولا سيما في تنقية purifying حديد الصب.
المركبات
نظرا لأن الأكسجين له كهرسالبية ، فإنه يكون روابط كيميائية مع كل العناصر الأخرى تقريبا ( وكان ذلك أصل كلمة أكسدة ) . العناصر القليلة التى إستطاعت الهروب من الأكسدة هى الغازات النبيلة . وأكثر الأكاسيد شهرة هو ثانى أكسيد الهيدروجين أو الماء H2O). كما أن هناك مركبات أخرى مشهورة تتضمن الكربون والأكسجين مثل ثانى أكسيد الكربون (CO2), الكحولات(R-OH), ألهيد (R-CHO), والأحماض الكربوكسيلية (R-COOH). كما أن الراديكالات المتأكسدة مثل كلورات (ClO3−), بيركلورات (ClO4−), كرومات (CrO42−), ثنائي كرومات (Cr2O72−), برمنجنات (MnO4−), والنيترات (NO3−) عوامل مؤكسدة قوية . وهناك فلزات عديدة مثل الحديد ترتبط مع الأكسجين أكسيد حديد ثلاثي (Fe2O3). أوزون (O3) يتكون بالتفريغ الكهرستاتيكي في وجود الأكسجين الجزيئي . جزيء الأكسجين الثنائي (O2)2 معروف ويتواجد كمكون بسيط في الأكسجين السائل . إيبوكسيد هو إثير تكون ذرة الأكسجين فيه جزء من حلقة ثلاثية الذرات .
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الأكاسيد
هي مركبات العناصر مع الأكسجين. ففي المركبات النموذجية ترتبط جميع ذرات الأكسجين مباشرة بذرات العناصر الأخرى، ولا يرتبط بعضها ببعض. وأحياناً تنسب إلى الأكاسيد المركبات التي تحتوي جزيئاتها على ذرات مرتبطة على التسلسل (فوق الأكاسيد، الأكاسيد العليا والأوزونيدات).
تتكون الأكاسيد النموذجية بأكسدة المركبات البسيطة بالأكسجين مباشرة. ويتم تحضيرها أيضاً بالتحلل الحراري للهدروكسيدات والكربونات والنترات والكبريتات الموافقة، وأملاح الحموض الأكسجينية الأخرى.
ولتسمية الأكاسيد يؤخذ بالحسبان عدد الأكاسيد التي يُكوّنها العنصر الواحد، فإذا كوّن العنصر مع الأكسجين أكسيداً واحداً فقط دُعي أكسيد العنصر كأكسيد الصوديوم Na2O، وأكسيد المغنزيوم MgO، وأكسيد الألمنيوم Al2O3. وإذا كوّن العنصر أكسيدين دُعي الأكسيد الأقل أكسجيناً باسم «أكسيد المعدني» أي بإضافة اللاحقة «ي» إلى اسم المعدن كأكسيد النحاسي Cu2O، ودعي الأكسيد الأكثر أكسجيناً باسم «أكسيد المعدن» كأكسيد النحاس CuO. أما الأكاسيد التي يحتوي جزيؤها على ذرتي أكسجين أو ثلاث أو أكثر من ذلك لكل ذرة معدن فتُدعى ثنائي الأكسيد أو ثلاثي الأكسيد كثنائي أكسيد الآزوت NO2، وثلاثي أكسيد الكروم CrO3 وغيرها. وإذا كوّن العنصر عدة أكاسيد فتدعى في العادة «بلا ماءات الحموض» anhydrides، وهي أكاسيد تتفاعل مع الماء معطية حموضاً. وهكذا مثلاً يكوّن الآزوت الأكاسيد التالية: N2O أكسيد الآزوتي، NO أكسيد الآزوت، N2O3 بلا ماء حمض الآزوتي، NO2 ثنائي أكسيد الآزوت، N2O5 بلا ماء حمض الآزوت، وأحياناً تسمى الأكاسيد وفق ترتيبها المتزايد بأول وثان وثالث ، كأول أكسيد الآزوت N2O، وثاني أكسيد الآزوت NO وغير ذلك.
تقسم الأكاسيد النموذجية وفق سلوكها الكيمياوي إلى النماذج التالية: أكاسيد أساسية basic oxides وأكاسيد حمضية acidic oxides وأكاسيد مذبذبة amphoteric oxides وأكاسيد محايدة neutral oxides.
فالأكاسيد الأساسية هي تلك التي تتفاعل مع الماء مكونة أسساً، وتتفاعل مع الحموض مكونة أملاحاً وماء مثل MgO، وتنحل الأكاسيد الحمضية في الماء مكونة حموضاً. وتتفاعل مع الأسس مكوّنة أملاحاً وماء مثل SO2. وتتفاعل الأكاسيد المذبذبة مع الحموض والأسس مثل ZnO، أما الأكاسيد المحايدة فلا تكوّن أملاحاً مثل CO وNO.
وإذا تتبعنا أكاسيد عناصر الدور الثالث في أعلى درجات أكسدتها: Cl2O7، SO3، P2O5، SiO2، Al2O3، MgO، Na2O3 فإننا نلاحظ تغيراً في الخاصيات الكيمياوية يظهر بوضوح عند الانتقال التدريجي من الأكسيد الأساسي النموذجي (أكسيد الصوديوم) إلى الأكاسيد الحمضية النموذجية ل[[لكبريت والكلور. ويمكن ملاحظة هذا التغير في الأكاسيد المختلفة للعنصر الواحد في درجات أكسدته المختلفة، كما في السلسلة التالية مثلاً: MnO، Mn2O3، MnO2، MnO3، Mn2O7، إذ يلاحظ الانتقال التدريجي من الأكسيد الأساسي للمنجنيز (II) إلى الأكسيد الحمضي للمنغنيز (VII).
يصادف معظم الأكاسيد في الطبيعة إلا أن أكثرها انتشاراً هو أكسيد الهدروجين (الماء) الذي يكوّن الكرة المائية، وتتكون الصخور من ثنائي أكسيد السيليسيوم SiO2، ومن بعض الأكاسيد الطبيعية كأكاسيد الحديد والألمنيوم وغيرهما. وتعد هذه الصخور مصدراً رئيساً لاستحصال المعادن. ويقوم ثنائي أكسيد الكربون CO2 بدور رئيس في الحياة وهو متوافر في الغلاف الجوي بنسبة 0.03%.
تساوي درجة أكسدة الأكسجين في الأكسيد -2، وفي فوق الأكسيد -1 كفوق أكسيد الباريوم BaO2، وفي الأكاسيد العليا -1/2 مثل أكسيد البوتاسيوم KO2، وفي الأوزونيدات -1/3 كأوزونيدات البوتاسيوم KO3.
النظائر


للأكسجين ثلاث نظائر مستقرة و10 نظائر مشعة . وكل النظائر المشعة لها عمر نصف أقل من ثلاث دقائق .
الإحتياطات



الأكسجين يمكن أن يكون سام عند الضغوط الجزيئية المرتفعة. كما ان هناك مشتقات للأكسجين مثل الأوزون (O3) ، الأكسجين الأحادي ، بيروكسيد الهيدروجين ، الجذور الهيدروكسيلية ، الأكاسيد الفائقة سامة للغاية . وقد قام جسم الإنسان بتطوير آلية للحماية من هذه المواد السامة . فمثلا الجلوتاثيون الطبيعي يعمل كمضاد للسموم ، كما يعمل البليروبين وهو مركب طبيعي يعتبر كمادة من الهيموجلبين . التركيزات العالية من الأكسجين تساع على الإشتعال السريع وينتج أخطار النيران والإنفجارات عند تواجد الوقود . وهذا أيضا يري على مركبات الأكسجين مثل الكلورات ، البير كلورات ، الداي كرومات . كما أن المواد التى لها جهد أكسدة عالي تسبب الحروق .
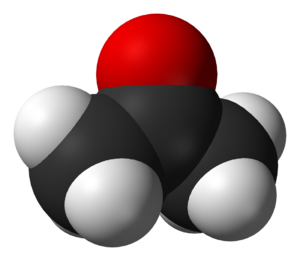
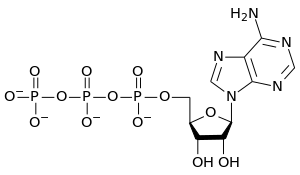
(oxygen is in red, carbon in black and hydrogen in white).
وقد كانت النيران التى قتلت أفراد طاقم أبوللو 1 في تجربة للإطلاق تنتشر بسرعة كبيرة لأن الأكسجين النقي كان في الضغط الجوي العادجي بدلا من ثلث الضغط الذى يستخدم في الإطلاق العادى (شاهد الضغط الجزئي) .
مشتقات الأكسجين تكون جذور حرة بسهولة ، وخاصة اثناء عمليات الأيض . لأنها يمكن أن تسبب ضرر كبير للخلايا والدى إن إيه ، ويقال أنها تسبب السرطان والشيخوخة .
استخداماته
يستخدم الأكسجين التجاري في المعالجة الحرارية للمعادن كلحم المعادن وقطعها وفي التقسية السطحية، وفي التعدين، وفي الطيران، وفي الغواصات المائية وغيرها. ويستعمل الأكسجين في الصناعة الكيمياوية في تحضير الوقود السائل الاصطناعي، وزيوت التشحيم، وحمض الكبريت، وحمض الآزوت، والميتانول، والنشادر، والأسمدة الآزوتية، وفوق أكاسيد المعادن، ونواتج أخرى.
ويستعمل الأكسجين السائل في الأعمال التفجيرية، وفي المحركات النفاثة، وفي الأعمال المختبرية. كذلك يستعمل الأكسجين الصرف المعبأ في أسطوانات للتنفس على ارتفاع عال في الطيران الفضائي وفي السباحة تحت الماء، وفي الإنعاش والإسعاف.[4]
انظر أيضا


- تجربة وينكلر للأكسجين المذاب للتعليمات حول تحديد كمية الأكسجين المذابة في الماء النقي .
- الإشتعال
- الأكسدة
- دور الأكسجين كغاز تنفس أثناء الغوص .
- إستنزاف الأكسجين في البيئة المائية .
- طبقة الأوزون
- مركبات أكسجين
- Oxygen sensor
وصلات خارجية
- Los Alamos National Laboratory - Oxygen
- Oxidizing Agents > Oxygen
- Oxygen (O2) Properties, Uses, Applications
- Roald Hoffmann article on "The Story of O"
- WebElements.com - Oxygen
- مجتمع بريستلى ، مهدى إلى جوزيف بريستلى ، الرجل الذى قام بإكتشاف الأكسجين
- موقع لمعلومات عن جوزيف بريستلى ، الرجل الذى إكتشف الأكسجين
- معمل لوس ألاموس القومي - أكسجين
- العناصر على الشبكة - الأكسجين
- الأكسجين أساسي
- سمية الأكسجين
- خواص وإستخدامات الأكسجين (O2)
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
المراجع
- معمل لوس ألاموس القومي - أكسجين
- قاعدة بيانات نيست للطيف
- النظائر والنوكليدات الطبعة الرابعة عشر ، تمثيل النوكليدات ، شركة جنرال إليكتريك ، 1989
المصادر
- تم ترجمة الصفحة من صفحة ويكيبيديا الإنجليزية.
- Agostini, D.; H. Iida, and A. Takahashi (1995). "Positron emission tomography with oxygen-15 of stunned myocardium caused by coronary artery vasospasm after recovery". British Heart Journal 73 (1): 69–72. doi:. PMID 7888266. http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=483759. Retrieved on 2007-12-16.
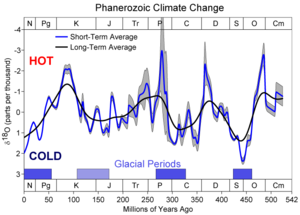
- Berner, Robert A. (1999-09-18). "Atmospheric oxygen over Phanerozoic time". Proceedings of the National Academy of Sciences of the USA 96 (20): 10955–57. doi:. PMID 10500106. http://www.pnas.org/cgi/content/full/96/20/10955. Retrieved on 2007-12-16.
- Britannica contributors (1911). "John Mayow". Encyclopaedia Britannica (11th edition ed.). Retrieved 2007-12-16.
{{cite book}}:|author=has generic name (help);|edition=has extra text (help) - Brown, Theodore L.; LeMay, Burslen (2003). Chemistry: The Central Science. Prentice Hall/Pearson Education, 958. ISBN 0130484504.
- Cacace, Fulvio; Giulia de Petris, and Anna Troiani (October 2001). "Experimental Detection of Tetraoxygen". Angewandte Chemie International Edition 40 (21): 4062–65. doi:.
- Campbell, Neil A. (2005). Biology, 7th Edition. San Francisco: Pearson - Benjamin Cummings. pp. 522–23. ISBN 0-8053-7171-0.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - Chiles, James R. (2001). Inviting Disaster: Lessons from the edge of Technology: An inside look at catastrophes and why they happen. New York: HarperCollins Publishers Inc. ISBN 0-06-662082-1.
- Cook, Gerhard A. (1968). "Oxygen". In Clifford A. Hampel (ed.). The Encyclopedia of the Chemical Elements. New York: Reinhold Book Corporation. pp. 499–512. LCCN 68-29938.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - Crabtree, R. (2001). The Organometallic Chemistry of the Transition Metals, 3rd edition, John Wiley & Sons, 152. ISBN 978-0471184232.
- Daintith, John (1994). Biographical Encyclopedia of Scientists. CRC Press. ISBN 0750302879.
- Desgreniers, S; Vohra, Y. K. & Ruoff, A. L. (1990). "Optical response of very high density solid oxygen to 132 GPa". J. Phys. Chem. 94: 1117–22. doi:.
- Dole, Malcolm (1965). "The Natural History of Oxygen" (PDF). The Journal of General Physiology 49: 5–27. doi:. PMID 5859927. http://www.jgp.org/cgi/reprint/49/1/5.pdf. Retrieved on 2007-12-16.
- Donald, Kenneth (1992). Oxygen and the Diver. England: SPA in conjunction with K. Donald. ISBN 1854211765.
- Emsley, John (2001). "Oxygen". Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, England, UK: Oxford University Press. pp. 297–304. ISBN 0198503407.
- Evans, David Hudson (2006). The Physiology of Fishes. CRC Press. p. 88. ISBN 0849320224.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - Fenical, William (September 1983). "Marine Plants: A Unique and Unexplored Resource", Plants: the potentials for extracting protein, medicines, and other useful chemicals (workshop proceedings). DIANE Publishing, 147. ISBN 1428923977.
- Freeman, Scott (2005). Biological Science, 2nd Edition. Upper Saddle River, NJ: Pearson - Prentice Hall. pp. 214, 586. ISBN 0-13-140941-7.
{{cite book}}: Cite has empty unknown parameter:|coauthors=(help) - Greenwood, N. N. (1997). Chemistry of the Elements (2nd Edition ed.). Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
{{cite book}}:|edition=has extra text (help); Unknown parameter|coauthors=ignored (|author=suggested) (help) - Harrison, Roy M. (1990). Pollution: Causes, Effects & Control (2nd Edition ed.). Cambridge: Royal Society of Chemistry. ISBN 0-85186-283-7.
{{cite book}}:|edition=has extra text (help) - Hirayama, Osamu; Kyoko Nakamura, Syoko Hamada and Yoko Kobayasi (1994-02-). "Singlet oxygen quenching ability of naturally occurring carotenoids". Lipids (Springer Berlin / Heidelberg) 29 (2): 149–50. doi:. http://www.springerlink.com/content/d67361221v12082m/. Retrieved on 2007-12-15.
- How Products are Made contributors (2002). "Oxygen", How Products are Made. The Gale Group, Inc. Retrieved on 2007-12-16.
- Jastrow, Joseph (1936). Story of Human Error. Ayer Publishing. p. 171. ISBN 0836905687. Retrieved 2007-12-16.
- Krieger-Liszkay*, Anja (2005). "Singlet oxygen production in photosynthesis". Journal of Experimental Botanics (Oxford Journals) 56: 337–46. doi:. PMID 15310815. http://jxb.oxfordjournals.org/cgi/content/full/56/411/337. Retrieved on 2007-12-16.
- Lide, David R. (2003). "Section 4, Properties of the Elements and Inorganic Compounds; Melting, boiling, and critical temperatures of the elements". CRC Handbook of Chemistry and Physics (84th Edition ed.). Boca Raton, Florida: CRC Press.
{{cite book}}:|edition=has extra text (help) - Lundegaard, Lars F.; Weck, Gunnar; McMahon, Malcolm I.; Desgreniers, Serge and Loubeyre, Paul (2006). "Observation of an O8 molecular lattice in the phase of solid oxygen". Nature 443: 201–04. doi:. http://www.nature.com/nature/journal/v443/n7108/abs/nature05174.html. Retrieved on 2008-01-10.
- Maksyutenko, P. (2006). "A direct measurement of the dissociation energy of water". J. Chem. Phys. 443: 125. doi:10.1063/1.2387163.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - Meyer, B.S. (September 19–21, 2005). "Nucleosynthesis and Galactic Chemical Evolution of the Isotopes of Oxygen" (PDF) in Workgroup on Oxygen in the Earliest Solar System. Proceedings of the NASA Cosmochemistry Program and the Lunar and Planetary Institute. 9022. Retrieved on 2007-01-22.
- Miller, J.R.; Berger, M.; Alonso, L.; Cerovic, Z.; Goulas, Y.; Jacquemoud, S.; Louis, J.; Mohammed, G.; Moya, I.; Pedros, R.; Moreno, J.F.; Verhoef, W.; Zarco-Tejada, P.J.. "Progress on the development of an integrated canopy fluorescence model". Geoscience and Remote Sensing Symposium, 2003. IGARSS '03. Proceedings. 2003 IEEE International. Retrieved on 2008-01-22.
- Morris, Richard (2003). The last sorcerers: The path from alchemy to the periodic table (Hardback). Washington, D.C.: Joseph Henry Press. ISBN 0309089050.
{{cite book}}:|format=requires|url=(help) - Parks, G. D.; Mellor, J. W. (1939). Mellor's Modern Inorganic Chemistry, 6th edition, London: Longmans, Green and Co.
- Priestley, Joseph (1775). "An Account of Further Discoveries in Air". Philosophical Transactions. 65: 384–94. doi:10.1098/rstl.1775.0039. Retrieved 2007-12-16.
- Raven, Peter H.; Ray F. Evert, Susan E. Eichhorn (2005). Biology of Plants, 7th Edition. New York: W.H. Freeman and Company Publishers, 115–27. ISBN 0-7167-1007-2.
- Roscoe, Henry Enfield (1883). A Treatise on Chemistry. D. Appleton and Co. p. 38.
{{cite book}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - Shimizu, K.; Suhara, K., Ikumo, M., Eremets, M. I. & Amaya, K. (1998). "Superconductivity in oxygen". Nature 393: 767–69. doi:.
- Smart, Lesley E. (2005). Solid State Chemistry: An Introduction, 3, CRC Press, 214. ISBN 978-0748775163.
- Stwertka, Albert (1998). Guide to the Elements (Revised Edition ed.). Oxford University Press. ISBN 0-19-508083-1.
{{cite book}}:|edition=has extra text (help) - Walker, J. (1980). "The oxygen cycle". In Hutzinger O. (ed.). Handbook of Environmental Chemistry. Volume 1. Part A: The natural environment and the biogeochemical cycles. Berlin; Heidelberg; New York: Springer-Verlag. p. 258. ISBN 0387096884.
- Wentworth Jr., Paul; Jonathan E. McDunn, Anita D. Wentworth, Cindy Takeuchi, Jorge Nieva, Teresa Jones, Cristina Bautista, Julie M. Ruedi, Abel Gutierrez, Kim D. Janda, Bernard M. Babior, Albert Eschenmoser, Richard A. Lerner (2002-12-13). "Evidence for Antibody-Catalyzed Ozone Formation in Bacterial Killing and Inflammation". Science 298 (5601): 2195–219. doi:. PMID 12434011.
- Werley, Barry L. (Edtr.) (1991). "Fire Hazards in Oxygen Systems". ASTM Technical Professional training, Philadelphia: ASTM International Subcommittee G-4.05.
- World of Chemistry contributors (2005). "John Mayow". World of Chemistry. Thomson Gale. Retrieved 2007-12-16.
{{cite book}}:|author=has generic name (help)
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. pp. E110. ISBN 0-8493-0464-4.
- ^ Jastrow, Joseph (1936). Story of Human Error. Ayer Publishing. p. 171. ISBN 0836905687.
- ^ Cook & Lauer 1968, p.499.
- ^ رياض حجازي. "الأكسجين". الموسوعة العربية.