كادميوم
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المظهر | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
رمادي فضي لامع
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الخصائص العامة | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الاسم، الرمز، الرقم | كادميوم, Cd, 48 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| النطق | /ˈkædmiəm/ KAD-mee-əm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| تصنيف العنصر | فلز انتقالي | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ملاحظات التصنيف | وأحياناً يُعتبر فلز بعد انتقالي | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المجموعة، الدورة، المستوى الفرعي | 12, 5, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الوزن الذري القياسي | 112.411 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| التوزيع الإلكتروني | [Kr] 5s2 4d10 2, 8, 18, 18, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الخصائص الطبيعية | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الطور | صلب | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الكثافة (بالقرب من د.ح.غ.) | 8.65 g·cm−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الكثافة السائلة عند ن.إ. | 7.996 گ·سم−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة الانصهار | 594.22 ك, 321.07 °C, 609.93 °F | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نقطة الغليان | 1040 ك, 767 °س, 1413 °ف | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارة الانصهار | 6.21 كج·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حرارة التبخر | 99.87 كج·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| السعة الحرارية المولية | 26.020 ج·مول−1·ك−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ضغط البخار | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الخصائص الذرية | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| حالات الأكسدة | 2, 1 (أكسيد قاعدي باعتدال) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سالبية كهربية | 1.69 (مقياس پولنگ) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| طاقات التأين | الأولى: 867.8 كج·مول−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الثانية: 1631.4 كج·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الثالثة: 3616 كج·مول−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نصف القطر الذري | 151 پم | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر تساهمي | 144±9 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نصف قطر ڤان در ڤالز | 158 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| متفرقات | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| البنية البلورية | hexagonal | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| الترتيب المغناطيسي | diamagnetic[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المقاومية الكهربائية | (22 °س) 72.7 nΩ·m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ناقلية حرارية | 96.6 W·m−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| التمدد الحراري | (25 °س) 30.8 µm·م−1·ك−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| سرعة الصوت (قضيب رفيع) | (20 °س) 2310 م·ث−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| معامل ينگ | 50 گپا | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| معامل القص | 19 گپا | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| معامل الحجم | 42 گپا | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| نسبة پواسون | 0.30 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| صلادة موس | 2.0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| صلادة برينل | 203 مپا | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| رقم تسجيل كاس | 7440-43-9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| أكثر النظائر استقراراً | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| المقالة الرئيسية: نظائر كادميوم | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
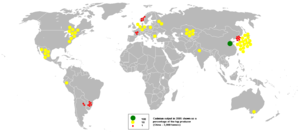
الكَدْمُيوم Cadmium، عنصر كيميائي وفلز ناعم يتراوح لونه بين الفضي والأبيض، يُستعمل في الطلاء وصنع السبائك، والرمز الكيميائي للكدميوم هو Cd. والطبقة الإلكترونية ما قبل الخارجية في ذرته شبه مشبعة (18 إلكتروناً) في حين تحوي الطبقة الخارجية إلكترونين s مع إشباع المدارات الداخلية d، ويوجد في الفصيلةII Bّّ (أو 2 ا) تحت الزنك في الجدول الدوري. ويوجد في كل عشرة ملايين جزء من القشرة الأرضية حوالي خمسة أجزاء من الكدميوم فقط. والكَدْمُيوم شبيه بعنصر الزنك. وهو يوجد مع معادن الزنك، ويمكن الحصول عليه بوصفه منتجاً جانبياً عند تكرير الزنك. واليابان هي المنتج الأول للكدميوم في العالم.
يشبه الكَدْمُيوم في سلوكه الكيمياوي عناصر المعادن القلوية الترابية: القلويات الترابية (العناصر ومركباتها) وخاصة المغنـزيوم Mg [ر]، فدرجة أكسدته +2، ولا يأخذ درجة أكسدة أعلى من ذلك بسبب ارتفاع كمون التأين الثالث اللازم لإبعاد إلكترون d، كما أن أكسيده صعب الانحلال في الماء، ويشكل الكدميوم أملاحاً كثيرة تشبه أملاح المغنـزيوم من حيث البنية البلورية والتركيب، كما يشكل مركبات ألكيلية مماثلة للمركبات التي يشكلها المغنـزيوم. وفعاليته أضعف، كما هو متوقع، من المعادن القلوية الترابية إذ إن نصف قطره أصغر وشحنة نواته أكبر.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الاستخدامات
البطاريات
تستخدم بطاريات النيكل-كدميوم وبطاريات الفضة-كادميوم، التي يمكن إعادة شحنها في الساعات والآلات الحاسبة، والعديد من المعدات الصغيرة.
استخدامات أخرى
تَستعمل الصناعاتُ الكدميوم في صنع السبائك ذات العائد السريع، ويستعمل كذلك غطاءً واقيا للفلزات الأخرى. وكثيراً مايستعمل الكدميوم بدلاً من الزنك في جلفنة الحديد والفولاذ (طليها بغطاء رقيق للحماية). ويوفر حماية طويلة المدى، ولكنها أقل نجاعة مما يوفره الزنك، إلا أنه يحتفظ بألوان أكثر إشراقاً لمدة أطول. وتستعمل قضبان الكادميوم في المفاعلات النووية للتحكم في التفاعلات النووية. لميله الكبير إلى التفاعل مع النيوترونات، إذ تستخدم قضبانه لتنظيم سير التفاعل النووي المتسلسل. كما يدخل في تركيب العديد من السبائك. وتزيد إضافة الكدميوم إلى النحاس من متانة النحاس مع المحافظة على ناقليته الكهربائية العالية، فيستخدم في صناعة الأسلاك الكهربائية التي تتعرض للاحتكاك المستمر، كما أن إضافته إلى سبيكة القصدير والرصاص المستعملة في صنع أحرف الطباعة تزيد من أمد استعمال هذه الأحرف. وتستعمل بعض مركبات الكادميوم، خاصة منها الكبريتيد، لصنع أصبغة معدنية.
الخصائص
العدد الذري للكدميوم 48، ووزنه الذري 112,41 وكثافته 8,65 جم/سم§ عند 20°م وينصهر الكادميوم عند 320,9°م، ويغلي عند 765°م. كتلته الحجمية 8.64غ/سم3، نصف قطره 1.56 أنگستروم، طاقة التبخر عند الدرجة 25 س تساوي 26.97 كيلو حريرة/مول. كمون التأين الأول (إلكترون فلط) 8.99، الثاني 16.905، الكمون النظامي (التحول إلى Cd2+) يساوي -0.403 فلط.
التاريخ
وقد اكتشف الكادميوم الألماني فريدريش شتروماير Friedrich Stromeyer عام 1817. إذ حصل على ثلاثة گرامات منه بإجراء عمليات كيمياوية معقدة على فلز كبريتيد الزنك المشوب بكبريتيد الكادميوم.
يختلف الكَدْمُيوم عن المعادن القلوية الترابية بصعوبة انحلال كبريتيده CdS، وبكون أكسيده ذا خواص أساسية أضعف، وبميله إلى تشكيل معقدات complexes خاصة معقدات نشادرية وسيانيدية. درجة انصهاره 320.9 ْ س ودرجة غليانه 767 ْ س منخفضتان ويعزى ذلك إلى بنيته الإلكترونية ((18+2) إلكتروناً) التي لا تساعد على تكوين رابطة معدن-معدن في الحالة الحرة.
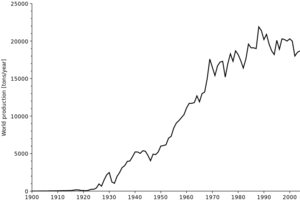
التواجد
يشكل الكدميوم 5 ×10-4 من القشرة الأرضية وزناً. وهو يرافق الزنك في البلند ZnS [ر. الزنك] بشكل كبريتيد الكدميوم لتشابههما الكبير. ويحصل عليه من هذا الفلز ناتجاً ثانوياً إذ يتقطّر قبل الزنك (درجة غليان الزنك 906 ْ س). يكون الكدميوم الحاصل على شكل بخار، يكثف فيما بعد وينقى بالتقطير. وبتنقية محلول كبريتات الزنك (الذي سيحلّل كهربائياً فيما بعد) يكون الكدميوم على شكل كبريتات ويرسَّب من المحلول بإضافة مسحوق الزنك إليه:
CdSO4 + Zn ZnSO4 +Cd
يذاب الكدميوم المرسب في حمض الكبريت H2SO4 ويحلّل كهربائياً بالطريقة السابقة نفسها، وتبلغ نقاوته 99.99%. وهو معدن لين يمكن قطعه وطرقه وسحبه بسهولة، بنيته الإلكترونية [Kr] 4d10 5s2 حيث [Kr] تدل على البنية الإلكترونية للغاز الخامل الكربتون.
الاستخراج
الدور الحيوي

والكدميوم سام، وقد أصيب العديد من الناس بالمرض إصابة حادة، أو تُوفوا مباشرة بعد أن استنشقوا غبار الكدميوم أو أبخرة أكسيد الكدميوم. وإذا دخلت كميات صغيرة من الكدميوم جسم الإنسان على فترات طويلة، فقد تسبب الأذى للكلى أيضًا وتشوه العظام. ويخشى بعض الناس أن تكون كميات سامة من الكدميوم قد لوثت البيئة نتيجة الاستعمال الصناعي للكدميوم على نطاق واسع.
خواصه الكيمياوية
يشبه الكدميوم الزنكَ في خواصه الكيمياوية، فهو لا يتأثر بالأكسجين أو الهواء الجاف في الدرجة العادية من الحرارة. إلا أنه بالتسخين يحترق الكدميوم مكوِّناً CdO البني اللون. وهو يتفاعل مع الكبريت بشدة إلا أنه يلزم التسخين لبدء التفاعل. أما مع الماء فهو لا يفكِّك الماء مع أنه أشد كهرجابية من الهدروجين، والمرجح أنه يحدث بدء تفاعل يؤدي إلى تكوّن طبقة عازلة من الأكسيد تمنع استمرار التفاعل:
Cd + H2O CdO + H2
إلا أنه يتفاعل مع الحموض مطلقا ًالهدروجين، خاصة مع حمض الكبريت وحمض كلور الماء، وينحل في حمض الآزوت الذي يتفاعل معه كمؤكسِد. أكسيد الكدميوم البني اللون ذو خواص أساسية واضحة فهو لا ينحل إلا في الحموض مكوناً أملاح الشاردة Cd2+. يحصل على الهدروكسيد Cd(OH)2 بإضافة هدروكسيد قلوي إلى محلول أحد أملاح الكدميوم، فيترسب بشكل كتلة هلامية بيضاء. وهو يتميز، كالأكسيد الموافق، بصفات أساسية فقط. ويشكِّل مع النشادر مركباً معقداً ذواباً في الماء:
Cd(OH)2 + 4NH4 OH [Cd(NH3)4] (OH)2 + 4H2O
محاليل أملاح الكدميوم لا لون لها. الكبريتات والنترات جيدة الانحلال في الماء. أما أملاح الحموض اللاعضوية الضعيفة فصعبة الانحلال. إن أملاح هاليدات الشاردة Cd2+ ذات درجة تأين ضعيفة، بخلاف نترات وكبريتات الكدميوم التي تكاد تكون كاملة التأين في المحاليل. للكدميوم العديد من المعقدات[ر: المعقَّد] مثل K2[CdCl4] وK2[(Cd(CN)4]. تستحضر ألكيلات الكدميوم CdR2 بتفاعل CdBr2 بروميد الكدميوم مع كواشف غرينيار مثل CH3MgBr في الإيتر، ومركبات الأريل بتفاعل CdBr2 مع أريلات الليثيوم في المحل نفسه. وثنائي ألكيلات الكدميوم أقل تطايراً وأقل فعالية من مركبات الزنك المماثلة.
السمية
 مقالة مفصلة: تسمم الكادميوم
مقالة مفصلة: تسمم الكادميوم
يوجد معدن الكادميوم في قشرة الأرض، ودائماً ما يتواجد مع الزنك. لا يمكن تجنبه في الصناعة كمنتج ثانوى حتمى من مستخلصات الزنك والرصاص والنحاس. وقبل استخدامه في الصناعة، فقد دخل البيئة بشكل أساسى من خلال التربة لأنه تم اكتشافه في المبيدات الحشرية والسماد.
ودخول معدن الكادميوم لجسم الإنسان يكون من خلال الأطعمة، والأطعمة الغنية به تزيد من تركيزه في جسم الإنسان ومن أمثلة هذه الأطعمة الكبد، عش الغراب (المشرووم)، المحار، الكاكاو، الطحالب البحرية الجافة، بلح البحر.
يتعرض الشخص لمعدلات الكادميوم العالية من التدخين. فتدخين التبغ ينقل تأثير الكادميوم للرئة ومن ثَّم يقوم الدم بنقله لباقى أعضاء الجسم بتأثيراته السامة.
والضرر يأتى أيضاً من خلال حياة الإنسان بجوار أماكن النفايات المحتوية عليه أو بالقرب من المصانع التى تطلق الكادميوم فث الهواء، أو الأشخاص التى تعمل في مجال صناعة التعدين. عندما يتنفس الشخص كميات كبيرة من الكادميوم فهذا يعمل على تدمير الرئتين بشكل حاد يؤدى إلى وفاة الإنسان فيما بعد. ينتقل معدن الكادميوم أولاً إلى الكبد من خلال الدم، وهناك يتحد مع البروتينات ليكون مركبات معقدة تنتقل بدورها للكلى. يتراكم معدن الكادميوم في الكلى حيث يدمر وظائفها ويسبب خروج البروتينات الأساسية والسكريات من الجسم ومزيد من التلف في أنسجة الكلى ويستغرق هذا مدة طويلة من الزمن ليحدث كل هذا الضمور في الكلى.
ومن الآثار السلبية على الصحة والمتسبب فيها معدن الكادميوم[2]:
- الإسهال
- آلام المعدة
- القىء الحاد
- كسور العظام
- اضطرابات في الجهاز التناسلى وفى بعض الأحيان حدوث العقم
- ضمور في الجهاز العصبى المركزى
- ضمور في وظائف الجهاز المناعي بالجسم
- اضطرابات نفسية
- احتمالية الإصابة بضمور في الصفات الوراثية، أو الإصابة بمرض السرطان
- إصابة الإنسان بالتسمم الغذائى من معدن الكادميوم يكون نادراً ويحدث بشكل أكبر من تلوث البيئة، أو الاستهلاك المزمن للأطعمة العالية بنسبة الكادميوم فيها
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
انظر أيضاً
المصادر
- ^ Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ المعادن الثقيلة.. سموم بيئية، فيدو
- http://www.arab-ency.com/index.php?module=pnEncyclopedia&func=display_term&id=7569&vid=40 الموسوعة العربية]
- [1]
غدير زيزفون. "كادميوم". الموسوعة العربية.
وصلات خارجية
- ATSDR Case Studies in Environmental Medicine: Cadmium Toxicity U.S. Department of Health and Human Services
- Agency for Toxic Substances and Disease Registry’s (ATSDR) Toxicological Profile for Cadmium
- European Union Risk Assessment Reports on Cadmium Metal and Cadmium Oxide
- IARC Monograph "Cadmium and Cadmium Compounds"
- National Pollutant Inventory - Cadmium and compounds
- Cadmium exposure pathfinder
- WebElements.com - Cadmium
- Warning Moose and Deer Liver
- National Institute for Occupational Safety and Health - Cadmium Page
- NLM Hazardous Substances Databank – Cadmium, Elemental
| الجدول الدوري | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Uub | Uut | Uuq | Uup | Uuh | Uus | Uuo | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||