التهاب اللفافة الناخر
| التهاب اللفافة الناخر | |
|---|---|
| الأسماء الأخرى | البكتريا الآكلة للحم، متلازمة البكتريا الآكلة للحم،[1] عدوى الأنسجة الرخوة الناخر، (NSTI)،[2] fasciitis necroticans |
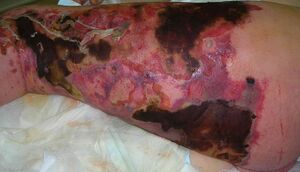 | |
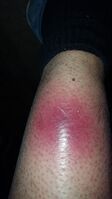
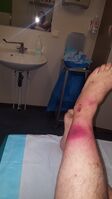
| شخص مصاب بالتهاب اللفافة الناخر. يظهر على الساق اليسرى احمرارًا شديدًا وموت الأنسجة. | |
| النطق | |
| التخصص | الأمراض المعدية |
| الأعراض | ألم مبرح، الحمى، تحول البشرة في المنطقة المصابة للون القرمزي[3] |
| البداية المعتادة | مفاجيء، سريع الانتشار[3] |
| المسببات | أنواع مختلفة من البكتريا،[4] فطر عرضي[5] |
| عوامل الخطر | ضعف المناعة، مثل الناتج عن مرض السكري أو السرطان، البدانة، إدمان الكحول، تعاطي المخدرات عن طريق الوريد، مرض الشريان المحيطي[2][3] |
| الطريقة التشخيصية | حسب الأعراض، التصوير الطبي[4] |
| التشخيص المفاضل | Cellulitis, pyomyositis, gas gangrene[6] |
| الوقاية | العناية بالجروح، غسيل اليدين[3] |
| العلاج | الجراحة لإزالة الجزء المصاب، المضادات الحيوية في الوريد [2][3] |
| Prognosis | ~30% وفيات[2] |
| التردد | 0.7 لكل 100.000 سنوياً[4] |
التهاب اللفافة الناخر (إنگليزية: Necrotizing fasciitis، اختصاراً، NF)، يُعرف أيضاً باسم المرض الآكل للحم (إنگليزية: flesh-eating disease)، هي عدوى تتسبب في موت مفاجيء للأنسجة الرخوة في الجسم.[3] وهو مرض خدير حيث يظهر فجأة وينتشر بسرعة.[3] عادة ما تتضمن الأعراض تحول الجلد في المنطقة المصابة للون الأحمر أو القرمزي، الألم الشديد، الحمى، والقيء.[3] المناطق الأكثر إصابة هي الأطراف والعجان.[2]
عادة، تدخل العدوى الجسم من خلال شق في الجلد مثل الجرح أو الحرق.[3] تشمل عوامل الخطر ضعف المناعة مثل مرض السكري أو السرطان، البدانة، إدمان الكحول، تعاطي المخدرات عن طريق الحقن، ومرض الشريان المحيطي.[2][3] لا ينتشر المرض عادة بين الأشخاص.[3] يصنف المرض إلى أربعة أنواع ، اعتمادًا على العضية المسببة للمرض.[4] ما بين 55 و80% من الحالات تنطوي على أكثر من نوع واحد من البكتيريا.[4] مكورات عنقودية ذهبية مقاومة للمثيسيلين (MRSA) تشارك في ما يصل إلى ثلث الحالات.[4] غالبًا ما يكون التصوير الطبي مفيدًا لتأكيد التشخيص.[4]
يمكن منع التهاب اللفافة الناخر من خلال العناية بالجروح وغسل اليدين.[3] عادة ما يتم علاجه بإجراء جراحة لإزالة الأنسجة المصابة والمضادات الحيوية عن طريق الوريد.[2][3] في كثير من الأحيان، تستخدم مجموعة من المضادات الحيوية، مثل پنسيلين جي وكليندامايسين وڤانكومايسين وجنتاميسين.[2] يؤدي التأخر في إجراء الجراحة لزيادة خطر الوفاة.[4] على الرغم من الأدوية المتقدمة، إلا أن خطر الوفاة يتراوح بين 25 و35%.[2]
يحدث التهاب اللفافة الناخر لحوالي 0.4 شخص لكل 100000 سنويًا في الولايات المتحدة، وحوالي 1 لكل 100000 في غرب أوروپ. [4] يتأثر كلا الجنسين بنسبة متساوية.[2] يصبح أكثر شيوعًا بين كبار السن ونادرًا عند الأطفال.[4] وُصف المرض على الأقل منذ زمن أبوقراط.[2] استخدم مصطلح "necrotizing fasciitis" لأول مرة عام 1952.[4][7]
الأعراض والعلامات
قد تشمل الأعراض الحمى والتورم والشكاوى من الألم المفرط. تشبه التغيرات الأولية للجلد التهاب النسيج الخلوي أو الخراج، مما يجعل التشخيص في المراحل المبكرة صعبًا. يحدث تصلب الجلد والأنسجة الرخوة والتورم خارج منطقة الإصابة بشكل شائع عند الأشخاص الذين يعانون من تغيرات نخرية مبكرة.[2] عادة ما يندمج الاحمرار والتورم مع الأنسجة الطبيعية المحيطة. قد يبدو الجلد المصاب لامعاً ومتشنجاً.[8] العلامات الأخرى الأكثر إيحاءاً بالتغيرات النخرية (ولكنها موجودة في مراحل لاحقة في 7 إلى 44٪ من الحالات) هي: تكون الفقاعات، النزيف تحت الجلد والذي يكون موجوداً قبل نخر الجلد[2] (يتحول الجلد للون الأحمر أو القرمزي والأسود بسبب تجلط الأوعية الدموية)،[8] تواجد الغازات في الأنسجة، انخفاض أو انعدام الإحساس في الجلد[2] (بسبب نخر الأعصاب الكامنة).[8] تطور المرض سريعاً إلى صدمة على الرغم من العلاج بالمضادات الحيوية هو مؤشر آخر على التهاب اللفافة الناخر. يُعرف التهاب اللفافة الناخر الذي يصيب الفخذ باسم غرغرينا فورنييه.[2]
ومع ذلك، فإن الأشخاص الذين يعانون من نقص المناعة (يعانون من السرطان، أو استخدام الكورتيكوستيرويد، أو العلاج الإشعاعي، أو العلاج الكيميائي، أو ڤيروس نقص المناعة البشرية/الإيدز، أو أجروا زرع أعضاء أو نخاع9 قد لا تظهر عليهم الأعراض النموذجية. الأشخاص الذين يعانون من نقص المناعة لديهم أيضًا خطر مضاعف للوفاة من الالتهابات الناخرة، لذلك يجب ملاحظة هذه المجموعة بشكل أكبر.[2]
-
الأعراض المبكرة للاتهاب اللفافة الناخر. تبدو المنطقة الوسطى داكنة بشكل أكبر أو مائلة للون الأحمر (القرمزي).
-
الأعراض المبكرة للالتهاب اللفافة الناخر. المنطقة الوسطى تحولت للون الأسود.
-
التهاب اللفافة الناخر من النوع الثالث ناتج عن الإصابة ببكتريا الضمة الجارحة.
الأسباب
عوامل الخطر
يتم تسجيل أكثر من 70٪ من الحالات لدى الأشخاص الذين يعانون من واحدة على الأقل من هذه الحالات السريرية: كبت المناعة، السكري، إدمان الكحول/تعاطي المخدرات/التدخين، الأورام الخبيثة، الأمراض الجهازية المزمنة. لأسباب غير واضحة، يحدث أحيانًا عند الأشخاص الذين يعانون من حالة عامة تبدو طبيعية.[9]
قد يحدث التهاب اللفافة الناخر في أي جزء من الجسم، ولكنه أكثر شيوعًا في الأطراف، العجان والأعضاء التناسلية. ينشأ عدد قليل فقط من هذه الحالات من الصدر والبطن. الصدمة هي السبب المعتاد للعدوى، مثل الحقن بالأدوية عن طريق الوريد، أو حقن الأنسولين، أو لدغات الحيوانات والحشرات، أو إدخال القسطرة، أو الناسور الذي يربط الجلد بأعضاء الجسم الداخلية. يمكن أن تؤدي التهابات الجلد مثل الخراج والقرح أيضًا إلى تعقيد التهاب اللفافة الناخر. تم اقتراح انتشار العدوى عن طريق الدم لأولئك المصابين بالتهاب البلعوم العقدي. بالنسبة لعدوى العجان والأعضاء التناسلية (غرغرينا فورنييه، فإن الصدمات وعدوى المسالك البولية والحصوات وغدة بارثولين هي الأسباب المعتادة.[2]
يمكن تقليل خطر الإصابة بالتهاب اللفافة الناخر من الجرح عن طريق العناية الجيدة بالجروح وغسل اليدين.[3]
البكتريا
يمكن تقسيم أنواع عدوى الأنسجة الرخوة إلى أربع فئات وفقًا لأنواع البكتيريا التي تصيب الأنسجة الرخوة. وصف نظام التصنيف هذا لأول مرة من قبل جوليانو وزملائه عام 1977.[4][2]
عدوى النوع الأول: هذا هو النوع الأكثر شيوعًا من العدوى، ويمثل 70 إلى 80٪ من الحالات. ينتج عن مزيج من أنواع البكتيري ، عادة في مناطق البطن أو الفخذ.[4] عادة ما يحدث هذا النوع من العدوى بسبب أنواع مختلفة من البكتريا الموجبة الجرام مثل المكورات العنقودية الذهبية، المكورات العقدية المقيحة، والمكورة المعوية، والبكتريا سالبة الجرام مثل الإشريشيا المعوية، عصيات القيح الأزرق، والعضيات اللاهوئية (جنس العصوانية والمطثية).[4] عادة ما يكون الأفراد المصابون من كبار السن مع أمراض مصاحبة مثل داء السكري والبادنة ونقص المناعة.[4] عادة، لا تكون الصدمة سبباً لمثل هذه العدوى. قد يستنبط التاريخ السابق لعدوى الخراريج أو انثقاب الأمعاء مع الانتقال البكتيري. تمثل عدوى المطثية 10٪ من عدوى النوع الأول. أنواع "المطثية" المعنية هي المطثية الحاطمة، المطثية المنتنة، والمطثية السورديلية، والتي تسبب عادةً الغرغرينا الغازية (المعروفة أيضًا بالنخر العضلي). تنتج "المطثية الحاطمة" نوعين من السموم القاتلة: ذيفان ألفا وذيفان ثيتا. يتسبب ذيفان ألفا في تراكم الصفائح الدموية المفرط الذي يسد الأوعية الدموية ويحرم الأعضاء الحيوية من إمدادات الأكسجين. يخق هذا بيئة حمضية تفتقر إلى الأكسجين لتكاثر البكتيريا. عندما يتم امتصاص مادة ذيفان-ألفا بواسطة الأنسجة الرخوة، يمكن أن تمنع هجرة خلايا الدم البيضاء من الأوعية الدموية إلى الأنسجة الرخوة، مما يضعف وظيفة البلعمة. يمكن أن يتسبب السمان معًا في تدمير خلايا الدم الحمراء في الأوعية الدموية، وتلف سلامة الأوعية الدموية، وتعطيل وظائف القلب.[citation needed]
التشخيص
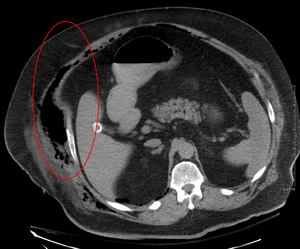
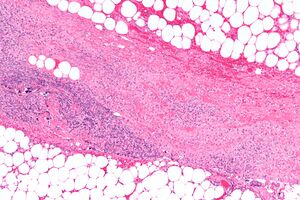
التشخيص المبكر صعب لأن المرض غالبا ما يبدو في وقت مبكر مثل التهاب الجلد السطحي البسيط.[4] في حين أن عددا من الطرائق المخبرية والتصويرية يمكن أن تثير الشك لالتهاب اللفافة الناخر، المعيار الذهبي لتشخيص واستكشاف جراحي في وضع مرتفع. عندما تكون في شك، يمكن إجراء شق صغيرة "ثقب المفتاح" في الأنسجة المتضررة، وإذا كان الإصبع يفصل بسهولة الأنسجة على طول الخط اللفافي، فان التشخيص مؤكد ويجب إجراء التنضير واسعة النطاق.[11]
التصوير المقطعي المحوسب (الأشعة المقطعية) على وشك الكشف عن حوالي 80٪ من الحالات بينما قد يتمكن التصوير بالرنين المغناطيسي من الالتقاط أكثر قليلا..[2]
التصوير الطبي
يلعب التصوير دورًا محدودًا في تشخيص التهاب اللفافة الناخر. يعد التأخير الزمني في إجراء التصوير مصدر قلق كبير. قد يُظهر التصوير الشعاعي البسيط انتفاخ الرئة تحت الجلد (غاز في النسيج تحت الجلد)، وهو ما يوحي بشدة بحدوث تغيرات نخرية، ولكنه ليس حساسًا بدرجة كافية لاكتشاف جميع الحالات، لأن التهابات الجلد الناخر التي تسببها بكتيريا المطثية غير المعدية عادة لا تظهر انتفاخ تحت الجلد. إذا كان التشخيص لا يزال موضع شك، فإن التصوير المقطعي المحوسب (CT) والتصوير بالرنين المغناطيسي (MRI) هما الأكثر حساسية من التصوير الشعاعي العادي. ومع ذلك، فإن كلا من الأشعة المقطعية والتصوير بالرنين المغناطيسي ليست حساسة بما يكفي لاستبعاد التغييرات الناخر تماماً.[2] قد يُظهر الفحص بالأشعة المقطعية سماكة اللفافة، وذمة، وغازات تحت الجلد، وتكون خراج.[2] في التصوير بالرنين المغناطيسي، عندما يحدث تجمع السوائل مع وجود التهاب ناخر، أو زيادة السماكة أو التحسين باستخدام حقن التباين، يجب الاشتباه بشدة إلى وجود التهاب اللفافة الناخر. وفي الوقت نفسه، يمكن أن يُظهر التصوير بتخطيط الصدى تكوين خراج سطحي، ولكنه ليس حساسًا بدرجة كافية لتشخيص التهاب اللفافة الناخر.[2] يمكن لفحص التصوير المقطعي المحوسب اكتشاف حوالي 80٪ من الحالات، بينما قد يلتقط التصوير بالرنين المغناطيسي أكثر قليلاً.[12]
نظام النقاط
يمكن استخدام نتيجة فحص مؤشر الخطر المخبري لالتهاب اللفافة لتصنيف الأشخاص الذين لديهم أعراض اِلْتِهابُ النّسِيجِ الخَلَوِي من أجل معرفة احتمالية تواجد مرض التهاب اللفافة. يستخدم هذا الفحص اعدادات سيرولوجية ستة: البروتين المتفاعل-C، عدد كريات الدم البيضاء الكامل، الهيموغلبين، الصوديوم، كرياتنين والغلوكوز. أي نتيجة أكبر من أو تساوي 6 [13] تعني وجوب الشك بمرض التهاب اللفافة. تكون معايير النتيجة كما يلي:
- البروتين المتفاعل-C (mg/L) ≥ 150: 4 نقاط
- عدد كريات الدم البيضاء (103/mm3 x)
- ˃15: 0 نقاط
- 15-25: نقطة واحدة
- ˂25: نقطتين
- الهيمجلوبين (g/dL)
- ˂13.5: 0 نقاط
- 11-13.5: نقطة واحدة
- ˃11: نقطتين
- الصوديوم (mmol/L) ˃135: نقطتين
- الكرياتينين (umol/L) ˂141: نقطتين
- الغلوكوز (mmol/L) ˂ 10: نقطة واحدة [13][14]
كما للدراسة الاستنتاجية لنتيجة الفحص، أي نتيجة ≥ 6 تعد كافية للشك بمرض التهاب اللفافة، ولكن أي نتيجة ˃6 لا تكفي لاستبعاد المرض. يجب وضع تشخيص اِلْتِهابُ النّسِيجِ الخَلَوِي والدمل في عين الاعتبار بسبب الأعراض المشابهة.[2]10% من المصابين بمرض التهاب اللفافة في الدراسة الأولية حصلوا على نتيجة.[15] ولكن أظهرت دراسة تصديقية أن المصابين بهذا المرض ونتيجة الفحص لديهم أكبر أو تساوي 6 تكون معدلات الوفاة والبتر لديهم أعلى.[16]
الوقاية
يمكن الوقاية من التهاب اللفافة الناخرج جزئياً بالعناية الجيدة بالجروح وغسل اليدين.[3]
العلاج
جراحة التنضير (إزالة الأنسجة المصابة) هي الدعامة الأساسية لعلاج التهاب اللفافة الناخر. غالباً ما يكون العلاج الطبي المبكر افتراضياً؛ وبالتالي، يجب أن تبدأ المضادات الحيوية بمجرد الاشتباه في الحالة. تؤخذ مزارع الأنسجة (بدلاً من مسحات الجرح) لتحديد المضادات الحيوية المناسبة، ويمكن تغيير المضادات الحيوية في ضوء النتائج. إلى جانب التحكم في ضغط الدم والترطيب، يجب بدء الدعم لأولئك الذين يعانون من علامات حيوية غير مستقرة وناتج بول منخفض.[2]
الجراحة
يجب إجراء عملية تنضير الجرح العدواني مبكرًا، عادةً بمجرد تشخيص عدوى الأنسجة الرخوة الناخر (NSTI). غالبًا ما تمتد الشقوق الجراحية إلى ما وراء مناطق التصلب (الأنسجة المتصلبة) لإزالة الأوعية الدموية التالفة المسؤولة عن التصلب. ومع ذلك، في بعض الأحيان يتم الحفاظ على الأنسجة الرخوة السيلوليتية من التنضير لتغطية الجلد لاحقًا للجرح. يمكن استخدام أكثر من عملية لإزالة الأنسجة الميتة الإضافية. في بعض الحالات التي يتأثر فيها أحد الأطراف بالتهاب اللفافة الناخر، قد يكون البتر هو العلاج الجراحي المفضل. بعد تنضير الجرح، يجب وضع الضمادات الكافية لمنع انكشاف عظام الوتر والغضروف حتى لا تجف هذه الهياكل ولتعزيز التئام الجروح.[2]
للعدوى التهاب اللفافة الناخر في منطقة العجان (غرغرينا فورنييه)، يمكن أن يكون تنضير الجروح والعناية بالجروح في هذه المنطقة صعبًا بسبب نواتج الإخراج التي غالبًا ما تجعل هذه المنطقة متسخة وتؤثر على عملية التئام الجروح. لذلك، يمكن أن تساعد التغييرات المنتظمة للضماد باستخدام نظام إدارة البراز في الحفاظ على نظافة الجرح في منطقة العجان. في بعض الأحيان، قد يكون من الضروري فغر القولون لتحويل نواتج الإخراج للحفاظ على نظافة الجرح في منطقة العجان.[2]
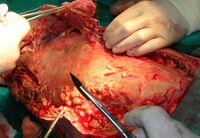
-
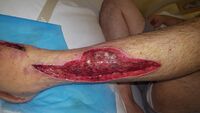
Wound after aggressive acute debridement of NF
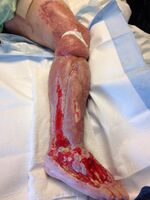
-
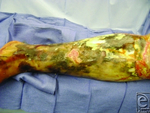
Necrotic tissue from the left leg surgically removed
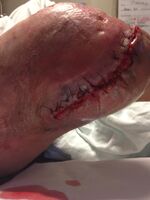
-
Postsurgical debridement and skin grafting
-
After knee disarticulation amputation
المضادات الحيوية
عادة ما يتم البدء بالمضادات الحيوية التجريبية بمجرد إجراء تشخيص NSTI، ثم تغييرها لاحقًا إلى العلاج بالمضادات الحيوية الموجهة بالمزرعة. في حالة NSTIs، تكون المضادات الحيوية التجريبية واسعة النطاق، وتغطي البكتيريا موجبة الجرام (بما في ذلك MRSA)، والبكتيريا سالبة الجرام، والبكتيريا اللاهوائية.[17]
بينما قارنت الدراسات الموكسيفلوكساسين (فلوروكينولون) والأموكسيسيلين كلافولانات (پنسلين) وقيمت مدة العلاج المناسبة (تتراوح من 7 إلى 21 يومًا)، لا توجد استنتاجات نهائية بشأن فعالية العلاج، أو المدة المثالية للعلاج، أو الآثار الضارة التي يمكن أن تحدث بسبب رداءة جودة الأدلة.[17]
علاجات أخرى
- المعالجة بالأكسجين عالي الضغط: بينما أظهرت الدراسات التي أجريت على البشر والحيوانات أن توتر الأكسجين المرتفع في الأنسجة يساعد على تقليل الوذمة، وتحفيز نمو الخلايا الليفية، وزيادة قدرة خلايا الدم البيضاء على المقاومة، وتثبيط إطلاق السموم البكتيرية، وزيادة فعالية المضادات الحيوية، [2] لم تُثبت أي تجارب عالية الجودة لدعم أو دحض استخدام العلاج بالأكسجين عالي الضغط في المرضى الذين يعانون من NSTIs.[17]
- الگلوبولين المناعي الوريدي (IVIG): لم يظهر فرق واضح بين استخدام الگلوبولين المناعي الوريدي والعلاج الوهمي في علاج NSTIs، وأظهرت إحدى الدراسات آثارًا ضائرة خطيرة باستخدام الگلوبولين المناعي الوريدي، بما في ذلك إصابات الكلى الحادة، وردود الفعل التحسسية، ومتلازمة التهاب السحايا العقيم، وفقر الدم الانحلالي، والتخثر، والعوامل المعدية.[17]
- AB103: قيمت الدراسة فعالية نوع جديد من العلاج الذي يؤثر على الاستجابة المناعية، يسمى AB103. أظهرت الدراسة عدم وجود اختلاف في معدل الوفيات باستخدام هذا العلاج، ولكن من الصعب استخلاص استنتاجات نهائية بسبب الأدلة منخفضة الجودة.[17]
- العلاج الداعم: يجب دائمًا توفير العلاج الداعم، بما في ذلك الترطيب عن طريق الوريد، والعناية بالجروح، ومضادات التخثر لمنع أحداث الانسداد التجلطي، والسيطرة على الألم، وما إلى ذلك، عند الحاجة.[citation needed]
علم الأوبئة
يصيب التهاب اللفافة الناخر حوالي 0.4 من كل 100000 شخص سنويًا في الولايات المتحدة.[4] تحدث حوالي 1000 حالة من حالات التهاب اللفافة الناخر سنويًا في الولايات المتحدة، لكن المعدلات آخذة في الازدياد. قد يكون هذا بسبب زيادة الوعي بهذه الحالة، مما يؤدي إلى زيادة الإبلاغ، أو الفوعة البكتيرية أو زيادة المقاومة البكتيرية ضد المضادات الحيوية.[2] في بعض مناطق العالم، ينتشر المرض بمعدل حالة من كل 100000 شخص.[4]
لوحظ ارتفاع معدلات التهاب اللفافة الناخر لدى المصابين بالبدانة أو السكري، وأولئك الذين يعانون من نقص المناعة أو المدمنين على الكحول، أو المصابين بمرض الشريان المحيطي. ومع ذلك، قد يحدث المرض أيضًا لدى الشباب البالغين الأصحاء الذين لا يعانون من أمراض كامنة. قد تزيد مضادات الالتهاب غير الستيروئيدية من معدلات عدوى التهاب اللفافة الناخر بسبب تعديل الاستجابة المناعية في الجسم، لأن مضادات الالتهاب غير الستيروئيدية تثبط إنزيمات cycloxygenase-1 and cycloxygenase-2 وهي مهمة في إنتاج الثرموبوكسان والپروستاگلاندين E2. الپروستاگلاندين مسؤولاً عن الحمى والالتهاب والألم. يقلل تثبيط إنتاج الپروستاگلاندين E2 من الاستجابة الالتهابية والتصاق الكريات البيضاء، وبالتالي يقلل من الاستجابة المناعية ضد الغزو البكتيري، مما يؤدي إلى الإصابة بعدوى الأنسجة الرخوة.[2]
التاريخ
حالات شهيرة

- في 13 يوليو 2021، توفيت إحدى مشاهير الإنترنت الصينيات بعد خضوعها لعملية شفط للدهون، مما أدى لإصابتها بعدوى البكتريا الآكلة للحم، وبقائها في العناية المركزة لشهرين. عانت الإنفلونسر من التهاب اللفافة الناخر بعد خضوعها للعلاج، وقد علقت لجنة الصحة في هانگژو الرخصة التجارية للعيادة الطبية في 17 يوليو 2021
قالت لجنة الصحة في هانگژ، أكبر مدينة في مقاطعة ژىجيانگ الشرقية، يوم الخميس، إن العيادة التي أجرت الإجراء يجب أن تعوض الأسرة مالياً وتوقف عملياتها التجارية. تفتقر عياد التجميل هواين الطبية إلى الفهم الصحيح للجراحة قبل إجرائها، وكانت لديها ممارسات غير صحيحة أثناء العملية ولم تقدم العلاج في الوقت المناسب بعد الجراحة. وقالت اللجنة في بيان إن أخطائها تسببت في مقتل الضحية.
كانت المرأة التي توفيت، ولقبها داي، مدوّنة أزياء تبلغ من العمر 33 عاماً ولديها حوالي 130 ألف متابع على موقع ويبو، وكانت معروفة بلقبها شياو ران. أجرت العملية في 2 مايو لإزالة الدهون من حول خصرها وبطنها وكذلك لتكبير ثدييها بعد يومين من شفط الدهون، اشتكت من آلام شديدة في الجسم وكانت تحارب الصدمة الطبية، وهي حالة خطيرة في بعض الأحيان ناجمة عن نقص تدفق الدم عبر الجسم.
اتصلت داي بسيارة إسعاف لنقلها إلى مستشفى أمراض القلب والأوعية الدموية في گرينتاون القريب، وفقاً لصورة من منشور على وسائل التواصل الاجتماعي كتبه صديقها المجهول. تم حذف المنشور في وقت لاحق. قال الأطباء في گرينتاون إن داي عانت من فشل في عدة أعضاء. في 5 مايو، نقلتها عائلتها إلى منشأة أخرى في المستشفى الثاني التابع لكلية الطب بجامعة ژىجيانگ تم تشخيص داي بإصابة أنسجة الجلد والتهاب اللفافة الناخر، وهو مرض يأكل اللحم يمكن أن ينتشر بسرعة وخطير للغاية.
أمضت المرأة شهرين في وحدة العناية المركزة قبل وفاتها. خلال ذلك الوقت، أجرى الأطباء عمليتين جراحيتين لمحاربة العدوى البكتيرية التي انتشرت في جميع أنحاء الجسم. وشككت أسرة داي في أهلية طبيب شفط الدهون الذي أجرى العملية في داي قالوا إن گاو تشيانگ كان طبيبا مبتدئا فقط، ونصت قاعدة عام 2009 الصادرة عن هيئة الصحة الحكومية على أن العمليات الجراحية التي تهدف إلى إزالة 2000 مل من الدهون أو أكثر يجب أن يقوم بها طبيب متمرس. تضمنت جراحة داي إزالة أكثر من تلك الكمية من الدهون.
في منشور على وسائل التواصل الاجتماعي، أعرب صديق داي عن إحباطه من الطريقة التي تعاملت بها العيادة التي أجرت شفط الدهون مع شكاوى المرأة. قالت صديقتها إن نسبة كبيرة من جلد داي - من ثدييها إلى بطنها - كانت متقرحة ومنتفخة. "أخبرتها مستشفى هوايان فقط أن تأخذ بعض الحبوب عندما أخبرتهم عن الألم. "لكن ذلك لم يخفف من أعراضها على الإطلاق". كما ورد في المقال.
أعرب العديد من الأشخاص عبر الإنترنت عن شفقتهم على داي على حسابها على ويبو هذا الأسبوع. لا ينبغي أن نلومها على اختيارها لإجراء جراحة شفط الدهون. كتب أحدهم "هو خيارها لإجراء الجراحة". "إنه خطأ مستشفى القمامة هذا. لقد تحملت الكثير من التعذيب. ارقدي بسلام أيتها الصغيرة ".
لم تكن داي أول ضحية رفيعة المستوى لعملية تجميل فاشلة في الصين القارية. في أكتوبر 2020، توفيت امرأة تبلغ من العمر 21 عاماً في مدينة تشانگژو بمقاطعة جيانگسو بشرق الصين أثناء إجراء جراحة لتكبير الثدي والأنف. تم اتهام المؤسسة التي أجريت لها الجراحة بأنها غير قادرة على التعامل مع حالات الطوارئ.
في عام 2019، توفيت امرأة تبلغ من العمر 28 عاماً بعد إجراء عملية جراحية في مدينة نانيانگ في هـِنان بوسط الصين، واتُهم المستشفى بعدم الحصول على الترخيص المناسب لإجراء عمليات التجميل. في عام 2010، توفي مغني مشهور في مسابقة الغناء التلفزيوني إثر تعرضه لحادث تخدير أثناء عملية تجميل.
انظر أيضاً
- Capnocytophaga canimorsus
- غرغرينا
- Mucormycosis, a rare fungal infection that can resemble necrotizing fasciitis (See type IV NF listing above)
- Noma (disease)
- Toxic shock syndrome
- Vibrio vulnificus
المصادر
- ^ Rakel, David; Rakel, Robert E. (2015). Textbook of Family Medicine (in الإنجليزية). Elsevier Health Sciences. p. 193. ISBN 9780323313087. Archived from the original on 2017-09-08.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع غ ف ق ك ل م ن هـ و ي أأ Hakkarainen, Timo W.; Kopari, Nicole M.; Pham, Tam N.; Evans, Heather L. (2014). "Necrotizing soft tissue infections: Review and current concepts in treatment, systems of care, and outcomes". Current Problems in Surgery. 51 (8): 344–62. doi:10.1067/j.cpsurg.2014.06.001. PMC 4199388. PMID 25069713.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض "Necrotizing Fasciitis: A Rare Disease, Especially for the Healthy". CDC. June 15, 2016. Archived from the original on 9 August 2016. Retrieved 13 August 2016.
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع Paz Maya, S; Dualde Beltrán, D; Lemercier, P; Leiva-Salinas, C (May 2014). "Necrotizing fasciitis: an urgent diagnosis". Skeletal Radiology. 43 (5): 577–89. doi:10.1007/s00256-013-1813-2. PMID 24469151. S2CID 9705500.
- ^ Ralston, Stuart H.; Penman, Ian D.; Strachan, Mark W. J.; Hobson, Richard (2018). Davidson's Principles and Practice of Medicine E-Book (in الإنجليزية). Elsevier Health Sciences. p. 227. ISBN 9780702070266.
- ^ Ferri, Fred F. (2013). Ferri's Clinical Advisor 2014 E-Book: 5 Books in 1 (in الإنجليزية). Elsevier Health Sciences. p. 767. ISBN 978-0323084314.
- ^ Wilson, B (1952). "Necrotizing fasciitis". The American Surgeon. 18 (4): 416–31. PMID 14915014.
- ^ أ ب ت Trent, Jennifer T.; Kirsner, Robert S. (2002). "Necrotizing fasciitis". Wounds. 14 (8): 284–92.
- ^ Pricop M, Urechescu H, Sîrbu A, Urtilă E (Mar 2011). "Fasceita necrozantă cervico-toracică: caz clinic și recenzie a literaturii de specialitate" [Necrotizing cervical fasciitis: clinical case and review of literature]. Revista de chirurgie oro-maxilo-facială și implantologie [Journal of oro-maxillo-facial surgery and implantology] (in الرومانية). 2 (1): 1–6. ISSN 2069-3850. Archived from the original on 2016-03-22. Retrieved 2016-04-07.
- ^ "UOTW#58 – Ultrasound of the Week". Ultrasound of the Week. 7 September 2015. Archived from the original on 18 July 2016. Retrieved 27 May 2017.
- ^ April, MD; Long, B (13 August 2018). "What Is the Accuracy of Physical Examination, Imaging, and the LRINEC Score for the Diagnosis of Necrotizing Soft Tissue Infection?". Annals of Emergency Medicine. 73 (1): 22–24. doi:10.1016/j.annemergmed.2018.06.029. PMID 30115465.
- ^ Puvanendran, R; Huey, JC; Pasupathy, S (October 2009). "Necrotizing fasciitis". Canadian Family Physician. 55 (10): 981–7. PMC 2762295. PMID 19826154.
- ^ أ ب . doi:10.1097/01.CCM.0000129486.35458.7D. PMID 15241098.
{{cite journal}}: Cite journal requires|journal=(help); Missing or empty|title=(help); Unknown parameter|الأخير1=ignored (help); Unknown parameter|الأخير2=ignored (help); Unknown parameter|الأخير3=ignored (help); Unknown parameter|الأخير4=ignored (help); Unknown parameter|الأخير5=ignored (help); Unknown parameter|الأول1=ignored (help); Unknown parameter|الأول2=ignored (help); Unknown parameter|الأول3=ignored (help); Unknown parameter|الأول4=ignored (help); Unknown parameter|الأول5=ignored (help); Unknown parameter|العدد=ignored (help); Unknown parameter|المجلد=ignored (help); Unknown parameter|سنة=ignored (help); Unknown parameter|صحيفة=ignored (help); Unknown parameter|صفحات=ignored (help); Unknown parameter|عنوان=ignored (help) - ^ "LRINEC scoring system for necrotising fasciitis".
- ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةWong 2004 - ^ Su, Yi-Chun; Chen, Hung-Wen; Hong, Yu-Cheng; Chen, Chih-Tsung; Hsiao, Cheng-Ting; Chen, I-Chuan (2008). "Laboratory risk indicator for necrotizing fasciitis score and the outcomes". ANZ Journal of Surgery. 78 (11): 968–72. doi:10.1111/j.1445-2197.2008.04713.x. PMID 18959694. S2CID 10467377.
- ^ أ ب ت ث ج Hua, C; Bosc, R; Sbidian, E; De Prost, N; Hughes, C; Jabre, P; Chosidow, O; Le Cleach, L (31 May 2018). "Interventions for necrotizing soft tissue infections in adults". The Cochrane Database of Systematic Reviews. 2018 (5): CD011680. doi:10.1002/14651858.CD011680.pub2. PMC 6494525. PMID 29851032.
- ^ أليس يان (2021-07-17). "شفط دهون يقتل إنفلونسر ببكتريا آكلة اللحم". www.scmp.com.
وصلات خارجية
| Classification | |
|---|---|
| External resources |
- CS1 الرومانية-language sources (ro)
- CS1 errors: unsupported parameter
- CS1 errors: missing title
- الصفحات بخصائص غير محلولة
- Short description is different from Wikidata
- Articles containing إنگليزية-language text
- Pages using Lang-xx templates
- Articles with unsourced statements from February 2021
- Articles with unsourced statements from September 2020
- Articles with Curlie links
- غرغرينا
- أمراض جرثومية
- Disorders of fascia
- التهابات
- أمراض جلدية مرتبطة بالجراثيم
- Necrosis
- أمراض نادرة
- RTTEM