بطارية صوديوم-أيون
بطارية صوديوم-أيون إنگليزية: Sodium-ion battery (NIB أو SIB) وهي نوع من البطاريات القابلة للشحن والتي تستخدم أيونات الصوديوم (Na+) كنواقل شحناتها. يتطابق مبدأ عملها و بنيتها الخلوية بشكل تقريبي مع أنواع بطارية ليثيوم-أيون (LIB)، ولكن في هذه الحالة استُبدل الليثيوم بالصوديوم.
تعد بطاريات صوديوم-أيون بديلاً ممكناً لتقنيات البطاريات المبنية بالليثيوم، ويرجع ذلك عموماً إلى انخفاض تكلفة الصوديوم وتوافره بكثرة.[1]نظراً لأن بطاريات صوديوم-أيون تستخدم مواد متوفرة ورخيصة، فمن المتوقع أن تكون أقل تكلفة من بطاريات ليثيوم-أيون. كما أن التأثيرات البيئية لبطاريات صوديوم-أيون فهي أقل أيضاً. على الرغم من أن بطاريات صوديوم-أيون أثقل وأكبر من بطاريات ليثيوم-أيون، إلا أنها مجدية لأنظمة تخزين الطاقة الثابتة بسبب لا أهمية تُذكر للوزن والحجم.[2]
تلقت بطاريات صوديوم-أيون اهتماماً أكاديمياً وتجارياً في 2010 و2020، ويرجع ذلك عموماً إلى التوزيع الجغرافي غير المتكافئ، والتأثير البيئي العالي والتكلفة العالية للعديد من المواد المطلوبة لبطاريات الليثيوم-أيون. ومن أهم هذه العناصر الليثيوم والكوبالت والنحاس والنيكل، لكنها وجودها غير إلزامي للعديد من أنواع بطاريات صوديوم-أيون.[3] أما أكبر ميزة لبطاريات صوديوم-أيون فهي الوفرة الطبيعية للصوديوم.[4]
اعتباراً من عام 2022، لم تعد لبطاريات صوديوم-أيون تلك الأهمية التجارية. فالتكنولوجيا غير مذكورة في تقرير إدارة معلومات الطاقة بالولايات المتحدة حول تقنيات تخزين هذه البطاريات.[5] ولا تستخدم المركبات الكهربائية بطاريات صوديوم-أيون. وتشمل تحديات الاعتماد المنخفض على كثافة الطاقة وعدم كفاية دورات الشحن والتفريغ.[6]
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
تاريخ
طُورت بطاريات صوديوم-أيون في السبعينيات وأوائل الثمانينيات. ومع ذلك، بحلول التسعينيات، أظهرت بطاريات ليثيوم-أيون المزيد من الوعود التجارية، مما تسبب في انخفاض الاهتمام ببطاريات صوديوم-أيون.[7][8]في أوائل عام 2010، شهدت بطاريات صوديوم-أيون انتعاشاً بسبب التكلفة المتزايدة للمواد الخام لبطاريات ليثيوم-أيون.[7]
مبدأ التشغيل
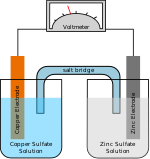
تتكون خلايا بطاريات صوديوم-أيون من كاثود يعتمد على مادة تحتوي على صوديوم، وأنود (ليس بالضرورة مادة قائمة على الصوديوم) وكهرل سائل يحتوي على أملاح صوديوم منفصلة القطبية الپروتونية أو مذيبات غير پروتونية. وأثناء الشحن، تنتقل أيونات الصوديوم من القطب السالب إلى القطب الموجب بينما تنتقل الإلكترونات عبر الدارة الخارجية. أثناء التفريغ، تحدث العملية العكسية.
المواد
تتطلب الخصائص الفيزيائية والكهروكيميائية للصوديوم مواد أخرى غير تلك المستخدمة في بطاريات ليثيوم-أيون.[9]
الأنودات (القطب الموجب)
تستخدم بطارية صوديوم-أيون الكربون الصلب، وهي مادة كربونية مختلطة تتكون من كربون غير قابل للگرفتة وغير لاوري وعديم الشكل. وقد اكتُشفت قدرة الكربون الصلب على امتصاص الصوديوم في عام 2000.[10] قُدّم هذا الأنود لنقل 300 mAh/g مع شكل طاقي منحدر أعلى من ⁓0.15 فولت مقابل Na/Na+. يمثل ما يقرب من نصف السعة وشكل مسطح طاقي (مسطح طاقي ذو مستوى أعلى) أقل من ⁓0.15 فولت V مقابل Na/Na+. تقدم أنودات الگرافيت لبطاريات ليثيوم-أيون سعة نموذجية من 300-360 mAh/g. تم عرض أول خلية صوديوم-أيون باستخدام الكربون الصلب في عام 2003 وأظهرت متوسط جهد كهربائي 3.7 فولت أثناء التفريغ.[11]يُفضل استخدام الكربون الصلب نظراً لتركيبته الممتازة من السعة وإمكانات العمل (المنخفضة) واستقرار دورة العمل.
في عام 2015، أظهر الباحثون أن الگرافيت يمكن أن يقحم الصوديوم في الإلكتروليتات القائمة على الإيثر. تم الحصول على سعات منخفضة تبلغ حوالي 100 mAh/g مع إمكانات عمل عالية نسبياً بين 0 – 1.2 V مقابل Na/Na+.[12]قدمت بعض أطوار تيتانات الصوديوم مثل Na2Ti3O7،[13][14][15] أو NaTiO2،[16] سعات حوالي 90–180 mAh/g في إمكانات العمل المنخفضة (< 1 V مقابل Na/Na+)، على الرغم من أن استقرار دورة العمل كان مقتصراً على بضع مئات من الدورات. وقد وصفت العديد من التقارير مواد الأنود التي تخزن الصوديوم عبر تفاعل سبيكة و/أو تفاعل تحويل.[7] يؤدي خلط معدن الصوديوم إلى فوائد تنظيم نقل أيون الصوديوم وحماية تراكم المجال الكهربائي عند أطراف تشعبات الصوديوم.[17]وقد ذكر وانگ وآخرون أن سطح سبيكة ذاتية التنظيم من أنتيمون نيكل (NiSb) قد ترسبت كيميائياً على معدن الصوديوم أثناء التفريغ. كما تنظم هذه الطبقة الرقيقة من NiSb الطلاء الكهروكيميائي الموحد لمعدن الصوديوم، مما يقلل من الجهد الزائد ويوفر تصفيحاً/تجريداً خالٍ من التشعبات لمعدن الصوديوم لأكثر من 100 ساعة بسعة مساحية عالية تبلغ 10 mAh cm-2.[18]
في دراسة أخرى، لي وآخرون. تحضير الصوديوم والقصدير المعدني Na 15Sn 4/Na من خلال تفاعل تلقائي.[19]يمكن أن يعمل هذا الأنود عند درجة حرارة عالية تبلغ 90 °C (194 °F) في إلكتروليت كربونات عند 1 mA cm-2 مع 1 mA h cm-2 وأظهرت الخلية الكاملة معدل دورة عمل ثابت لـ 100 دورة بكثافة حالية تبلغ 2 درجة مئوية.[19] على الرغم من قدرة سبائك الصوديوم على العمل في درجات حرارة قصوى وتنظيم النمو التغصني، يحد التوتر الإجهادي الشديد الذي تعاني منه المادة في سياق دورات التخزين المتكررة من استقرار الدورة، خاصة في الخلايا كبيرة الحجم. وقد حقق باحثون من جامعة طوكيو للعلوم 478 mAh/g بجزيئات نانو من المغنسيوم، واُعلن عن ذلك في ديسمبر 2020.[20]
في عام 2021، جرب باحثون من الصين الهيكل متعدد الطبقات MoS 2 كنوع جديد من الأنود لبطاريات صوديوم-أيون. كما جمعت عملية إعادة التبلور والذوبان بشكل مكثف طبقة الكربون المغلفة بطبقة من الكربون صفائح نانوية MoS2 على سطح الأنابيب النانوية الكربونية N-doped المشتقة من [[پوليإيميد]. يمكن لهذا النوع من C-MoS2/NCNTs تخزين 348mAh/g عند 2A/g، مع استقرار دورة العمل بنسبة 82٪ بعد 400 دورة عند 1A/g.[21] TiS2 هي مادة أخرى محتملة لبطاريات صوديوم-أيون بسبب هيكلها متعدد الطبقات، ولكن لا يزال يتعين عليها التغلب على مشكلة تلاشي السعة، نظراً لأن TiS2 تعاني من ضعف الحركية الكهروكيميائية واستقرار هيكلي ضعيف نسبياً. في عام 2021، استخدم باحثون من مدينة ننگبو بالصين TiS2 المُسبَق البوتاسيوم، وقدرة معدل تقديم تبلغ 165.9mAh/g واستقرار دورة العمل بنسبة 85.3٪ من السعة بعد 500 دورة.[22]
استُخدم گرافين جسيمات جانوس في بطاريات صوديوم-أيون التجريبية لزيادة كثافة الطاقة. ويوفر أحد الجانبين مواقع تفاعل بينما يوفر الآخر فصلاً بين الطبقات. وقد بلغت كثافة الطاقة 337 mAh/g.[23]
الكاثودات (القطب السالب)
تخزن كاثودات صوديوم-أيون الصوديوم عبر الإقحام. نظراً لارتفاع كثافة الوصل وإمكانات التشغيل والقدرات العالية، فقد حظيت الكاثودات القائمة على أكاسيد المعادن الانتقالية للصوديوم بأكبر قدر من الاهتمام. للإبقاء على التكاليف منخفضة، يحاول البحث تقليل العناصر المكلفة مثل Co، Cr، Ni أو V. يمكن لأكسيد Na2/3Fe1/2Mn1/2O2 من النوع P2 من موارد الحديد والمنغنيز الوفيرة بالأرض تخزين 190 mAh/g بشكل عكسي بمتوسط جهد تفريغ يبلغ 2.75 V مقابل Na/Na+ باستخدام زوج الأكسدة والإرجاع Fe3+/4+ - على قدم المساواة أو أفضل من كاثودات ليثيوم-أيون التجارية مثل LiFePO4 أو LiMn2O4.[24] ومع ذلك، فإن طبيعتها التي تعاني من نقص الصوديوم قد قللت من كثافة الطاقة. كما بُذلت جهود كبيرة في تطوير أكاسيد الصوديوم الأكثر ثراءً. وقد أُثبت أن الخليط Na0.76Mn0.5Ni0.3Fe0.1Mg0.1O2 من النوع P3/P2/O3 قدرته على توصيل 140 mAh/g بمتوسط جهد تفريغ يبلغ 3.2 V مقابل Na/Na+ في عام 2015.[25] على وجه الخصوص، يمكن للأكسيد NaNi1/4Na1/6Mn2/12Ti4/12Sn1/12O2 من النوع O3 توفير 160 mAh/g بمتوسط جهد يبلغ 3.22 V vs Na/Na+،[26] في حين أن سلسلة من أكاسيد مطعمة بالنيكل من حساب العناصر المتفاعلة NaaNi(1−x−y−z)MnxMgyTizO2 يمكنها توفير 57 mAh/g في "خلية كاملة" صوديوم-أيون مع أنود كربون صلب في المتوسط جهد التفريغ 3.2 فولت باستخدام زوج الأكسدة والاختزال Ni2+/4+ .[27]يكون هذا الأداء في التكوين الكامل للخلايا أفضل أو على قدم المساواة مع أنظمة ليثيوم-أيون التجارية. فقد أظهرت مادة الكاثود Na0.67Mn1−xMgxO2 قدرة تفريغ 175 mAh/g لـ Na0.67Mn0.95Mg0.05O2. كما يحتوي هذا الكاثود على عناصر وفيرة فقط.[28] أظهرت مواد الكاثود بالنحاس البديل Na0.67Ni0.3−xCuxMn0.7O2 قدرة عالية قابلة للإرجاع مع احتفاظ أفضل بالقدرة. على عكس القطب الكهربي الخالي من النحاس Na0.67Ni0.3−xCuxMn0.7O2، توفر كاثودات النحاس المُستبدلة تخزيناً أفضل للصوديوم. ومع ذلك، فإن الكاثودات التي تحتوي على النحاس أكثر تكلفة.[29]
أخذ البحث أيضاً الكاثودات المبينة على متعددات الشحنات بعين الاعتبار حيث توفر هذه الكاثودات كثافة ضغط أقل، مما يقلل من كثافة الطاقة على حساب الأنيون الضخم. قد يتم تعويض هذا عن طريق الرابطة التساهمية الأقوى من متعددات الشحنات التي تؤثر بشكل إيجابي على دورة العمل والسلامة. من بين الكاثودات القائمة على متعددات الشحنات، أظهر فوسفات ڤناديوم الصوديوم[30]و الفلوروفوسفات[31]أظهر ثباتاً ممتازاً في دورة العمل، وفي الأخير، قدرة عالية مقبولة (⁓120 mAh/g) عند متوسط جهد تفريغ عالي (⁓3.6 V مقابل Na/Na+).[32]
ناقشت عدة تقارير استخدام العديد من أزرق پروسيا ونظائره (PBAs)، مع الشكل المعين الأوجه Na2MnFe(CN)6 الذي يوفر سعة 150–160 mAh/g ومتوسط جهد تفريغ 3.4 فولت[33][34][35]كما أظهر وأبيض پروسيا معيني الأوجه Na1.88(5)Fe[Fe(CN)6]·0.18(9)H2O عرض السعة الأولية لـ 158 mAh/g والاحتفاظ بقدرة 90٪ بعد 50 دورة.[36]
الكهارل
يمكن لبطاريات صوديوم-أيون أن تستخدم كهارل مائية وغير مائية. ينتج عن نافذة الاستقرار الكهروكيميائية المحدودة للمياه انخفاض الفولتية وكثافة الطاقة المحدودة. تعمل المذيبات غير المائية القطبية إستر كربونات على تمديد نطاق الجهد. وتشمل هذه كربونات الإثيلين، ثنائي ميثيل الكربونات، ثنائي إيثيل الكربونات، وكربونات الپروپلين. يستخدم الكهرل غير المائي الأكثر شيوعاً سداسي فلوروفوسفات الصوديوم كملح مذاب في خليط من هذه المذيبات. بالإضافة إلى ذلك، يمكن لإضافات الكهرل تحسين مقاييس الأداء.[بحاجة لمصدر]
مقارنة
تتمتع بطاريات صوديوم-أيون بالعديد من المزايا مقارنة بتقنيات البطاريات المنافسة. بالمقارنة مع بطاريات ليثيوم-أيون، تتميز بطاريات صوديوم-أيون بتكلفة أعلى إلى حد ما، وكثافة طاقة أقل قليلاً، وخصائص أمان أفضل، وخصائص توصيل طاقة مماثلة.
يقارن الجدول أدناه كيفية أداء بطاريات صوديوم-أيون بشكل عام مقابل تقنيتي البطاريات القابلة للشحن المعمول بها في السوق حالياً: بطارية ليثيوم-أيون والبطارية بطارية الرصاص-الحمض القابلة للشحن.[27][37]
| بطارية صوديوم-أيون | بطارية ليثيوم-أيون | بطارية الرصاص-الحمض | |
|---|---|---|---|
| التكلفة بسعة كيلوواط/ساعة | $40–77[3] | $137 (وسطياً في عام 2020).[38] | $100–300[39] |
| كثافة الطاقة الحجمية | 250–375 W·h/L، استناداً النماذج المبدأية[40] | 200–683 W·h/L[41] | 80–90 W·h/L[42] |
| كثافة الطاقة الثقالية (طاقة نوعية) | 75–165 W·h/kg، استناداً إلى النماذج المبدأية وإعلانات المنتجات[40][43] | 120–260 W·h/kg[41] | 35–40 Wh/kg[42] |
| دورات العمل بعمق تفريغ 80٪[أ] | Hundreds to thousands.[44] | 3,500[39] | 900[39] |
| السلامة | منخفضة الخطورة للبطاريات المائية، وعالية للصوديوم في بطاريات الكربون | عالية الخطورة[ب] | متوسطة الخطورة |
| المواد | أرضية وفيرة | نادرة | سامة |
| ثبات دورة العمل | عالية (تفريغ ذاتي قليل) | عالية (تفريغ ذاتي قليل) | معتدل (تفريغ ذاتي عالي) |
| كفاءة التيار المستمر تفريغ وشحن | حتى 92%[44] | 85–95%[45] | 70–90%[46] |
| نطاق درجة حرارة[ت] | −20 °C إلى 60 °C[44] | مقبول:−20 °C إلى 60 °C.
أمثلي: 15 °C إلى35 °C[47] |
−20 °C إلى 60 °C[48] |
التسويق
تعمل الشركات في جميع أنحاء العالم على تطوير بطاريات صوديوم-أيون القابلة للتنفيذ تجارياً. الشركات المتنافسة:
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
أكويون إنرجي
كانت أكويون إنرجي (بين عامي 2008 و2017) شركة بحيثة فرعية من جامعة كارنگي ملون. اعتمدت بطارياتهم على سلبية فوسفات تيتانيوم الصوديوم، إيجابية ثاني أكسيد المنجنيز، وپركلورات الصوديوم المنحلة بالكهرباء. بعد حصولها على قروض حكومية وخاصة، تقدمت الشركة بطلب الإفلاس في عام 2017. تم بيع أصولها إلى الشركة المصنعة الصينية جولين-تيتانز، التي تخلت عن معظم براءات اختراع أكويون.[49][50][51]
فاراديون المحدودة
فاراديون المحدودة، هي شركة تابعة لشركة رليانس للصناعات الهندية.[52]يستخدم تصميم الخلية كاثودات أكسيد مع أنود كربون صلب كهرل سائل. تتمتع الخانات الخلوية بكثافات طاقة مماثلة لبطاريات ليثيوم-أيون التجارية (160 واط/كجم على مستوى الخلية) مع أداء معدل جيد حتى 3C وعمر دورة العمل من 300 (100٪ عمق التفريغ) إلى أكثر من 1000 دورة (80٪ عمق التفريغ). أظهرت حزم البطاريات الخاصة بها استخدامها لتطبيقات الدراجات الإلكترونية والسكوتر الإلكتروني.[27] لقد أظهرت نقل خلايا صوديوم-أيون في الحالة القصيرة (عند 0 فولت)، مما أدى إلى القضاء على خطورة النقل التجاري لهذه الخلايا.[53] وهي شريكة مع AMTE Power plc[54](المعروفة سابقاً باسم بطاريات AGM المحدودة).[55][56][57][58]
في الخامس من ديسمبر 2022، قامت فاراديون بتركيب أول بطارية صوديوم-أيون لها للأمة في نيو ساوث ويلز بأستراليا.[59]
تيامات
برزت شركة تيامات من CNRS/ CEA ومشروع H2020 التابع للاتحاد الأوروبي - يسمى NAIADES.[60] تركز تقنية الشركة على تطوير خلايا اسطوانية بتنسيق 18650 تعتمد على مواد متعددة الشحنة. وقد حققت كثافة طاقة تتراوح بين 100 Wh/kg إلى 120 Wh/kg. تستهدف التكنولوجيا التطبيقات في أسواق الشحن والتفريغ السريع. تتراوح كثافة الطاقة بين 2 و5 Wh/kg، مما يوفر زمن شحن يبلغ 5 دقائق. العمر الافتراضي هو 5000+ دورة إلى 80٪ من السعة.[61][62][63][64]
شركة هينا لتقنيات البطاريات
شركة هينا المحدودة لتقنيات البطاريات هي فرع من أكاديمية العلوم الصينية (CAS). الشركة تعزز الأبحاث التي أجرتها مجموعة البروفيسور هو يونگ-شنگ في معهد الفيزياء في CAS. تعتمد بطاريات HiNa على كاثود أكسيد Na-Fe-Mn-Cu وأنود الكربون القائم على الأنثراسيت. يمكنها توفير كثافة طاقة تبلغ 120 Wh/kg. في عام 2019، أُفيد عن قيام HiNa بتركيب بنك طاقة ببطارية صوديوم-أيون 100 kWh في شرق الصين.[65]
ناترون إنرجي
تستخدم ناترون إنرجي، وهي فرع من جامعة ستانفورد، نظائر أزرق پروسيا لكل من الكاثود والأنود مع كهرل مائي.[66]
ألترس إيهبي
ألترس إيهبي هو فرع من مركز آنگسترم للبطاريات المتقدمة الذي تديره البروفيسورة كرستينا إيدستروم في جامعة أوپسالا. تقدم الشركة نظير أزرق پروسيا بأساس الحديد للقطب الموجب في بطاريات صوديوم-أيون غير المائية التي تستخدم الكربون الصلب كقطب موجب.[67]
CATL
أعلنت الشركة الصينية المصنعة للبطاريات CATL في عام 2021 أنها ستطرح بطارية تعتمد على صوديوم-أيون في السوق بحلول عام 2023.[68] والتي تستخدم نظير أزرق پروسيا للإلكترود الموجب والكربون المسامي للقطب السالب. لقد زعموا أن كثافة الطاقة المحددة تبلغ 160 Wh/kg في بطارية الجيل الأول.[43] كما خططت الشركة لإنتاج حزمة بطارية هجينة تتضمن خلايا صوديوم-أيون وخلايا ليثيوم-أيون.[69]
انظر أيضاً
- قائمة أنواع البطاريات
- بطارية فلز قلوي-أيون
- بطارية ليثيوم-أيون
- بطارية صوديوم-أيون
- بطارية پوتاسيوم-أيون
- بطارية قابلة للشحن
- بطارية الماء الملحي
ملاحظات
- ^ The number of charge-discharge cycles a battery supports depends on multiple considerations, including depth of discharge, rate of discharge, rate of charge, and temperature. The values shown here reflect generally favorable conditions.
- ^ See Lithium-ion battery safety.
- ^ تؤثر درجة الحرارة على سلوك الشحن والسعة وعمر البطارية، وتؤثر على كل من هذه الأشياء بشكل مختلف، في نطاقات درجات حرارة مختلفة لكل منها. القيم الواردة هنا هي نطاقات عامة لتشغيل البطارية.
المراجع
- ^ "The Future Roadmap for Sodium-Ion Batteries | Blackridge Research". www.blackridgeresearch.com (in الإنجليزية الأمريكية). Retrieved 2022-10-26.
- ^ Peters, Jens; Buchholz, Daniel; Passerini, Stefano; Weil, Marcel (2016-05-09). "Life cycle assessment of sodium-ion batteries". Energy & Environmental Science (in الإنجليزية). 9 (5): 1744–1751. doi:10.1039/C6EE00640J. ISSN 1754-5706. S2CID 56536013.
- ^ أ ب Peters, Jens F.; Peña Cruz, Alexandra; Weil, Marcel (2019). "Exploring the Economic Potential of Sodium-Ion Batteries". Batteries (in الإنجليزية). 5 (1): 10. doi:10.3390/batteries5010010.
- ^ Abraham, K. M. (2020). "How Comparable Are Sodium-Ion Batteries to Lithium-Ion Counterparts?". ACS Energy Letters. 5 (11): 3544–3547. doi:10.1021/acsenergylett.0c02181.
- ^ U.S. Department of Energy. "Battery Storage in the United States: An Update on Market Trends" (PDF). U.S. Energy Information Administration. p. 13. Retrieved 13 March 2021.
- ^ Marc Walter; Maksym V. Kovalenko; Kostiantyn V. Kravchyk (2020). "Challenges and benefits of post-lithium-ion batteries". New Journal of Chemistry. 44 (5): 1678. doi:10.1039/C9NJ05682C.
- ^ أ ب ت Sun, Yang-Kook; Myung, Seung-Taek; Hwang, Jang-Yeon (2017-06-19). "Sodium-ion batteries: present and future". Chemical Society Reviews. 46 (12): 3529–3614. doi:10.1039/C6CS00776G. ISSN 1460-4744. PMID 28349134.
- ^ Yabuuchi, Naoaki; Kubota, Kei; Dahbi, Mouad; Komaba, Shinichi (2014-12-10). "Research Development on Sodium-Ion Batteries". Chemical Reviews. 114 (23): 11636–11682. doi:10.1021/cr500192f. ISSN 0009-2665. PMID 25390643.
- ^ Nayak, Prasant Kumar; Yang, Liangtao; Brehm, Wolfgang; Adelhelm, Philipp (2018). "From Lithium-Ion to Sodium-Ion Batteries: Advantages, Challenges, and Surprises". Angewandte Chemie International Edition (in الإنجليزية). 57 (1): 102–120. doi:10.1002/anie.201703772. ISSN 1521-3773. PMID 28627780.
- ^ Dahn, J. R.; Stevens, D. A. (2000-04-01). "High Capacity Anode Materials for Rechargeable Sodium‐Ion Batteries". Journal of the Electrochemical Society. 147 (4): 1271–1273. Bibcode:2000JElS..147.1271S. doi:10.1149/1.1393348. ISSN 0013-4651.
- ^ Barker, J.; Saidi, M. Y.; Swoyer, J. L. (2003-01-01). "A Sodium-Ion Cell Based on the Fluorophosphate Compound NaVPO4 F". Electrochemical and Solid-State Letters. 6 (1): A1–A4. doi:10.1149/1.1523691. ISSN 1099-0062.
- ^ Jache, Birte; Adelhelm, Philipp (2014). "Use of Graphite as a Highly Reversible Electrode with Superior Cycle Life for Sodium-Ion Batteries by Making Use of Co-Intercalation Phenomena". Angewandte Chemie International Edition. 53 (38): 10169–10173. doi:10.1002/anie.201403734. ISSN 1521-3773. PMID 25056756.
- ^ Senguttuvan, Premkumar; Rousse, Gwenaëlle; Seznec, Vincent; Tarascon, Jean-Marie; Palacín, M.Rosa (2011-09-27). "Na2Ti3O7: Lowest Voltage Ever Reported Oxide Insertion Electrode for Sodium Ion Batteries". Chemistry of Materials. 23 (18): 4109–4111. doi:10.1021/cm202076g. ISSN 0897-4756.
- ^ Rudola, Ashish; Saravanan, Kuppan; Mason, Chad W.; Balaya, Palani (2013-01-23). "Na2Ti3O7: an intercalation based anode for sodium-ion battery applications". Journal of Materials Chemistry A. 1 (7): 2653–2662. doi:10.1039/C2TA01057G. ISSN 2050-7496.
- ^ Rudola, Ashish; Sharma, Neeraj; Balaya, Palani (2015-12-01). "Introducing a 0.2V sodium-ion battery anode: The Na2Ti3O7 to Na3−xTi3O7 pathway". Electrochemistry Communications. 61: 10–13. doi:10.1016/j.elecom.2015.09.016. ISSN 1388-2481.
- ^ Ceder, Gerbrand; Liu, Lei; Twu, Nancy; Xu, Bo; Li, Xin; Wu, Di (2014-12-18). "NaTiO2: a layered anode material for sodium-ion batteries". Energy & Environmental Science. 8 (1): 195–202. doi:10.1039/C4EE03045A. ISSN 1754-5706.
- ^ "Northwestern SSO". prd-nusso.it.northwestern.edu. Retrieved 2021-11-19.
- ^ Wang, L.; Shang, J.; Huang, Q.; Hu, H.; Zhang, Y.; Xie, C.; Luo, Y.; Gao, Y.; Wang, H.; Zheng, Z. (2021). "Northwestern SSO". Advanced Materials. 33 (41): e2102802. doi:10.1002/adma.202102802. PMID 34432922. S2CID 237307044. Retrieved 2021-11-19.
- ^ أ ب "Northwestern SSO". prd-nusso.it.northwestern.edu. Retrieved 2021-11-19.
- ^ Kamiyama, Azusa; Kubota, Kei; Igarashi, Daisuke; Youn, Yong; Tateyama, Yoshitaka; Ando, Hideka; Gotoh, Kazuma; Komaba, Shinichi (December 2020). "MgO‐Template Synthesis of Extremely High Capacity Hard Carbon for Na‐Ion Battery". Angewandte Chemie International Edition. 60 (10): 5114–5120. doi:10.1002/anie.202013951. PMC 7986697. PMID 33300173.
- ^ Liu, Yadong; Tang, Cheng; Sun, Weiwei; Zhu, Guanjia; Du, Aijun; Zhang, Haijiao (2021-06-09). "In-situ conversion growth of carbon-coated MoS2/N-doped carbon nanotubes as anodes with superior capacity retention for sodium-ion batteries". Journal of Materials Science & Technology. 102: 8–15. doi:10.1016/j.jmst.2021.06.036. S2CID 239640591.
- ^ Huang, Chengcheng; Liu, Yiwen; Zheng, Runtian (2021-08-07). "Interlayer gap widened TiS2 for highly efficient sodium-ion storage". Journal of Materials Science & Technology. 107: 64–69. doi:10.1016/j.jmst.2021.08.035. S2CID 244583592.
- ^ Lavars, Nick (2021-08-26). "Two-faced graphene offers sodium-ion battery a tenfold boost in capacity". New Atlas (in الإنجليزية الأمريكية). Retrieved 2021-08-26.
{{cite web}}: CS1 maint: url-status (link) - ^ Komaba, Shinichi; Yamada, Yasuhiro; Usui, Ryo; Okuyama, Ryoichi; Hitomi, Shuji; Nishikawa, Heisuke; Iwatate, Junichi; Kajiyama, Masataka; Yabuuchi, Naoaki (June 2012). "P2-type Nax[Fe1/2Mn1/2]O2 made from earth-abundant elements for rechargeable Na batteries". Nature Materials. 11 (6): 512–517. Bibcode:2012NatMa..11..512Y. doi:10.1038/nmat3309. ISSN 1476-4660. PMID 22543301.
- ^ Keller, Marlou; Buchholz, Daniel; Passerini, Stefano (2016). "Layered Na-Ion Cathodes with Outstanding Performance Resulting from the Synergetic Effect of Mixed P- and O-Type Phases". Advanced Energy Materials. 6 (3): 1501555. doi:10.1002/aenm.201501555. ISSN 1614-6840. PMC 4845635. PMID 27134617.
- ^ Kendrick, E.; Gruar, R.; Nishijima, M.; Mizuhata, H.; Otani, T.; Asako, I.; Kamimura, Y. (May 22, 2014). "Tin-Containing Compounds United States Patent No. US 10,263,254" (PDF).
- ^ أ ب ت Bauer, Alexander; Song, Jie; Vail, Sean; Pan, Wei; Barker, Jerry; Lu, Yuhao (2018). "The Scale-up and Commercialization of Nonaqueous Na-Ion Battery Technologies". Advanced Energy Materials. 8 (17): 1702869. doi:10.1002/aenm.201702869. ISSN 1614-6840.
- ^ Billaud, Juliette; Singh, Gurpreet; Armstrong, A. Robert; Gonzalo, Elena; Roddatis, Vladimir; Armand, Michel (2014-02-21). "Na0.67Mn1−xMgxO2(0<=x<=2):a high capacity cathode for sodium-ion batteries". Energy & Environmental Science. 7: 1387–1391. doi:10.1039/c4ee00465e.
- ^ Wang, Lei; Sun, Yong-Gang; Hu, Lin-Lin; Piao, Jun-Yu; Guo, Jing; Manthiram, Arumugam; Ma, Jianmin; Cao, An-Min (2017-04-09). "Copper-substituted Na0.67Ni0.3−xCuxMn0.7O2 cathode materials for sodium-ion batteries with suppressed P2–O2 phase transition". Journal of Materials Chemistry A. 5 (18): 8752–8761. doi:10.1039/c7ta00880e.
- ^ Uebou, Yasushi; Kiyabu, Toshiyasu; Okada, Shigeto; Yamaki, Jun-Ichi. "Electrochemical Sodium Insertion into the 3D-framework of Na3M2(PO4)3 (M=Fe, V)". The Reports of Institute of Advanced Material Study, Kyushu University (in اليابانية). 16: 1–5. hdl:2324/7951.
- ^ Barker, J.; Saidi, Y.; Swoyer, J. L. "Sodium ion Batteries United States Patent No. US 6,872,492 Issued March 29, 2005" (PDF).
- ^ Kang, Kisuk; Lee, Seongsu; Gwon, Hyeokjo; Kim, Sung-Wook; Kim, Jongsoon; Park, Young-Uk; Kim, Hyungsub; Seo, Dong-Hwa; Shakoor, R. A. (2012-09-11). "A combined first principles and experimental study on Na3V2(PO4)2F3 for rechargeable Na batteries". Journal of Materials Chemistry. 22 (38): 20535–20541. doi:10.1039/C2JM33862A. ISSN 1364-5501.
- ^ Goodenough, John B.; Cheng, Jinguang; Wang, Long; Lu, Yuhao (2012-06-06). "Prussian blue: a new framework of electrode materials for sodium batteries". Chemical Communications. 48 (52): 6544–6546. doi:10.1039/C2CC31777J. ISSN 1364-548X. PMID 22622269. S2CID 30623364.
- ^ Song, Jie; Wang, Long; Lu, Yuhao; Liu, Jue; Guo, Bingkun; Xiao, Penghao; Lee, Jong-Jan; Yang, Xiao-Qing; Henkelman, Graeme (2015-02-25). "Removal of Interstitial H2O in Hexacyanometallates for a Superior Cathode of a Sodium-Ion Battery". Journal of the American Chemical Society. 137 (7): 2658–2664. doi:10.1021/ja512383b. ISSN 0002-7863. PMID 25679040. S2CID 2335024.
- ^ Lu, Y.; Kisdarjono, H.; Lee, J. J.; Evans, D. "Transition metal hexacyanoferrate battery cathode with single plateau charge/discharge curve United States Patent No. 9,099,718 Issued August 4, 2015; Filed by Sharp Laboratories of America, Inc. on October 3, 2013" (PDF).
- ^ Brant, William R.; Mogensen, Ronnie; Colbin, Simon; Ojwang, Dickson O.; Schmid, Siegbert; Häggström, Lennart; Ericsson, Tore; Jaworski, Aleksander; Pell, Andrew J.; Younesi, Reza (2019-09-24). "Selective Control of Composition in Prussian White for Enhanced Material Properties". Chemistry of Materials. 31 (18): 7203–7211. doi:10.1021/acs.chemmater.9b01494. ISSN 0897-4756. S2CID 202881037.
- ^ Yang, Zhenguo; Zhang, Jianlu; Kintner-Meyer, Michael C. W.; Lu, Xiaochuan; Choi, Daiwon; Lemmon, John P.; Liu, Jun (2011-05-11). "Electrochemical Energy Storage for Green Grid". Chemical Reviews. 111 (5): 3577–3613. doi:10.1021/cr100290v. ISSN 0009-2665. PMID 21375330. S2CID 206894534.
- ^ "Battery Pack Prices Cited Below $100/kWh for the First Time in 2020, While Market Average Sits at $137/kWh". Bloomberg NEF. 16 December 2020. Retrieved 15 March 2021.
- ^ أ ب ت Energy Storage Technology and Cost Characterization Report. U.S. Department Of Energy. July 2019. p. iix. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. https://www.energy.gov/sites/prod/files/2019/07/f65/Storage%20Cost%20and%20Performance%20Characterization%20Report_Final.pdf. Retrieved on 15 March 2021. - ^ أ ب Abraham, K. M. (23 October 2020). "How Comparable Are Sodium-Ion Batteries to Lithium-Ion Counterparts?". ACS Energy Letters (pdf). American Chemical Society. 5 (11): 3546. doi:10.1021/acsenergylett.0c02181.
- ^ أ ب Automotive Li-Ion Batteries: Current Status and Future Perspectives. U.S. Department Of Energy. 2019-01-01. p. 26. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. https://www.osti.gov/servlets/purl/1561559. Retrieved on 15 March 2021. - ^ أ ب May, Geoffrey J.; Davidson, Alistair; Monahov, Boris (2018-02-01). "Lead batteries for utility energy storage: A review". Journal of Energy Storage (in الإنجليزية). 15: 145–157. doi:10.1016/j.est.2017.11.008. ISSN 2352-152X.
- ^ أ ب "CATL Unveils Its Latest Breakthrough Technology by Releasing Its First Generation of Sodium-ion Batteries". www.catl.com. Retrieved 2021-07-29.
- ^ أ ب ت "Performance". Faradion Limited. Retrieved 17 March 2021.
The (round trip) energy efficiency of sodium-ion batteries is 92% at a discharge time of 5 hours.
- ^ Lithium Ion Battery Test - Public Report 5. ITP Renewables. September 2018. p. 13. Archived from the original. You must specify the date the archive was made using the
|archivedate=parameter. https://arena.gov.au/assets/2015/08/battery-test-centre-report-5.pdf. Retrieved on 17 March 2021. ""The data shows all technologies delivering between 85–95% DC round-trip efficiency."" - ^ ""Battery Storage Technologies for Electrical Applications: Impact in Stand-Alone Photovoltaic Systems"" (pdf). mdpi.com. November 2017. p. 13. Retrieved 17 March 2021.
Lead–acid batteries have a ... round trip-efficiency (RTE) of ~70–90%
- ^ Ma, Shuai (December 2018). ""Temperature effect and thermal impact in lithium-ion batteries: A review"". Progress in Natural Science: Materials International (pdf). 28 (6): 653–666. doi:10.1016/j.pnsc.2018.11.002. S2CID 115675281. Retrieved 17 March 2021.
- ^ Hutchinson, Ronda (June 2004). "Temperature effects on sealed lead acid batteries and charging techniques to prolong cycle life" (PDF) (pdf). Sandia National Labs: 10. doi:10.2172/975252. S2CID 111233540. Retrieved 17 March 2021.
{{cite journal}}: Cite journal requires|journal=(help) - ^ "Aqueous electrolyte energy storage device".
- ^ "Large format electrochemical energy storage device housing and module".
- ^ "Composite anode structure for aqueous electrolyte energy storage and device containing same".
- ^ "Reliance takes over Faradion for £100 million". electrive.com (in الإنجليزية الأمريكية). 2022-01-18. Retrieved 2022-10-29.
- ^ {{{1}}} patent {{{2}}} Filed by Faradion Limited on August 22, 2014.
- ^ "Faradion announces a collaboration and licensing deal with AMTE Power". Faradion (in الإنجليزية البريطانية). 2021-03-10. Retrieved 2021-11-07.
- ^ "ULTRA Safe AMTE A5" (PDF). May 2020.
- ^ "Dundee in running as battery cell pioneer AMTE Power closes in on UK 'gigafactory' site". www.scotsman.com (in الإنجليزية). 5 October 2021. Retrieved 2021-11-07.
- ^ Rudola, Ashish; Rennie, Anthony J. R.; Heap, Richard; Meysami, Seyyed Shayan; Lowbridge, Alex; Mazzali, Francesco; Sayers, Ruth; Wright, Christopher J.; Barker, Jerry (2021). "Commercialisation of high energy density sodium-ion batteries: Faradion's journey and outlook". Journal of Materials Chemistry A (in الإنجليزية). 9 (13): 8279–8302. doi:10.1039/d1ta00376c. ISSN 2050-7488. S2CID 233516956.
- ^ The Tesla Domain (November 6, 2022) (in en), THIS UK BASED SODIUM BATTERY THREATENS TO CHANGE THE EV INDUSTRY FOREVER!!, https://www.youtube.com/watch?v=JRNdOo3qQ-0, retrieved on 2022-11-27
- ^ https://faradion.co.uk/first-faradion-battery-installed-in-australia/
- ^ "Sodium to boost batteries by 2020". 2017 une année avec le CNRS. 2018-03-26. Retrieved 2019-09-05.
- ^ Broux, Thibault; Fauth, François; Hall, Nikita; Chatillon, Yohann; Bianchini, Matteo; Bamine, Tahya; Leriche, Jean‐Bernard; Suard, Emmanuelle; Carlier, Dany; Reynier, Yvan; Simonin, Loïc; Masquelier, Christian; Croguennec, Laurence (April 2019). "High Rate Performance for Carbon‐Coated Na 3V 2(PO20−4)F 3 in Na‐Ion Batteries". Small Methods (in الإنجليزية). 3 (4): 1800215. doi:10.1002/smtd.201800215. ISSN 2366-9608. S2CID 106396927.
- ^ Ponrouch, Alexandre; Dedryvère, Rémi; Monti, Damien; Demet, Atif E.; Ateba Mba, Jean Marcel; Croguennec, Laurence; Masquelier, Christian; Johansson, Patrik; Palacín, M. Rosa (2013). "Towards high energy density sodium ion batteries through electrolyte optimization". Energy & Environmental Science. 6 (8): 2361. doi:10.1039/c3ee41379a. ISSN 1754-5692.
- ^ Hall, N.; Boulineau, S.; Croguennec, L.; Launois, S.; Masquelier, C.; Simonin, L. (October 13, 2015). "Method for preparing a Na3V2(PO4)2F3 particulate material United States Patent Application No. 2018/0297847" (PDF).
- ^ "Tiamat |".
- ^ "Sodium-ion Battery Power Bank Operational in East China---Chinese Academy of Sciences". english.cas.cn. Retrieved 2019-09-05.
- ^ Patel, Prachi (2021-05-10). "Sodium-Ion Batteries Poised to Pick Off Large-Scale Lithium-Ion Applications". IEEE Spectrum: Technology, Engineering, and Science News (in الإنجليزية). Retrieved 2021-07-29.
- ^ "Researchers develop electric vehicle battery made from seawater and wood". Electric & Hybrid Vehicle Technology International (in الإنجليزية البريطانية). 2021-06-17. Retrieved 2021-07-29.
- ^ Reuters (2021-07-29). "China's CATL unveils sodium-ion battery - a first for a major car battery maker". Reuters (in الإنجليزية). Retrieved 2021-11-07.
{{cite news}}:|last=has generic name (help) - ^ Lykiardopoulou, Loanna (2021-11-10). "3 reasons why sodium-ion batteries may dethrone lithium". TNW. Retrieved 2021-11-13.
وصلات خارجية
- Ma, Bingyuan; Lee, Youngju; Bai, Peng (2021). "Dynamic Interfacial Stability Confirmed by Microscopic Optical Operando Experiments Enables High-Retention-Rate Anode-Free Na Metal Full Cells". Advanced Science (in الإنجليزية). 8 (12): 2005006. doi:10.1002/advs.202005006. ISSN 2198-3844. PMC 8224441. PMID 34194939.
- CS1 الإنجليزية الأمريكية-language sources (en-us)
- CS1 maint: url-status
- CS1 اليابانية-language sources (ja)
- CS1 الإنجليزية البريطانية-language sources (en-gb)
- CS1 errors: generic name
- Short description matches Wikidata
- Articles containing إنگليزية-language text
- مقالات ذات عبارات بحاجة لمصادر
- أنواع البطاريات
- بطاريات فلز-أيون