حبوب منع الحمل المركبة
حبوب منع الحمل المركبة (COCP)
| |
| خلفية | |
| B.C. type | ? |
| أول سنة | 1960 (الولايات المتحدة) |
| Failure rates (first year) | |
| الإستخدام الأمثل | 0.3% |
| الإستخدام النموذجي | 9% |
| الإستخدام | |
| مدة التأثير | 1 - 4 أيام |
| Reversibility | نعم |
| User reminders | تؤخذ في نفس الموعد كل يوم خلال الـ 24 ساعة |
| المتابعة الطبية | 6 أشهر |
| المزايا والعيوب | |
| الحماية من الأمراض المنقولة بالإتصال الجنسي | لا |
| الفترات | منظم، وغالباً ما يكون أخف وأقل إيلاماً |
| Weight | لا يوجد تأثير مثبت |
| المميزات | أدلة على انخفاض مخاطر الوفيات وانخفاض معدلات الوفيات في جميع أنواع السرطان. [1] احتمال انخفاض مخاطر المبيض و سرطان بطانة الرحم. [2][بحاجة لمصدر][بحاجة لمصدر] قد يعالج حب الشباب، متلازمة تكيس المبايض، اضطراب ما قبل الطمث الاكتئابي، انتباذ بطاني رحمي[بحاجة لمصدر] |
| المخاطر | زيادة طفيفة محتملة في بعض أنواع السرطان. [3][4] زيادة طفيفة عكوسة في تجلط الأوردة العميقة؛ سكتة، [5] مرض قلبي وعائي[6] |
| ملاحظات طبية | |
| تتأثر بالمضادات الحيوية ريفامپيسين، [7] وعشب Hypericum (نبتة سانت جونز) وبعض مضادات الصرع، وكذلك القيء أو الإسهال. الحذر إذا كان لديك تاريخ من الصداع النصفي. | |
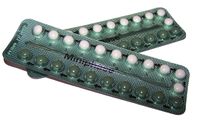
حبوب منع الحمل المركبة (COCP)، والتي يشار إليها غالباً باسم حبوب منع الحمل أو بالعامية باسم "الحبوب"، هي وسيلة من وسائل تحديد النسل التي يتم تناولها عن طريق الفم من قبل النساء. وهو يشتمل على مزيج من الإستروجن (عادةً إيثينيل إستراديول) و الپروجسترون (على وجه التحديد پروجستين). عندما يؤخذ بشكل صحيح، فإنه يغير الدورة الشهرية للتخلص من الإباضة ومنع الحمل.
تمت الموافقة عليها لأول مرة كموانع للحمل في الولايات المتحدة في عام 1960، وهي شكل شائع جداً لتحديد النسل. يتم استخدامها من قبل أكثر من 100 مليون امرأة في جميع أنحاء العالم ونحو 12 مليون امرأة في الولايات المتحدة. [8]من عام 2015 إلى عام 2017، أبلغت 12.6٪ من النساء اللائي تتراوح أعمارهن بين 15 و 49 عاماً في الولايات المتحدة عن استخدام وسائل منع الحمل عن طريق الفم، مما يجعلها ثاني أكثر وسائل منع الحمل شيوعاً في هذه الفئة العمرية بينما تعقيم الإناث هي الطريقة الأكثر شيوعاً. [9] يختلف الاستخدام بشكل كبير حسب البلد، [10] والعمر والتعليم والحالة الاجتماعية. على سبيل المثا، ثلث النساء اللواتي تتراوح أعمارهن بين 16 و 49 عاماً في المملكة المتحدة يستخدمن حالياً إما حبوب منع الحمل المركبة أو حبوب منع الحمل الپروجستيرونية فقط (POP)، [11][12] مقارنة بأقل من 3٪ من النساء في اليابان (اعتباراً من 1950-2014 ). [13]
موانع الحمل الفموية المركبة مدرجة في قائمة منظمة الصحة العالمية للأدوية الأساسية. [14] كانت حبوب منع الحمل عاملاً محفزاً لـ الثورة الجنسية. [15]
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الاستخدام الطبي
الاستخدام لمنع الحمل
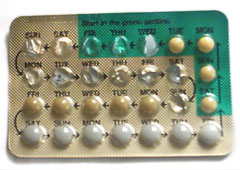
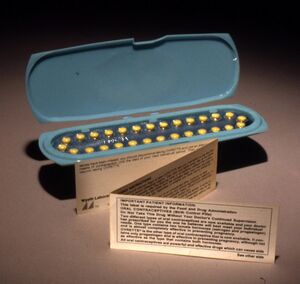
حبوب منع الحمل المركبة الفموية هي نوع من الأدوية التي يتم تناولها عن طريق الفم ويومياً في نفس الوقت من اليوم لمنع الحمل. [16][17] هناك العديد من التركيبات أو العلامات التجارية المختلفة، ولكن متوسط العبوة مصمم بحيث يتم تناوله على مدار 28 يوماً أو دورة شهرية. في أول 21 يوماً من الدورة، تتناول المستخدمات حبة يومية تحتوي على هرمونات (هرمون الاستروجين والبروجستيرون). الأيام السبعة الأخيرة من الدورة هي أيام خالية من الهرمونات. تحتوي بعض العبوات على 21 حبة فقط ومن ثم يُنصح المستخدمات بعدم تناول أي حبوب للأسبوع التالي. تحتوي العبوات الأخرى على 7 أقراص إضافية من دواء غفل، أو الحبوب غير النشطة بيولوجياً. تحتوي بعض التركيبات الأحدث على 24 يوماً من حبوب الهرمونات النشطة، تليها 4 أيام من العلاج الوهمي (تشمل الأمثلة Yaz 28 و Loestrin 24 Fe) أو حتى 84 يوماً من حبوب الهرمون النشطة، تليها 7 أيام من الحبوب الوهمية (موسمي). [16] ستصاب المرأة التي تتناول حبوب منع الحمل بالنزيف في وقت ما خلال تناول حبوب الدواء الغفل أو بدون تناول حبوب منع الحمل، وستظل محمية من الحمل خلال هذا الوقت. ثم بعد 28 يوماً، أو 91 يوماً اعتماداً على النوع الذي تستخدمه، تبدأ المستخدمات حزمة جديدة ودورة جديدة. [18]
الفعالية
إذا تم استخدامه تماماً وفقاً للتعليمات، فإن المخاطرة المقدرة للحمل هي 0.3 ٪، أو أن حوالي 3 من كل 1000 امرأة تستخدم حبوب منع الحمل المركبة ستحمل في غضون عام واحد. [19] ومع ذلك، غالباً ما يكون الاستخدام المعتاد غير دقيق بسبب أخطاء التوقيت أو الحبوب المنسية أو الآثار الجانبية غير المرغوب فيها. مع الاستخدام النموذجي، تبلغ المخاطرة المقدرة للحمل حوالي 9 ٪، أو حوالي 9 من كل 100 امرأة تستخدم حبوب منع الحمل المركبة ستحمل في غضون عام واحد. [20] يعتمد معدل فشل الاستخدام المثالي على مراجعة معدلات الحمل في التجارب السريرية، ويستند معدل فشل الاستخدام النموذجي إلى متوسط مرجح للتقديرات المأخوذة من المسوح الوطنية الأمريكية لنمو الأسرة (NSFG) لعامي 1995 و 2002، والتي تم تصحيحها بسبب نقص الإبلاغ عن عمليات الإجهاض. . [21]
هناك عدة عوامل تجعل فعالية الاستخدام النموذجي أقل من فعالية الاستخدام المثالي:
- أخطاء من جانب أولئك الذين يقدمون إرشادات حول كيفية استخدام الطريقة
- أخطاء من جانب المستخدمة
- وعي المستخدمة بعدم الامتثال للتعليمات.
على سبيل المثال، قد تحصل المرأة التي تستخدم وسائل منع الحمل الهرمونية فموياً على معلومات غير صحيحة من قبل مقدم الرعاية الصحية فيما يتعلق بتكرار تناوله، أو تنسى تناول حبوب منع الحمل يوماً ما، أو ببساطة لا تذهب إلى الصيدلية في الوقت المحدد لتجديد الوصفة الطبية.
توفر حبوب منع الحمل المركبة (COCPs) وسيلة فعالة لمنع الحمل من الحبة الأولى إذا تم البدء بها في غضون خمسة أيام من بداية الدورة الشهرية (خلال خمسة أيام من اليوم الأول من الحيض). إذا بدأت في أي وقت آخر في الدورة الشهرية، فإن COCPs توفر وسائل منع حمل فعالة فقط بعد 7 أيام متتالية من استخدام الحبوب الفعالة، لذلك يجب استخدام طريقة احتياطية لمنع الحمل (مثل الواقي الذكري) حتى يتم تناول الحبوب الفعالة لمدة 7 أيام متتالية. يجب أن تؤخذ حبوب منع الحمل المركبة (COCPs) في نفس الوقت تقريباً كل يوم. [22][23]
يبدو أن فعالية حبوب منع الحمل المركبة الفموية متشابهة سواء تم تناول الأقراص الفعالة بشكل مستمر لفترات طويلة من الوقت أو إذا تم تناولها لمدة 21 يوماً نشطاً و 7 أيام كدواء وهمي. [24]
قد تتأثر فعالية وسائل منع الحمل بوسائل عديدة. في أي من هذه الحالات، يجب استخدام طريقة احتياطية حتى يتم استئناف الاستخدام المتواصل للأقراص الفعالة (لمدة 7 أيام متتالية)، أو يتم إيقاف الدواء المتفاعل أو معالجة المرض. [22]
العوامل التي قد تساهم في انخفاض الفعالية:[22]
- تفويت تناول أكثر من حبة من الحزمة،
- التأخير في بدء الحزمة التالية من الحبوب النشطة (أي تمديد فترة الحبوب الخالية من حبوب منع الحمل أو غير الفعالة أو الدواء الوهمي إلى ما بعد 7 أيام)،
- سوء امتصاص الأمعاء للحبوب الفعالة بسبب القيء أو الإسهال،
- التفاعلات الدوائية مع الحبوب الفعالة التي تقلل من مستويات هرمون الاستروجين أو البروجسترون المانعة للحمل. [22]
وفقاً لإرشادات مراكز السيطرة على الأمراض والوقاية منها، لا تعتبر حبوب منع الحمل "قد تم تفويتها" إلا إذا مرت 24 ساعة أو أكثر منذ آخر حبة تم تناولها. إذا مر أقل من 24 ساعة، تعتبر حبوب منع الحمل "متأخرة" .[19]
دور الدواء الغفل
إن دور الدواء الغفل ذو شقين: للسماح للمستخدمة بمواصلة روتين تناول حبوب منع الحمل كل يوم ومحاكاة متوسط الدورة الشهرية. من خلال الاستمرار في تناول حبوب منع الحمل يومياً، تظل المستخدمات في العادة اليومية حتى خلال الأسبوع بدون هرمونات. لا يؤثر عدم تناول الحبوب خلال أسبوع الدواء الغفل على فعالية حبوب منع الحمل، بشرط استئناف الابتلاع اليومي للحبوب الفعالة في نهاية الأسبوع. [25]
يحاكي الأسبوع الوهمي، أو الخالي من الهرمونات، في حزمة حبوب منع الحمل التي تبلغ مدتها 28 يوماً، متوسط الدورة الشهرية، على الرغم من أن الأحداث الهرمونية خلال دورة حبوب منع الحمل تختلف اختلافاً كبيراً عن تلك الخاصة بدورة الطمث الطبيعية. نظراً لأن حبوب منع الحمل تمنع الإباضة (ستتم مناقشتها أكثر في قسم آلية العمل)، لا تعاني مستخدمات تحديد النسل من فترات طمث حقيقية. بدلاً من ذلك، فإن نقص الهرمونات لمدة أسبوع هو الذي يسبب النزيف الانسحابي. [17] يُعتقد أن نزيف الانسحاب الذي يحدث أثناء التوقف عن تناول الحبوب الفعالة مطمئن، وهو تأكيد مادي على عدم الحمل. [26] نزيف الانسحاب يمكن التنبؤ به أيضاً. يمكن أن يكون النزيف الاختراقي غير المتوقع من الآثار الجانبية المحتملة للأنظمة النشطة طويلة المدى. [27]
نظراً لأنه من المألوف أن تصاب النساء في فترة الحيض بفقر الدم، فقد تحتوي بعض حبوب الدواء الغفل على مكمل الحديد. [28][29] فهذا يجدد مخازن الحديد التي قد تنضب أثناء الحيض. بالإضافة إلى ذلك، يتم أحياناً تقوية حبوب منع الحمل، مثل حبوب منع الحمل المركبة، بـ حمض الفوليك حيث يوصى بتناول مكملات حمض الفوليك في الأشهر المسبقة للحمل لتقليل احتمالية عيب الأنبوب العصبي عند الرضع. [30][31]
الامتناع او التقليل من دواء الغفل
إذا كانت تركيبة حبوب منع الحمل أحادية الطور، بمعنى أن كل حبة هرمونية تحتوي على جرعة ثابتة من الهرمونات، فمن الممكن تخطي النزيف الانسحابي وتظل محمية من الحمل عن طريق تخطي حبوب الدواء الغفل تماماً والبدء مباشرة بالعلبة التالية. إن محاولة ذلك باستخدام تركيبات أقراص ثنائية أو ثلاثية الطور تحمل مخاطر متزايدة من حدوث نزيف مفاجئ وقد يكون غير مرغوب فيه. ومع ذلك، فإنه لن يزيد من مخاطر الحمل.
بدءاً من عام 2003، تمكنت النساء أيضاً من استخدام نسخة من حبوب منع الحمل مدتها ثلاثة أشهر. [32] على غرار تأثير استخدام تركيبة الجرعات الثابتة وتخطي أسابيع الدواء الغفل لمدة ثلاثة أشهر، تعطي الحبوب الموسمية فوائد فترات أقل تواتر، في العيب المحتمل للنزيف الاختراقي. سيزونيك هو نسخة أخرى يتم فيها استبدال أسبوع الدواء الغفل كل ثلاثة أشهر بأسبوع من جرعة منخفضة من هرمون الاستروجين.
تم أيضاً تعبئة نسخة من حبوب منع الحمل المركبة للتخلص تماماً من حبوب الدواء الغفل والنزيف الانسحابي. تم تسويقه باسم Anya أو Lybrel، وقد أظهرت الدراسات أنه بعد سبعة أشهر، لم تعد 71 ٪ من المستخدمات يعانين من أي نزيف مفاجئ، وهو الأثر الجانبي الأكثر شيوعاً المتمثل في الذهاب لفترات أطول من الوقت دون فترات راحة من الحبوب الفعالة.
بينما يلزم إجراء المزيد من الأبحاث لتقييم السلامة طويلة المدى لاستخدام حبوب منع الحمل المركبة بشكل مستمر، فقد أظهرت الدراسات أنه قد لا يكون هناك اختلاف في الآثار الضارة قصيرة المدى عند مقارنة الاستخدام المستمر مقابل الاستخدام الدوري لحبوب منع الحمل. [33]
الاستخدام غير المانع للحمل
تم استخدام الهرمونات الموجودة في حبوب منع الحمل أيضاً لعلاج حالات طبية أخرى، مثل متلازمة المبيض متعدد الأكياس (متلازمة تكيس المبايض)، انتباذ بطاني رحمي، العضال الغدي، حب الشباب، الشعرانية، انقطاع الطمث، تقلصات الدورة الشهرية، صداع الدورة الشهرية، غزارة الطمث (نزيف الحيض المفرط)، فقر الدم المرتبط بالحيض أو الورم الليفي وعسر الطمث (الحيض المؤلم).[20][34] إلى جانب حب الشباب، لم توافق إدارة الغذاء والدواء الأمريكية على موانع الحمل الفموية للاستخدامات المذكورة سابقاً على الرغم من الاستخدام المكثف لهذه الحالات. [35]
متلازمة تكيس المبايض
متلازمة تكيس المبايض، أو PCOS، هي متلازمة تسببها اختلالات هرمونية. غالباً ما يكون لدى النساء المصابات بمتلازمة تكيس المبايض مستويات من هرمون الاستروجين أعلى من الطبيعي طوال الوقت لأن دوراتهن الهرمونية ليست منتظمة. [17] بمرور الوقت، يمكن أن تؤدي المستويات العالية من هرمون الاستروجين غير المقيد إلى تضخم بطانة الرحم، أو فرط نمو الأنسجة في الرحم. من المرجح أن يصبح هذا النمو الزائد سرطانياً أكثر من نسيج بطانة الرحم الطبيعي. [36] وبالتالي، على الرغم من اختلاف البيانات، إلا أنه متفق عموماً من قبل معظم مجمعات أمراض النساء على أنه نظراً لارتفاع مستويات هرمون الاستروجين لدى النساء المصابات بمتلازمة تكيس المبايض، فإنهن أكثر عرضة للإصابة بتضخم بطانة الرحم. [37]لتقليل هذا الخطر، يوصى غالباً بأن تأخذ النساء المصابات بالـ PCOS موانع الحمل الهرمونية لتنظيم هرموناتهن. يوصى باستخدام كل من حبوب منع الحمل المركبة وطرق البروجستين فقط. حبوب منع الحمل المركبة مفضلة لدى النساء اللواتي يعانين أيضاً من حب الشباب غير المنضبط وأعراض الشعرانية، أو نمو الشعر ذي النمط الذكوري، لأن حبوب منع الحمل المركبة يمكن أن تساعد في علاج هذه الأعراض. [17]
بطانة الرحم
بالنسبة لألم الحوض المرتبط بالانتباذ البطاني الرحمي، تعتبر حبوب منع الحمل المركبة علاجاً طبياً من الدرجة الأولى، جنباً إلى جنب مع مضادات الالتهاب غير الستيروئيدية ومنبهات GnRH ومثبطات الأروماتاز. [38] تعمل حبوب منع الحمل المركبة على قمع نمو أنسجة بطانة الرحم خارج الرحم. هذا يعمل على تقليل آثاره الالتهابية. [17] لا تقضي حبوب منع الحمل المركبة، جنباً إلى جنب مع العلاجات الطبية الأخرى المذكورة أعلاه، على نمو أنسجة الرحم خارج الرحم، بل تقلل الأعراض فقط. الجراحة هي العلاج الوحيد النهائي. أظهرت الدراسات التي تبحث في معدلات تكرار آلام الحوض بعد الجراحة أن الاستخدام المستمر لـ حبوب منع الحمل المركبة أكثر فعالية في الحد من تكرار الألم من الاستخدام الدوري. [39]
العضال الغدي
على غرار الانتباذ البطاني الرحمي، غالباً ما يتم علاج العضال الغدي باستخدام حبوب منع الحمل المركبة لقمع نمو أنسجة بطانة الرحم التي نمت إلى عضل الرحم. على عكس الانتباذ البطاني الرحمي، فإن الليفونورجيتريل المحتوي على اللولب الرحمي يكون أكثر فعالية في الحد من آلام الحوض في العضال الغدي من حبوب منع الحمل المركبة. [17]
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
حب الشباب
توصف موانع الحمل الفموية المركبة أحياناً كدواء لعلاج حب الشباب الخفيف أو المعتدل، على الرغم من عدم موافقة إدارة الغذاء والدواء الأمريكية على أي منها لهذا الغرض الوحيد. [40] تمت الموافقة على أربع موانع حمل فموية مختلفة لعلاج حب الشباب المعتدل إذا كان الشخص يبلغ من العمر 14 أو 15 عاماً على الأقل، وقد بدأ الحيض بالفعل ويحتاج إلى وسائل منع الحمل. وتشمل هذه الأدوية Ortho Tri-Cyclen وEstrostep و Beyaz و YAZ.[41][42][43]
انقطاع الطمث
على الرغم من أن حبوب منع الحمل توصف أحياناً للحث على الحيض وفقاً لجدول زمني منتظم للنساء اللائي تزعجهن دورات الحيض غير المنتظمة، إلا أنها في الواقع تثبط الدورة الشهرية الطبيعية ثم تحاكي الدورة الشهرية العادية التي تبلغ 28 يوماً.
توصف أحياناً للنساء اللاتي يعانين من ضعف الدورة الشهرية بسبب ثالوث الأنثى الرياضية موانع الحمل الفموية كأقراص والتي يمكن أن تؤدي إلى دورات نزيف حيض. [44]ومع ذلك، فإن السبب الأساسي للحالة هو نقص الطاقة ويجب معالجته عن طريق تصحيح عدم التوازن بين السعرات الحرارية التي يتم تناولها والسعرات الحرارية التي يتم حرقها عن طريق التمرين. لا ينبغي استخدام موانع الحمل الفموية كعلاج أولي للثالوث الرياضي. [44]
موانع الاستعمال
في حين أن موانع الحمل الفموية المركبة تعتبر بشكل عام دواء آمناً نسبياً، إلا أنها ممنوعة للأشخاص الذين يعانون من حالات طبية معينة. تنشر منظمة الصحة العالمية ومراكز السيطرة على الأمراض والوقاية منها إرشادات، تسمى معايير الأهلية الطبية، بشأن سلامة وسائل منع الحمل في سياق الإجراءات الطبية الظروف. يمكن أن يزيد الإستروجين بجرعات عالية من خطر إصابة الشخص بجلطات الدم. يعاني جميع مستخدمي حبوب منع الحمل المركبة من زيادة طفيفة في خطر الإصابة بالجلطات الدموية الوريدية مقارنةً بغير المستخدمين؛ هذه المخاطر هي الأكبر خلال السنة الأولى من استخدام حبوب منع الحمل المركبة. [45]النساء اللواتي يعانين من أي حالة طبية موجودة مسبقاً تزيد أيضاً من خطر الإصابة بجلطات الدم لديهم زيادة كبيرة في خطر الإصابة بأحداث التخثر باستخدام حبوب منع الحمل المركبة. [45] تشمل هذه الحالات، على سبيل المثال لا الحصر، ارتفاع ضغط الدم، مرض قلبي وعائي (مثل مرض القلب الصمامي أو مرض القلب الإقفاري [46])، تاريخ الانصمام الخثاري أو الانسداد الرئوي، والحوادث الوعائية الدماغية، والميل الوراثي لتكوين جلطات دموية (مثل العامل الخامس لايدن الوراثي) .[47] هناك حالات تؤدي، عند ارتباطها باستخدام حبوب منع الحمل المركبة، إلى زيادة مخاطر الآثار الضارة بخلاف تجلط الدم. على سبيل المثال، النساء اللواتي لديهن تاريخ من الصداع النصفي مع الأورة يكون لديهن مخاطر متزايدة بالسكتة عند استخدام حبوب منع الحمل المركبة، و المدخنات فوق سن 35 عاماً ويستخدمون حبوب منع الحمل المركبة هن أكثر عرضة لخطر احتشاء قلبي. [48]
كما يُمنع تناول حبوب منع الحمل المركبة أيضاً للأشخاص المصابين بمرض السكري المتقدم، وأورام الكبد، الورم الحميد الكبدي أو تليف كبدي حاد.[20][47] يتم استقلاب حبوب منع الحمل المركبة في الكبد وبالتالي يمكن أن يؤدي مرض الكبد إلى تقليل التخلص من الدواء. يجب على الأشخاص الذين يعانون من سرطان الثدي المعروف أو المشتبه به، أو سرطان بطانة الرحم، أو نزيف الرحم غير المبرر ألا يأخذوا حبوب منع الحمل المركبة لتجنب المخاطر الصحية. [46]
يجب على النساء المعروفات أنهن حوامل ألا يأخذن حبوب منع الحمل المركبة. يُنصح أيضاً النساء المرضعات بعد الولادة بعدم البدء بـ حبوب منع الحمل المركبة إلا بعد 4 أسابيع من الولادة بسبب زيادة خطر الإصابة بجلطات الدم. [19] في حين أظهرت الدراسات نتائج متضاربة حول تأثيرات COCPs على مدة الرضاعة وكمية الحليب، توجد مخاوف بشأن المخاطر العابرة لـ COCPs على إنتاج حليب الثدي عند بدء الرضاعة الطبيعية في وقت مبكر بعد الولادة. [49] نظراً للمخاطر المذكورة والمخاوف الإضافية المتعلقة بالرضاعة، لا يُنصح النساء المرضعات ببدء COCPs حتى ستة أسابيع على الأقل بعد الولادة، في حين أن النساء اللواتي لا يرضعن من الثدي وليس لديهن عوامل خطر أخرى لجلطات الدم قد يبدأن COCPs بعد 21 يوماً بعد الولادة. [50][48] يعد فرط كولسترول الدم وفرط شحوم الدم من موانع الاستعمال حالياً، لكن الأدلة التي تظهر أن حبوب منع الحمل المركبة تؤدي إلى نتائج أسوأ في هذه الفئة ضعيفة. [17][19] السمنة لا تعتبر موانع لأخذ حبوب منع الحمل االمركبة.[19]
الآثار الجانبية
من المتفق عليه عموماً أن المخاطر الصحية لموانع الحمل الفموية أقل من مخاطر الحمل والولادة، [51] و"الفوائد الصحية لأي طريقة لمنع الحمل أكبر بكثير من أي المخاطر الناتجة عنها".[52] جادلت بعض المنظمات بأن مقارنة وسيلة منع الحمل مع عدم استخدام وسيلة (الحمل) ليست مرتبطة- وبدلاً من ذلك، يجب أن تكون المقارنة بين في درجات الأمان بين وسائل منع الحمل المتاحة. [53]
الشائع
تشير المصادر المختلفة إلى حالات مختلفة من الآثار الجانبية. التأثير الجانبي الأكثر شيوعاً هو النزيف الاختراقي. ذكرت مقالة مراجعة فرنسية عام 1992 أن ما يصل إلى 50٪ من المستخدمات الجدد لأول مرة يتوقفن عن تناول حبوب منع الحمل قبل نهاية العام الأول بسبب الانزعاج من الآثار الجانبية مثل النزيف المفاجئ وانقطاع الطمث. [54] وجدت دراسة أجراها معهد كينزي عام 2001 لاستكشاف تنبؤات التوقف عن تناول موانع الحمل الفموية أن 47٪ من 79 امرأة توقفن عن تناول حبوب منع الحمل. [55] وجدت إحدى الدراسات التي أجريت عام 1994 أن النساء اللواتي يستخدمن حبوب منع الحمل تراجعت بنسبة 32 ٪ أكثر من أولئك الذين لا يستخدمون وسائل منع الحمل.[56]
من ناحية أخرى، يمكن للحبوب في بعض الأحيان تحسين حالات مثل عسر الطمث ومتلازمة ما قبل الحيض وحب الشباب، [57]وتقليل أعراض الانتباذ البطاني الرحمي ومتلازمة المبيض المتعدد الكيسات، وتقليل خطر الإصابة بفقر الدم. [58] يقلل استخدام موانع الحمل الفموية أيضاً من خطر الإصابة بسرطان المبيض وسرطان بطانة الرحم مدى الحياة. [59][60][61]
قد يحدث الغثيان والقيء والصداع والانتفاخ وألم الثدي وتورم الكاحلين / القدمين (احتباس السوائل) أو تغير الوزن. قد يحدث نزيف مهبلي بين فترات ضائعة/غير منتظمة، خاصة خلال الأشهر القليلة الأولى من الاستخدام. [62]
القلب والأوعية الدموية
تزيد موانع الحمل الفموية المشتركة من خطر الجلطات الدموية الوريدية (بما في ذلك تجلط الأوردة العميقة (DVT) والانصمام الرئوي (PE)).[63]
في حين أن الجرعات المنخفضة من الاستروجين في حبوب موانع الحمل الفموية قد يكون لها خطر أقل للإصابة بالسكتة واحتشاء قلبي مقارنة بحبوب الاستروجين ذات الجرعات العالية (50 ميكروغرام / باليوم)، لا تزال مستخدمات حبوب منع الحمل ذات الجرعات المنخفضة من هرمون الاستروجين يعانين من زيادة مقارنة بغير المستخدمات. [64] تكون هذه المخاطر أكبر عند النساء اللواتي لديهن عوامل خطر إضافية، مثل التدخين (الذي يزيد المخاطر بشكل كبير) والاستخدام المستمر للحبوب لفترة طويلة، خاصة عند النساء فوق سن 35 عاماً. [65]
يبلغ الخطر الإجمالي المطلق للتخثر الوريدي لكل 100000 امرأة في الاستخدام الحالي لوسائل منع الحمل الفموية المشتركة 60 تقريباً، مقارنة بـ 30 لدى غير المستخدمات. [66] يختلف خطر الإصابة بالجلطات الدموية باختلاف أنواع حبوب منع الحمل؛ بالمقارنة مع موانع الحمل الفموية المركبة التي تحتوي على الليفونورجستريل (LNG)، وبنفس جرعة الإستروجين ومدة الاستخدام، فإن معدل الخثار الوريدي العميق لموانع الحمل الفموية المركبة مع نوريثيستيرون هو 0.98، مع نورگيستيمات 1.19، مع ديزوگيسترل (DSG) 1.82، مع جيستودين 1.86 ، مع دروسپيرينون (DRSP) 1.64، ومع سيپروتيرون أسيتات 1.88. [66] بالمقارنة، تحدث الجلطات الدموية الوريدية في 100-200 لكل 100.000 امرأة حامل كل عام. [66]
أظهرت إحدى الدراسات زيادة خطر الإصابة بجلطات الدم بنسبة تزيد عن 600٪ لدى النساء اللائي يتناولن حبوب منع الحمل المركبة مع دروسبيرينون مقارنة بغير المستخدمات، مقارنة مع النساء اللاتي يتناولن حبوب منع الحمل التي تحتوي على الليفونورجيستريل بنسبة 360٪. [67] بدأت إدارة الغذاء والدواء الأمريكية (FDA) دراسات لتقييم صحة أكثر من 800000 امرأة يتناولن حبوب منع الحمل المركبة COCPs ووجدت أن خطر الإصابة بالجلطات الدموية الوريدية كان أعلى بنسبة 93٪ بالنسبة للنساء اللواتي تناولن COCPs دروسبيرينون لمدة 3 أشهر أو أقل و 290٪ أعلى من أجل النساء اللائي يتناولن COCPs دروسبيرينون لمدة 7-12 شهراً، مقارنة بالنساء اللائي يتناولن أنواعاً أخرى من موانع الحمل الفموية. [68]
بناءً على هذه الدراسات، في عام 2012، قامت إدارة الغذاء والدواء بتحديث الملصق الخاص بدروسبيرينون COCPs لتشمل تحذيراً من أن موانع الحمل التي تحتوي على دروسبيرينون قد تكون أكثر عرضة لجلطات دموية خطيرة. [69]
قالب:Risk of venous thromboembolism with hormone therapy and birth control pills (QResearch/CPRD)
السرطان
لم تدعم مراجعة منهجية في عام 2010 زيادة خطر الإصابة بالسرطان بشكل عام لدى مستخدمات حبوب منع الحمل المركبة، ولكنها وجدت زيادة طفيفة في خطر الإصابة بـسرطان الثدي بين المستخدمات الحاليات، والتي تختفي بعد 5-10 سنوات من توقف الاستخدام. [70]
التأثيرات الوقائية
تقلل حبوب منع الحمل المركبة من مخاطر سرطان المبيض، سرطان بطانة الرحم،[22] وسرطان القولون والمستقيم. [3][57][71]وجدت دراستان كبيرتان نُشرتا في عام 2010 انخفاضاً كبيراً في الخطر النسبي المعدل لوفيات سرطان المبيض وسرطان بطانة الرحم لدى مستخدمات موانع الحمل الفموية بشكل دائم مقارنة بنساء لم تستخدمنها أبداً. [1][72]
يقلل استخدام موانع الحمل الفموية (حبوب منع الحمل) لمدة خمس سنوات أو أكثر من خطر الإصابة بسرطان المبيض في الحياة اللاحقة بنسبة 50٪. [71] يقلل الاستخدام المشترك لوسائل منع الحمل عن طريق الفم من خطر سرطان المبيض بنسبة 40٪ وخطر سرطان بطانة الرحم بنسبة 50٪ بنساء لم تستخدمنها أبداً. يزداد الحد من المخاطر مع مدة الاستخدام، مع انخفاض بنسبة 80٪ في خطر الإصابة بسرطان المبيض وسرطان بطانة الرحم مع الاستخدام لأكثر من 10 سنوات. يستمر الحد من مخاطر الإصابة بسرطان المبيض وبطانة الرحم لمدة 20 عاماً على الأقل.[22]
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
زيادة المخاطر
أفاد تقرير صادر عام 2005 عن مجموعة عمل الوكالة الدولية لأبحاث السرطان (IARC) أن موانع الحمل الفموية تزيد من خطر الإصابة بسرطان الثدي (بين المستخدمات الحاليات والحديثات)، [3] عنق الرحم و الكبد (بين المعرضات لخطر منخفض للإصابة بفيروس التهاب الكبد B). [3] خلص التحليل التلوي لعام 2013 إلى أن كل استخدام لحبوب منع الحمل يرتبط بزيادة طفيفة في خطر الإصابة بسرطان الثدي (الخطر النسبي 1.08) وانخفاض خطر الإصابة بسرطان القولون والمستقيم (الخطر النسبي 0.86) وسرطان بطانة الرحم ( الخطر النسبي 0.57). يزداد خطر الإصابة بسرطان عنق الرحم لدى المصابين بفيروس الورم الحليمي البشري.[73]لوحظت زيادة طفيفة مماثلة في خطر الإصابة بسرطان الثدي في تحليلات تلوية أخرى.[74][75]
الوزن
وجدت مراجعة منهجية لكوكران 2013 أن دراسات موانع الحمل الهرمونية المركبة لم تظهر فرقاً كبيراً في الوزن عند مقارنتها بالدواء الغفل أو عدم وجود مجموعات تخلل. [76]لم تكن الأدلة قوية بما يكفي للتأكد من أن وسائل منع الحمل لا تسبب بعض التغيير في الوزن، ولكن لم يتم العثور على تأثير كبير. [76] ووجدت هذه المراجعة أيضاً أن "النساء لم يتوقفن عن استخدام حبوب منع الحمل أو اللاصقة بسبب تغير الوزن". [76]
الجنسانية
حبوب منع الحمل المركبة قد تزيد من ترطيب المهبل. [77] تعاني النساء الأخريات من انخفاض في الرغبة الجنسية أثناء تناول حبوب منع الحمل، أو انخفاض في الترطيب. [77][78] يشكك بعض الباحثين في وجود علاقة سببية بين استخدام COCP وانخفاض الرغبة الجنسية؛ [79] وجدت دراسة أجريت عام 2007 على 1700 امرأة أن مستخدمات COCP لم يشهدن أي تغيير في الإشباع الجنسي.[80]اختبرت دراسة معملية أُجريت عام 2005 عن الإثارة التناسلية أربعة عشر امرأة قبل وبعد أن بدأن في تناول الـ COCPs. وجدت الدراسة أن النساء عانين من مجموعة واسعة من الاستجابات الاستثارية بعد البدء في استخدام حبوب منع الحمل. كانت الانخفاضات والزيادات في مقاييس الاستثارة شائعة بشكل متساوٍ. [81][82]
قامت دراسة أجريت عام 2006 على 124 امرأة في سن اليأس بقياس الگلوبيولين المرتبط بالهرمونات الجنسية (SHBG)، بما في ذلك قبل وبعد التوقف عن تناول حبوب منع الحمل الفموية. كان لدى النساء اللائي استمرن في استخدام موانع الحمل الفموية مستويات SHBG أعلى بأربع مرات من أولئك الذين لم يستخدموه مطلقاً، وظلت المستويات مرتفعة حتى في المجموعة التي توقفت عن استخدامه. [83][84] من الناحية النظرية، قد تكون الزيادة في SHBG استجابة فسيولوجية لزيادة مستويات الهرمون، ولكنها قد تقلل من المستويات الحرة للهرمونات الأخرى، مثل الأندروجينات، بسبب عدم خصوصية ارتباط الهرمونات الجنسية.
وجدت دراسة أُجريت عام 2007 أن حبوب منع الحمل يمكن أن يكون لها تأثير سلبي على الجاذبية الجنسية: وجد العلماء أن الراقصات اللواتي كن في حالة شبق يتلقون بقشيش أكثر بكثير من أولئك الذين لم يكن كذلك، في حين أن أولئك الذين يتناولون حبوب منع الحمل الفموية لم يكن لديهن مثل هذه الأرباح. [85]
الاكتئاب
تم ربط المستويات المنخفضة من السروتونين، وهو ناقل عصبي في الدماغ، بـ الاكتئاب. أظهرت المستويات العالية من الإستروجين، كما هو الحال في الجيل الأول من حبوب منع الحمل المركبة، والبروجستين، كما هو الحال في بعض موانع الحمل التي تحتوي على البروجستين فقط، أنها تخفض مستويات السروتونين في الدماغ عن طريق زيادة تركيز إنزيم الدماغ الذي يقلل من السروتونين. اقترحت مجموعة متزايدة من الأدلة البحثية أن موانع الحمل الهرمونية قد يكون لها تأثير سلبي على الصحة النفسية للمرأة. [86][87][88] في عام 2016، أظهرت دراسة دنماركية كبيرة شملت مليون امرأة (تمت المتابعة من يناير 2000 إلى ديسمبر 2013) أن استخدام COCPs، خاصة بين المراهقات، كان مرتبطاً بزيادة خطر الإصابة بالاكتئاب اللاحق بشكل كبير إحصائياً، على الرغم من أحجام التأثيرات صغيرة (على سبيل المثال، تم وصف 2.1٪ من النساء اللواتي تناولن أي شكل من أشكال تحديد النسل عن طريق الفم لأول مرة بمضادات الاكتئاب، مقارنة بـ 1.7٪ من النساء في المجموعة الضابطة). [87] وبالمثل، في عام 2018، نُشرت النتائج المستخلصة من دراسة جماعية سويدية واسعة النطاق على الصعيد الوطني للتحقيق في تأثير موانع الحمل الهرمونية على الصحة النفسية بين النساء (العدد = 815662، الذين تتراوح أعمارهم بين 12 و 30 عاماً)، والتي تم نشرها، مما يبرز الارتباط بين وسائل منع الحمل الهرمونية والاستخدام اللاحق للعقاقير المؤثرة على العقل للنساء في سن الإنجاب. [88] كان هذا الارتباط كبيراً بشكل خاص للمراهقات الصغار (الذين تتراوح أعمارهم بين 12 و 19 عاماً) .[88]يدعو المؤلفون إلى مزيد من البحث في تأثير أنواع مختلفة من موانع الحمل الهرمونية على الصحة النفسية للشابات. [88]
من المعروف أن موانع الحمل التي تحتوي على البروجستين فقط تؤدي إلى تفاقم حالة النساء المصابات بالاكتئاب بالفعل.[89][90]ومع ذلك، فإن الكتب المرجعية الطبية الحالية حول وسائل منع الحمل [22] والمنظمات الرئيسية مثل ACOG الأمريكية,[91] منظمة الصحة العالمية ,[92] و RCOG في المملكة المتحدة [93] توافق على أن الأدلة الحالية تشير إلى أن جرعة منخفضة من موانع الحمل الفموية المركبة من غير المرجح أن تزيد من خطر الإصابة بالاكتئاب، ومن غير المرجح أن تؤدي إلى تفاقم الحالة لدى النساء المصابات بالاكتئاب حالياً.
ارتفاع ضغط الدم
البراديكينين يخفض ضغط الدم عن طريق التسبب في تمدد الأوعية الدموية. بعض الإنزيمات قادرة على تكسير البراديكينين (الإنزيم المحول للأنجيوتنسين، أمينوبيبتيداز P). يمكن أن يزيد البروجسترون من مستويات أمينوبيبتيداز P (AP-P)، وبالتالي يزيد من انهيار البراديكينين، مما يزيد من خطر الإصابة بارتفاع ضغط الدم. [94]
تأثيرات أخرى
الآثار الجانبية الأخرى المرتبطة بجرعات منخفضة من COCPs هي الثر الأبيض (زيادة إفرازات المهبل)، وانخفاض في تدفق الدورة الشهرية، ألم الثدي (إيلام الثدي)، وانخفاض في حب الشباب. تشمل الآثار الجانبية المرتبطة بجرعات عالية من COCPs الغثيان، القيء، والزيادات في ضغط الدم، والكلف (تغير لون بشرة الوجه)؛ لا ترتبط هذه التأثيرات بشدة بتركيبات الجرعات المنخفضة.[بحاجة للاستشهاد الطبي]
يبدو أن الإستروجين الزائد، مثل من حبوب منع الحمل، يزيد من مستويات الكوليسترول في الصفراء ويقلل من حركة المرارة، مما قد يؤدي إلى حصاة صفراوية. [95] البروجستين الموجودة في تركيبات معينة من حبوب منع الحمل يمكن أن تحد من فعالية تمارين الأثقال لزيادة كتلة العضلات. [96] يحدث هذا التأثير بسبب قدرة بعض البروجستين على تثبيط مستقبلات الأندروجن. تزعم إحدى الدراسات أن حبوب منع الحمل قد تؤثر على ما تفضله المرأة من روائح جسد الرجل، مما قد يؤثر بدوره على اختيار الشريك. [97][98][99]يرتبط استخدام موانع الحمل الفموية المشتركة بانخفاض خطر الإصابة بانتباذ بطاني رحمي، مما يعطي خطراً نسبياً للانتباذ البطاني الرحمي يبلغ 0.63 أثناء الاستخدام النشط، ولكن مع جودة أدلة محدودة وفقاً لـمراجعة منهجية. [100]
تقلل موانع الحمل الفموية المركبة إجمالي مستويات التستوستيرون بحوالي 0.5 نانومول / لتر، وهرمون التستوستيرون الحر بنسبة 60٪ تقريباً، وتزيد من كمية الجلوبيولين المرتبط بالهرمون الجنسي (SHBG) بنحو 100 نانومول / لتر. تم العثور على موانع الحمل التي تحتوي على الجيل الثاني من البروجستين و / أو جرعات الاستروجين من حوالي 20-25 ملغ EE ليكون لها تأثير أقل على تركيزات SHBG. [101] قد تؤدي وسائل منع الحمل الفموية المركبة أيضاً إلى تقليل كثافة العظام. [102]
التفاعلات الدوائية
تقلل بعض الأدوية من تأثير حبوب منع الحمل ويمكن أن تسبب نزيف اختراقي، أو تزيد من فرصة الحمل. وتشمل هذه الأدوية مثل ريفامپيسين وباربيتيورات وفنيتوين وكاربامازپين. بالإضافة إلى ذلك، يتم إعطاء تنبيهات حول المضادات الحيوية واسعة النطاق، مثل أمپيسيلين و دوكسيسايكلين، والتي قد تسبب مشاكل "من خلال إضعاف البكتيريا المسؤولة عن إعادة تدوير استراديول الإيثينيل من الأمعاء الغليظة "( BNF 2003) .[103][104][105][106]
تم أيضاً تورط نبتة القديس يوحنا الطبية التقليدية بسبب تنظيمها لنظام P450 في الكبد والذي يمكن أن يزيد من استقلاب الإيثينيل استراديول ومكونات البروجستين لبعض وسائل منع الحمل الفموية المركبة.[107]
آلية العمل
تم تطوير حبوب منع الحمل المركبة COCPs لمنع الإباضة عن طريق قمع إطلاق الگونادوتروپين. موانع الحمل الهرمونية المركبة، بما في ذلك COCPs، تمنع التطور الجريبي وتمنع الإباضة كآلية أساسية للعمل .[108][109][110][111]
يقلل الارتجاع السلبي للبروجستوجين من تواتر النبض لهرمون مطلق لموجهة الغدد التناسلية (GnRH) الذي يطلقه الوطاء، مما يقلل من إفراز هرمون منبه للجريب (FSH) وبشكل كبير يقلل من إفراز الهرمون المنشط للجسم الأصفر (LH) بواسطة النخامية الأمامية. انخفاض مستويات هرمون FSH يمنع نمو الجريبات، مما يمنع زيادة مستويات إستراديول. الارتجاع السلبي للبروجستيرون ونقص الارتجاع الإيجابي من هرمون الاستروجين على إفراز LH يمنع تدفقه في منتصف الدورة. إن تثبيط نمو المسام وغياب تدفق الهرمون المنشط للجسم الأصفر يمنعان الإباضة.[108][109][110]
تم تضمين الإستروجين في الأصل في موانع الحمل الفموية للتحكم بشكل أفضل في الدورة (لتثبيت بطانة الرحم وبالتالي تقليل حدوث نزيف اختراق)، ولكن وجد أيضاً أنه يثبط نمو المسام ويساعد على منع الإباضة. الارتجاع السلبي للإستروجين على الغدة النخامية الأمامية يقلل بشكل كبير من إفراز هرمون FSH، مما يثبّط نمو المسام ويساعد على منع الإباضة. [108][109][110]
آلية أساسية أخرى لعمل جميع موانع الحمل التي تحتوي على البروجستيرون وهي منع تغلل الحيوانات المنوية عبر عنق الرحم في الجهاز التناسلي العلوي (الرحم و قناة فالوب) عن طريق تقليل محتوى الماء وزيادة لزوجة مخاط عنق الرحم. [108]
للإستروجين والبروجستيرون الموجودان في COCPs تأثيرات أخرى على الجهاز التناسلي، ولكن لم يُثبِت أن هذه التأثيرات تساهم في فعاليتها في منع الحمل: [108]
- تباطؤ حركة البوق ونقل البويضات مما قد يتعارض مع الإخصاب.
- ضمور بطانة الرحم وتغيير محتوى ميتالوپروتيناز، والذي قد يعيق حركة الحيوانات المنوية وحيويتها، أو يمنع الانغراس نظرياً.
- وذمة بطانة الرحم، والتي قد تؤثر على انغراس البويضة.
توجد أدلة غير كافية حول ما إذا كانت التغييرات في بطانة الرحم يمكن أن تمنع بالفعل الانغراس. تعتبر آليات العمل الأولية فعالة جداً لدرجة أن إمكانية الإخصاب أثناء استخدام COCP صغيرة جداً. نظراً لأن الحمل يحدث على الرغم من تغييرات بطانة الرحم عندما تفشل آليات العمل الأولية، فمن غير المرجح أن تلعب تغييرات بطانة الرحم دوراً مهماً، إن وجد، في الفعالية الملحوظة لـ COCPs. [108]
التركيبة
تأتي موانع الحمل الفموية في مجموعة متنوعة من الصيغ، بعضها يحتوي على إستروجن و پروجستن، وبعضها يحتوي فقط على پروجستوجين. تختلف جرعات الهرمونات المكونة أيضاً باختلاف المنتجات، وبعض الحبوب هي أحادية الطور (تقدم نفس جرعة الهرمونات كل يوم) بينما البعض الآخر متعددة الأطوار (الجرعات تختلف كل يوم). يمكن أيضاً تقسيم حبوب منع الحمل المركبة (COCPs) إلى مجموعتين، تلك التي تحتوي على البروجستين التي تمتلك نشاط الأندروجن (نوريثيستيرون أسيتات، إيثينوديول ثنائي الأسيتات، ليڤونورجيستريل، نورجيستريل، نورجيستيمات ، ديسوجيستريل، جيستودين) أو مضادات الأندروجين (سيپروتيرون أسيتات النشط، خلات الكلورمادينون، دروسپيرينون، دينوجست، نومجستيرول أسيتات). تم تصنيف COCPs بشكل غير متسق إلى حد ما في "أجيال" في الأدبيات الطبية بناءً على وقت تقديمها. [112][113]
- يُعرَّف الجيل الأول من COCPs أحياناً على أنه تلك التي تحتوي على البروجستين، نوريتينودريل، نوريثيستيرون، نوريثيستيرون أسيتات، أو أسيتات إيتينوديول؛ [112] ويتم تعريفها أحياناً على أنها جميع COCPs التي تحتوي على ≥ 50 ميكروغرام من إيتانول إيستراديول [113]
- يُعرَّف الجيل الثاني من COCPs أحياناً بأنه تلك التي تحتوي على البروجستين نورجيستريل أو الليفونورجيستريل؛ [112] وأحياناً يتم تعريفها على أنها تلك التي تحتوي على البروجستين، نوريثيستيرون، نوريثيستيرون أسيتات، إيثينوديول أسيتات، نورجيستريل، ليفونورجيستريل، أو نورجيستيمات و <50 ميكروغرام إيثينيل إستراديول [113]
- يُعرَّف الجيل الثالث من COCPs أحياناً على أنه تلك التي تحتوي على البروجستين ديسوجيستريل أو جيستودين؛ [113] وأحياناً يتم تعريفها على أنها تلك التي تحتوي على ديسوجيستريل أو جيستودين أو نورجستيمت.[112]
- يُعرَّف الجيل الرابع من COCPs أحياناً بأنه تلك التي تحتوي على البروجستين دروسبيرينون؛ [112] وأحياناً يتم تعريفها على أنها تلك التي تحتوي على دروسبيرينون أو دينوجيست أو نوميجيستيرول أسيتات. [113]
التاريخ
بحلول الثلاثينيات من القرن الماضي، كان أندريه ستينهاش قد عزل وحدد بنية هرمونات الستيرويد ووجد أن الجرعات العالية من الأندروجن، الإستروجن أو الپروجسترون تثبط الإباضة ,[121][122][123][124]
لكن الحصول على هذه الهرمونات، التي تم إنتاجها من المستخلصات الحيوانية، من شركات الأدوية الأوروبية كان مكلفاً للغاية.[125]
في عام 1939، طور راسل ماركر، أستاذ الكيمياء العضوية في جامعة پنسلڤانيا، طريقة لتخليق الپروجسترون من مادة ساپوجينين الستيرويدية، في البداية باستخدام سارسابوجينين من sarsaparilla، والتي ثبت أنها باهظة الثمن. بعد ثلاث سنوات من البحث النباتي المكثف، اكتشف مادة بداية أفضل بكثير، الصابونين من اليام المكسيكي غير صالح للأكل (ديسقوريا مكسيكية وديسقوريا مركبة) في الغابات المطيرة في ڤيراكروز بالقرب من أوريزابا. يمكن تحويل الصابونين في المختبر إلى مادة ديوسجينين اجليكون. غير قادر على اهتمام الراعي البحثي Parke-Davis بالإمكانيات التجارية لتخليق البروجسترون من اليام المكسيكي، ترك ماركر ولاية بنسلفانيا وشارك في تأسيس سينتكس مع شريكين في مدينة المكسيك. عندما غادر سينتكس بعد عام واحد، بدأت تجارة الباسكو المكسيكية وبدأت فترة صناعة الستيرويد المكسيكية. كسرت سينتكس احتكار شركات الأدوية الأوروبية لهرمونات الستيرويد، مما خفض سعر البروجسترون 200 ضعف تقريباً خلال السنوات الثماني المقبلة.[126][127][128]
في منتصف القرن العشرين، تم تمهيد الطريق لتطوير موانع الحمل الهرمونية، لكن شركات الأدوية والجامعات والحكومات لم تظهر أي اهتمام بمتابعة البحث .[129]
الپروجسترون لمنع الإباضة
أظهر ميكبيس وزملاؤه أن هرمون البروجسترون، الذي يُعطى عن طريق الحقن، يثبط التبويض في الحيوانات لأول مرة في عام 1937. [130]
في أوائل عام 1951، التقى عالم وظائف الأعضاء الإنجابية گريگوري پنكس، الرائد في أبحاث الهرمونات والمؤسس المشارك لـ مؤسسة وستر للبحوث الطبية الحيوية (WFEB) في شروزبري، ماساتشوستس، لأول مرة بمؤسسة حركة تحديد النسل الأمريكية مارگريت سانگر في عشاء منهاتن استضافه أبراهام ستون، المدير الطبي ونائب رئيس جمعية تنظيم الأسرة الأمريكية (PPFA)، الذي ساعد پنكس في الحصول على منحة صغيرة من PPFA لبدء أبحاث منع الحمل الهرمونية. [131][132][133]بدأ البحث في 25 أبريل 1951 مع اختصاصي فسيولوجيا الإنجاب مين تشوه تشانگ ليكرر ويوسع تجارب عام 1937 الخاصة بـ ميكبيس وآخرون. التي تم نشرها في عام 1953 وأظهرت أن حقن البروجسترون تثبط التبويض في الأرانب .[130] في أكتوبر 1951، رفضت جي دي سيرل وشركاه طلب پنكس بتمويل أبحاثه حول موانع الحمل الهرمونية، لكنها احتفظت به كمستشار واستمر في تقديم مركبات كيميائية لتقييمها.[125][134][135]
في مارس 1952، كتبت سانگر مذكرة موجزة تشير إلى بحث پنكس لصديقتها القديمة، والمناصرة لحقوق المرأة وفعل الخير كاثرين ديكستر ماكورميك، االتي زارت جمعية تنظيم الأسرة الأمريكية وشريكها المؤسس والصديق القديم هدسن هوگلاند في يونيو 1952 للتعرف على أبحاث وسائل منع الحمل هناك. محبطاً عندما توقف البحث بسبب عدم اهتمام جمعية تنظيم الأسرة الأمريكية والتمويل الضئيل، رتبت ماكورميك اجتماعاً في محطة WFEB في 6 يونيو 1953 مع سانگر وهوگلاند، حيث قابلت پنكس لأول مرة الذي التزم بتوسيع وتسريع البحث بشكل كبير مع ماكورميك التي قدمت خمسين ضعفاً لتمويل لـ جمعية تنظيم الأسرة الأمريكية.[134][136]
عيّن پنكس وماكورميك أستاذ الطب السريري في هارڤارد في أمراض النساء جون روك، رئيس قسم أمراض النساء في المستشفى المجاني للنساء والخبير في علاج العقم لقيادة البحث السريري مع النساء. في مؤتمر علمي في عام 1952، اكتشف پنكس وروك، اللذان كانا يعرفان بعضهما البعض لسنوات عديدة، أنهما يستخدمان أساليب مماثلة لتحقيق أهداف معاكسة. في عام 1952، تسبب روك في حالة انقطاع الإباضة " الحمل الكاذب" لمدة ثلاثة أشهر بين ثمانين من مرضى العقم مع جرعات فموية متزايدة تدريجياً من هرمون الاستروجن (5 إلى 30 ملغ / يوم ثنائي إيثيل ستيلبوستيرول) وبروجستيرون (50 إلى 300 ملغ / يوم)، وخلال الأشهر الأربعة التالية أصبحت 15٪ من النساء حوامل.[134][137][138]
في عام 1953، بناءً على اقتراح پنكس، تسبب روك في حدوث حالة عدم إباضة لمدة ثلاثة أشهر "الحمل الكاذب" في سبعة وعشرين من مرضى العقم مع 300 ملجم / يوم بنظام البروجسترون فقط لمدة 20 يوماً من أيام الدورة 5-24 تليها أيام خالية من حبوب منع الحمل لإحداث نزيف انسحابي. [139] أنتج هذا نفس معدل الحمل بنسبة 15٪ خلال الأشهر الأربعة التالية دون انقطاع الطمث من نظام الإستروجين والبروجسترون المستمر السابق. [139] لكن 20٪ من النساء عانين من نزيف مفاجئ وفي الدورة الأولى تم قمع الإباضة في 85٪ فقط من النساء، مما يشير إلى أنه ستكون هناك حاجة لجرعات فموية أعلى وأكثر تكلفة من أجل تثبيط الإباضة بشكل دائم. [139] وبالمثل، وجد إيشيكاوا وزملاؤه أن تثبيط الإباضة يحدث فقط في "نسبة" من الحالات التي تحتوي على 300 ملجم / يوميا من البروجسترون الفموي. [140] على الرغم من التثبيط غير الكامل للإباضة عن طريق هرمون البروجسترون الفموي، لم تحدث أي حالات حمل في الدراستين، على الرغم من أن هذا قد يكون ببساطة بسبب الصدفة. [140][141] ومع ذلك، ذكر إيشيكاوا وزملاؤه أن مخاط عنق الرحم عند النساء اللواتي يتناولن البروجسترون عن طريق الفم أصبح منيعاً للحيوانات المنوية، وقد يكون هذا سبباً في عدم حدوث حمل. [140][141]
تم التخلي عن البروجسترون كمثبط للتبويض عن طريق الفم بعد هذه الدراسات السريرية بسبب الجرعات العالية والمكلفة المطلوبة، والتثبيط غير الكامل للتبويض، وكثرة حدوث النزيف الاختراقي. [130][142] وبدلاً من ذلك، سوف يلجأ الباحثون إلى المركبات بروجستيرونية المفعول الاصطناعية الأكثر فاعلية لاستخدامها في وسائل منع الحمل عن طريق الفم في المستقبل. [130][142]
البروجستين لمنع الإباضة
طلب بنكس من معارفه في شركات الأدوية أن يرسلوا له مركبات كيميائية ذات نشاط بروجستيروني. فحص تشانگ ما يقرب من 200 مركب كيميائي في الحيوانات ووجد أن أكثر ثلاثة مركبات واعدة هي سينتكس نوريثيستيرون وسيرال نوريتينودريل ونوريثاندرولون .[143]
قام الكيميائيون كارل دجراسي، لويس ميرامونتس، وجورج روزنكرانز في سينتكس في مكسيكو سيتي بتصنيع أول بروجستين نوريثيستيرون فموي في عام 1951. وكان فرانك ب. كولتون في سيرال في سكوكي، إلينوي قد صنع البروجستين عالي الفعالية عن طريق الفم نوريتينودريل (أيزومر من نوريثيستيرون) في عام 1952 ونوريتاندرولون في عام 1953 .[125]
Iفي ديسمبر 1954، بدأ روك الدراسات الأولى لإمكانية تثبيط الإباضة بجرعات 5-50 ملليجرام من البروجستين الفموي لمدة ثلاثة أشهر (لمدة 21 يوماً لكل دورة - أيام 5-25 تليها أيام خالية من حبوب منع الحمل لإنتاج النزيف الانسحابي) في خمسين من مرضى العقم في بروكلن، مساتشوستس. جرعات نوريثيستيرون أو نوريتينودريل 5 ملجم جرعات وجميع جرعات نوريثاندرولون قمعت الإباضة ولكنها تسببت في نزيف اختراقي، ولكن جرعات أعلى من نوريثيستيرون أو نوريتينودريل قمعت الإباضة دون نزيف اختراقي وأدت إلى معدل حمل 14٪ في الأشهر الخمسة التالية. اختارت بنكس وروك نوريتينودريل من سيرل لإجراء التجارب الأولى على موانع الحمل لدى النساء، مشيرين إلى افتقارها التام إلى الأندروجين مقابل سينتكس نوريثيستيرون الطفيف جداً في اختبارات الحيوانات.[144][145]
موانع الحمل المركبة الفموية
تم اكتشاف تلوث نوريتينودريل (ونوريثيستيرون) لاحقاً بنسبة صغيرة من الإستروجن مسترانول (وسيط في تركيبهما)، مع نورتينودريل في دراسة روك 1954-5 التي تحتوي على 4-7٪ مسترانول. عندما أدى تنقية النورتينودريل لاحتواء أقل من 1٪ مسترانول إلى حدوث نزيف اختراقي، فقد تقرر إدخال 2.2٪ مسترانول عمداً، وهي نسبة لم تكن مرتبطة بالنزيف الاختراقي، في تجارب منع الحمل الأولى على النساء في عام 1956. تم إعطاء تركيبة نوريتينودريل ومسترانول اسم الملكية إنوڤيد .[145][146]
بدأت أول تجربة لإنوڤيد في منع الحمل بقيادة سيلسو رامون گارسيا وإدريس رايس راي في أبريل 1956 في ريو پيدراس، پورتو ريكو. [147][148][149][150][151][152][153][استشهاد مفرط] بدأت تجربة منع الحمل الثانية لإينوفيد (ونوريثيستيرون) بقيادة إدوارد تي تايلر في يونيو 1956 في لوس أنجلس، كاليفورنيا.[128][154] في 23 يناير 1957، عقدت سيرل ندوة لمراجعة أبحاث أمراض النساء ووسائل منع الحمل على إنوڤيد حتى عام 1956 وخلصت إلى أن محتوى إنوڤيد من الاستروجين يمكن أن ينخفض بنسبة 33 ٪ لتقليل حدوث الآثار الجانبية المعدية المعوية الاستروجينية دون زيادة كبيرة في حدوث نزيف اختراقي.[155]
الإتاحة العامة
الولايات المتحدة
في 10 يونيو 1957، وافقت إدارة الغذاء والدواء (FDA) على إينوفيد؛ 10 ملجم (9.85 ملجم نوريتينودريل و 150 ميكروغرام مسترانول) لاضطرابات الدورة الشهرية، بناءً على بيانات من استخدامه من قبل أكثر من 600 امرأة. أظهرت العديد من التجارب الإضافية على موانع الحمل أن إينوفيد بجرعات 10 و 5 و 2.5 ملجم فعالة للغاية. في 23 يوليو 1959، قدمت شركة سيرال طلباً إضافياً لإضافة وسائل منع الحمل كمؤشر معتمد لجرعات 10 و 5 و 2.5 ملجم من إينوفيد. رفضت إدارة الغذاء والدواء الأمريكية (FDA) النظر في الطلب حتى وافقت سيرال على سحب أشكال الجرعات الأقل من التطبيق. في 9 مايو 1960، أعلنت إدارة الغذاء والدواء أنها ستوافق على إينوفيد 10 ملجم لاستخدام كوسيلة منع للحمل، وفعلت ذلك في 23 يونيو 1960. في تلك المرحلة، كان إينوفيد 10 ملجم قيد الاستخدام العام لمدة ثلاث سنوات، ووفقاً لتقدير متحفظ، استخدمته نصف مليون امرأة على الأقل.[150][156][157]
على الرغم من اعتماد إدارة الغذاء والدواء (FDA) لاستخدام موانع الحمل، إلا أن سيرال لم تسوق أبداً اينوفيد 10 ملجم كمانع للحمل. بعد ثمانية أشهر، في 15 فبراير 1961، وافقت إدارة الغذاء والدواء الأمريكية على إينوفيد 5 ملجم لاستخدام وسائل منع الحمل. في يوليو 1961 ، بدأت سيرال أخيراً تسويق اينوفيد 5 ملجم (5 ملجم نوريتينودريل و 75 ميكروغرام مسترانول) للأطباء كوسيلة لمنع الحمل.[156][158]
على الرغم من أن إدارة الغذاء والدواء وافقت على أول موانع حمل فموية في عام 1960، إلا أن موانع الحمل لم تكن متاحة للنساء المتزوجات في جميع الولايات حتى گريسوولد ضد كونيتيكت في عام 1965 ولم تكن متاحة للنساء غير المتزوجات في جميع الولايات حتى آيزنشتات ضد بيرد في عام 1972.[129][158]
أول تقرير حالة منشور عن جلطة دموية وانصمام رئوي لدى امرأة تستخدم إينوفيد (إينوفيد 10 ملجم في الولايات المتحدة) بجرعة 20 ملجم/يوم لم يظهر حتى نوفمبر 1961 ، بعد أربع سنوات من الموافقة عليه، وفي ذلك الوقت كانت تستخدمه أكثر من مليون امرأة.[150][159][160] قد يستغرق الأمر ما يقرب عقداً من الدراسات الوبائية للتثبت بشكل قاطع من زيادة خطر الخثار الوريدي لدى مستخدمات موانع الحمل الفموية وزيادة خطر السكتة واحتشاء قلبي لدى مستخدمات موانع الحمل الفموية المدخنات أو لديهن ارتفاع ضغط الدم أو عوامل الخطر الأخرى القلبية الوعائية أو الدماغية.[156] تم تسليط الضوء على مخاطر موانع الحمل الفموية في كتاب عام 1969 قضية الأطباء ضد حبوب منع الحمل للصحفية النسوية باربرا سيمان التي ساعدت في ترتيب 1970 جلسات نيلسون پل هيرينگز الذي دعا إليها السناتور گايلورد نلسون .[161] تم إجراء الجلسات من قبل أعضاء مجلس الشيوخ الذين كانوا جميعاً رجالاً وكان الشهود في الجولة الأولى من الجلسات جميعاً من الرجال، مما دفع أليس ولفسون وناشطات أخريات إلى الاحتجاج على جلسات الاستماع وجذب انتباه وسائل الإعلام.[158] أدى عملهم إلى إلزام إدراج النشرة الداخلية للدواء مع موانع الحمل الفموية لشرح الآثار الجانبية المحتملة والمخاطر للمساعدة في تسهيل الموافقة المستنيرة.[162][163][164]تحتوي موانع الحمل الفموية القياسية بالجرعة الحالية على جرعة إستروجين تقل بمقدار الثلث عن أول موانع حمل فموية يتم تسويقها وتحتوي على جرعات أقل من البروجستين المختلف والأكثر فاعلية في مجموعة متنوعة من الصيغ.[22][156][158]
ابتداء من عام 2015، أصدرت بعض الولايات تشريعات تسمح للصيادلة بوصف موانع الحمل الفموية. وقد تم النظر في مثل هذا التشريع لمعالجة النقص في الأطباء وتقليل الحواجز التي تحول دون تحديد النسل للنساء. [165] حالياً، يمتلك الصيادلة في أوريگون وكاليفورنيا وكولورادو وهاواي وماريلاند ونيو مكسيكو سلطة وصف وسائل منع الحمل بعد تلقي التدريب والشهادة من مجلس الصيدلة في ولايتهم. [166][167] تنظر ولايات أخرى في هذا التشريع، بما في ذلك إلينوي ومينيسوتا وميسوري ونيو هامپشر. [165]
أستراليا
أول موانع الحمل الفموية التي تم تقديمها خارج الولايات المتحدة كانت أنوڤلار من شـِرِنگ (نوريثيستيرون أسيتات 4 ملغ + إيثينيل إستراديول 50 ميكروغرام) في 1 يناير 1961 في أستراليا.[168]
ألمانيا
أول وسيلة لمنع الحمل تم تقديمها في أوروبا كانت أنوڤلار شـِرِنگ في 1 يونيو 1961 في ألمانيا الغربية.[168] تمت دراسة الجرعة الهرمونية المنخفضة، التي لا تزال قيد الاستخدام، من قبل طبيب أمراض النساء البلجيكي فرديناند پيترز .[169][170]
المملكة المتحدة
قبل منتصف الستينيات، لم تطلب المملكة المتحدة موافقة مسبقة على تسويق الأدوية. كانت جمعية تنظيم الأسرة البريطانية (FPA) من خلال عياداتها في ذلك الوقت المزود الرئيسي لخدمات تنظيم الأسرة في المملكة المتحدة وقدمت فقط وسائل منع الحمل التي كانت مدرجة في القائمة المعتمدة لوسائل منع الحمل (التي تأسست عام 1934). في عام 1957، بدأت سيرال تسويق إينوفيد (إينوفيد 10 ملجم في الولايات المتحدة) لاضطرابات الدورة الشهرية. في عام 1957 أيضا، أنشأت FPA مجلسا للتحقيق في التحكم في الخصوبة (CIFC) لاختبار ومراقبة موانع الحمل الفموية التي بدأت في اختبار الحيوانات على موانع الحمل الفموية وفي عامي 1960 و 1961 بدأت ثلاث تجارب سريرية كبيرة في برمنگهام، سلاو، ولندن.[150][171]
في مارس 1960، بدأ FPA في برمنگهام تجارب نوريتينودريل 2.5 ملغ + ميسترانول 50 ميكروغرام، ولكن حدث معدل حمل مرتفع في البداية عندما احتوت الحبوب عن طريق الخطأ على 36 ميكروغرام فقط من ميسترانول- استمرت التجارب مع نورتينودريل 5 ملغ + ميسترانول 75 ميكروغرام (كونوفيد في المملكة المتحدة، إينوفيد 5 مجم في الولايات المتحدة).[172] في أغسطس 1960، بدأت FPA في سلاو تجارب نوريتينودريل 2.5 ملغ + ميسترانول 100 ميكروغرام (كونوفيد-E في المملكة المتحدة، إينوفيد-E في الولايات المتحدة)..[173] في مايو 1961 ، بدأت FPA بلندن تجارب على أنوفلار من شرنگ.[174]
في أكتوبر 1961، بناءً على توصية من المجلس الاستشاري الطبي لـ CIFC، أضافت FPA كونوفيد سيرال إلى قائمتها المعتمدة لوسائل منع الحمل .[175] في 4 ديسمبر 1961، أعلن إينوك پاول، ثم وزير الصحة، أنه يمكن وصف حبوب منع الحمل الفموية كونوفيد من خلال NHS بسعر مدعوم 2 شلن شهرياً.[176][177] في عام 1962، تمت إضافة أنوفلار من شرنگ و كونوفيد-E من شركة سيرال إلى قائمة موانع الحمل المعتمدة من FPA.[150][173][174]
فرنسا
في 28 ديسمبر 1967، شرّع قانون نويرث وسائل منع الحمل في فرنسا، بما في ذلك حبوب منع الحمل. [178] حبوب منع الحمل هي أكثر وسائل تحديد النسل شيوعاً في فرنسا، وخاصة بين الشابات. وتمثل 60 ٪ من وسائل منع الحمل المستخدمة في فرنسا. ظل معدل الإجهاض مستقراً منذ إدخالها. [179]
اليابان
في اليابان، أدى الضغط من الجمعية الطبية اليابانية إلى منع الموافقة على حبوب منع الحمل للاستخدام العام لما يقرب من 40 عاماً. تمت الموافقة على استخدام حبوب "الجيل الثاني" ذات الجرعة العالية في حالات المشاكل النسائية، ولكن ليس لتحديد النسل. أثارت الرابطة اعتراضين رئيسيين هما المخاوف المتعلقة بالسلامة بشأن الاستخدام طويل الأمد للحبوب، والمخاوف من أن يؤدي استخدام حبوب منع الحمل إلى تقليل استخدام الواقي الذكري وبالتالي زيادة معدلات الإصابة المنقولة جنسياً (الأمراض المنقولة بالاتصال الجنسي).[180]
ومع ذلك، عندما وافقت وزارة الصحة والرعاية الاجتماعية على استخدام الفياگرا في اليابان بعد ستة أشهر فقط من تقديم الطلب، بينما لا تزال تدعي أن حبوب منع الحمل تتطلب مزيداً من البيانات قبل الموافقة، تعالت أصوات المجموعات النسائية. [181] تمت الموافقة على استخدام حبوب منع الحمل لاحقاً في يونيو 1999. ومع ذلك، لم تصبح شائعة في اليابان. [182] وفقاً للتقديرات، تستخدم 1.3٪ فقط من 28 مليون أنثى يابانية في سن الإنجاب حبوب منع الحمل، مقارنة بـ 15.6٪ في الولايات المتحدة. تتطلب إرشادات الوصفات الطبية التي أقرتها الحكومة من مستخدمات حبوب منع الحمل زيارة الطبيب كل ثلاثة أشهر لفحص الحوض والخضوع لاختبارات للأمراض المنقولة جنسياً وسرطان الرحم. في الولايات المتحدة وأوروبا، على النقيض من ذلك، تعد زيارة العيادة السنوية أو نصف السنوية معياراً لمستخدمات حبوب منع الحمل. ومع ذلك، بدءاً من عام 2007، طلبت عيادات طب التوليد والنسائيات اليابانية زيارة سنوية فقط لمستخدمات حبوب منع الحمل، مع إجراء فحوصات متعددة سنوياً موصى بها فقط للأشخاص الأكبر سناً أو المعرضين لخطر متزايد من الآثار الجانبية.[183] اعتباراً من عام 2004، شكلت الواقيات الذكرية 80٪ من استخدام وسائل منع الحمل في اليابان، وهذا قد يفسر معدلات اليابان المنخفضة نسبياً للإصابة بالإيدز. [183]
المجتمع والثقافة
تمت الموافقة على حبوب منع الحمل من قبل إدارة الغذاء والدواء في أوائل الستينيات؛ انتشر استخدامه بسرعة في أواخر ذلك العقد، مما أحدث تأثيراً اجتماعياً هائلاً. وضعت مجلة التايم الحبة على غلافها في أبريل، 1967. [184][185] في المقام الأول، كانت أكثر فاعلية من معظم طرق منع الحمل السابقة القابلة للعكس، مما أعطى النساء سيطرة غير مسبوقة على خصوبتهن .[186] كان استخدامه منفصلاً عن الجماع، ولم يتطلب أي استعدادات خاصة في وقت النشاط الجنسي قد تتداخل مع العفوية أو الإحساس، وكان اختيار تناول حبوب منع الحمل أمراً خاصاً. ساعد هذا المزيج من العوامل في جعل حبوب منع الحمل شائعة للغاية في غضون بضع سنوات من تقديمها. [126][158]
كلوديا گولدين، من بين آخرين، يجادلون بأن هذه التكنولوجيا الجديدة لوسائل منع الحمل كانت لاعباً رئيسياً في تشكيل الدور الاقتصادي الحديث للمرأة، من حيث أنها أطالت العمر الذي تزوجت فيه المرأة لأول مرة مما سمح لها بالاستثمار في التعليم والأشكال الأخرى لرأس المال البشري وكذلك أصبحت عموماً أكثر توجهاً نحو الحياة المهنية. بعد فترة وجيزة من تقنين حبوب منع الحمل، كانت هناك زيادة حادة في معدلات الالتحاق بالجامعة وتخرج النساء.[187]من وجهة نظر اقتصادية، قللت حبوب منع الحمل من تكلفة البقاء في المدرسة. القدرة على التحكم في الخصوبة دون التضحية بالعلاقات الجنسية سمحت للمرأة بوضع خطط تعليمية ووظيفية طويلة الأجل. [188] نظراً لأن حبوب منع الحمل كانت فعالة جداً وسرعان ما انتشرت على نطاق واسع ، فقد زادت أيضاً من الجدل حول العواقب الأخلاقية والصحية لـالجنس قبل الزواج والاختلاط. لم يحدث من قبل أن كان النشاط الجنسي منفصلاً عن الإنجاب. بالنسبة للزوجين اللذين يستخدمان حبوب منع الحمل، أصبح الجماع مجرد تعبير عن الحب، أو وسيلة للمتعة الجسدية، أو كليهما؛ لكنه لم يعد يعتبر وسيلة للتكاثر. في حين أن هذا كان صحيحاً بالنسبة لوسائل منع الحمل السابقة، إلا أن معدلات فشلها المرتفعة نسبياً واستخدامها الأقل انتشاراً فشلت في التأكيد على هذا التمييز بوضوح كما فعلت حبوب منع الحمل. أدى انتشار استخدام موانع الحمل الفموية إلى قيام العديد من الشخصيات والمؤسسات الدينية بمناقشة الدور المناسب للجنس وعلاقته بالإنجاب. أعادت كنيسة الروم الملكيين الكاثوليك على وجه الخصوص، بعد دراسة ظاهرة موانع الحمل الفموية، التأكيد على التعاليم المذكورة حول تحديد النسل في المنشور البابوي لعام 1968 السير الذاتية للإنسان. كرر المنشور التعاليم الكاثوليكية الراسخة بأن وسائل منع الحمل الاصطناعية تشوه طبيعة الجنس والغرض منه. [189] على الجانب الآخر، قبلت الكنائس الأنجليكانية وغيرها من الكنائس البروتستانتية، مثل الكنيسة الإنجيلية في ألمانيا (EKD) حبوب منع الحمل المركبة الفموية. [190]
بدأ مجلس الشيوخ الأمريكي جلسات الاستماع حول حبوب منع الحمل في عام 1970 حيث تم سماع وجهات نظر مختلفة من المهنيين الطبيين. قال الدكتور مايكل نيوتن، رئيس كلية أمراض النساء والتوليد :
لم يتضح بعد الدليل على أن هذه لا تزال تسبب السرطان في الواقع أو مرتبطة به. قدمت اللجنة الاستشارية لإدارة الغذاء والدواء تعليقات حول هذا الأمر، أنه إذا لم تكن هناك أدلة كافية تشير إلى ما إذا كانت هذه الحبوب مرتبطة بتطور السرطان أم لا، وأعتقد أن هذا لا يزال ضعيفاً؛ عليك توخي الحذر بشأنهم، لكن لا أعتقد أن هناك دليلاً واضحاً، بطريقة أو بأخرى، على أنها تسبب السرطان أو لا تسببه. [191]
قال طبيب آخر، هو د. روي هيرتز من مجلس السكان، إن أي شخص يأخذ هذا يجب أن يعرف "معرفتنا وجهلنا في هذه الأمور" وأنه يجب توعية جميع النساء بهذا الأمر حتى تتمكن من اتخاذ قرار حبوب منع الحمل أم لا. [191]
أعلن وزير الصحة والتعليم والرعاية الاجتماعية في ذلك الوقت، روبرت فينش، أن الحكومة الفيدرالية قد قبلت بياناً تحذيرياً وسطياً سيصاحب جميع مبيعات حبوب منع الحمل. [191]
النتيجة على الثقافة الشعبية
سمح إدخال حبوب منع الحمل في عام 1960 لمزيد من النساء بالعثور على فرص عمل ومواصلة تعليمهن. نتيجة حصول المزيد من النساء على الوظائف والتعليم، كان على أزواجهن البدء في تولي المهام المنزلية مثل الطهي. [192] الرغبة في إيقاف التغيير الذي كان يحدث من حيث معايير الجنس في الأسرة الأمريكية، فإن العديد من الأفلام والبرامج التلفزيونية وغيرها من عناصر الثقافة الشعبية تصور ما يجب أن تكون عليه الأسرة الأمريكية المثالية. فيما يلي سرد بعض الأمثلة:
القصائد
- الحبة مقابل كارثة منجم سبرينگهيل كانت قصيدة العنوان لمجموعة عام 1968 بقلم ريتشارد بروتيگان. .[193]
الموسيقى
- المغنية لوريتا لين علقت على كيفية عدم اضطرار النساء للاختيار بين العلاقة والعمل في ألبومها لعام 1974 بأغنية بعنوان " The Pill"، والتي تحكي قصة استخدام المرأة المتزوجة للدواء لتحرير نفسها من دورها التقليدي كزوجة وأم.[194]
التأثير البيئي
المرأة التي تستخدم حبوب منع الحمل المركبة تفرز من البول والبراز الطبيعي الإستروجن والإسترون (E1) وإستراديول (E2) والإستروجن الصناعي إيثينيل إستراديول (EE2).[195] يمكن أن تمر هذه الهرمونات عبر محطات معالجة المياه وإلى الأنهار. [196] تستخدم الأشكال الأخرى من وسائل منع الحمل، مثل لصاقة منع الحمل، نفس هرمون الاستروجن الاصطناعي (EE2) الموجود في موانع الحمل الفموية، ويمكن أن تضيف إلى التركيز الهرموني في الماء عند غسله في المرحاض. [197] يظهر أن هذا الإخراج يلعب دوراً في التسبب في اضطراب الغدد الصماء، والذي يؤثر على التطور الجنسي والتكاثر، في مجموعات الأسماك البرية في أجزاء من الجداول الملوثة بمخلفات الصرف الصحي المعالجة.[195][198] دعمت دراسة أجريت في الأنهار البريطانية الفرضية القائلة بأن حدوث وشدة مجموعات الأسماك البرية ثنائية الجنس كانت مرتبطة بشكل كبير بتركيزات E1 و E2 و EE2 في الأنهار. [195]
وجدت مراجعة لأداء محطة الحمأة المنشطة أن معدلات إزالة الإستروجن تتفاوت بشكل كبير ولكن متوسطها 78٪ للإسترون، و 91٪ للإستراديول، و 76٪ لإيثينيل إستراديول (تكون تركيزات نفايات إستريول السائلة بين تلك الخاصة بالإسترون والإستراديول، ولكن الإستريول أقل فعالية في إعاقة عمل اضطراب الغدد الصماء بالنسبة للأسماك). [199] اقترحت العديد من الدراسات أن الحد من النمو السكاني من خلال زيادة الوصول إلى وسائل منع الحمل، بما في ذلك حبوب منع الحمل، يمكن أن يكون استراتيجية فعالة لـ التخفيف من تغير المناخ وكذلك التكيف. [200][201] وفقاً لتوماس واير، فإن وسائل منع الحمل هي "التكنولوجيا الأكثر خضرة" نظراً لفعاليتها من حيث التكلفة في مكافحة الإحترار العالمي - كل 7 دولارات يتم إنفاقها على موانع الحمل ستقلل انبعاثات الكربون العالمية بمقدار طن واحد على مدى أربعة عقود، مع تحقيق نفس النتيجة مع تتطلب التقنيات منخفضة الكربون 32 دولاراً. [202]
انظر أيضاً
- Estradiol-containing oral contraceptive
- Hormone replacement therapy (HRT)
- List of estrogens available in the United States
- List of progestogens available in the United States
- Progestogen-only injectable contraceptive
المراجع
- ^ أ ب Hannaford PC, Iversen L, Macfarlane TV, Elliott AM, Angus V, Lee AJ (March 2010). "Mortality among contraceptive pill users: cohort evidence from Royal College of General Practitioners' Oral Contraception Study". BMJ. 340: c927. doi:10.1136/bmj.c927. PMC 2837145. PMID 20223876.
- ^ "Oral Contraceptives and Cancer Risk". National Cancer Institute. 22 Feb 2018. Retrieved 10 May 2020.
- ^ أ ب ت ث IARC working group (2007). "Combined Estrogen-Progestogen Contraceptives" (PDF). IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. 91.
- ^ Collaborative Group on Hormonal Factors in Breast Cancer (June 1996). "Breast cancer and hormonal contraceptives: collaborative reanalysis of individual data on 53 297 women with breast cancer and 100 239 women without breast cancer from 54 epidemiological studies". Lancet. 347 (9017): 1713–27. doi:10.1016/S0140-6736(96)90806-5. PMID 8656904. S2CID 36136756. Archived from the original on 2019-01-23. Retrieved 2018-12-16.
- ^ Kemmeren JM, Tanis BC, van den Bosch MA, Bollen EL, Helmerhorst FM, van der Graaf Y, Rosendaal FR, Algra A (May 2002). "Risk of Arterial Thrombosis in Relation to Oral Contraceptives (RATIO) study: oral contraceptives and the risk of ischemic stroke". Stroke. 33 (5): 1202–8. doi:10.1161/01.STR.0000015345.61324.3F. PMID 11988591.
- ^ Baillargeon JP, McClish DK, Essah PA, Nestler JE (July 2005). "Association between the current use of low-dose oral contraceptives and cardiovascular arterial disease: a meta-analysis". The Journal of Clinical Endocrinology and Metabolism. 90 (7): 3863–70. doi:10.1210/jc.2004-1958. PMID 15814774.
- ^ "Birth Control Pills - Birth Control Pill - The Pill".
- ^ Mosher WD, Martinez GM, Chandra A, Abma JC, Willson SJ (December 2004). "Use of contraception and use of family planning services in the United States: 1982-2002" (PDF). Advance Data (350): 1–36. PMID 15633582. all US women aged 15–44
- ^ "Current Contraceptive Status Among Women Aged 15–49: United States, 2015–2017". www.cdc.gov. 2019-06-07. Retrieved 2019-08-02.
- ^ UN Population Division (2006). World Contraceptive Use 2005 (PDF). New York: United Nations. ISBN 978-92-1-151418-6. women aged 15–49 married or in consensual union
- ^ Delvin D (2016-06-15). "Contraception – the contraceptive pill: How many women take it in the UK?".
- ^ Taylor T, Keyse L, Bryant A (2006). Contraception and Sexual Health, 2005/06 (PDF). London: Office for National Statistics. ISBN 978-1-85774-638-9. Archived from the original (PDF) on 2007-01-09. British women aged 16–49: 24% currently use the pill (17% use Combined pill, 5% use Minipill, 2% don't know type)
- ^ Yoshida H, Sakamoto H, Leslie A, Takahashi O, Tsuboi S, Kitamura K (June 2016). "Contraception in Japan: Current trends". Contraception. 93 (6): 475–7. doi:10.1016/j.contraception.2016.02.006. PMID 26872717.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Harris G (2010-05-03). "The Pill Started More Than One Revolution". The New York Times. Retrieved 2015-09-21.
- ^ أ ب "How to Use Birth Control Pills | Follow Easy Instructions". www.plannedparenthood.org. Retrieved 2017-11-29.
- ^ أ ب ت ث ج ح خ Callahan TL, Caughey AB (2013). Blueprints obstetrics & gynecology (6th ed.). Baltimore, MD: Lippincott Williams & Wilkins. ISBN 9781451117028. OCLC 800907400.
- ^ "Birth Control Pills All Guides".
- ^ أ ب ت ث ج World Health Organization (2016). Selected practice recommendations for contraceptive use (Third ed.). Geneva: World Health Organization. p. 150. hdl:10665/252267. ISBN 9789241565400. OCLC 985676200.
- ^ أ ب ت Curtis KM, Tepper NK, Jatlaoui TC, Berry-Bibee E, Horton LG, Zapata LB, Simmons KB, Pagano HP, Jamieson DJ, Whiteman MK (July 2016). "U.S. Medical Eligibility Criteria for Contraceptive Use, 2016". MMWR. Recommendations and Reports. 65 (3): 1–103. doi:10.15585/mmwr.rr6503a1. PMID 27467196.
- ^ Trussell J (May 2011). "Contraceptive failure in the United States". Contraception. 83 (5): 397–404. doi:10.1016/j.contraception.2011.01.021. PMC 3638209. PMID 21477680.
- ^ أ ب ت ث ج ح خ د Speroff L, Darney PD (2005). "Oral Contraception". A Clinical Guide for Contraception (4th ed.). Philadelphia: Lippincott Williams & Wilkins. pp. 21–138. ISBN 978-0-7817-6488-9.
- ^ FFPRHC (2007). "Clinical Guidance: First Prescription of Combined Oral Contraception" (PDF). Archived from the original (PDF) on 2007-07-04. Retrieved 2007-06-26.
- ^ Edelman, Alison; Micks, Elizabeth; Gallo, Maria F.; Jensen, Jeffrey T.; Grimes, David A. (2014-07-29). "Continuous or extended cycle vs. cyclic use of combined hormonal contraceptives for contraception". The Cochrane Database of Systematic Reviews (7): CD004695. doi:10.1002/14651858.CD004695.pub3. ISSN 1469-493X. PMC 6837850. PMID 25072731.
- ^ "Last Week of Birth Control Pills".
- ^ Gladwell M (2000-03-10). "John Rock's Error". The New Yorker. Archived from the original on 11 May 2013. Retrieved 2009-02-04.
- ^ Mayo Clinic staff. "Birth control pill FAQ: Benefits, risks and choices". Mayo Clinic. Retrieved 1 February 2013.
- ^ "US Patent:Oral contraceptive:Patent 6451778 Issued on September 17, 2002 Estimated Expiration Date: July 2, 2017". PatentStorm LLC. Archived from the original on June 13, 2011. Retrieved 2010-11-19.
- ^ Hercberg S, Preziosi P, Galan P (April 2001). "Iron deficiency in Europe". Public Health Nutrition. 4 (2B): 537–45. doi:10.1079/phn2001139. PMID 11683548.
- ^ Viswanathan, Meera; Treiman, Katherine A.; Doto, Julia Kish; Middleton, Jennifer C.; Coker-Schwimmer, Emmanuel JL; Nicholson, Wanda K. (2017). Folic Acid Supplementation: An Evidence Review for the U.S. Preventive Services Task Force. U.S. Preventive Services Task Force Evidence Syntheses, formerly Systematic Evidence Reviews. Rockville (MD): Agency for Healthcare Research and Quality (US). PMID 28151610.
- ^ Bhutta, Zulfiqar (April 2012). "Clinical utility of folate-containing oral contraceptives". International Journal of Women's Health (in الإنجليزية). 4: 185–90. doi:10.2147/IJWH.S18611. ISSN 1179-1411. PMC 3346209. PMID 22570577.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ FDA (2003-09-25). "FDA Approves Seasonal Oral Contraceptive". Food and Drug Administration. Archived from the original on 2006-10-07. Retrieved 2006-11-09.
- ^ Edelman, A; Micks, E; Gallo, MF; Jensen, JT; Grimes, DA (29 July 2014). "Continuous or extended cycle vs. cyclic use of combined hormonal contraceptives for contraception". The Cochrane Database of Systematic Reviews (7): CD004695. doi:10.1002/14651858.CD004695.pub3. PMC 6837850. PMID 25072731.
- ^ CYWH Staff (2011-10-18). "Medical Uses of the Birth Control Pill". Retrieved 1 February 2013.
- ^ "Information for Consumers (Drugs) - Find Information about a Drug". www.fda.gov. Retrieved 2017-12-13.
- ^ Barakat RR, Park RC, Grigsby PW, et al. Corpus: Epithelial Tumors. In: Principles and Practice of Gynecologic Oncology, 2nd, Hoskins WH, Perez CA, Young RC (Eds), Lippincott-Raven Publishers, Philadelphia 1997. p.859
- ^ Hardiman P, Pillay OC, Atiomo W (May 2003). "Polycystic ovary syndrome and endometrial carcinoma". Lancet. 361 (9371): 1810–2. doi:10.1016/s0140-6736(03)13409-5. PMID 12781553. S2CID 27453081.
- ^ "ACOG Endometriosis FAQ".
- ^ Zorbas KA, Economopoulos KP, Vlahos NF (July 2015). "Continuous versus cyclic oral contraceptives for the treatment of endometriosis: a systematic review". Archives of Gynecology and Obstetrics. 292 (1): 37–43. doi:10.1007/s00404-015-3641-1. PMID 25644508. S2CID 23340983.
- ^ Huber J, Walch K (January 2006). "Treating acne with oral contraceptives: use of lower doses". Contraception. 73 (1): 23–9. doi:10.1016/j.contraception.2005.07.010. PMID 16371290.
- ^ Chang L. "Birth Control of Acne". WebMD, LLC. Retrieved 1 February 2013.
- ^ "DailyMed - ORTHO TRI CYCLEN- norgestimate and ethinyl estradiol ORTHO CYCLEN- norgestimate and ethinyl estradiol". dailymed.nlm.nih.gov. Retrieved 2017-12-13.
- ^ "Beyaz Package Insert" (PDF). FDA.
- ^ أ ب American Medical Society for Sports Medicine (24 April 2014), Five Things Physicians and Patients Should Question, American Medical Society for Sports Medicine, http://www.choosingwisely.org/doctor-patient-lists/american-medical-society-for-sports-medicine/, retrieved on 29 July 2014
- ^ أ ب Black, Amanda; Guilbert, Edith; Costescu, Dustin; Dunn, Sheila; Fisher, William; Kives, Sari; Mirosh, Melissa; Norman, Wendy V.; Pymar, Helen; Reid, Robert; Roy, Geneviève (April 2017). "No. 329-Canadian Contraception Consensus Part 4 of 4 Chapter 9: Combined Hormonal Contraception". Journal of Obstetrics and Gynaecology Canada. 39 (4): 229–268.e5. doi:10.1016/j.jogc.2016.10.005. ISSN 1701-2163. PMID 28413042.
- ^ أ ب Cooper, Danielle B.; Adigun, Rotimi; Shamoon, Zafar (2019), Oral Contraceptive Pills, StatPearls Publishing, PMID 28613632, http://www.ncbi.nlm.nih.gov/books/NBK430882/, retrieved on 2019-08-05
- ^ أ ب "Can Any Woman Take Birth Control Pills?". WebMD. Retrieved 8 May 2016.
- ^ أ ب Medical eligibility criteria for contraceptive use. World Health Organization. Reproductive Health and Research,, World Health Organization (Fifth ed.). Geneva, Switzerland. 2015. ISBN 978-92-4-154915-8. OCLC 932048744.
{{cite book}}: CS1 maint: location missing publisher (link) CS1 maint: others (link) - ^ Lopez, Laureen M; Grey, Thomas W; Stuebe, Alison M; Chen, Mario; Truitt, Sarah T; Gallo, Maria F (2015-03-20). Cochrane Fertility Regulation Group (ed.). "Combined hormonal versus nonhormonal versus progestin-only contraception in lactation". Cochrane Database of Systematic Reviews (in الإنجليزية) (3): CD003988. doi:10.1002/14651858.CD003988.pub2. PMID 25793657.
- ^ "Classifications for Combined Hormonal Contraceptives | CDC". www.cdc.gov (in الإنجليزية الأمريكية). 2020-04-09. Retrieved 2020-12-07.
- ^ Crooks RL, Baur K (2005). Our Sexuality. Belmont, CA: Thomson Wadsworth. ISBN 978-0-534-65176-3.[صفحة مطلوبة]
- ^ WHO (2005). Decision-Making Tool for Family Planning Clients and Providers Appendix 10: Myths about contraception
- ^ Holck S. "Contraceptive Safety". Special Challenges in Third World Women's Health. 1989 Annual Meeting of the American Public Health Association. Retrieved 2006-10-07.
- ^ Serfaty D (October 1992). "Medical aspects of oral contraceptive discontinuation". Advances in Contraception. 8 Suppl 1: 21–33. doi:10.1007/bf01849448. PMID 1442247. S2CID 11876371.
- ^ Sanders SA, Graham CA, Bass JL, Bancroft J (July 2001). "A prospective study of the effects of oral contraceptives on sexuality and well-being and their relationship to discontinuation". Contraception. 64 (1): 51–8. doi:10.1016/S0010-7824(01)00218-9. PMID 11535214.
- ^ Yolton DP, Yolton RL, López R, Bogner B, Stevens R, Rao D (November 1994). "The effects of gender and birth control pill use on spontaneous blink rates". Journal of the American Optometric Association. 65 (11): 763–70. PMID 7822673.
- ^ أ ب Huber JC, Bentz EK, Ott J, Tempfer CB (September 2008). "Non-contraceptive benefits of oral contraceptives". Expert Opinion on Pharmacotherapy. 9 (13): 2317–25. doi:10.1517/14656566.9.13.2317. PMID 18710356. S2CID 73326364.
- ^ Nelson, Randy J. (2005). An introduction to behavioral endocrinology (3rd ed.). Sunderland, Mass: Sinauer Associates. ISBN 978-0-87893-617-5.[صفحة مطلوبة]
- ^ Vo C, Carney ME (December 2007). "Ovarian cancer hormonal and environmental risk effect". Obstetrics and Gynecology Clinics of North America. 34 (4): 687–700, viii. doi:10.1016/j.ogc.2007.09.008. PMID 18061864.
- ^ Bandera CA (June 2005). "Advances in the understanding of risk factors for ovarian cancer". The Journal of Reproductive Medicine. 50 (6): 399–406. PMID 16050564.
- ^ Pragout, D.; Laurence, V.; Baffet, H.; Raccah-Tebeka, B.; Rousset-Jablonski, C. (December 2018). "[Contraception and cancer: CNGOF Contraception Guidelines]". Gynécologie, Obstétrique, Fertilité & Sénologie. 46 (12): 834–844. doi:10.1016/j.gofs.2018.10.010. ISSN 2468-7189. PMID 30385358.
- ^ "Apri oral : Uses, Side Effects, Interactions, Pictures, Warnings & Dosing".
- ^ Blanco-Molina A, Monreal M (February 2010). "Venous thromboembolism in women taking hormonal contraceptives". Expert Review of Cardiovascular Therapy. 8 (2): 211–5. doi:10.1586/erc.09.175. PMID 20136607. S2CID 41309800.
- ^ Roach RE, Helmerhorst FM, Lijfering WM, Stijnen T, Algra A, Dekkers OM (August 2015). "Combined oral contraceptives: the risk of myocardial infarction and ischemic stroke". The Cochrane Database of Systematic Reviews. 8 (8): CD011054. doi:10.1002/14651858.CD011054.pub2. PMC 6494192. PMID 26310586.
- ^ Rang HP, Dale MM, Ritter JM, Flower RJ, Henderson G (2012). "The reproductive system". Rang and Dale's pharmacology (7th ed.). Edinburgh: Elsevier/Churchill Livingstone. p. 426. ISBN 978-0-7020-3471-8.
- ^ أ ب ت ESHRE Capri Workshop Group (2013). "Venous thromboembolism in women: a specific reproductive health risk". Human Reproduction Update. 19 (5): 471–82. doi:10.1093/humupd/dmt028. PMID 23825156.
- ^ Lidegaard Ø, Milsom I, Geirsson RT, Skjeldestad FE (July 2012). "Hormonal contraception and venous thromboembolism". Acta Obstetricia et Gynecologica Scandinavica. 91 (7): 769–78. doi:10.1111/j.1600-0412.2012.01444.x. PMID 22568831. S2CID 2691199.
- ^ Dunn N (April 2011). "The risk of deep venous thrombosis with oral contraceptives containing drospirenone". BMJ. 342: d2519. doi:10.1136/bmj.d2519. PMID 21511807. S2CID 42721801.
- ^ "Highlights of Prescribing Information for Yasmin" (PDF). FDA.
- ^ Cibula D, Gompel A, Mueck AO, La Vecchia C, Hannaford PC, Skouby SO, Zikan M, Dusek L (2010). "Hormonal contraception and risk of cancer". Human Reproduction Update. 16 (6): 631–50. doi:10.1093/humupd/dmq022. PMID 20543200.
- ^ أ ب Bast RC, Brewer M, Zou C, Hernandez MA, Daley M, Ozols R, Lu K, Lu Z, Badgwell D, Mills GB, Skates S, Zhang Z, Chan D, Lokshin A, Yu Y (2007). "Prevention and early detection of ovarian cancer: mission impossible?". Cancer Prevention. Recent Results in Cancer Research. Vol. 174. pp. 91–100. doi:10.1007/978-3-540-37696-5_9. ISBN 978-3-540-37695-8. PMID 17302189.
{{cite book}}:|journal=ignored (help) - ^ Vessey M, Yeates D, Flynn S (September 2010). "Factors affecting mortality in a large cohort study with special reference to oral contraceptive use". Contraception. 82 (3): 221–9. doi:10.1016/j.contraception.2010.04.006. PMID 20705149.
- ^ Gierisch JM, Coeytaux RR, Urrutia RP, Havrilesky LJ, Moorman PG, Lowery WJ, Dinan M, McBroom AJ, Hasselblad V, Sanders GD, Myers ER (November 2013). "Oral contraceptive use and risk of breast, cervical, colorectal, and endometrial cancers: a systematic review". Cancer Epidemiology, Biomarkers & Prevention. 22 (11): 1931–43. doi:10.1158/1055-9965.EPI-13-0298. PMID 24014598.
- ^ Anothaisintawee T, Wiratkapun C, Lerdsitthichai P, Kasamesup V, Wongwaisayawan S, Srinakarin J, Hirunpat S, Woodtichartpreecha P, Boonlikit S, Teerawattananon Y, Thakkinstian A (September 2013). "Risk factors of breast cancer: a systematic review and meta-analysis". Asia-Pacific Journal of Public Health. 25 (5): 368–87. doi:10.1177/1010539513488795. PMID 23709491. S2CID 206616972.
- ^ Zhu H, Lei X, Feng J, Wang Y (December 2012). "Oral contraceptive use and risk of breast cancer: a meta-analysis of prospective cohort studies". The European Journal of Contraception & Reproductive Health Care. 17 (6): 402–14. doi:10.3109/13625187.2012.715357. PMID 23061743. S2CID 33708638.
- ^ أ ب ت Lopez, Laureen M.; Edelman, Alison; Chen, Mario; Otterness, Conrad; Trussell, James; Helmerhorst, Frans M. (2013-07-02). Lopez, Laureen M (ed.). "Progestin-only contraceptives: effects on weight". The Cochrane Database of Systematic Reviews (7): CD008815. doi:10.1002/14651858.CD008815.pub3. ISSN 1469-493X. PMC 3855691. PMID 23821307.
- ^ أ ب Hatcher RD, Nelson AL (2004). "Combined Hormonal Contraceptive Methods". In Hatcher RD (ed.). Contraceptive technology (18th ed.). New York: Ardent Media, Inc. pp. 403, 432, 434. ISBN 978-0-9664902-5-1.
- ^ Speroff, Leon (2005). A clinical guide for contraception (4th ed.). Hagerstown, MD: Lippincott Williams & Wilkins. p. 72. ISBN 978-0-7817-6488-9.
- ^ Weir GC, DeGroot LJ, Grossman A, Marshall JF, Melmed S, Potts JT (2006). Endocrinology (5th ed.). St. Louis, Mo: Elsevier Saunders. p. 2999. ISBN 978-0-7216-0376-6.[صفحة مطلوبة]
- ^ Westhoff CL, Heartwell S, Edwards S, Zieman M, Stuart G, Cwiak C, Davis A, Robilotto T, Cushman L, Kalmuss D (April 2007). "Oral contraceptive discontinuation: do side effects matter?". American Journal of Obstetrics and Gynecology. 196 (4): 412.e1–6, discussion 412.e6–7. doi:10.1016/j.ajog.2006.12.015. PMC 1903378. PMID 17403440.
- ^ Seal BN, Brotto LA, Gorzalka BB (August 2005). "Oral contraceptive use and female genital arousal: methodological considerations". Journal of Sex Research. 42 (3): 249–58. doi:10.1080/00224490509552279. PMID 19817038. S2CID 10402534.
- ^ Higgins JA, Davis AR (July 2014). "Contraceptive sex acceptability: a commentary, synopsis and agenda for future research". Contraception. 90 (1): 4–10. doi:10.1016/j.contraception.2014.02.029. PMC 4247241. PMID 24792147.
- ^ Panzer C, Wise S, Fantini G, Kang D, Munarriz R, Guay A, Goldstein I (January 2006). "Impact of oral contraceptives on sex hormone-binding globulin and androgen levels: a retrospective study in women with sexual dysfunction". The Journal of Sexual Medicine. 3 (1): 104–13. doi:10.1111/j.1743-6109.2005.00198.x. PMID 16409223.
Description of the study results in Medical News Today: "Birth Control Pill Could Cause Long-Term Problems With Testosterone, New Research Indicates". January 4, 2006. - ^ Panzer C, Wise S, Fantini G, Kang D, Munarriz R, Guay A, Goldstein I (January 2006). "Impact of oral contraceptives on sex hormone-binding globulin and androgen levels: a retrospective study in women with sexual dysfunction". The Journal of Sexual Medicine. 3 (1): 104–13. doi:10.1111/j.1743-6109.2005.00198.x. PMID 16409223.
- ^ Miller G, Tybur JM, Jordan BD (November 2007). "Ovulatory cycle effects on tip earnings by lap dancers: economic evidence for human estrus?". Evolution and Human Behavior. 28 (6): 375–381. CiteSeerX 10.1.1.154.8176. doi:10.1016/j.evolhumbehav.2007.06.002.
- ^ Kulkarni J (July 2007). "Depression as a side effect of the contraceptive pill". Expert Opinion on Drug Safety. 6 (4): 371–4. doi:10.1517/14740338.6.4.371. PMID 17688380. S2CID 8836005.
- ^ أ ب Skovlund CW, Mørch LS, Kessing LV, Lidegaard Ø (November 2016). "Association of Hormonal Contraception With Depression". JAMA Psychiatry. 73 (11): 1154–1162. doi:10.1001/jamapsychiatry.2016.2387. PMID 27680324.
- ^ أ ب ت ث Zettermark S, Perez Vicente R, Merlo J (2018-03-22). "Hormonal contraception increases the risk of psychotropic drug use in adolescent girls but not in adults: A pharmacoepidemiological study on 800 000 Swedish women". PLOS ONE. 13 (3): e0194773. Bibcode:2018PLoSO..1394773Z. doi:10.1371/journal.pone.0194773. PMC 5864056. PMID 29566064.
- ^ Burnett-Watson K (October 2005). "Is The Pill Playing Havoc With Your Mental Health?". Archived from the original on 2007-03-20. Retrieved 2007-03-20.
{{cite journal}}: Cite journal requires|journal=(help), which cites: - ^ Young EA, Kornstein SG, Harvey AT, Wisniewski SR, Barkin J, Fava M, Trivedi MH, Rush AJ (August 2007). "Influences of hormone-based contraception on depressive symptoms in premenopausal women with major depression". Psychoneuroendocrinology. 32 (7): 843–53. doi:10.1016/j.psyneuen.2007.05.013. PMC 2100423. PMID 17629629.
- ^ ACOG Committee on Practice Bulletins-Gynecology (2006). "ACOG Practice Bulletin No. 73: Use of Hormonal Contraception in Women with Coexisting Medical Conditions". Obstetrics & Gynecology. 107 (6): 1453–72. doi:10.1097/00006250-200606000-00055. PMID 16738183.
- ^ World Health Organization (2004). "Low-dose combined oral contraceptives". Medical Eligibility Criteria for Contraceptive Use (third ed.). Geneva: Low-dose combined oral contraceptives. hdl:10665/42907. ISBN 978-92-4-156266-9.[صفحة مطلوبة]
- ^ FFPRHC (2006). "The UK Medical Eligibility Criteria for Contraceptive Use (2005/2006)" (PDF). Archived from the original (PDF) on 2007-06-19. Retrieved 2007-03-31.
- ^ Cilia La Corte AL, Carter AM, Turner AJ, Grant PJ, Hooper NM (December 2008). "The bradykinin-degrading aminopeptidase P is increased in women taking the oral contraceptive pill". Journal of the Renin-Angiotensin-Aldosterone System. 9 (4): 221–5. doi:10.1177/1470320308096405. PMID 19126663. S2CID 206729914.
- ^ "Gallstones". NDDIC. July 2007. Archived from the original on 2010-08-11. Retrieved 2010-08-13.
- ^ Raloff J (2013-09-23). "Birth control pills can limit muscle-training gains". Science News. Retrieved 2018-10-22.
- ^ "Love woes can be blamed on contraceptive pill: research – ABC News (Australian Broadcasting Corporation)". ABC News. Abc.net.au. 2008-08-14. Retrieved 2010-03-20.
- ^ Kollndorfer K, Ohrenberger I, Schöpf V (2016). "Contraceptive Use Affects Overall Olfactory Performance: Investigation of Estradiol Dosage and Duration of Intake". PLOS ONE. 11 (12): e0167520. Bibcode:2016PLoSO..1167520K. doi:10.1371/journal.pone.0167520. PMC 5176159. PMID 28002464.
- ^ Roberts SC, Gosling LM, Carter V, Petrie M (December 2008). "MHC-correlated odour preferences in humans and the use of oral contraceptives". Proceedings. Biological Sciences. 275 (1652): 2715–22. doi:10.1098/rspb.2008.0825. PMC 2605820. PMID 18700206.
- ^ Vercellini P, Eskenazi B, Consonni D, Somigliana E, Parazzini F, Abbiati A, Fedele L (2010). "Oral contraceptives and risk of endometriosis: a systematic review and meta-analysis". Human Reproduction Update. 17 (2): 159–70. doi:10.1093/humupd/dmq042. PMID 20833638.
- ^ Zimmerman Y, Eijkemans MJ, Coelingh Bennink HJ, Blankenstein MA, Fauser BC (2013). "The effect of combined oral contraception on testosterone levels in healthy women: a systematic review and meta-analysis". Human Reproduction Update. 20 (1): 76–105. doi:10.1093/humupd/dmt038. PMC 3845679. PMID 24082040.
- ^ Scholes D, Hubbard RA, Ichikawa LE, LaCroix AZ, Spangler L, Beasley JM, Reed S, Ott SM (September 2011). "Oral contraceptive use and bone density change in adolescent and young adult women: a prospective study of age, hormone dose, and discontinuation". The Journal of Clinical Endocrinology and Metabolism. 96 (9): E1380–7. doi:10.1210/jc.2010-3027. PMC 3167673. PMID 21752879.
- ^ The effects of broad-spectrum antibiotics on Combined contraceptive pills is not found on systematic interaction metanalysis (Archer, 2002), although "individual patients do show large decreases in the plasma concentrations of ethinylestradiol when they take certain other antibiotics" (Dickinson, 2001). "experts on this topic still recommend informing oral contraceptive users of the potential for a rare interaction" (DeRossi, 2002) and this remains current (2006) UK Family Planning Association advice Archived 2007-02-08 at the Wayback Machine.
- ^ Archer JS, Archer DF (June 2002). "Oral contraceptive efficacy and antibiotic interaction: a myth debunked". Journal of the American Academy of Dermatology. 46 (6): 917–23. doi:10.1067/mjd.2002.120448. PMID 12063491.
- ^ Dickinson BD, Altman RD, Nielsen NH, Sterling ML (November 2001). "Drug interactions between oral contraceptives and antibiotics". Obstetrics and Gynecology. 98 (5 Pt 1): 853–60. doi:10.1016/S0029-7844(01)01532-0. PMID 11704183. S2CID 41354899.
- ^ DeRossi SS, Hersh EV (October 2002). "Antibiotics and oral contraceptives". Dental Clinics of North America. 46 (4): 653–64. CiteSeerX 10.1.1.620.9933. doi:10.1016/S0011-8532(02)00017-4. PMID 12436822.
- ^ Berry-Bibee, Erin N.; Kim, Myong-Jin; Tepper, Naomi K.; Riley, Halley E. M.; Curtis, Kathryn M. (December 2016). "Co-administration of St. John's wort and hormonal contraceptives: a systematic review". Contraception. 94 (6): 668–677. doi:10.1016/j.contraception.2016.07.010. ISSN 1879-0518. PMID 27444983.
- ^ أ ب ت ث ج ح Nelson AL, Cwiak C (2011). "Combined oral contraceptives (COCs)". In Hatcher RA, Trussell J, Nelson AL, Cates W, Kowal D, Policar MS (eds.). Contraceptive technology (20th revised ed.). New York: Ardent Media. pp. 249–341. ISBN 978-1-59708-004-0. ISSN 0091-9721. OCLC 781956734. pp. 257–258:
Mechanism of action
COCs prevent fertilization and, therefore, qualify as contraceptives. There is no significant evidence that they work after fertilization. The progestins in all COCs provide most of the contraceptive effect by suppressing ovulation and thickening cervical mucus, although the estrogens also make a small contribution to ovulation suppression. Cycle control is enhanced by the estrogen.
Because COCs so effectively suppress ovulation and block ascent of sperm into the upper genital tract, the potential impact on endometrial receptivity to implantation is almost academic. When the two primary mechanisms fail, the fact that pregnancy occurs despite the endometrial changes demonstrates that those endometrial changes do not significantly contribute to the pill's mechanism of action. - ^ أ ب ت Speroff L, Darney PD (2011). "Oral contraception". A clinical guide for contraception (5th ed.). Philadelphia: Lippincott Williams & Wilkins. pp. 19–152. ISBN 978-1-60831-610-6.
- ^ أ ب ت Levin ER, Hammes SR (2011). "Estrogens and progestins". In Brunton, Chabner BA, Knollmann BC (eds.). Goodman & Gilman's pharmacological basis of therapeutics (12th ed.). New York: McGraw-Hill Medical. pp. 1163–1194. ISBN 978-0-07-162442-8.
- ^ Glasier, Anna (2010). "Contraception". In Jameson, J. Larry; De Groot, Leslie J. (eds.). Endocrinology (6th ed.). Philadelphia: Saunders Elsevier. pp. 2417–2427. ISBN 978-1-4160-5583-9.
- ^ أ ب ت ث ج Nelson AL, Cwiak C (2011). "Combined oral contraceptives". In Hatcher RA, Trussell J, Nelson AL, Cates W Jr, Kowal D, Policar MS (eds.). Contraceptive technology (20th revised ed.). New York: Ardent Media. pp. 253–254. ISBN 978-1-59708-004-0. ISSN 0091-9721. OCLC 781956734.
Ten different progestins have been used in the COCs that have been sold in the United States. Several different classification systems for the progestins exist, but the one most commonly used system recapitulates the history of the pill in the United States by categorizing the progestins into the so-called "generations of progestins." The first three generations of progestins are derived from 19-nortestosterone. The fourth generation is drospirenone. Newer progestins are hybrids.
First-generation progestins. First-generation progestins include noretynodrel, norethisterone, norethisterone acetate, and etynodiol diacetate… These compounds have the lowest potency and relatively short half-lives. The short half-life did not matter in the early, high-dose pills but as doses of progestin were decreased in the more modern pills, problems with unscheduled spotting and bleeding became more common.
Second-generation progestins. To solve the problem of unscheduled bleeding and spotting, the second generation progestins (norgestrol and levonorgestrel) were designed to be significantly more potent and to have longer half-lives than norethisterone-related progestins ... The second-generation progestins have been associated with more androgen-related side-effects such as adverse effect on lipids, oily skin, acne, and facial hair growth.
Third-generation progestins. Third-generation progestins (desogestrel, norgestimate and elsewhere, gestodene) were introduced to maintain the potent progestational activity of second-generation progestins, but to reduce androgeneic side effects. Reduction in androgen impacts allows a fuller expression of the pill's estrogen impacts. This has some clinical benefits… On the other hand, concern arose that the increased expression of estrogen might increase the risk of venous thromboembolism (VTE). This concern introduced a pill scare in Europe until international studies were completed and correctly interpreted.
Fourth-generation progestins. Drospirenone is an analogue of spironolactone, a potassium-sparing diuretic used to treat hypertension. Drospirenone possesses anti-mineralocorticoid and anti-androgenic properties. These properties have led to new contraceptive applications, such as treatment of premenstrual dysphoric disorder and acne… In the wake of concerns around possible increased VTE risk with less androgenic third-generation formulations, those issues were anticipated with drospirenone. They were clearly answered by large international studies.
Next-generation progestins. More recently, newer progestins have been developed with properties that are shared with different generations of progestins. They have more profound, diverse, and discrete effects on the endometrium than prior progestins. This class would include dienogest (United States) and nomegestrol (Europe). - ^ أ ب ت ث ج Speroff L, Darney PD (2011). "Oral contraception". A clinical guide for contraception (5th ed.). Philadelphia: Lippincott Williams & Wilkins. p. 40. ISBN 978-1-60831-610-6.
- ^ Lara Marks (2001). Sexual Chemistry: A History of the Contraceptive Pill. Yale University Press. pp. 73–75, 77–78. ISBN 978-0-300-08943-1.
- ^ Annetine Gelijns (1991). Innovation in Clinical Practice: The Dynamics of Medical Technology Development. National Academies. pp. 167–. NAP:13513.
- ^ Robert W. Blum (22 October 2013). Adolescent Health Care: Clinical Issues. Elsevier Science. pp. 216–. ISBN 978-1-4832-7738-7.
- ^ Andrea Tone; Elizabeth Siegel Watkins (8 January 2007). Medicating Modern America: Prescription Drugs in History. NYU Press. pp. 117–119. ISBN 978-0-8147-8301-6.
- ^ John L. McGuire (2000). Pharmaceuticals, 4 Volume Set. Wiley. p. 1580,1599. ISBN 978-3-527-29874-7.
- ^ Bhasker Rao (1 January 1998). Clinical Gynecology (4Th ed.). Orient Blackswan. pp. 163–. ISBN 978-81-250-1622-9.
- ^ A. Labhart (6 December 2012). Clinical Endocrinology: Theory and Practice. Springer Science & Business Media. pp. 571–. ISBN 978-3-642-96158-8.
- ^ Goldzieher JW, Rudel HW (October 1974). "How the oral contraceptives came to be developed". JAMA. 230 (3): 421–5. doi:10.1001/jama.230.3.421. PMID 4606623.
- ^ Goldzieher JW (May 1982). "Estrogens in oral contraceptives: historical perspectives". The Johns Hopkins Medical Journal. 150 (5): 165–9. PMID 7043034.
- ^ Perone N (Spring 1993). "The history of steroidal contraceptive development: the progestins". Perspectives in Biology and Medicine. 36 (3): 347–62. doi:10.1353/pbm.1993.0054. PMID 8506121. S2CID 46312750.
- ^ Goldzieher JW (Spring 1993). "The history of steroidal contraceptive development: the estrogens". Perspectives in Biology and Medicine. 36 (3): 363–8. doi:10.1353/pbm.1993.0066. PMID 8506122. S2CID 28975213.
- ^ أ ب ت Maisel AQ (1965). The Hormone Quest. New York: Random House. OCLC 543168.
- ^ أ ب Asbell B (1995). The Pill: A Biography of the Drug That Changed the World. New York: Random House. ISBN 978-0-679-43555-6.
- ^ Lehmann PA, Bolivar A, Quintero R (March 1973). "Russell E. Marker. Pioneer of the Mexican steroid industry". Journal of Chemical Education. 50 (3): 195–9. Bibcode:1973JChEd..50..195L. doi:10.1021/ed050p195. PMID 4569922.
- ^ أ ب Vaughan P (1970). The Pill on Trial. New York: Coward-McCann. OCLC 97780.
- ^ أ ب Tone A (2001). Devices & Desires: A History of Contraceptives in America. New York: Hill and Wang. ISBN 978-0-8090-3817-6.
- ^ أ ب ت ث Pincus G, Bialy G (1964). Drugs Used in Control of Reproduction. Advances in Pharmacology. Vol. 3. pp. 285–313. doi:10.1016/S1054-3589(08)61115-1. ISBN 9780120329038. PMID 14232795.
The original observation of Makepeace et al. (1937) that progesterone inhibited ovulation in the rabbit was substantiated by Pincus and Chang (1953). In women, 300 mg of progesterone per day taken orally resulted in ovulation inhibition in 80% of cases (Pincus, 1956). The high dosage and frequent incidence of breakthrough bleeding limited the practical application of the method. Subsequently, the utilization of potent 19-norsteroids, which could be given orally, opened the field to practical oral contraception.
{{cite book}}:|journal=ignored (help) - ^ Nance K. "Jonathan Eig on 'The Birth of the Pill'". Chicago Tribune.
- ^ "The Birth of the Pill | W. W. Norton & Company".
- ^ Manning K (17 October 2014). "Book review: 'The Birth of the Pill,' and the reinvention of sex, by Jonathan Eig" – via washingtonpost.com.
- ^ أ ب ت Reed J (1978). From Private Vice to Public Virtue: The Birth Control Movement and American Society Since 1830. New York: Basic Books. ISBN 978-0-465-02582-4.
- ^ Speroff L (2009). A Good Man: Gregory Goodwin Pincus: The Man, His Story, The Birth Control Pill. Portland, Oregon: Arnica. ISBN 978-0-9801942-9-6.
- ^ Fields A (2003). Katharine Dexter McCormick: Pioneer for Women's Rights. Westport, Conn.: Prager. ISBN 978-0-275-98004-7.
- ^ McLaughlin L (1982). The Pill, John Rock, and the Church: The Biography of a Revolution. Boston: Little, Brown. ISBN 978-0-316-56095-5.
- ^ Rock J, Garcia CR, Pincus G (1957). "Synthetic progestins in the normal human menstrual cycle". Recent Progress in Hormone Research. 13: 323–39, discussion 339–46. PMID 13477811.
- ^ أ ب ت Pincus G (December 1958). "The hormonal control of ovulation and early development". Postgraduate Medicine. 24 (6): 654–60. doi:10.1080/00325481.1958.11692305. PMID 13614060.
- ^ أ ب ت Pincus, Gregory (1959). Progestational Agents and the Control of Fertility. Vitamins & Hormones. Vol. 17. pp. 307–324. doi:10.1016/S0083-6729(08)60274-5. ISBN 9780127098173. ISSN 0083-6729.
Ishikawa et al. (1957) employing the same regime of progesterone administration also observed suppression of ovulation in a proportion of the cases taken to laparotomy. Although sexual intercourse was practised freely by the subjects of our experiments and those of Ishikawa el al., no pregnancies occurred. Since ovulation presumably took place in a proportion of cycles, the lack of any pregnancies may be due to chance, but Ishikawa et al. (1957) have presented data indicating that in women receiving oral progesterone the cervical mucus becomes impenetrable to sperm.
- ^ أ ب Diczfalusy E (December 1965). "Probable mode of action of oral contraceptives". BMJ. 2 (5475): 1394–9. doi:10.1136/bmj.2.5475.1394. PMC 1847181. PMID 5848673.
At the Fifth International Conference on Planned Parenthood in Tokyo, Pincus (1955) reported an ovulation inhibition by progesterone or norethynodrel1 taken orally by women. This report indicated the beginning of a new era in the history of contraception. ... That the cervical mucus might be one of the principal sites of action was suggested by the first studies of Pincus (1956, 1959) and of Ishikawa et al. (1957). These investigators found that no pregnancies occurred in women treated orally with large doses of progesterone, though ovulation was inhibited only in some 70% of the cases studied. ... The mechanism of protection in this method—and probably in that of Pincus (1956) and of Ishikawa et al. (1957)—must involve an effect on the cervical mucus and/or endometrium and Fallopian tubes.
- ^ أ ب Annette B. Ramírez de Arellano; Conrad Seipp (10 October 2017). Colonialism, Catholicism, and Contraception: A History of Birth Control in Puerto Rico. University of North Carolina Press. pp. 107–. ISBN 978-1-4696-4001-3.
Still, neither of the two researchers was completely satisfied with the results. Progesterone tended to cause "premature menses," or breakthrough bleeding, in approximately 20 percent of the cycles, an occurrence that disturbed the patients and worried Rock.17 In addition, Pincus was concerned about the failure to inhibit ovulation in all the cases. Only large doses of orally administered progesterone could insure the suppression of ovulation, and these doses were expensive. The mass use of this regimen as a birth control method was thus seriously imperiled.
- ^ Chang MC (September 1978). "Development of the oral contraceptives". American Journal of Obstetrics and Gynecology. 132 (2): 217–9. doi:10.1016/0002-9378(78)90928-6. PMID 356615.
- ^ Garcia CR, Pincus G, Rock J (November 1956). "Effects of certain 19-nor steroids on the normal human menstrual cycle". Science. 124 (3227): 891–3. Bibcode:1956Sci...124..891R. doi:10.1126/science.124.3227.891. PMID 13380401.
- ^ أ ب Rock J, García C (1957). "Observed effects of 19-nor steroids on ovulation and menstruation". Proceedings of a Symposium on 19-Nor Progestational Steroids. Chicago: Searle Research Laboratories. pp. 14–31. OCLC 935295.
- ^ Pincus G, Rock J, Garcia CR, Ricewray E, Paniagua M, Rodriguez I (June 1958). "Fertility control with oral medication". American Journal of Obstetrics and Gynecology. 75 (6): 1333–46. doi:10.1016/0002-9378(58)90722-1. PMID 13545267.
- ^ Segal SJ (2003). "The Pill and the IUD Modernized Contraception". Under the Banyan Tree: A Population Scientist's Odyssey. Oxford: Oxford University Press. pp. [https://archive.org/details/underbanyantreep00sega/page/70 70–78]. ISBN 978-0-19-515456-6.
- ^ García CR (December 2004). "Development of the pill". Annals of the New York Academy of Sciences. 1038: 223–6. Bibcode:2004NYASA1038..223G. doi:10.1196/annals.1315.031. PMID 15838117. S2CID 25550745.
- ^ Strauss JF, Mastroianni L (January 2005). "In memoriam: Celso-Ramon Garcia, M.D. (1922-2004), reproductive medicine visionary". Journal of Experimental & Clinical Assisted Reproduction. 2 (1): 2. doi:10.1186/1743-1050-2-2. PMC 548289. PMID 15673473.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ أ ب ت ث ج Junod SW, Marks L (April 2002). "Women's trials: the approval of the first oral contraceptive pill in the United States and Great Britain". Journal of the History of Medicine and Allied Sciences. 57 (2): 117–60. doi:10.1093/jhmas/57.2.117. PMID 11995593. S2CID 36533080.
- ^ Ramírez de Arellano AB, Seipp C (1983). Colonialism, Catholicism, and Contraception: A History of Birth Control in Puerto Rico. Chapel Hill: University of North Carolina Press. ISBN 978-0-8078-1544-1.
- ^ Rice-Wray E (1957). "Field Study with Enovid as a Contraceptive Agent". Proceedings of a Symposium on 19-Nor Progestational Steroids. Chicago: Searle Research Laboratorie. pp. 78–85. OCLC 935295.
- ^ Marsh M, Ronner W (2008). The Fertility Doctor: John Rock and the Reproductive Revolution. Baltimore: The Johns Hopkins University Press. pp. 188–197. ISBN 978-0-8018-9001-7.
- ^ Tyler ET, Olson HJ (April 1959). "Fertility promoting and inhibiting effects of new steroid hormonal substances". Journal of the American Medical Association. 169 (16): 1843–54. doi:10.1001/jama.1959.03000330015003. PMID 13640942.
- ^ Winter IC (1957). "Summary". Proceedings of a Symposium on 19-Nor Progestational Steroids. Chicago: Searle Research Laboratories. pp. 120–122. OCLC 935295.
- ^ أ ب ت ث Marks L (2001). Sexual Chemistry: A History of the Contraceptive Pill. New Haven: Yale University Press. ISBN 978-0-300-08943-1.
- ^ Winter IC (May 1970). "Industrial pressure and the population problem--the FDA and the pill". JAMA. 212 (6): 1067–8. doi:10.1001/jama.212.6.1067. PMID 5467404.
- ^ أ ب ت ث ج Watkins ES (1998). On the Pill: A Social History of Oral Contraceptives, 1950–1970. Baltimore: Johns Hopkins University Press. ISBN 978-0-8018-5876-5.
- ^ Winter IC (March 1965). "The incidence of thromboembolism in Enovid users". Metabolism. 14 (Supplement): SUPPL:422–8. doi:10.1016/0026-0495(65)90029-6. PMID 14261427.
- ^ Jordan WM, Anand JK (November 18, 1961). "Pulmonary embolism". Lancet. 278 (7212): 1146–1147. doi:10.1016/S0140-6736(61)91061-3.
- ^ Seaman B (1969). The Doctors' Case Against the Pill. New York: P. H. Wyden. ISBN 978-0-385-14575-6.
- ^ FDA (June 11, 1970). "Statement of policy concerning oral contraceptive labeling directed to users". Federal Register. 35 (113): 9001–9003.
- ^ FDA (January 31, 1978). "Oral contraceptives; requirement for labeling directed to the patient". Federal Register. 43 (21): 4313–4334.
- ^ FDA (May 25, 1989). "Oral contraceptives; patient package insert requirement". Federal Register. 54 (100): 22585–22588.
- ^ أ ب "Prescriptive Authority for Pharmacists: Oral Contraceptives". www.pharmacytimes.com. Retrieved 2019-08-02.
- ^ "Pharmacist Prescribing for Hormonal Contraceptive Medications". NASPA. Retrieved 2019-08-02.
- ^ "Pharmacists Authorized to Prescribe Birth Control in More States". NASPA. 2017-05-04. Retrieved 2019-08-02.
- ^ أ ب "History of Schering AG". Archived from the original on April 15, 2008. Retrieved 2007-12-06.
{{cite web}}: CS1 maint: bot: original URL status unknown (link) - ^ Karl Van den Broeck "Gynaecoloog Ferdinand Peeters: De vergeten stiefvader van de pil" (Gynecologist Ferdinand Peeters: The forgotten stepfather of the pill) in Knack Extra #4, March 5, 2010, pp. 6–13. (In Dutch.)
- ^ Hope A (May 24, 2010). "The little pill that could". Flanders Today.
- ^ Mears E (November 1961). "Clinical trials of oral contraceptives". British Medical Journal. 2 (5261): 1179–83. doi:10.1136/bmj.2.5261.1179. PMC 1970272. PMID 14471934.
- ^ Eckstein P, Waterhouse JA, Bond GM, Mills WG, Sandilands DM, Shotton DM (November 1961). "The Birmingham oral contraceptive trial". British Medical Journal. 2 (5261): 1172–9. doi:10.1136/bmj.2.5261.1172. PMC 1970253. PMID 13889122.
- ^ أ ب Pullen D (October 1962). ""Conovid-E" as an oral contraceptive". British Medical Journal. 2 (5311): 1016–9. doi:10.1136/bmj.2.5311.1016. PMC 1926317. PMID 13972503.
- ^ أ ب Mears E, Grant EC (July 1962). ""Anovlar" as an oral contraceptive". British Medical Journal. 2 (5297): 75–9. doi:10.1136/bmj.2.5297.75. PMC 1925289. PMID 14471933.
- ^ "Annotations". British Medical Journal. 2 (5258): 1007–9. October 1961. doi:10.1136/bmj.2.3490.1009. PMC 1970146. PMID 20789252.
"Medical News". BMJ. 2 (5258): 1032–1034. 1961. doi:10.1136/bmj.2.5258.1032. S2CID 51696624. - ^ Chàvez L, Takahashi A, Yoshimoto T, Su CC, Sugawara T, Fujii Y (March 1990). "Morphological changes in normal canine basilar arteries after transluminal angioplasty". Neurological Research. 12 (1): 12–6. doi:10.1136/bmj.2.5266.1584. PMID 1970619. S2CID 8849008.
- ^ "Subsidizing birth control". Time. Vol. 78, no. 24. December 15, 1961. p. 55. Archived from the original on February 5, 2008.
- ^ Dourlen Rollier AV (October 1972). "[Contraception: yes, but...]". Fertilité, Orthogénie. 4 (4): 185–8. PMID 12306278.
- ^ "The Aids Generation: the pill takes priority?". Science Actualities. 2000. Retrieved 2006-09-07.
- ^ "Djerassi on birth control in Japan – abortion 'yes,' pill 'no'" (Press release). Stanford University News Service. 1996-02-14. Archived from the original on 2007-01-06. Retrieved 2006-08-23.
- ^ Wudunn, Sheryl (27 April 1999). "Japan's Tale of Two Pills: Viagra and Birth Control". The New York Times.
- ^ Efron S (3 June 1999). "Japan OKs Birth Control Pill After Decades of Delay". Los Angeles Times.
- ^ أ ب Aiko Hayashi (2004-08-20). "Japanese Women Shun The Pill". CBS News. Retrieved 2006-06-12.
- ^ "The Pill". Time. April 7, 1967. Archived from the original on February 19, 2005. Retrieved June 16, 2020.
- ^ Westhoff, Carolyn (15 December 2015). "How Obamacare Explains the Rising Popularity of IUDs". Public Health Now at Columbia University. Retrieved 2020-06-17.
- ^ "The Birth Control Pill: A History" (PDF).
- ^ Goldin C, Katz L (2002). "The Power of the Pill: Oral Contraceptives and Women's Career and Marriage Decisions" (PDF). Journal of Political Economy. 110 (4): 730–770. CiteSeerX 10.1.1.473.6514. doi:10.1086/340778. S2CID 221286686.
- ^ "The Pill". Equality Archive. 2017-03-01. Retrieved 2017-03-09.
- ^ Weigel G (2002). The Courage to Be Catholic: Crisis, Reform, and the Renewal of the Church. Basic Books.
- ^ "Pillenverbot bleibt Streitfrage zwischen den Konfessionen". Focus Online.
- ^ أ ب ت "1970 Year in Review". UPI.
- ^ Winnick C (1968). "The Beige Epoch: Depolarization of Sex Roles in America". The Annals of the American Academy of Political and Social Science. 376: 18–24. doi:10.1177/000271626837600103. JSTOR 1037799. S2CID 145158114.
- ^ "Richard Brautigan: The Pill versus The Springhill Mine Disaster". www.brautigan.net. Retrieved 2017-12-01.
- ^ "The pill and the marriage revolution | The Clayman Institute for Gender Research". gender.stanford.edu. Archived from the original on 2017-12-12. Retrieved 2017-12-01.
- ^ أ ب ت Williams RJ, Johnson AC, Smith JJ, Kanda R (May 2003). "Steroid estrogens profiles along river stretches arising from sewage treatment works discharges". Environmental Science & Technology. 37 (9): 1744–50. Bibcode:2003EnST...37.1744W. doi:10.1021/es0202107. PMID 12775044.
- ^ "Not Quite Worry-Free". Environment. 45 (1): 6–7. Jan–Feb 2003. doi:10.1080/00139150309604545. S2CID 218496430.
- ^ Batt S (Spring 2005). "Pouring Drugs Down the Drain" (PDF). Herizons. 18 (4): 12–3. Archived from the original (PDF) on 2012-03-15. Retrieved 2011-12-04.
- ^ Zeilinger J, Steger-Hartmann T, Maser E, Goller S, Vonk R, Länge R (December 2009). "Effects of synthetic gestagens on fish reproduction". Environmental Toxicology and Chemistry. 28 (12): 2663–70. doi:10.1897/08-485.1. PMID 19469587.
- ^ Johnson AC, Williams RJ, Simpson P, Kanda R (May 2007). "What difference might sewage treatment performance make to endocrine disruption in rivers?". Environmental Pollution. 147 (1): 194–202. doi:10.1016/j.envpol.2006.08.032. PMID 17030080.
- ^ Malcolm Potts; Leah Marsh (February 2010). "THE POPULATION FACTOR: How does it relate to climate change?" (PDF). OurPlanet.com. Archived from the original (PDF) on 4 March 2016. Retrieved 22 June 2015.
- ^ Cafaro P. "Alternative Climate Wedges – Population Wedge". Philip Cafaro. Retrieved 22 June 2015.
- ^ Wire T (10 September 2009). "Contraception is 'greenest' technology". London School of Economics. Retrieved 22 June 2015.
External links
- The Birth Control Pill—CBC Digital Archives
- The Birth of the Pill—slide show by Life magazine
- CS1 maint: unflagged free DOI
- CS1 maint: location missing publisher
- CS1 maint: others
- CS1 الإنجليزية الأمريكية-language sources (en-us)
- مقالات بالمعرفة بحاجة لذكر رقم الصفحة بالمصدر from August 2012
- CS1 errors: periodical ignored
- CS1 maint: bot: original URL status unknown
- Missing redirects
- Short description is different from Wikidata
- Articles with unsourced statements from April 2017
- Articles with unsourced statements from August 2020
- Articles with hatnote templates targeting a nonexistent page
- Articles with unsourced statements from December 2020
- Citation overkill
- Articles tagged with the inline citation overkill template from March 2021
- Combined oral contraceptives
- Hepatotoxins
- Sexual revolution
- World Health Organization essential medicines