تليف كيسي
| تليف كيسي | |
|---|---|
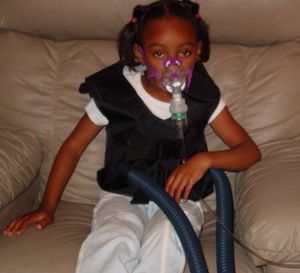 | |
| A breathing treatment for cystic fibrosis, using a mask nebuliser and a ThAIRapy Vest | |
| التبويب والمصادر الخارجية | |
| التخصص | علم الوراثة الطبي, طب الأطفال, طب الصدر |
| ICD-10 | E84. |
| ICD-9-CM | 277.0 |
| OMIM | 219700 |
| DiseasesDB | 3347 |
| MedlinePlus | 000107 |
| eMedicine | ped/535 |
| Patient UK | فشل عرض الخاصية P1461: لم يتم العثور على الخاصية P1461. تليف كيسي |
| MeSH | D003550 |
التليف الكيسي (Cystic Fibrosis) هو مرض وراثي يحدث فيه خلل استقلابي في عمل الغدد خارجية الإفراز مما يؤثر بصورة كبيرة على وظائف كثيرة في الجسم.
أعراض الافراد المصابين بالتليف الكيسي تعتمد على سن الفرد، ومدى هذا المرض يؤثر على أجهزة محددة، قبل العلاج، تطاول اثار التليف الكيسي أجهزة التنفس، والهضم، والتكاثر الجنسي. الاعراض الأخرى راجع يبدو من خلال ما تبقى من مرحلة الطفولة وأوائل مرحلة البلوغ. وتشمل هذه المشاكل مع استمرار النمو، بداية من امراض الرئه، والصعوبات المتزايدة مع سوء امتصاص الفيتامينات والمواد المغذيه من قبل الجهاز الهضمي. وبالإضافة إلى ذلك، صعوبات مع الخصوبه.
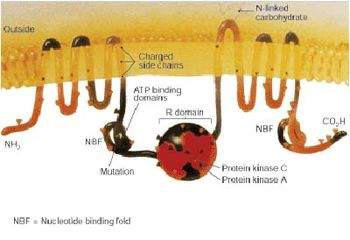
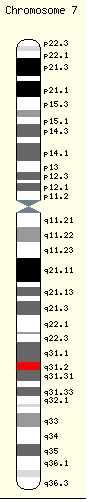
حدَّد الباحثون في عام 1989م المورِّث (الجين) الشاذ الذي يسبب التليف الكيسي، ويُوجد هذا المورِّث على الصبغيّ (الكروموزوم) السابع وهو زوج من 23 زوجاً من الصبغيِّات الموجودة في خلايا الإنسان. ويكون الشخص الذي لديه صبغيان من صبغيِّات التليُّف الكيسي على هذا الزوج مصابًا بالمرض. ويُسمى الذين يحملون مورثة طبيعية ومورِّثة واحدة من مورِّثات التليُّف الكيسي حاملي المرض ولا يكونون مصابين بالمرض. واحتمال وراثة طفل أبواه حاملان للمرض هي واحد في كل أربع حالات.
ويفقد المصابون بهذا المرض وزنهم، ويعانون من السعال المستمر، وخمجات الصدر. ويصاب قرابة 10% من الأطفال حديثي الولادة، المصابين بالمرض بانسداد يسمى العِلّوص العِقي يتطلب جراحة عاجلة. ويستطيع الأطباء تشخيص المرض باختبار العَرق الذي يختبر الملح الزائد في العَرَق.
يعاني المصابون بالتليف الكيسي من سوء التغذية، لأن المادة المخاطية تسد قناة البنكرياس مما يمنع الانسياب الطبيعي للخمائر (الإنزيمات) الهاضمة، التي تعمل على تفتيت الطعام داخل الأمعاء. كما تسد منافذ الهواء في الرئتين وتصبحان عُرضة للعدوى السريعة.
وكان ضحايا مرض التليف الكيسي فيما مضى يموتون في طفولتهم. أما اليوم فإن فرصة البقاء على قيد الحياة حتى سن البلوغ تصل إلى75%. وتهدف وسائل العلاج الحديثة إلى جعل منافذ الهواء في الرئتين نظيفة قدر الإمكان، باستخدام وسائل العلاج الطبيعي. ويمكن اتخاذ إجراءات وقائية ضد خمجات الصدر، أو علاجها، للتقليل من الضرر الذي يصيب الرئة. وأصبح بالإمكان منذ ثمانينيَّات القرن العشرين زراعة القلب والرئة لبعض الأطفال الكبار، والشباب البالغين، المصابة رئاتهم بضرر بالغ.
لا يوجد علاج للتليف الكيسي، ويموت كثير من المصابين بالتليف الكيسي في الثلاثينات من العمر من فشل الرئه ورغم فشل مع العديد من العلاجات الجديدة التي يجري عرض متوسط العمر المتوقع للشخص مع راجع آخذ في الازدياد. في نهاية المطاف، وكثيرا ما يكون لازما زرع الرئه.
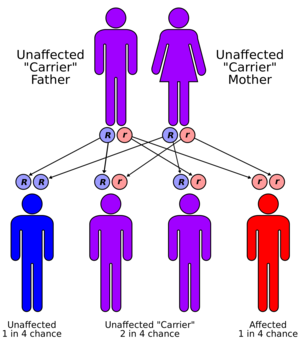
وراثية التليف الكيسي
التليف الكيسي يَعتبر صفة غير جنسية متنحية.
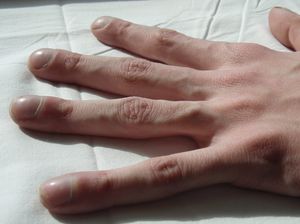
التشخيص
يفقد المصابون بمرض التليف الكيسي وزنهم، ويعانون من السعال المستمر، وخمجات الصدر. ويصاب قرابة 10% من الأطفال حديثي الولادة، المصابين بالمرض بانسداد يسمى العِلّوص العِقي يتطلب جراحة عاجلة. ويستطيع الأطباء تشخيص المرض باختبار العَرق الذي يختبر الملح الزائد في العَرَق.الافراد المصابين بالتليف الكيسي يمكن تشخيصها قبل الولادة عن طريق الفحص الوراثي أو في مرحلة الطفولة المبكره عن طريق اختبار العرق.
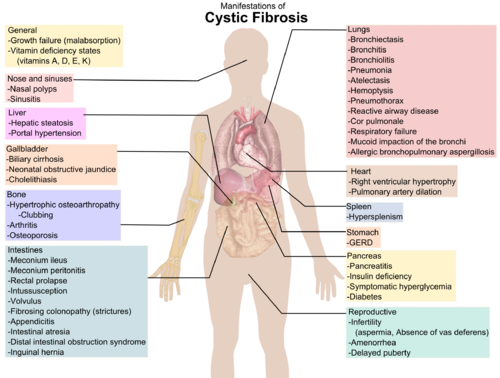
المضاعفات
يعاني المصابون بالتليف الكيسي من سوء التغذية، لأن المادة المخاطية تسد قناة البنكرياس مما يمنع الانسياب الطبيعي للخمائر (الإنزيمات) الهاضمة، التي تعمل على تفتيت الطعام داخل الأمعاء. كما تسد منافذ الهواء في الرئتين وتصبحان عُرضة للعدوى السريعة
المعالجة
وكان ضحايا مرض التليف الكيسي فيما مضى يموتون في طفولتهم. أما اليوم فإن فرصة البقاء على قيد الحياة حتى سن البلوغ تصل إلى75%. وتهدف وسائل العلاج الحديثة إلى جعل منافذ الهواء في الرئتين نظيفة قدر الإمكان، باستخدام وسائل العلاج الطبيعي. ويمكن اتخاذ إجراءات وقائية ضد خمجات الصدر، أو علاجها، للتقليل من الضرر الذي يصيب الرئة. وأصبح بالإمكان منذ ثمانينيَّات القرن العشرين زراعة القلب والرئة لبعض الأطفال الكبار، والشباب البالغين، المصابة رئاتهم بضرر بالغ.
علم الأوبئة
| التحور | التواتر worldwide[2] |
|---|---|
| ΔF508 | 66%-70%[3] |
| G542X | 2.4% |
| G551D | 1.6% |
| N1303K | 1.3% |
| W1282X | 1.2% |
| All others | 27.5% |
التاريخ

مراجع
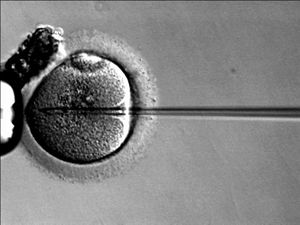
Gene therapy has been explored as a potential cure for cystic fibrosis. Ideally, gene therapy attempts to place a normal copy of the CFTR gene into affected cells. Transferring the normal CFTR gene into the affected epithelium cells would result in the production of functional CFTR in all target cells, without adverse reactions or an inflammation response. Studies have shown that to prevent the lung manifestations of cystic fibrosis, only 5-10% the normal amount of CFTR gene expression is needed.[4] Multiple approaches have been tested for gene transfer, such as liposomes and viral vectors in animal models and clinical trials. However, both methods were found to be relatively inefficient treatment options.[5] The main reason is that very few cells take up the vector and express the gene, so the treatment has little effect. Additionally, problems have been noted in cDNA recombination, such that the gene introduced by the treatment is rendered unusable.[6]
انظرأيضا
المصادر
- ^ Kliegman, Robert; Richard M Kliegman (2006). Nelson essentials of pediatrics. St. Louis, Mo: Elsevier Saunders. ISBN 0-8089-2325-0.
{{cite book}}: CS1 maint: multiple names: authors list (link) - ^ Araújo FG, Novaes FC, Santos NP; et al. (2005). "Prevalence of deltaF508, G551D, G542X, and R553X mutations among cystic fibrosis patients in the North of Brazil". Braz. J. Med. Biol. Res. 38 (1): 11–5. doi:10.1590/S0100-879X2005000100003. PMID 15665983.
{{cite journal}}: Explicit use of et al. in:|author=(help); Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - ^ خطأ استشهاد: وسم
<ref>غير صحيح؛ لا نص تم توفيره للمراجع المسماةkumar2007 - ^ Ramalho AS, Beck S, Meyer M, Penque D, Cutting GR, Amaral MD (2002). "Five percent of normal cystic fibrosis transmembrane conductance regulator mRNA ameliorates the severity of pulmonary disease in cystic fibrosis". Am. J. Respir. Cell Mol. Biol. 27 (5): 619–27. PMID 12397022.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - ^ Tate S, Elborn S (2005). "Progress towards gene therapy for cystic fibrosis". Expert Opin Drug Deliv. 2 (2): 269–80. doi:10.1517/17425247.2.2.269. PMID 16296753.
{{cite journal}}: Unknown parameter|month=ignored (help) - ^ http://www.ncbi.nlm.nih.gov/entrez/dispomim.cgi?id=219700
قراءات أضافية
- Fungal etiology in CF-associated infections reviewed extensively by Pihet et al.: Pihet M, Carrere J, Cimon B, Chabasse D, Delhaes L, Symoens F, Bouchara JP (2009). "Occurrence and relevance of filamentous fungi in respiratory secretions of patients with cystic fibrosis--a review". Med Mycol. 47 (4): 387–97. doi:10.1080/13693780802609604. PMID 19107638.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - Mowska, Patryk, Daniel Lorentzen, Katherine Excoffon, Joseph Zabner, Paul B. McCray, William M. Nauseef, Corinne Dupuy, and Botond Bánfi. A novel host defense system of airways is defective in cystic fibrosis. American Journal of Respiratory and Critical Care Medicine, 1 Nov. 2006. Web. 26 Nov. 2009
- Childers M, Eckel G, Himmel A, Caldwell J. A new model of cystic fibrosis pathology: lack of transport of glutathion and its thiocyanate conjugates. Med Hypotheses. 2007;68(1):101-12.
- Conner GE, Salathe M, Forteza R Lactoperoxidase and hydrogen peroxide metabolism in the airway, AmJ Respir Crit Care Med 2002 Dec 15;166 (12 Pt2):S57-1 Review
- Conner GE, Wijkstrom-Frei C, Randell SH, Fernandez VE, Salathe M. The lactoperoxidase system links anion transport to host defense in cystic fibrosis. FEBS Lett. 2007;581(2):271-8.
- Minarowski Ł, Sands D, Minarowska A, Karwowska A, Sulewska A, Gacko M, Chyczewska E. Thiocyanate concentration in saliva of cystic fibrosis patients. Folia Histochem Cytobiol. 2008;46(2):245-6.
- Rada B, Leto TL. Redox warfare between airway epithelial cells and Pseudomonas : dual oxidase versus pyocyanin. Immunol. Res. 2008
- Fischer H. Mechanism and function of DUOX in epithelia of the lung. Antioxid Redox Signal. 2009;11(10):1-13.
- Pedemonte N, Caci E, Sondo E, Caputo A, et al. Thiocyanate transport in resting & IL-4-stimulated human bronchial epithelial cells: role of pendrin and anion channels. J Immunol. 2007;178(8):5144-53.
- Wijkstrom-Frei C, El-Chemaly S, Ali-Rachedi R, Gerson C, Cobas MA, Forteza R, Salathe M, Conner GE. Lactoperoxidase and human airway host defense. Am J Respir Cell Mol Biol 2003;29(2):206-12.
- Xu Y, Szep S, Lu Z. The antioxidant role of thiocyanate in the pathogenesis of cystic fibrosis and other inflammation related diseases, PNAS. 2009; Early edition, November 16