علاج جيني
العلاج بالمورِّثات Gene therapy تقنية خاصة بمعالجة الأمراض عن طريق تزويد خلايا جسم المريض بمورثة (جين أو وحدة وراثية) لتصحيح مورثة معينة أو التعويض عن مورثة مفقودة. وهذه التقنية تساعد الأطباء، إمّا على تصحيح النقص في فعالية (وظائف) خلايا المريض، أو حفز الخلايا على القيام بوظائف جديدة. ولايزال العلاج بالمورثات في مرحلة النمو المبكرة، ولا يعتبر في نفس الوقت معالجة شائعة، غير أنه يفتح أبواب الأمل في معالجة بعض الأمراض المستعصية على العلاج حاليًا؛ مثل مرض فقر الدم المنجليّ، والأيدز، وتليُّف البنكرياس الحوصلي، وبعض أنواع مرض السرطان، والمرض القلبي الوعائي.
العلاج الجيني إنگليزية: Gene Therapy هي عملية ادخال مورثات سليمة إلى الخلايا لتصحيح عمل المورثات الغير فعالة بغية علاج المرض. يرى العلماء أن العلاج الجيني قد يكون وسيلة فعالة لعلاج العديد من الأمراض الوراثية الناتجة من عطب مورثة واحدة مثل مثل الثلاسيميا والناعور وفقر الدم المنجلي والتليف الكيسي وغيرها من الأمراض.
ترجع أول تجربة لاستخدام العلاج الجيني إلى عام 1990 عندما قام الطبيبان فرنش أندرسون ومايكل بلاز بمحاولة علاج طفلة مصابة بمرض عوز المناعة المشترك الشديد بادخال المورثة المختصة بتقوية جهاز المناعة في جسم الإنسان. لاقت التجربة نجاح جزئي حيث استطاع العلاج تقوية الجهاز المناعي للطفلة بنسبة 40%.
مبدأ العلاج وأنواعه
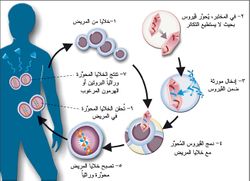
يشتمل العلاج بالمورثات على ثلاث خطوات رئيسية هي: 1- إزالة خلايا من جسم المريض. 2- إدخال مورثات تصحيحية من أشخاص آخرين أو من أحياء أخرى إلى داخل تلك الخلايا. 3- إعادة الخلايا المستبدلة إلى جسم المريض بوساطة نقل الدم. وحالما تدخل هذه الخلايا إلى الجسم، تعالج المورثات الجديدة المرض بصورة تلقائية. ويقوم الأطباء بتكرار هذه العملية إلى أن يستطيع جسم المريض تزويد نفسه بالمورثات الجديدة من خلال النمو العاديّ للخلايا. استخدم الأطباء الأمريكيون أسلوب العلاج بالمورثات الجينية لأول مرة في عام 1990م في معاهد الصحة الوطنية في بثسدا، مريلاند في الولايات المتحدة.
واستخدام العلاج بالمورثات موضوع مثير للجدل، إذ يخشى بعض الناس من أن مثل هذه المعالجة قد تؤدي إلى تغيير البنية الأساسية للبشر بشكل دائم، إذا استخدمت مورثات مأخوذة من أعراق أخرى. ولتحقيق المراقبة الدقيقة لهذه العملية، فإنهم يقترحون عدم استخدامها إلا بعد الحصول على موافقة الحكومات عليها.
يمكن استخدام العلاج على كل من الخلايا الجسمية أو الجذعية، ولكن معظم التجارب انصبت على استخدام الخلايا الجسمية كهدف رئيسي لصعوبة التعامل مع الخلايا البرعمية.
يوجد عدة طرق مستخدمة لإيصال المورثة للخلايا المستهدفة في العلاج الجيني أكثرها شيوعا هو إدخال المورثات إلى مواقع غير محددة في جسم المريض وبالتالي محاولة نقل المورثة لأكبر عدد من الخلايا، أو من خلال استبدال المورثة المعطوبة بمورثة سليمة عن طريق عمليات التأشيب المثلي وغيرها من الطرق.
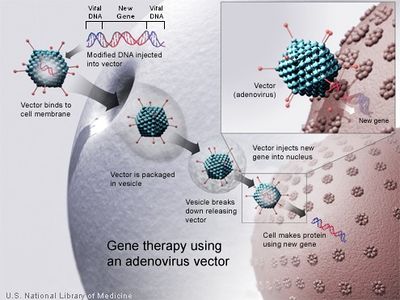
هي تقانة تجريبية وراثية - طبية حديثة سريعة النمو تستخدم فيها المورثات (الجينات) genes لمعالجة مرض ما أو منع حدوثه. وفي المستقبل القريب ستتيح للأطباء فرص إدخال مورثة أو مورثات طبيعية أو محوَّرة وراثياً في خلايا المريض لمعالجته، حيث تنتج هذه المورثات بروتينات تُصلح عمل الخلايا المريضة، وذلك بدلاً من إعطائه عقاقير دوائية لهذه الغاية، أو تعريضه لعمل جراحي أو معالجة بالأشعة أو غير ذلك من طرائق المعالجة المتاحة حالياً (الشكل 1). ومن أجل ذلك يجرى حالياً اختبار عدة توجهات للمعالجة الوراثية أو الجينية، ومن أهمها ما يأتي:
ـ استبدال نسخة سليمة من المورثة بمورثة طافرة سببت المرض.
ـ تثبيط inactivating مورثة طافرة تسبب حالة مرضية معينة.
ـ إدخال مورثة جديدة في الجسم، قادرة على مقاومة المرض.
اسـتخدام المعالجة الوراثية
إن استخدام المعالجة الوراثية واسع جداً، ويعرف حالياً أن أكثر من 4200 مرض ينجم عن تغيرات في المورثات (الأمراض الوراثية)، وأن عدداً غير محدود من الأمراض يتأثر جزئياً بالتكوين الوراثي للفرد، وأن كثيراً من هذه الأمراض والشذوذات لا علاج شاف لها سوى بالمعالجة الوراثية. وعلى سبيل المثال، هناك طفل مصاب بالناعور (سيولة الدم)، وهو مرض تسببه مورثة غير سليمة تجعل الكبد غير قادر على إنتاج عامل تخثر الدم الثامن blood clotting factor VIII. يمكن معالجة هذا الطفل بوضع نسخ سليمة من المورثة التي ترمِّز لإنتاج العامل المذكور في خلايا كبده، فينتج الكبد كميات مناسبة من عامل تخثر الدم VIII ويؤدي ذلك إلى شفاء الطفل. وفي الوقت ذاته فإن المورثات في نطافه تظل كما هي، ومن ثم تنتقل إلى نسله.
تُعد المعالجة الوراثية في الوقت الراهن معالجة واعدة لعدد من الأمراض الوراثية، مثل التليّف الكيسي cystic fibrosis والناعور ومرض ألزهايمر Alzheimer’s disease، وغيرها. ومنها ما هو غير وراثي، مثل بعض حالات مرض السرطان وعدد من الإصابات الڤيروسية مثل مرض عوز المناعة المكتسب acquired immunodeficiency syndrome (AIDS) والسكري diabetes mellitus والتهاب المفاصل arthritis. ولكنها لا تزال تسبب بعض الأخطار التي تتطلب التغلب عليها كي تكون معالجتها سليمة ومأمونة، فمثلاً في عام 2000 سجل العلماء الفرنسيون استخدام المعالجة الوراثية لعلاج رضيعتين مصابتين بمرض مميت هو نقص المناعة المتجمع الوخيم severe combined immunodeficiency disease (SCID)، وعلى الرغم من نجاح العملية تطور في كل منهما مرض نادر شبيه بابيضاض الدم leukemia، ويُعتقد أنه نجم عن تلك المعالجة. وفي هذا اليوم فإنها تعدّ أساساً لأمراض لا تتوافر علاجات لها. ويُقدر عدد ما أُجري من معالجات وراثية في الولايات المتحدة الأمريكية حتى اليوم بأكثر من 4000 معالجة.
كما تستخدم المعالجة الوراثية لدراسة طريقة تغيير عمل الخلايا. فمثلاً تجرى بحوث على تنشيط خلايا الجهاز المناعي في الجسم لمهاجمة الخلايا السرطانية، وعلى إدخال مقاومة لڤيروس نقص المناعة المكتسب AIDS.
أنواع المعالجة الوراثية
للمعالجة الوراثية نوعان: معالجة وراثية «جسمانية» somatic تنقل فيها المورثات «المعالِجة» إلى الخلايا لتصحيح مرض معين في الفرد ذاته، وآثارها عادة تنتهي بانتهاء حياته، وأخرى تُنقل فيها تلك المورثات إلى الأعراس gametes أو الجنين، فتكون آثارها عادة دائمة تنتقل من الفرد المعالَج إلى نسله.
ومن المعلوم أنه لا يمكن إدخال مورثة ما مباشرة إلى خلايا الكائن الحي، إذ لابد من استخدام ناقل أو وسيط vector لهذا الغرض [ر. الهندسة الوراثية]. والڤيروسات هي الأكثر استعمالاً بسبب قدرتها الفريدة على دخول الدنا في الخلايا، وتستعمل الڤيروسات بعد جعلها بحالة غير ممرضة وغير قادرة على التكاثر ضمن الخلايا. وتستخدم ريتروڤيروسات الفأر في دراسات عديدة لإيصال المورثات المرغوبة إلى الخلايا المستهدفة. وتتكون المادة الوراثية في الرتروڤيروس من الحمض الريبي النووي منقوص الأكسجين (الدنا DNA). وهي تنتج أنزيماً يسمى المُنتسخة العكسية reverse transcriptase يستطيع تحويل الرنا إلى الدنا فيصير الأخير بدوره جزءاً من دنا الخلايا المستقبلة (المستهدفة). ولابد من تثبيط الرتروڤيروسات حين استخدامها في المعالجة الوراثية لجعلها مأمونة الاستعمال. كما تستخدم الحُمات الجُدريّة poxviruses للغاية نفسها. يمكن الإشارة أيضاً إلى استخدام أشكال ملطَّفَة من الحُمات الغدية adenoviruses (الشكل 2) في معالجة مرض التليّف الكيسي، إذ تمتلك هذه الڤيروسات انجذاباً طبيعياً نحو الرئتين وتكون مرتبطة مع الأمراض التنفسية. كما يجري اليوم تقصي العلاج المذكور لأمراض أخرى كالسرطان والإيدز AIDS وأمراض القلب الوعائية. ولكبر حجم جينوم ڤيروس القوباء herpes simplex virus فإنه يستعمل لإدخال أكثر من مورثة علاجية واحدة في الڤيروس فيفيد ذلك في علاج أكثر من مرض وراثي، وهذا الڤيروس بالغ الأهمية لقدرته على إصابة عدة أنواع من النسج، بما فيها الكبد والعضلات والرئة والأعصاب والمعثكلة (البنكرياس)، وكذلك الأورام. ولكن هذا الڤيروس يعاني مشكلات مهمة منها أنه يسبب التهاباً للدماغ encephalitis إذا ما تكاثر بحرية في خلاياه، كما أنه يقتل الخلايا التي يصيبها، وتُجرى اليوم بحوث عديدة للتغلب على هذه الآثار.
يحاول الباحثون استخدام المعالجة الوراثية للتغلب على مشكلة مرتبطة بعمل جراحي يُعرف باسم رأب الوعاء بالبالون balloon angioplasty. ويستخدم فيه إِسْتَنت stent (هو في هذه الحالة هيكل أنبوبي) لفتح الشرايين المسدودة. ولكن هذا الإجراء يؤدي إلى رض trauma شرياني، فيباشر الجسم عملية إبلال طبيعية ينجم عنها خلايا عديدة في الشريان المُعالج تؤدي إلى عودة تضيقه أو إغلاقه. والمعالجة الوراثية التي يُعمل على تطويرها لمنع هذا الـتأثير الجانبي هي في تغطية الإستنت بجلّ ذواب يحتوي على نواقل مورثات تُقلِّل نشاط العملية الترميمية للرض.
يجري في معظم التجارب السريرية للعلاج الجيني أخذ خلايا من دم المريض أو نقي عظامه فتحضن في المختبر، وتعرض إلى ڤيروسات تحمل المورثة المرغوبة فتدخل الڤيروسات إلى الخلايا وتصير المورثة جزءاً من دنا الخلايا المذكورة، ومن ثم تعاد الخلايا إلى المريض حقناً في الوريد، وهذه المعالجة من خارج الجسم exvivo. وفي تجارب أخرى تستخدم جسيمات شحمية liposomes لنقل المورثات المرغوبة إلى الخلايا ضمن جسم المريض، وهذه المعالجة من داخل الجسم invivo لأن المورثة تنتقل إلى خلايا المريض ضمن جسمه.
استخدمت المعالجة الوراثية أول مرة عام 1990 في معالجة مرض وراثي نادر يدعى نقص أنزيم نازع أمين الأدينوزين adenosine deaminase (ADA)، وهو أنزيم ضروري لعمل الجهاز المناعي على نحو صحيح. ولا يمتلك المصابون به مورثات ADA طبيعية ومن ثم لا يتم إنتاج الأنزيم المذكور فيهم. وتظهر أعراض نقص مناعي شديد في الأطفال المصابين به ويتعرضون بالتالي لإصابات متعددة وشديدة قد تهدد حياتهم. وهنالك علاج لهذا المرض يدعى PEG-ADA إلا أنه باهظ التكاليف (أكثر من 60 ألف دولار في السنة) ويعطى حقناً في الوريد طوال حياة المريض. وكان من أسباب اختيار هذا المرض للعلاج الجيني كونه مسبباً عن مورثة واحدة مما يزيد من احتمالات نجاح العلاج، إضافة إلى أن كميات الـ ADA لا تحتاج إلى تنظيم دقيق جداً وإن كميات صغيرة من الأنزيم مفيدة في العلاج، كما أن الجسم يتحمل جيداً كميات أكبر منه.
أخطار المعالجة الوراثية
بالرغم من سرعة تطور المعالجة الوراثية عند الإنسان لا تزال هنالك أسئلة تقنية كثيرة تحيط بها، ومن أهمها ما يأتي:
ـ احتمال دخول الڤيروسات الناقلة للمورثات السليمة إلى خلايا أخرى في الخلايا المستهدفة، واحتمال اندماج المورثة المنقولة في مواقع غير صحيحة من دنا الخلايا المستقبلة مما قد يؤدي إلى احتمال حدوث السرطان.
ـ احتمال ضئيل بوصول الدنا إلى الخلايا التناسلية مما يؤدي إلى إحداث تغيرات قابلة للتوريث، مثلاً عند حقن الدنا مباشرة في ورم سرطاني أو عند استخدام جسيم شحمي لنقل المورثة.
ـ احتمال إظهار المورثة المنقولة لأثرها على نحو زائد مما يؤدي إلى إنتاج كمية كبيرة من البروتين الناقص بحيث يؤدي إلى حدوث أضرار، أو أن تسبب المورثات المنقولة ذاتها أضراراً صحية، أو أن يسبب الناقل الڤيروسي التهاباً أو رد فعل مناعي، أو انتقال الڤيروس من شخص إلى آخر أو إلى البيئة.
ومن أهم الصعوبات
ـ تحديد وسائل أسهل وأفضل لنقل المورثات إلى جسم المريض.
ـ إن العلاج الجيد للسرطان ونقص المناعة المكتسب (الإيدز) وأمراض أخرى يتطلب إيجاد نواقل vectors يمكن حقنها في الجسم مباشرة، فتبحث نفسها عن الخلايا المستهدفة (مثل الخلايا السرطانية) في جميع أنحاء الجسم لتدمج بعد ذلك المورثة المنقولة ضمن دنا الخلايا المذكورة.
ـ كما هي الحال في أي تقنية جديدة أخرى، فإنه لابد من استعمالها بحكمة كبيرة منعاً من احتمال إحداثها أضراراً كبيرة. وتتوافر اليوم تنظيمات جيدة لاستخدام المعالجة الوراثية في تصحيح الأخطاء الوراثية، ولكن هناك اعتراضات اجتماعية وأخلاقية عليها، وأسئلة صعبة ستواجه العاملين في هذا الحقل مستقبلاً وخاصة عندما تصبح تقنيات هذا العلاج أكثر سهولة، وفي مقدمتها:
ـ احتمال تحوير الخلايا الجنسية في الإنسان مما يؤدي إلى نقل ذلك إلى الأجيال القادمة. وفي الوقت الحاضر لا توافق الدوائر المختصة في الدول التي تمارس فيها هذه البحوث على المعالجة الوراثية تناسلياً.
ـ احتمال استخدام التقنية لتطوير قدرات الإنسان مثلاً تحسين الذكاء والذاكرة والقوة البدنية بوساطة التدخل الوراثي؛ مما يؤدي إلى أن تصير هذه المعاملة (رفاهية) موفَّرة للغني وصاحب النفوذ فحسب، مما قد يؤدي إلى ظهور تعريفات جديدة للأفراد الطبيعيين ستستبعد الأفراد المتوسطي الذكاء.
الآفاق المسـتقبلية
إن أفضل ما ينجم عن المعالجة الوراثية توفير معالجة وحيدة (أو متكررة على نحو معقول) تمكّن من إصلاح خلايا كافية لتوفير الشفاء الدائم للمرض الوراثي. ومع أن هذا النجاح الكامل غير متوقع في المراحل المبكرة من استخدام هذه التقنية، إلا أنه سيظل الهدف الرئيسي للعلماء الباحثين في هذا الحقل. وسيؤدي ذلك أيضاً إلى تحسين القدرة على توقع حدوث المرض بدلاً من الانتظار حتى حدوثه، ويكون ذلك من دراسة المعلومات الوراثية الخاصة بالإنسان وخاصة «الأخطاء» في بعضها، ويتوقع أن تتوفر بحلول عام 2020 القدرة العلمية والتقنية لمسح المعلومات لما لا يقل عن 5000 مرض. وقد ذكر فرنسيس كولِنز Francis Collins من المعاهد القومية للصحة في الولايات المتحدة الأمريكية أنه سيصبح بالإمكان أن يخبر الطبيب مريضاً أن احتمال إصابته بالسكري هي أعلى من المعدَّل بخمس مرات، أو أن احتمال إصابته بمرض ألزهايمر Alzheimer أقل بثلاث مرات. وبالتالي فإن هذه التخمينات ستؤدي إلى تركيز الاهتمام بالوقاية من حدوث المرض، وسيستطيع المريض آنذاك تحاشي المرض بوساطة المعالجة الوراثية.
ويتوقع وُلتر غيلبرت Walter Gilbert من جامعة هارفرد Harvard أنه «عند معرفة أن خللاً ما أصاب مورثة ما، مؤدياً إلى حالة مرضية، فإن استبدال مورثة سليمة بها سيمنع حدوث المرض». ويُنتظر أيضاً أن تتوافر في المستقبل مجموعات من المورثات السليمة بحيث يستطيع الطبيب اختيار المناسب منها ومن ثم حقن ملايين من نسخها في الجسم، ولاسيما مع التطور الكبير في تقنية استنساخ المورثات.
إن العديد من السرطانات الشائعة، بما فيها سرطانات الرئة والثدي والقولون مسبب من 5 ـ10 مورثات غير سليمة، ويرى كولِنز أن توافر القدرة على تغيير مورثة أو اثنتين منها قد يمكِّن من إيقاف نمو السرطان وتحسين قدرة الجسم على مقاومته. وبهذا يقول وليم فرِنش آندرسون W.French Anderson من جامعة جنوبي كاليفورنيا أنه بحلول عام 2020 ستُمَكِّن المعالجة الوراثية من توفير العلاج لمجموعة كبيرة من الأمراض المستعصية في الوقت الحاضر. على هذا فإن هذا الطب الوراثي سيُمَكِّن من تحديد مكوِّنات جسم الإنسان الأساسية من جهة ومن معرفة كيف يمكن تغييرها إذا اقتضى الأمر ذلك من جهة أخرى.
النواقل
بالانجليزية تعني(vectors) يوجد عدة أنواع من النواقل التي تستخدم في العلاج الجيني ويمكن تقسيمها بشكل عام إلى نواقل فيروسية ونواقل غير فيروسية وطور الباحثون نوع من النواقل يمزج ما بين النوعان الرئيسيان.
النواقل الفيروسية
معظم الفيروسات تنقل المحتوى الوراثي لها للخلية المستهدفة كجزء من دورة حياتها. ولهذا استخدم العلماء فيروسات معدلة وراثياً كوسيلة نقل للجين إلى الخلايا المستهدفة. من الفيروسات التي استخدمت كنواقل الفيروسات الغدية والفيروسات المرتبطة بالفيروسات الغدية والفيروسات القهقرية. بعض المشاكل التي قد تحدث عند استخدام النواقل الفيروسية استعادة الفيروس للنشاط الإمراضي له وبالتالي إصابة المرضى بأمراض أخرى كما حدث في إحدى التجارب السريرية عند إصابة 3 من أصل 9 مرضى بأبيضاض الدم. من المشاكل الأخرى عدم وجود ضمانات بأن النواقل ستقوم باستهداف الخلايا المطلوبة أو قيام الفيروسات بإدخال المواد الوراثية للخلية في المكان الغير صحيح وبالتالي إعطاب عمل مورثات أخرى.
Somatic gene therapy
الفيروسات الارتجاعية
الفيروسات الغدية
Adeno-associated viruses
Envelope protein pseudotyping of viral vectors
Replication-Competent Vectors
Replication-Competent Vectors
Cis and trans-acting elements
فيروس الهربس البسيط
أساليب غير الفيروسية
Injection of Naked DNA
Physical Methods to Enhance Delivery
Electroporation
Gene Gun
Sonoporation
Magnetofection
Chemical Methods to Enhance Delivery
Oligonucleotides
Lipoplexes and polyplexes
Dendrimers
أساليب الهجين
التطورات الرئيسية في العلاج الجيني
1970s and earlier
1990
1995-2000
2001-2005
2005 to present
مشاكل والأخلاق
في الثقافة الشعبية
- In the TV series Dark Angel gene therapy is mentioned as one of the practices performed on transgenics and their surrogate mothers at Manticore, and in the episode Prodigy, Dr. Tanaka uses a groundbreaking new form of gene therapy to turn Jude, a premature, vegetative baby of a crack/cocaine addict, into a boy genius.
- Gene therapy is a crucial plot element in the video game Metal Gear Solid, where it has been used to enhance the battle capabilities of enemy soldiers.
- Gene therapy plays a major role in the sci-fi series Stargate Atlantis, as a certain type of alien technology can only be used if one has a certain gene which can be given to the members of the team through gene therapy.
- Gene therapy also plays a major role in the plot of the James Bond movie Die Another Day.
- Gene therapy plays a recurring role in the present-time sci-fi television program ReGenesis, where it is used to cure various diseases, enhance athletic performance and produce vast profits for bio-tech corporations. (e.g. an undetectable performance-enhancing gene therapy was used by one of the characters on himself, but to avoid copyright infringement, this gene therapy was modified from the tested-to-be-harmless original, which produced a fatal cardiovascular defect)
- Gene therapy is the basis for the plot line of the film I Am Legend.[1]
- Gene therapy is an important plot key in the game Bioshock where the game contents refer to plasmids and [gene] splicers.
- The book Next by Michael Crichton unravels a story in which fictitious biotechnology companies experiment with gene therapy.
- In the television show Alias, a breakthrough in molecular gene therapy is discovered, whereby a patient's body is reshaped to identically resemble someone else. Protagonist Sydney Bristow's best friend was secretly killed and her "double" resumed her place.
- In the videogame Metroid Prime, the Space Pirates use gene therapy to create Elite Pirates.
انظر أيضاً
- Antisense therapy
- DNA
- Full Genome Sequencing
- Gene therapy for color blindness
- هندسة الجينات
- إطالة الحياة
- List of life extension related topics
- Pharmacological gene therapy
- Predictive Medicine
- تقييم التكنولوجيا
- Therapeutic gene modulation
الهامش
- ^ "A Real-life 'I Am Legend?' Researcher Champions Development Of 'Reovirus' As Potential Treatment For Cancer". Sciencedaily.com. 2008-05-09. Retrieved 2010-08-17.
- Tinkov, S., Bekeredjian, R., Winter, G., Coester, C., Polyplex-conjugated microbubbles for enhanced ultrasound targeted gene therapy,2008 AAPS Annual Meeting and Exposition, 16–20 November, Georgia World Congress Center, Atlanta, GA, USA, (http://www.aapsj.org/abstracts/AM_2008/AAPS2008-000838.PDF)
- Gardlík R, Pálffy R, Hodosy J, Lukács J, Turna J, Celec P (2005). "Vectors and delivery systems in gene therapy". Med Sci Monit. 11 (4): RA110–21. PMID 15795707.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - Staff (November 18, 2005). "Gene Therapy" (FAQ). Human Genome Project Information. Oak Ridge National Laboratory. Retrieved 2006-05-28.
- Salmons B, Günzburg WH (1993). "Targeting of retroviral vectors for gene therapy". Hum Gene Ther. 4 (2): 129–41. doi:10.1089/hum.1993.4.2-129. PMID 8494923.
{{cite journal}}: Unknown parameter|month=ignored (help) - Baum C, Düllmann J, Li Z; et al. (2003). "Side effects of retroviral gene transfer into hematopoietic stem cells". Blood. 101 (6): 2099–114. doi:10.1182/blood-2002-07-2314. PMID 12511419.
{{cite journal}}: Explicit use of et al. in:|author=(help); Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - Horn PA, Morris JC, Neff T, Kiem HP (2004). "Stem cell gene transfer—efficacy and safety in large animal studies". Mol. Ther. 10 (3): 417–31. doi:10.1016/j.ymthe.2004.05.017. PMID 15336643.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: multiple names: authors list (link) - Wang, Hongjie (2005). "A capsid-modified helper-dependent adenovirus vector containing the beta-globin locus control region displays a nonrandom integration pattern and allows stable, erythroid-specific gene expression". Journal of Virology. 79 (17): 10999–1013. doi:10.1128/JVI.79.17.10999-11013.2005. PMC 1193620. PMID 16103151.
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help); Unknown parameter|month=ignored (help) - Gene therapy. Italians first to use stem cells. Abbott A. Nature. 1992 Apr 9;356(6369):465
وصلات خارجية
- Gene Therapy: Molecular Bandage? University of Utah's Genetic Science Learning Center
- The American Society of Gene & Cell Therapy
- The European Society of Gene Therapy
- 2003 news relating to gene therapy
- Research Group at Cambridge, UK working on overcoming current hurdles to successful gene therapy
- Council for Responsible Genetics
- Molecular Medicine and Gene Therapy at Lund University
- Dossier on gene therapy and clinical trials
- Gene Therapy Net The startpoint for all the information about gene therapy
- Cancer-genetherapy.com Site focusing on cancer gene therapy
- Gene Therapy Review.
- Gene Therapy News Network Excellent resource for latest news on Gene Therapy and Genetic Medicine.
المصادر
- [1]
- *أسامة عارف العوا. "علاج جيني". الموسوعة العربية.