عملية كظومة
| الديناميكا الحرارية |
|---|
 |
في الديناميكا الحرارية، العملية الكظمية أو الأديباتيكية[1]إنگليزية: Adiabatic هو الإجراء الديناميكي الحراري التي لا يوجد فيها تبادل حراري بين المنظومة والوسط المحيط. أي أنه معزول حرارياً.
الغاز المثالي (الحالة الانعكاسية فقط)
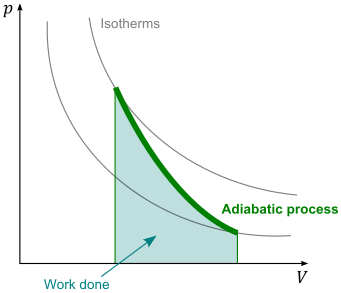
 مقالة مفصلة: عملية كظومة قابلة للعكس
مقالة مفصلة: عملية كظومة قابلة للعكس
تعطى المعادلة الرياضية لغاز مثالي تحت تأثير عملية انعكاسية بالعلاقة:
حيث P الضغط, V الحجم المولي النوعي, و
تكون الحرارة النوعية لضغط ثابت, الحرارة النوعية لحجم ثابت وγ هي معامل أديباتي.
عدد درجات الحرية مقسومة على 2 (3/2 للغاز أحادي الذرة, 5/2 للغاز ثنائي الذرة).
بالنسبة لغاز مثالي أحادي الذرة, , ولغاز ثنائي الذرة (مثل النيتروجين، والأكسجين، المكونات الرئيسية في الغلاف الجوي للأرض أو الهواء. . لاحظ أن الصيغة السابقة مشروعة فقط في حال الغازات المثالية وليس غازات بوز-أينشتاين أو غازات فيرمي.
للعمليات الكظومة الانعكاسية, يكون التعبير التالي صحيحا أيضا
حيث T الحرارة المطلقة.
يمكن كتابة هذا أيضا بالصورة
اشتقاق الصيغة المتصلة
يقتضي تعريف العملية الأديباتية بأن الانتقال الحراري للنظام هو صفر، . وفقا لـالقانون الأول للثرموديناميكا,
حيث أن dU هي التغير في الطاقة الداخلية للنظام وδW هو الشغل المبذول بواسطة النظام. إن أي شغل مبذول (δW) يجب أن يتم على حساب الطاقة الداخلية U، بما أنه لاتوجد حرارة داخلة إلى النظام من المحيط. يعرف شغل الضغط-الحجم δW للنظام بأنه
لكن، P لا تبقى ثابتة أثناء العملية الكظومة وإنما تتغير مع تغير V.
يكون من الأفض معرفة كيفية ارتباط dP وdV أثناء انجاز العملية الكظومة. تعطى الطاقة الداخلية لغاز مثالي بالعلاقة
حيث R هو ثابت الغاز العام وn عدد المولات في النظام (ثابت).
بمفاضلة المعادلة (3) وباستعمال قانون الغاز المثالي، , ينتج
المعادلة (4) يعبر عنها غالبا لأن .
والان بتعويض المعادلات (2) و(4) في المعادلة (1) نحصل على
بالتبسيط:
وبقسمة كلا الطرفين على PV:
بعد مكاملة كلا الطرفين من إلى V ومن إلى P وبتغيير الأطراف على الترتيب،
برفع كلا الطرفين للأس,
وبعزل الإشارة السالبة لبيان أن
لذا,
و
اشتقاق الصيغة المتقطعة
يكون التغير في الطاقة الداخلية لنظام ما، مقاسا من الحالة 1 إلى الحالة 2 مساويا لـ:
في الوقت يكون الشغل المبذول بواسطة التغير في الضغط الحجمي نتيجة لهذه العملية مساويا لـ:
بما أننا بصدد عملية كظومة، ينبغي أن تكون المعادلة التالية صحيحة
من الاشتقاق السابق,
بإعادة الترتيب (4) نحصل على
بالتعويض في (2)
بالتكامل،
بالتعويض ,
باعتبار,
باستخدام قانون الغاز المثالي وبافتراض كمية مولية ثابتة (كما هو الحال عادة في الحالات العملية)،
من الصيغة المتصلة،
أو
وبالتعويض في التعبير السابق ،
بتعويض هذا التعبير و(1) في (3) نحصل على
بالتبسيط،
بالتبسيط،
بالتبسيط،
انظر أيضا
- ديناميكا حرارية
- دورة كارنو
- Cyclic process
- First law of thermodynamics
- Heat burst
- Isobaric process
- Isenthalpic process
- Isentropic process
- Isochoric process
- Isothermal process
- Polytropic process
- Entropy (classical thermodynamics)
- Quasistatic equilibrium
- Total air temperature
- Adiabatic engine
- Magnetic refrigeration
مراجع
- ^ منهج الفيزياء للصف الثالث الثانوي - الفصل الدراسي الأول -ط 2008- التعليم السعودي