بنية كيميائية
البنية الكيميائية Chemical structure هي ترتيب الذرات أو الجزيئات أو الإيونات في المركبات الكيميائية في مختلف حالاتها الفيزيائية.
ويقتصر وصف بنية الغازات المكوَّنة من جزيئات دائمة الحركة العشوائية على بنية تلك الجزيئات، وينطبق ذلك أيضاً على السوائل بوجه عام مع أن حركات جزيئاتها أقل اتساعاً مما هي عليه في الغازات. أما الأجسام الصلبة فالجسيمات التي تتكون منها سواء كانت ذرات أو جزيئات أو أيونات تشغل مواضع متوسطة محدَّدة، وينتج من هذا أنه ينبغي النظر في بنية الجسم الصلب من دون الاهتمام بمكوناته. فالجسم الصلب المتبلور هو وحده الذي يتميز بترتيب جسيماته ترتيباً منظَّماً ومحدَّداً، أما الجسم الصلب شبه الزجاجي (اللابلوري) الذي ينتج من ازدياد لزوجته ازدياداً كبيراً فما هو إلا امتداد للحالة السائلة من دون ترتيب نوعي للأجزاء التي يتكون منها.[1]
بنية الجزيئات والأيونات المتعددة الذرات
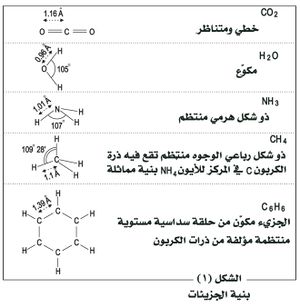
إن الروابط الداخلية بين الذرات ذات طبيعة تساهمية (مشتركة) ، فإذا كان الجزيء أو الأيون ثنائي الذرة مثل ClO-,HCl فالمعلومات الوحيدة عن بنيته هي المسافة بين النوى. أما إذا كان الجزيء أو الإيون يتألف من ثلاث ذرات على الأقل فإن وصفه يتطلب معلوماتٍ زاويَّة، لأن واحدة على الأقل من ذراته تتبادل عدة روابط تساهمية ينبغي أخذ اتجاهاتها المتبادلة بالحسبان، ويبين الشكل ـ1 أمثلة على ذلك.
تنتظم الجزيئات أو الإيونات أو الذرات في كثيرٍ من الأجسام الصلبة بترتيب هندسي دقيق يؤلف ما يسمى بالبلورات. ويعود عددٌ كبير من خواص هذه البلورات إلى هذا الترتيب. وقد أظهر انعراج الأشعة السينية في البلورات، الذي تُعزى فكرته إلى الفيزيائي الألماني ماكس فون لاوي Laue في عام 1912، أن مادة البلورة تنتظم على شكل شبكة ثلاثية الأبعاد تشغل الذرات أو الإيونات أو الجزيئات العُقّد فيها. ويكون لكل بلورة شكل متوازي السطوح عنصري يدعى الخلية الأولية، وفي داخل كل خلية أولية مجموعة مميَّزة من الجسيمات هي العقيدات، التي يولّد تكرارُها وفق المحاور الثلاثة الشبكة البلورية. وترتبط الجسيمات داخل البلورة فيما بينها بقوى الروابط الكيمياوية التي تتعلق أنماطها بأنماط البلورات نفسها، كما يؤدي وصف كل نمط منها إلى الاقتراب من البنية الحقيقية.
بنية البلورات الأيونية
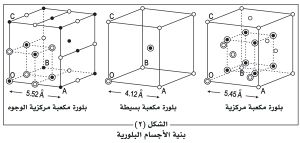
تتكون الجسيمات من إيونات متعاكسة الشحنة، مثل الإيون الموجب +Na والإيون السالب Cl+ في بلورة كلور الصوديوم NaCl، وتضمن اتحادها فيما بينها قوى ذات طبيعة كهربائية ساكنة أو روابط إيونية، وتحقق هذه القوى التوازنَ في البلورة فتبدو معتدلة تماماً. ويدعى عدد الإيونات الأعظمي الذي يتجمع حول إيونٍ محدَّد «العدد التساندي أو التناسقي» nombre de coordination لهذا الإيون، ويساوي هذا العدد 6 في بلورة كلور الصوديوم NaCl، و8 في بلورة كلور السيزيوم CsCl، لأن Cs+ أكبر من Na+. وتقود الكيفية التي يتم وفقها تَجمع الإيونات إلى تشكيل أنماط مختلفة من البلورات الإيونية كما يبين الشكل 2.
إن الطاقة الشبكية لبلورة إيونية التي تنطلق عند تشكُّل بلورةٍ ما بدءاً من إيوناتها المنفصلة، هي أساساً ذات طبيعة كهربائية ساكنة وهي طاقة كبيرة من مرتبة 180 كيلو كالوري/مول في حالة NaCl، مما يجعل درجة انصهار البلورات الإيونية عالية.
وقد مكَّنت معرفة المسافات بين الإيونات في البلورات، بافتراض أن الإيونات كروية، من حساب نصف قطر إيوني مميَّز لكل إيون معين ومستقل عن نوعية البلورة التي ينتمي إليها الأيون. وقد وجد أن ْNa+= 0.95 Aْ؛ وCl -=1.81Aْ؛ و ْCs+=1.69A؛ (Aْ: أنجستروم).
بنية البلورات الذرية
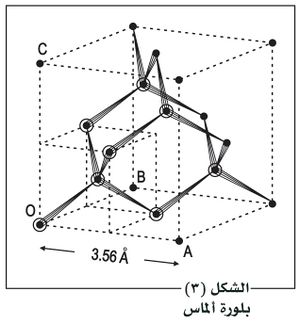
تكون الجسيمات في هذه البلورات ذرات معتدلة مرتبطة بروابط تساهمية (مشتركة)، والرابطة التساهمية، على عكس الرابطة الإيونية، رابطة موجّهة ومحدودة العدد بدءاً من ذرةٍ ما. وليست بنية البلورات الذرية متراصة تراص بنية البلورات الإيونية، بل إنها غالباً ما تكون ذات فجوات. وعلى العكس فإن الرابطة التساهمية تكون محددة الموضع، صلدة، قصيرة وقوية: فالبلورات الذرية تتصف بأنها عازلة كهربائياً وقاسية وقليلة الانصهار. ومنها مثلاً بلورات الكربون (الماس) والسيليكون Si والجرمانيوم Ge، والكربورنْدَم CSi، والكوارتز SiO2، وغيرها ويمكن وصف بنية الماس بأنها مكونة من شبكتين، من ذرات الكربون تنزاح إحداهما عن الأخرى بمقدار ربع قطر العقدة المكعبية، وهذا يؤدي إلى تكون ذرة كربون موجودة في مركز رباعي الوجوه المنتظم تشغل رؤوسه ذرات الكربون الأربع الأكثر قرباً من الأولى بحيث تساوي المسافة كربون ـ كربون 1.54ْ A، وهي المسافة عينها بين ذرات الكربون في السلاسل الكربونية الأليفاتية aliphatique.
بنية البلورات الجزيئية
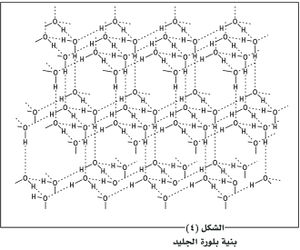
الجسيمات هنا هي جزيئات المادة وترتبط الذرات داخل هذه الجزيئات بروابط تساهمية، ويتضمن التماسكَ بين الجزيئات في البلورات قوى تجاذب تسمى قوى فان درفالس Van derwaals وهي القوى نفسها التي تقوم بإبعاد الغازات الحقيقية عن الحالة الكاملة.وهي قوى ضعيفة فلاتستطيع الحفاظ على تماسك البلورة إلا إذا كان الهيجان الحراري ضئيلاً، مما يجعل البلورات الجزيئية لينة ودرجات انصهارها منخفضة: فدرجة انصهار بلورات كلٍ من الكبريت واليود نحو 120ْس، والبنزِين 5.4ْس benzene، ودرجات انصهار بلورات الهيدروجين والأكسجين والآزوت والكلور أقل كثيراً من درجة الحرارة العادية.
ومن البلورات الجزيئية الجليد وفيه يتم التماسك بروابط هدروجينية، ويشبه ترتيب ذرتي الأكسجين فيه ترتيب ذرتي الكربون في الماس إلا أن تناظر البلورة سداسي (الشكل 4) وتؤلف المجموعةُ شبكةً كثيرة الفجوات، ويؤدي الانصهار بتحطيم روابطها الهدروجينية إلى انهيار بنية الجليد وازديادٍ كتلته الحجمية.
بنية البلورات المعدنية
تتصف البلورات المعدنية بأنها شديدة التراص، وأكثرها شيوعاً:
- الشبكة المكعبة ذات الكثافة العظمى المركزية الوجوه وتُحاط كل ذرة فيها باثنتي عشرة ذرة مثل (الألمنيوم Al والفضة Ag والنحاس Cu والنيكل Ni والذهب Au ...).
- الشبكة السداسية المتراصة تراصَّ الشبكة السابقة مثل (المغنسيوم Mg والكادميوم Cd والزنك Zn، ...)، وهناك بعض المعادن القلوية، والحديد Fe في الدرجة العادية من الحرارة يكون لها شبكة مكعبة مركزية وأقل تراصاً مما هي عليه في المعادن السابقة.
وتشغل ذرات المعدن العقد في الشبكة المعدنية، وتشترك فيما بينها بإلكترون تساهمي واحد على الأقل، وهذه الإلكترونات هي التي تضمن تماسك البلورة كما تضمن الناقلية الحرارية والناقلية الكهربائية. أما الخواص الميكانيكية كقابلية التصفيح والسحب والطرق فإنها تنتج من إمكان انزلاق الذرات بعضها فوق بعض وتختلف هذه الخواص تبعاً لنمط البنية.
إن بنية الخلائط المكونة من اتحاد معادن بعضها ببعض أو بذرة لا معدنية، تشبه بنية المعادن النقية في أن الرابطة المعدنية فيها هي أيضاً التي تضمن تماسكها، ولكن يمكن أن يطرأ على ترتيب الذرات تعديلات بحسب تركيب الخليطة، ويمكن من وجهة النظر هذه أن يميز في حالة الخلائط الثنائية ما يلي:
- المحاليل الصلبة لمعدنين مثل الفضة والذهب Ag-Au، النحاس والنيكل Cu-Ni في الحالة التي تكون فيها شبكات المعادن النقية من نمط واحد والخلايا الأولية البلورية ذات أبعاد متقاربة. ولا يلاحظ في هذه الحالة إلا تغير مستمر في أبعاد الخلايا الأولية وذلك حسب تركيب الخليطة المعدنية.
- المحاليل الصلبة التوغلية: وتكون فيها بعض الذرات فقط ذات أبعاد صغيرة صغراً يمكنها من أن تتوغل في الفراغ البلوري لشبكة بعض المعادن مولِّدة فيها فقط تشوهاً طفيفاً. وهذه هي حالة الآزوت أو الكربون في شبكة الحديد البلورية، وكذلك حالة الهدروجين في شبكة البلاديوم.
- المركبات بين المعادن: وفيها يكون للمعادن التي تكونها بُنى بلورية مختلفة. في هذه الحالة يُظهر التغير التدريجي لتركيب الخليطة الكيمياوي عدة أطوار متعاقبة a، b، g، e، h ذات بنى بلورية مختلفة ويتفق كل طور منها مع بنية إلكترونية محدَّدة وأحياناً معقدة. وهذه هي حالة خلائط الشبه (النحاس الأصفر)
ß (CuZn)و( ε (CuZn3)، γ (Cu5Zn3.
بنية الجزيئات الضخمة والإيونات الضخمة
يصادف في الكيمياء عضوية كانت أو لا عضوية جزيئات ضخمة وإيونات ضخمة، وتعتمد معرفة بنيتها أولاً على بنية القاعدة أو العقيدة وتكرارها ثم على بنية البلورة عند اللزوم، ويتميز من هذه الجزيئات والإيونات اعتماداً على بنيتها ما يلي:
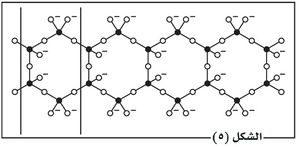
- الجزيئات الضخمة والأيونات الضخمة الخيطية الشكل filiforme أو وحيدة البعدunidimentionnel وتتألف على العموم من ارتباط أعداد كبيرة من المجموعات الذرية المتماثلة (اللازمة motif) تراوح بين 100 و1000، ومن الجزيئات الخيطية الشكل الكبريت ومتعدد الإتيلين والسليلوز، وغيرها، ومن الإيونات الخيطية الشكل مثل سيليكات ثنائي الكالسيوم والمغنسيوم (الشكل 5).
وتعد الجزيئات الضخمة الخيطية الشكل أساس الصناعات اللدائنية. وتقدم السيلكات ثنائيات الكلسيوم مثالاً على الشوارد الضخمة (Si4O11)n6n.
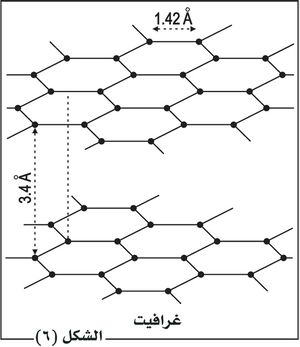
- الجزيئات الضخمة والأيونات الضخمة الصفيحية lamellaires أو الثنائية البعد، كالغرافيت (الشكل 6) ، وفيها تكون ذرات الكربون منضَّدة في مستويات متوازية بحسب شكل سداسي منتظم، بحيث يتشكل في كل مستوٍ جزيءٌ ضخم ثنائي البعد، ترتبط فيه كل ذرة كربون بجاراتها القريبة التي تبعد عنها 1.42Aْ بثلاث روابط تساهمية موجهة بـ 210ْ ناتجة عن التهجين المثلثي sp2.
وتكون المسافة في هذه الحالة بين مستو وآخر أكبر مما هي عليه في المستوي إذ تقارب ْ3.4A ويكون الارتباط أضعف مما يُكسب الغرافيت ملمساً دهنياً وخواص تزليقية.
ويشاهد الشيءُ نفسه في السيليكات، كالتالك، وفي ألُمينات السيليكون كالميكا السهلة التصفيح، والأرجيلات (الغضاريات) Argiles المكونة من أيونات موجبة ضخمة [Al(OH)4]n2n++ وسالبة ضخمة (SiO5)n2n- متوضعة في صفائح متوازية ومتناوبة تدخل فيما بينها جزيئات الماء وتؤدي إلى انتفاخها ومرونتها.
- الجزيئات الضخمة والإيونات الضخمة الثلاثية البعد: من الأمثلة عليها الماس وهو بلورة ذرية تكون فيها كل الروابط متماثلة، وكذلك السيليس Silice المتبلور منه وغير المتبلور. ومن الأيونات الضخمة ثلاثية البعد الفِلْدِسْبات feldspaths والزيوليت Zéolites وألمينات السيليكون: ويمكن تمثيل بنية إيون الزيوليت بأن هناك في السيليس عدداً من الذرات 14Si حل محلها من دون أي تشويه يذكر عددٌ مماثل من الذرات 13Al التي تقل شحنة نواتها عن شحنة نواة السيليكون بشحنة موجبة واحدة. وبذلك تكون شحنة المجموعة سالبة، أي يتكون أنيون ضخم ثلاثي البعد من ألمينات السيليكون Macronion. ويتم التعادل الكهربائي بواساطة كاتيونات أصغرية Microcations مثل K+ أو Ca2+ أو غيرهما سهلة التبادل. ويفسِّر هذا استعمال الزيئوليت في تحلية المياه الطبيعية.
انظر أيضا
- Pauli exclusion principle
- Lipinski's Rule of Five, describing molecular properties of drugs
- QSAR, quantitative structure-affinity relationship
- Chemical property
- Molecular property
- Physical property
- Crystallographic database
المصادر
- ^ فايز فلوح. "البنية الكيمياوية". الموسوعة العربية. Retrieved 2012-04-23.
مراجع للاستزادة
- رشيد مرادبية، الكيمياء العامة (الجزء الأول)، ترجمة صلاح يحياوي (مطبوعات الجزائر).
- C.Chaussin & G.Hilly, Cours de chimic ( Dunod, Paris 1963).
- Masson et cie,Pécis de chimie generle, Tome II 3éme Edition (Saint - Jermain Paris -VI 1974).
- B.Pullman, “La structure moleculaire”, Que sais-je ( Paris 1973).