كمون كيميائي
في الكيمياء الفيزيائية،الكمون الكيميائي (إنگليزية: chemical potential) يرمز له بالرمز µ،
نبذة من الأسس
وقد وضعه الفيزيائي والرياضي الأمريكي ويلارد جيبس، الذي عرفه كما يلي:
"إذا أضفنا كمية متناهية في الصغر من مادة ما، لأي كتلة في حالة التوازن، بحيث تبقى الكتلة متجانسة ويبقى الأنتروبي والحجم ثابتين، يعطى عندها الكمون الكيميائي بالزيادة في طاقة الكتلة مقسومة على المادة المضافة لتلك الكتلة".
أشار جيبس أيضا إلى أن أي عنصر كيميائي، أو تركيب من عناصر بأي نسب معروفة قد يعتبر مادة متجانسة، سواء قادرة أو غير قادرة على الوجود بنفسها.
مثال
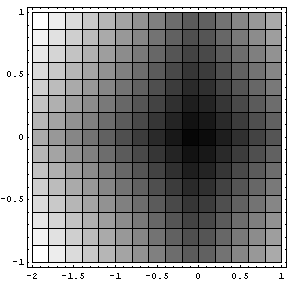
لنفترض تابع كمون كيميائي معرف على مساحة ثنائية البعد موضحة في الشكل جانبا. تميل الجزيئات إلى التحرك من المناطق ذات الكمون الكيميائي العالي (الذي يبدو بلون باهت في المخطط) إلى المناطق ذات الكمون الكيميائي المنخفض (الذي يبدو بلون غامق في المخطط).
مختلف الخواص التحريكية الحرارية تحدد ماهية الكمون الكيميائي. لنعتبر مثلاً ذرات مشحونة ضمن سائل ما. تدرج الضغط في السائل قد يدفع الجزيئات من جهة لأخرى. وتدرج الكمون الكهربائي قد يدفع الجزيئات في الاتجاه المعاكس. الكمون الكيميائي يأخذ تأثيرا الضغط والكهرباء بعين الاعتبار ويعطي توزعا جديدا للكمون تتحرك وفقه الجزيئات في السائل.
تاريخ
قدم جيبس في عام 1873 مقالة وضح فيها الخطوط الأولية لمعادلته الجديدة القادرة على تنبؤ أو تخمين نشوء مختلف النظم الطبيعية وذلك عند احتكاك الأجسام أو النظم ببعضها. استطاع جيبس بعد دراسة تفاعل مواد متجانسة مع بعضها، تحديد ثلاث حالات للتوازن: مستقر، متعادل، غير مستقر، وإذا كان التفاعل سيتم أم لا. في عام 1873، اعتمد جيبس على هذه الهيكلية في تقديم مبدأ الكمون الكيميائي الذي يأخذ بعين الإعتبار التفاعلات الكيميائية وحالة الأجسام المخلفة كيميائيا عن بعضها. يقول جيبس ملخصا نتائجه في عام 1873:
حيث تشير ε إلى الطاقة الداخلية للجسم، و η تشتير إلى أنتروبية الجسم، و هو حجم الجسم.
مصطلحات
يعتمد مصطلح الكمون الكيميائي على السياق الذي يستخدم فيه:
- عند الكلام عن الأنظمة التحريكية الحرارية، يشير الكمون الكيميائي إلى الكمون الكيميائي التحريكي الحراري. في هذا السياق، فإن الكمون الكيميائي هو تغير الخصائص التحريكية الحرارية لتابع الحالة خلال التغير في عدد الجزيئات. حسب الشروط التجريبية، فإن التغير في الخصائص التحريكية الحرارية لتابع الحالة يكون إما الطاقة الداخلية، أو الإنتالبية، أو طاقة جيبس أو طاقة هيلمهولتز. إن الاستخدام للكمون الكيميائي في هذا السياق محصور في الكيميائيين التجريبيين، والفيزيائيين، والمهندسين الكيميائيين.
- يستخدم الكيميائيون النظريون والفيزيائيون غالبا مصطلح الكمون الكيميائي للدلالة على الكمون الكيميائي الإلكتروني المتعلق بالاشتقاق الوظيفي للكثافة الوظيفية، ويسمى أحيانا بالطاقة الوظيفية الموجودة في نظرية الكثافة الوظيفية.
- يستخدم الفيزيائيون أحيانا مصطلح الكمون الكيميائي في توصيف الأنظمة النسبية للجسيمات الأولية.
الكمون الكيميائي الدينامي الحراري
الكمون الكيميائي لنظام دينامي حراري هو كمية التغير في طاقة النظام عند إضافة جزيء واحد، مع بقاء الأنتروبية والحجم ثابتين. إذا حوى النظام على صنفين من الجزيئات، فإنه يعرف كتغير في الطاقة عند ازدياد عدد جزيئات الأصناف جزيئا واحدا. الكمون الكيميائي هو متغير أساسي في الديناميكا الحرارية وهو يقترن بعدد الجزيئات.
للكمون الكيميائي أهمية كبيرة عند دراسة نظم الجزيئات المتفاعلة. لنفترض حالة بسيطة من صنفين، حيث يتحول جزيء من الصنف الأول إلى جزيء من الصنف الثاني والعكس صحيح. هذا المثال هو لمزيج مشبع من الماء السائل (الصنف الأول)، وبخار الماء (الصنف الثاني). إذا كان النظام في حالة توازن، فإن الكمونين الكيميائيين لكلا الصنفين يجب أن يكونا متساويين. ومن جهة أخرى، فإن أي زيادة في إحدى الكمونات الكيميائية سينتج عنه تحرير غير عكوس لطاقة النظام بشكل حرارة (راجع القانون الثاني في الديناميكا الحرارية) عندما تتحول تلك الأصناف ذات الكمون الكيميائي المتزايد إلى أصناف أخرى، أو كسب للطاقة (بشكل حراري) إذا حدث تحول عكوس. تكون شروط التوازن في التفاعلات الكيميائية، معقدة أكثر لوجود أكثر من صنفين.