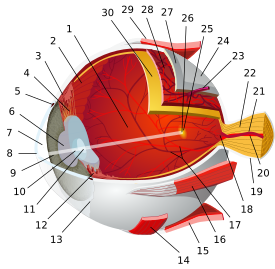
خلية مولر الدبقية
خلية مولر الدبقية (إنگليزية: Müller glia)، أو خلايا مولر (إنگليزية: Müller cells)، هي نوع من الخلايا الدبقية الشبكية ، تم التعرف عليها ووصفها لأول مرة بواسطة هينريتش مولر.[1] توجد في شبكية الفقاريات ، والتي تعمل كخلايا داعمة للخلايا العصبية ، كما تفعل جميع الخلايا الدبقية. هم النوع الأكثر شيوعًا من الخلايا الدبقية الموجودة في شبكية العين. بينما توجد أجسامهم الخلوية في الطبقة النووية الداخلية للشبكية ، فإنها تمتد عبر الشبكية بأكملها.[2]
يتمثل الدور الرئيسي لخلايا مولر في الحفاظ على الاستقرار الهيكلي والوظيفي لخلايا الشبكية. يتضمن ذلك تنظيم البيئة خارج الخلية عن طريق امتصاص الناقلات العصبية ، وإزالة الحطام ، وتنظيم مستويات ايونات البوتاسيوم ، وتخزين الجليكوجين ، والعزل الكهربائي للمستقبلات والخلايا العصبية الأخرى ، والدعم الميكانيكي للشبكية العصبية.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
التطور
مولر الدبقية مشتقة من الناحية التطورية من مجموعتين متميزتين من الخلايا. إنها الخلية الدبقية الشبكية الوحيدة التي تشترك في سلالة خلوية مشتركة مع الخلايا العصبية الشبكية. ومع ذلك ، فقد ثبت أن مجموعة فرعية من مولر الدبقية تنشأ من خلايا القمة العصبية.[3] يجب أن تكون حاسمة في نمو شبكية العين في الفئران ، حيث تعمل كمحفزات لنمو الشبكية وتكوين الأنسجة عبر آلية استريز غير محددة بوساطة.[4] تم أيضًا تضمين مولر الدبقية في العمل كخلايا إرشادية للمحاور العصبية النامية في شبكية عين الفرخ..[5] الدراسات باستخدام نموذج السمك الصغير المخطط من متلازمة آشر قد تضمن دور لمولر الدبقية في التخلق مشبكي ، وتشكيل نقاط المشبك العصبي[6]
الدعم العصبي
كخلايا دبقية ، تؤدي خلايا مولر الدبقية دورًا ثانويًا ولكن مهمًا للخلايا العصبية . على هذا النحو ، فقد ثبت أنها تعمل كوسيط مهم للناقل العصبي ( أستيل كولين و حمض الغاما-أمينوبيوتيريك علي وجه التحديد) تدهور والمحافظة علي بيئة شبكية مواتية في السلاحف.[7] كما تم إثبات أهمية مولر الدبقية في تحريض إنزيم المخلق للجلوتامين في أجنة الدجاج,[8] وهو عامل مهم في تنظيم تركيزات الجلوتامين والأمونيا في الجهاز العصبي المركزي . تم تحديد مولر الدبقية بشكل أكبر على أنها أساسية لنقل الضوء عبر شبكية الفقاريات نظرًا لشكلها الفريد من نوعه ، والتوجه داخل شبكية العين ، وخصائصها الفيزيائية الأكثر ملاءمة.[9]
الاستخدام في الأبحاث
تتم حاليًا دراسة مولر الدبقية لدورها في التجديد العصبي ، وهي ظاهرة غير معروفة الحدوث في البشر.[10] تم إجراء دراسات لهذه الغاية من خلايا مولر الدبقية في كل من شبكية سمك الزرد والدجاج[11][12] مع بقاء الآلية الجزيئية الدقيقة للتجديد غير واضحة. أظهرت دراسات أخرى أجريت على الفئران أن الإفراط في التعبير عن Ascl1 في مولر الدبقية بالتزامن مع إعطاء مثبط هيستون دي اسيتيلاز يسمح بتجديد الخلايا العصبية في شبكية العين من مولر الدبقية.[13] أثبتت الدراسات التي أجريت على النماذج البشرية أن مولر الدبقية لديها القدرة على العمل كخلايا جذعية في شبكية العين البالغة وهي من أسلاف المستقبلات الضوئية للعصويات.[14]
ينتج عن تلف خلايا الشبكية أن تخضع خلايا مولر للدباق . تختلف نتيجة الاستجابة باختلاف الضرر والكائن الحي الذي حدث فيه هذا الضرر.[2][15] لقد ثبت في أسماك الزرد أن مولر الدبقية تخضع للتمايز في الخلايا السلفية متعددة القدرات . يمكن لخلية سلفية ان تنقسم فيما بعد و تتمايز في عدد من أنواع الخلايا في شبكية العين، بما في ذلك خلايا مستقبلة للضوء ، التي ربما تكون قد تعرضت للتلف أثناء الإصابة.[16] بالإضافة إلى ذلك ، أظهر المزيد من الأبحاث أن مولر الدبقية تعمل كمجمعات للضوء في عين الثدييات ، على غرار لوحة الألياف الضوئية ، وتوجيه الضوء إلى مستقبلات الضوء العصوية والمخروطية[9]
Aquaporin-4 في خلية مولر في الفئران ، ينقل الماء إلى الجسم الزجاجي.[17][18]
تم الإبلاغ عن أن خلايا مولر يمكن أن تتلف بسبب جرعة زائدة من النياسين.[19][20]
انظر أيضاً
المصادر
- ^ Müller, Heinrich (1851). "Zur Histologie der Netzhaut" (PDF). Zeitschrift für Wissenschaftliche Zoologie. 3: 234–237.
- ^ أ ب Goldman, Daniel (July 2014). "Müller glia cell reprogramming and retina regeneration". Nature Reviews Neuroscience. 15 (7): 431–442. doi:10.1038/nrn3723. PMC 4249724. PMID 24894585.
- ^ Hamon, Annaïg; et al. (October 2015). "Müller Glial Cell-Dependent Regeneration of the Neural Retina: An Overview Across Vertebrate Model Systems". Developmental Dynamics. 245 (7): 727–738. doi:10.1002/DVDY.24375. PMC 4900950. PMID 26661417.
- ^ Bhattacharjee, J; Sanyal, S (1975). "Developmental origin and early differentiation of retinal Müller cells in mice". Journal of Anatomy. 120 (Pt 2): 367–72. PMC 1231976. PMID 1201967.
- ^ Meller, K.; Tetzlaff, W. (1976). "Scanning electron microscopic studies on the development of the chick retina". Cell and Tissue Research. 170 (2). doi:10.1007/bf00224296.
- ^ Phillips, J. B.; Blanco-Sanchez, B.; Lentz, J. J.; Tallafuss, A.; Khanobdee, K.; Sampath, S.; Jacobs, Z. G.; Han, P. F.; Mishra, M.; Titus, T. A.; Williams, D. S.; Keats, B. J.; Washbourne, P.; Westerfield, M. (2011). "Harmonin (Ush1c) is required in zebrafish Muller glial cells for photoreceptor synaptic development and function". Disease Models & Mechanisms. 4 (6): 786–800. doi:10.1242/dmm.006429. PMC 3209648. PMID 21757509.
- ^ Sarthy, P.; Lam, D. M. (1978). "Biochemical studies of isolated glial (muller) cells from the turtle retina". The Journal of Cell Biology. 78 (3): 675–84. doi:10.1083/jcb.78.3.675. PMC 2110200. PMID 29902.
- ^ Linser, P.; Moscona, A. A. (1979). "Induction of glutamine synthetase in embryonic neural retina: Localization in Muller fibers and dependence on cell interactions". Proceedings of the National Academy of Sciences. 76 (12): 6476–80. Bibcode:1979PNAS...76.6476L. doi:10.1073/pnas.76.12.6476. PMC 411888. PMID 42916.
- ^ أ ب Franze, K.; Grosche, J.; Skatchkov, S. N.; Schinkinger, S.; Foja, C.; Schild, D.; Uckermann, O.; Travis, K.; Reichenbach, A.; Guck, J. (2007). "Muller cells are living optical fibers in the vertebrate retina". Proceedings of the National Academy of Sciences. 104 (20): 8287–92. Bibcode:2007PNAS..104.8287F. doi:10.1073/pnas.0611180104. PMC 1895942. PMID 17485670.
{{cite journal}}: Unknown parameter|lay-date=ignored (help); Unknown parameter|lay-source=ignored (help); Unknown parameter|lay-url=ignored (help) - ^ WebVision: Regeneration in the Visual System of Adult Mammals
- ^ Fausett, B. V.; Goldman, D. (2006). "A Role for α1 Tubulin-Expressing Müller Glia in Regeneration of the Injured Zebrafish Retina". Journal of Neuroscience. 26 (23): 6303–13. doi:10.1523/jneurosci.0332-06.2006. PMID 16763038.
- ^ Raymond, Pamela A; Barthel, Linda K; Bernardos, Rebecca L; Perkowski, John J (2006). "Molecular characterization of retinal stem cells and their niches in adult zebrafish". BMC Developmental Biology. 6: 36. doi:10.1186/1471-213X-6-36. PMC 1564002. PMID 16872490.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Jorstad, Nikolas L.; Wilken, Matthew S.; Grimes, William N.; Wohl, Stefanie G.; VandenBosch, Leah S.; Yoshimatsu, Takeshi; Wong, Rachel O.; Rieke, Fred; Reh, Thomas A. (August 2017). "Stimulation of functional neuronal regeneration from Müller glia in adult mice". Nature. 548 (7665): 103–107. Bibcode:2017Natur.548..103J. doi:10.1038/nature23283. PMC 5991837. PMID 28746305.
- ^ Giannelli, Serena G.; Demontis, Gian Carlo; Pertile, Grazia; Rama, Paolo; Broccoli, Vania (2011). "Adult Human Müller Glia Cells Are a Highly Efficient Source of Rod Photoreceptors". Stem Cells. 29 (2): 344–56. doi:10.1002/stem.579. PMID 21732491.
- ^ Bringmann, Andreas; Iandiev, Ianors; Pannicke, Thomas; Wurm, Antje; Hollborn, Margrit; Wiedemann, Peter; Osborne, Neville N.; Reichenbach, Andreas (November 2009). "Cellular signaling and factors involved in Müller cell gliosis: Neuroprotective and detrimental effects". Progress in Retinal and Eye Research. 28 (6): 423–451. doi:10.1016/j.preteyeres.2009.07.001. PMID 19660572.
- ^ Bernardos, R. L.; Barthel, L. K.; Meyers, J. R.; Raymond, P. A. (2007). "Late-Stage Neuronal Progenitors in the Retina Are Radial Muller Glia That Function as Retinal Stem Cells". Journal of Neuroscience. 27 (26): 7028–40. doi:10.1523/JNEUROSCI.1624-07.2007. PMC 6672216. PMID 17596452.
- ^ Simó, Rafael; Villarroel, Marta; Corraliza, Lídia; Hernández, Cristina; Garcia-Ramírez, Marta (2010). "The Retinal Pigment Epithelium: Something More than a Constituent of the Blood-Retinal Barrier—Implications for the Pathogenesis of Diabetic Retinopathy". Journal of Biomedicine and Biotechnology. 2010: 1–15. doi:10.1155/2010/190724. PMC 2825554. PMID 20182540.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ Jo, A. O.; Ryskamp, D. A.; Phuong, T. T. T.; Verkman, A. S.; Yarishkin, O.; MacAulay, N.; Kri Aj, D. (2015). "TRPV4 and AQP4 Channels Synergistically Regulate Cell Volume and Calcium Homeostasis in Retinal Muller Glia". Journal of Neuroscience. 35 (39): 13525–37. doi:10.1523/JNEUROSCI.1987-15.2015. PMC 4588615. PMID 26424896.
- ^ "Eye damage linked to popular over-the-counter vitamin that lowers cholesterol can be reversed". Science X network: Medical Xpress. 29 October 2019.
- ^ Lee, Jessica G.; Patel, Anu; Bertolucci, Alessandra; Rosen, Richard B. (2019). "Optical Coherence Tomography, Fluorescein Angiography, and Electroretinography Features of Niacin Maculopathy: New Insight Into Pathogenesis". Journal of VitreoRetinal Diseases. 3: 247412641987756. doi:10.1177/2474126419877567. ISSN 2474-1264.
وصلات خارجية
- New Hope For Regenerating Damaged Human Retina: Sleeping Stem Cells Successfully Awakened
- Müller cells at Virginia-Maryland Regional College of Veterinary Medicine
- Reichenbach, Andreas; Faude, Frank; Enzmann, Volker; Bringmann, Andreas; Pannicke, Thomas; Francke, Mike; Biedermann, Bernd; Kuhrt, Heidemarie; Stolzenburg, Jens-Uwe; Skatchkov, Serguei N.; Heinemann, Uwe; Wiedemann, Peter; Reichelt, Winfried (1997). "The Müller (Glial) Cell in Normal and Diseased Retina: A Case for Single-Cell Electrophysiology". Ophthalmic Research. 29 (5): 326–40. doi:10.1159/000268031. PMID 9323724.
- NIF Search - Muller Cell via the Neuroscience Information Framework