التحفيز العميق للدماغ
| أحمد مغربي ساهم بشكل رئيسي في تحرير هذا المقال
|
| التحفيز العميق للدماغ Deep brain stimulation | |
|---|---|
| تدخل | |
 | |
| MeSH | D046690 |
| MedlinePlus | 007453 |
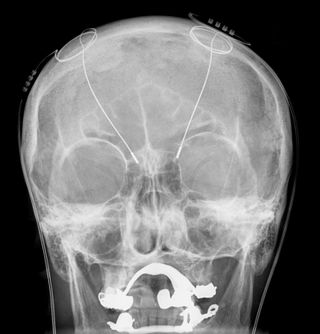
التحفيز العميق للدماغ Deep brain stimulation (DBS)، هو علاج جراحي بإدخال جهاز طبي يسمى منظم الدماغ والذي يرسل نبضات كهربائية إلى مناطق محددة من الدماغ. اختيار التحفيز العميق لمناطق معينة من الدماغ يوفر فوائد علاجئية سواء لحالات المقاومة للعلاج أو للاضطرابات العاطفية مثل الألم المزمن، مرض پاركنسون، الرعاش والديستونيا.[1] بالرغم من التاريخ الطويل للتحفيز العميق للدماغ،[2] فإن المبادئ والآليات الأساسية له لا تزال غامضة.
المكونات والحالات
الكيمياء الحيوية
التطبيقات
مرض پاركنسون
الألم المزمن
الاكتئاب الحاد
يقوم العلاج بالتحفيز العميق للدماغ على إيصال موجات كهرومغناطيسية إلى مناطق عميقة في الدماغ. ويجري التحفيز عبر وضع أسلاك كهربائية في مناطق معيّنة على الرأس كي تنطلق منها موجات كهرومغناطيسية لتصل إلى مراكز في وسط منتصف الدماغ، يُعتَقَد بعلاقتها مع الإدراك والعواطف والمزاج. ولحد الآن، نجحت هذه الطريقة في علاج أمراض نفسية تتضمّن الكآبة.[3] ولذا رأت هيلين مايبرگ، وهي اختصاصية في جامعة إموري بولاية أتلانتا، أن هذا النجاح يبرهن أن المفهوم الراسخ عن علاقة عمل الدماغ (وأيضاً اضطراباته) بمواد كيماوية معيّنة فيه، تتهاوى كليّاً. وشدّدت مايبرگ على أن سقوط المفهوم الكيماوي، يحفّز على ضرورة التفكير في مقاربة مختلفة لفهم العلاقة بين الدماغ والفكر والعواطف، ترتكز على التكامل الديناميكي التفاعلي في هذا العضو المُعقّد. وأيّاً كانت البدائل، لا أقل من القول إن عقوداً طويلة من ركون العلم إلى التصوّر الكيماوي لعمل الدماغ وآليات مرضه، تتهاوى راهناً بطريقة مُدوّية. ولكن هذه المعطيات تفيد في فهم تعقيد ظاهرة الكآبة.
بقول آخر، باتت الكآبة الآن، في العقد الثاني من القرن 21، تعاني زمناً علمياً صعباً، بل ربما مأسوياً ومسدود الأفق. ليس لعباً على الكلمات، بل لا يتعلق الأمر بمجرد تحفيز الذهن كي لا يسقط في الإغفاء على حرير وعود خلابة، في شأن أحد أقدم الأمراض النفسية التي عرفها البشر، إذ تعيش أدوية علاج الكآبة (مع ما يرافقها من نظريات علمية ونماذج أساسية في البحوث) على وقع انهيارات ضخمة، بما يذكّر بمعاناة الشعوب وعوالِم السياسة في أزمنة انهيار الامبراطوريات الكبرى مثل الدولة العثمانية والاتحاد السوڤيتي التي أدارها قياصرة موسكو عقوداً مديدة.
متلازمة تورت
الشلل


عام 2011 تعرض جيرت-يان أوسكام تعرض لحادث دراجة نارية في الصين أصابه بالشلل من الوركين إلى أسفل. حالياً، مع مجموعة من الأجهزة، منحه العلماء السيطرة على الجزء السفلي من جسده مرة أخرى. قال أوسكام في تصريح صحفي: "على مدى 12 عامًا، كنت أحاول استعادة قدمي. لقد تعلمت الآن كيفية المشي بشكل طبيعي".
في دراسة نُشرت يوم الأربعاء في مجلة ناتشر، وصف باحثون في سويسرا عمليات زرع توفر "جسرًا رقميًا" بين مخ أوسكام وحبله الشوكي، متجاوزًا الأجزاء المصابة. سمح هذا الاكتشاف للسيد أوسكام، 40 عامًا، بالوقوف والمشي والصعود على منحدر شديد الانحدار بمساعدة المشاة فقط. بعد مرور أكثر من عام على إدخال الغرسة، احتفظ بهذه القدرات وأظهر بالفعل علامات الشفاء العصبي، والمشي باستخدام العكازات حتى عندما تم إيقاف المزروعة.[4]
بحسب جريجوار كورتين، إخصائي الحبل الشوكي في المعهد الفيدرالي السويسري للتكنولوجيا في لوزان: "لقد استوعبنا أفكار جيرت-جان، وترجمنا هذه الأفكار إلى تحفيز للحبل الشوكي لإعادة تأسيس الحركة الإرادية". أضافت جوسلين بلوخ، عالمة الأعصاب في جامعة لوزان التي وضعت الغرسة في مخ السيد أوسكام، "لقد كان خيالًا علميًا في البداية بالنسبة لي، لكنه أصبح حقيقيًا اليوم".
كان هناك عدد من التطورات في العلاج التكنولوجي لإصابات الحبل الشوكي في العقود الأخيرة. عام 2016، تمكنت مجموعة من العلماء بقيادة الدكتور كورتين من استعادة القدرة على المشي في القرود المشلولة، وساعد آخر رجلًا على استعادة السيطرة على يده المشلولة. عام 2018، ابتكرت مجموعة مختلفة من العلماء، بقيادة الدكتور كورتين أيضًا، طريقة لتحفيز المخ باستخدام مولدات النبضات الكهربائية، مما يسمح للمصابين بالشلل الجزئي بالمشي وركوب الدراجات مرة أخرى. عام 2022، سمحت إجراءات تحفيز المخ الأكثر تقدمًا للأشخاص المصابين بالشلل بالسباحة والمشي وركوب الدراجة في غضون يوم واحد من العلاج.
خضع السيد أوسكام لإجراءات تحفيز في السنوات السابقة، واستعاد بعض القدرة على المشي، ولكن في النهاية توقف تحسنه. في المؤتمر الصحفي، قال السيد أوسكام إن تقنيات التحفيز هذه تركته يشعر بأن هناك شيئًا غريبًا في الحركة، مسافة غريبة بين عقله وجسده. لقد غيرت الواجهة الجديدة هذا، حيث قال: "كان التحفيز من قبل يسيطر علي، والآن أنا أتحكم في التحفيز."
في الدراسة الجديدة، استفادت واجهة المخ-العمود الفقري، كما أسماها الباحثون، من وحدة فك ترميز الذكاء الاصطناعي لقراءة مقاصد السيد أوسكام - يمكن اكتشافها كإشارات كهربائية في مخه- ومطابقتها مع حركات العضلات. تم الحفاظ على مسببات الحركة الطبيعية، من الفكر إلى النية إلى الفعل. الإضافة الوحيدة، كما وصفها الدكتور كورتين، كانت الجسر الرقمي الذي يمتد على الأجزاء المصابة من العمود الفقري.
قال أندرو جاكسون، عالم الأعصاب في جامعة نيوكاسل، الذي لم يشارك في الدراسة: "إنها تثير أسئلة مثيرة للاهتمام حول الاستقلالية، ومصدر الأوامر. أنت تواصل طمس الحدود الفلسفية بين ما هو المخ وما هي التكنولوجيا ".
وأضاف الدكتور جاكسون أن العلماء في هذا المجال كانوا ينظّرون حول ربط المخ بمحفزات الحبل الشوكي لعقود من الزمن، لكن هذا يمثل المرة الأولى التي يحققون فيها مثل هذا النجاح في مريض بشري. قال: "من السهل القول، إن القيام بذلك أصعب بكثير".
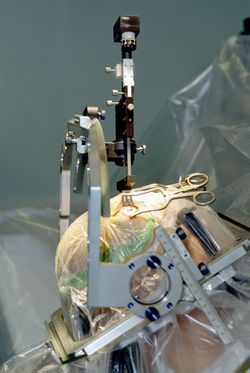
لتحقيق هذه النتيجة، قام الباحثون أولاً بزرع أقطاب كهربائية في جمجمة السيد أوسكام وعموده الفقري. ثم استخدم الفريق برنامج التعلم الآلي لملاحظة أي أجزاء من المخ تضيء أثناء محاولته تحريك أجزاء مختلفة من جسده. كان مفكك الشفرة هذا قادرًا على مطابقة نشاط أقطاب كهربائية معينة بنوايا معينة: أضاء أحد التكوين كلما حاول السيد أوسكام تحريك كاحليه، وآخر عندما حاول تحريك وركيه.
ثم استخدم الباحثون خوارزمية أخرى لربط غرسة المخ بالعمود الفقري، والتي تم تعيينها لإرسال إشارات كهربائية إلى أجزاء مختلفة من جسده، مما يؤدي إلى الحركة. كانت الخوارزمية قادرة على حساب الاختلافات الطفيفة في اتجاه وسرعة كل تقلص واسترخاء عضلي. ولأن الإشارات بين المخ والعمود الفقري تُرسل كل 300 مللي ثانية، يمكن للسيد أوسكام تعديل استراتيجيته بسرعة بناءً على ما كان يعمل وما لم يكن كذلك. خلال جلسة العلاج الأولى يمكنه أن يلف عضلات وركه.
على مدى الأشهر القليلة التالية، صقل الباحثون واجهة المخ-العمود الفقري لتناسب بشكل أفضل الإجراءات الأساسية مثل المشي والوقوف. اكتسب السيد أوسكام مشية صحية إلى حد ما وتمكن من اجتياز الدرجات والمنحدرات بسهولة نسبية، حتى بعد شهور دون علاج. علاوة على ذلك، بعد عام من العلاج، بدأ يلاحظ تحسنًا واضحًا في حركته دون مساعدة من واجهة المخ-العمود الفقري. وثق الباحثون هذه التحسينات في اختبارات تحمل الوزن، والتوازن والمشي.
الآن، يمكن للسيد أوسكام أن يمشي بطريقة محدودة حول منزله، والصعود إلى السيارة والنزول منها والوقوف في البار لتناول مشروب. قال لأول مرة إنه يشعر وكأنه الشخص المسيطر.
أقر الباحثون بوجود قيود في عملهم. من الصعب التمييز بين النوايا الدقيقة في المخ، وعلى الرغم من أن واجهة المخ-العمود الفقري الحالية مناسبة للمشي، إلا أنه ربما لا يمكن قول الشيء نفسه لاستعادة حركة الجزء العلوي من الجسم. يعتبر العلاج أيضًا غازيًا، ويتطلب عمليات جراحية متعددة وساعات من العلاج الطبيعي. النظام الحالي لا يعالج كل شلل الحبل الشوكي.
لكن الفريق كان يأمل في أن تؤدي التطورات الإضافية إلى جعل العلاج أكثر سهولة وفعالية بشكل منهجي. قال الدكتور كورتين: "هذا هو هدفنا الحقيقي، لجعل هذه التكنولوجيا متاحة في جميع أنحاء العالم لجميع المرضى الذين يحتاجون إليها."
تطبيقات سريرية أخرى
المضاعفات المحتملة والآثار الجانبية
انظر أيضاً
- جراحة الأعصاب
- Stereotactic surgery
- جراحة نفسية
- Neuroprosthetics
- زراعة المخ
- Vagus nerve stimulation
- Electroconvulsive therapy
مرئيات
| الغرسات الدماغية في علاج الشلل. |
الهوامش
- ^ Kringelbach ML, Jenkinson N, Owen SLF, Aziz TZ (2007). "Translational principles of deep brain stimulation". Nature Reviews Neuroscience. 8:623–635. PMID 17637800.
- ^ Gildenberg PL (2005). "Evolution of neuromodulation". Stereotact Funct Neurosurg, 83(2–3), 71–79. PMID 16006778.
- ^ "الكآبة ترسم أفقاً لنهاية «الدماغ الكيماوي»". دار الحياة. 2013-09-01. Retrieved 2013-09-03.
- ^ "A Paralyzed Man Can Walk Naturally Again With Brain and Spine Implants". نيويورك تايمز. 2023-05-24. Retrieved 2023-05-24.
المصادر
- Appleby BS, Duggan PS, Regenberg A, Rabins PV (2007). "Psychiatric and neuropsychiatric adverse events associated with deep brain stimulation: A meta-analysis of ten years' experience". Movement Disorders 22:1722–1728 PMID 17721929
- Bekar L, Libionka W, Tian G, Xu Q, Torres A, Wang X, Lovatt D, Williams E, Takano T, Schnermann J, Bakos R, Nedergaard M (2008). "Adenosine is crucial for deep brain stimulation–mediated attenuation of tremor". Nature Medicine, v.14, n.1, pp. 75–80.
- Fins JJ. Deep Brain Stimulation (2004) In, Encyclopedia of Bioethics, 3rd Edition. Post, SG, Editor-in-Chief. New York: MacMillan Reference. Volume 2, pp. 629–634.
- Gildenberg Philip L and Tasker, Ronald R (1998). Textbook of stereotactic and functional neurosurgery, McGraw-Hill Publishing.
- Gildenberg Philip L (2005). "Evolution of neuromodulation". Stereotact Funct Neurosurg, 83(2–3), 71–79. PMID 16006778
- Kringelbach ML, Jenkinson N, Owen SLF, Aziz TZ (2007). "Translational principles of deep brain stimulation". Nature Reviews Neuroscience. 8:623–635. PMID 17637800
- McIntyre CC, Grill WM (2000). "Selective microstimulation of central nervous system neurons". Annals of Biomedical Engineering 38:219–233. PMID 10784087
- McIntyre CC, Grill WM, Sherman DL, Thakor NV (2004). "Cellular effects of deep brain stimulation: model-based analysis of activation and inhibition". Journal of Neurophysiology 91:1457–1469. PMID 14668299
- Ropper Allan H and Brown, Robert H. (2005) Adams and Victor's Principles of Neurology (8th Edition), McGraw-Hill Medical Publishing. ISBN 0-07-141620-X