اللوكيميا الليمفاوية المزمنة
| اللوكيميا الليمفاوية المزمنة | |
|---|---|
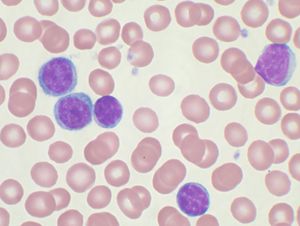 | |
| Peripheral blood smear showing CLL cells | |
| التبويب والمصادر الخارجية | |
| التخصص | علم الدم |
| ICD-10 | C91.1 |
| ICD-9-CM | 204.9 |
| ICD-O | 9823/3 |
| DiseasesDB | 2641 |
| MedlinePlus | 000532 |
| eMedicine | med/370 |
| Patient UK | فشل عرض الخاصية P1461: لم يتم العثور على الخاصية P1461. اللوكيميا الليمفاوية المزمنة |
| MeSH | D015462 |
ابيضاض الدم الليمفاوي المزمن إنگليزية: Chronic Lymphocytic Leukemia - CLL هو مرض سرطاني يصيب الخلية الليمفية من نوع B. يصيب البالغين و خاصة الأفراد التي تتراوح أعمارهم ما بين 60- 80 عاما خاصة في أوروبا و أمريكا الشمالية، و ينتشر بين الذكور بنسبة أعلى من الإناث (1:2). يشكل ما نسبته 25% من الإصابات بمختلف أمراض ابيضاض الدم. في أمريكا الشمالية، معدل الإصابة السنوي للرجال 3.35-3.69 لكل 000 100 شخص, أما بالنسبة للنساء هو 1.61-1.92 لكل 000 100 شخص. يتصف المرض بالتراكم التصاعدي للخلايا الليمفية في نخاع العظم و العقد الليمفية، وبالتالي انتقال المرض تدريجيا إلى بقية الأعضاء المصنعة للدم. يتم إيعاز المرض إلى خلل جزيئي يؤدي إلى تأخير أو إعطاب عملية استموات الخلايا.
أسباب المرض
بخلاف بقية أنواع ابيضاض الدم، لم يتم ربط الإصابة بالمرض مع عوامل مخطرة بيئية أو التعرض لأي مركبات كيميائية أو أشعة. أحد العوامل المخطرة المرض هو وجود إصابة بهذا المرض أو أية اضطرابات تكاثر ليمفي في أحد أفراد العائلة، وجد أن مصاب من كل 10 أشخاص مصابين بابيضاض الدم الليمفي المزمن لديهم إصابة عائلية بالمرض.
الفيزيولوجيا المرضية
وجد الباحثون أن من ميزات المرض هو تراكم و تكدس الخلايا الليمفية و ليس من الانقسام الغير طبيعي للخلايا. و من هنا تم ربط المرض بعملية استموات الخلايا. تتم عملية استموات الخلايا من خلال طريقين رئيسين هما الطريق الداخلي (المتقدرات/ميتكوندريا) و الطريق الخارجي (TNF). تتضمن عمليات نقل إشارة وتنشيط و تثبيط مركبات معينة تؤدي بالنهاية لتحفيز عملية استموات الخلايا.
في ابيضاض الدم الليمفي المزمن تتدخل عدة بروتينات في الطريقين الداخلي و الخارجي مما يؤدي إلى تثبيط عملية استموات الخلايا. مثل هذه البروتينات bcl-2 و NF-KB و Akt. و وجد أيضا أن بعض الاضطرابات الوراثية الخلوية تؤدي إلى إخلال في عمل المورثة p53 المسؤولة عن تثبيط الأورام.
الأعراض
معظم حالات اكتشاف المرض تتم بالصدفة من خلال الفحوصات الروتينية أو بسبب ظهور أعراض فقر الدم أو تضخم متماثل في الغدد الليمفية و خاصة التي تقع في منطقة العنق و الإبط، تظهر 3/2 الحالات تضخم في الكبد و الطحال. و تظهر بعض الحالات تضخم في اللوزتين و بعض الكدمات لقلة الصفائح الدموية.
العلامات المخبرية
تظهر الفحوصات المخبرية ارتفاع في أعداد كريات الدم البيضاء الليمفية و وجودها بما نسبته 40% أو أكثر في نخاع العظم. في صورة الدم، تظهر الخلايا بأحجام صغيرة و كمية السايتوبلازم تكون ضئيلة و لا تظهر النوية بشكل واضح.
يشاهد في صورة الدم خلايا تعرف باسم سلائف الليمفيات، و تكون كبيرة الحجم مقارنة بالكريات الليمفية و لا تزيد عن 5%. في بعض الحالات المرضية تشاهد بنسبة أعلى، في تلك الحالة يتم تشخيص الحالة كنوع من أنواع المرض و يسمى ابيضاض الدم الليمفي المزمن/سلائف الليمفيات.
فحص نخاع العظم
يشكل فحص نخاع العظم أهمية كبيرة في عملية تشخيص المرض، و متابعة العلاج. تكمن أهميته في النقاط التالية:
- وسيلة لتحديد مآل و مرحلة المرض: عندما يكون نخاع العظم مكدس بالخلايا الليمفية مع عديد قليل جدا من المناطق الدهنية (النمط المنتشر)، هذا يؤشر إلى أن المرض في مرحلة متأخرة و بالعادة يكون مآل المرض سيئ. و قد يكون نمط نخاع العظم خلالي مع وفرة المساحات الدهنية أو يكون نمط عقدي الشكل. بعض الإصابات تظهر مزيج من النمطين الأخيرين.
- تحديد طبيعة و مسبب قلة الحُمُر و الصفائح: يساعد فحص نخاع العظم على تحديد مسبب قلة الخلايا في الدم و بالتالي معالجة المسبب.
- التشخيص التفريقي مع الأمراض الأخرى: يتم ملاحظة نمط ترشيح الخلايا الليمفية يساعد على تشخيص ابيضاض الدم الليمفي المزمن من بقية الأمراض التي تتشابه معه.
- متابعة واستجابة المريض للعلاج.
مآل المرض
هناك عدة عوامل لها دور في تحديد مآل المرض.
| عوامل محددة لمآل المرض | |||
| العامل | جيد | سييء | |
|---|---|---|---|
| مرحلة المرض | بينت A راي (0-I) | بينت B,C راي (II-IV) | |
| الجنس | انثى | ذكر | |
| مدة تضاعف الليمفيات | بطيئ | سريع | |
| نمط خزعة نخاع العظم | عقدي | منتشر | |
| الوراثة الخلوية | حذف 13q4 | حذف 17p، حذف 11q23، تثلث صبغي 12 | |
| مورثة VH | مطفرة | طبيعية | |
| تعبير CD38 | قليل | مرتفع | |
| تعبير ZAP-70 | قليل | مرتفع | |
أنظمة تحديد مرحلة المرض
هنالك نظامان يستخدمان لتحديد مرحلة المرض، النظام الأول، نظام راي (1975)، قسمت مجموعة راي المرض لعدة مراحل:
- 0 تتصف بارتفاع كريات الدم البيضاء الليمفية
- I مرحلة 0 + تضخم في الغدد الليمفية
- II مرحلة 0 + تضخم في الكبد أو الطحال أو كلاهما + تضخم أو عدم تضخم الغدد الليمفية
- III مرحلة 0 + فقر دم + تضخم أو عدم تضخم في كل من الكبد و الطحال و الغدد الليمفية.
- IV مرحلة 0 + هبوط في الصفائح + وجود أو عدم وجود فقر الدم و تضخم الأعضاء.
النظام الآخر هو نظام بينت (1981). طور بينت هذا النظام بالإعتماد على دراستين فرنسيتين. يتم تقسيم مراحل المرض بالإعتماد على عدد الأعضاء المتضخمة (العنق و الإبط و المنطقة الأربية و الكبد و الطحال) كالتالي:
- A لا يوجد أي تضخم أو تضخم عضوين أو أقل
- B تضخم من 3 أعضاء إلى 5
- C وجود فقر دم و قلة في الصفائح الدموية.
الوراثة الخلوية
أظهرت الأبحاث أن ما نسبته 80% على الأقل من حالات الإصابة بالمرض تحوي على اضطراب وراثي خلوي أو أكثر. يتم تشخيص هذه الاضطرابات بواسطة فحص التهجين الموضعي المتألق، لما لها من دور في تحديد مآل المرض. صدرت دراسة في عام 2000 قام بها دونر و مجموعته بدراسة 325 مريض و خرجوا بمجموعة من الاضطرابات الوراثية الخلوية و رتبوها حسب دورها في مآل المرض من السيئ إلى الجيد.
| الاضطرابات الوراثية الخلوية حسب دراسة دونر مرتبة حسب دورها في مآل المرض | |||
| الاضطرابات الوراثية الخلوية | نسبة الإصابة | ||
|---|---|---|---|
| حذف 17p | 7% | ||
| حذف 11q | 17% | ||
| تثلث صبغي 12 | 14% | ||
| نمط نووي طبيعي | 18% | ||
| حذف 13q4 | 36% | ||
| غيرها | 8% | ||
مورثة VH
كان الاعتقاد السائد أن المرض يحدث في الخلايا الليمفية التي تحوي نسخة طبيعية من مورثة VH. إلا أنه اكتشف حديثا أن أكثر من نصف حالات المرضى (55%) يحملون مورثة VH مُطفّرة. تكمن اهمية حدوث هذه الطفرة لتعزز قدرة الخلايا الليمفية على إنتاج أضداد متخصصة. وجدت الدراسات أن الأشخاص الذين يحملون النسخة المطفرة من المورثة يكون مآل المرض أفضل من المرضى الذين يحملون النسخة الطبيعية. يتم التحري عن هذه الطفرة إما بقياس كميات CD38 في الخلايا الليمفية أو التحري عن التعبير الجيني لمورثة ZAP-70. كلاهما ينتج بكميات أكبر في حالة المورثة الطبيعية.
التشخيص التفريقي
تشتبه بعض الأمراض في الأعراض و الظواهر مما تجعل مهمة التشخيص صعبة في بعض الأحيان مثل هذه الأمراض متلازمة ريختر و ابيضاض الدم الليمفي المزمن العائلي و كثرة الليمفيات البائية الوحيدة و متعددة النسيلة.
تم تطوير نظام نقاط حتى يتم التفريق بين ابيضاض الدم الليمفي المزمن و غيره وذلك بالاعتماد على وجود بعض المؤشرات. هناك 5 مؤشرات يتم التحري عنها بواسطة جهاز عداد الخلايا. كل منها يشكل نقطة واحدة. تحسب النقاط بعدها و يتم تشخيص المرض بالاعتماد على تلك المؤشرات.
العلاج
تتم معالجة المرض بعدة طرق
- العلاج الكيميائي: و يستخدم للقضاء على الخلايا السرطانية و منعها من الانقسام مثل كلورامبوسيل (Chlorambucil) و فلودارابين (Fludarabine).
- العلاج الإشعاعي: يتم تعريض المريض للأشعة العلاجية لتقليص حجم الغدد الليمفية والتي لا تستجيب للعلاج الكيميائي.
- الأضداد وحيدة النسيلة: يتم توجيه هذه الأضداد إلى الخلايا السرطانية للقضاء عليها.
- زراعة نخاع العظم.
المصادر
المراجع
- Daniel Catovsky, Chronic Lymphocytic Leukemia. In Hoffbrand V, Tuddenham E and Catovsky D ed. Postgraduate Haematology. Blackwell Publishing;2005:619-634.
- Hoffbrand V, Moss P, Pettit J. Essential Haematology. Blackwell Publishing;2006:188-196.
- James B Johnston, Chronic Lymphocytic Leukemia. In Greer J, Forester J, Lukens J, Rodgers G, Paraskevas F, Glader B ed. Wintrobe's Clinical Hematology, 11th edition. Lippincott Williams and Wilkins Publishing;2004:2235-2258.
| هذه بذرة مقالة عن العلوم الطبية تحتاج للنمو والتحسين، فساهم في إثرائها بالمشاركة في تحريرها. |