بلمرة
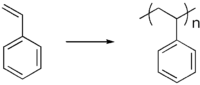
البلمرة أو التبلمر polymerization، هي عملية ارتباط الجزيئات الصغيرة بعضها ببعض، ويسمى الجزيء الصغير الوحدة المتكررة repeating unit أو أحادي الحد monomer وتعني باليونانية الجزء الواحد، وبتكرر الارتباط، تعطي الوحدات المتكررة جزيئاً ضخماً يدعى المتبلمر polymer، وتعني باليونانية المتعدد الأجزاء. فالبولي إثيلين المادة البلاستيكية شائعة الاستعمال، ينتج من تفاعل تبلمر الإثلين بشروط مناسبة من درجة حرارةٍ عاليةٍ (200ْس)، وضغطٍ عالٍ (1000 ضغط جوي) بوجود كميات ضئيلة من فوق أكسيد الهدروجين حافزاً. ويمكن استعمال أي فوق أكسيد آخر. وتدعى العملية في هذه الحالة تبلمر ضم addition polymerization.[1]
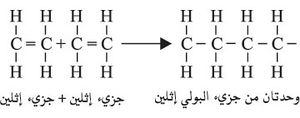
ويتباين عدد الوحدات المتكررة n في السلسلة المتبلمرة من العشرات إلى عشرات الألوف، وعندما يكون عدد الوحدات المتكررة صغيراً نسبياً يدعى المركب قليل الجزيئات oligomer ويحتل مكاناً وسطاً بين أحاديات الحد (المونوميرات) والمتبلمرات ويراوح وزنها الجزيئي بين 500 و5000.
والجزيئات الضخمة الناتجة من التبلمر ليست متماثلة، إذ يصادف في المتبلمر نفسه سلاسل طويلة جداً ذات وزنٍ جزيئيٍ عالٍ وأخرى قصيرة. ولهذا يعبّر عن الوزن الجزيئي للمتبلمر بوزنه الجزيئي الوسطي. فمادة متبلمرة وزنها الجزيئي 100000 واحدة كتل ذرية (و ك ذ) ربما تحوي جزيئات كتلتها الجزيئية 85000 و ك ذ، وجزيئات أخرى كتلتها الجزيئية 125000 و ك ذ.
والجدير بالذكر أن خواص أحادي الحد تختلف اختلافاً جذرياً عن خواص المتبلمر، فقد يكون الأول سائلاً في حين يكون الثاني سائلاً أو صلباً، وقد يكون الأول قابلاً للالتهاب في حين قد يستعمل الثاني للوقاية من الحرائق.
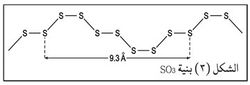
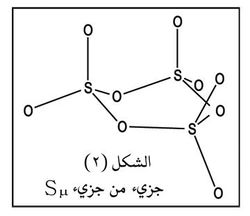
وقد توصل الكيميائيون العضويون في القرن العشرين إلى تطوير طرائق استحضار متبلمرات متنوعة الخصائص تفي بالغرض المصنوعة من أجله. إلا أن تكونها لا يقتصر على مجال مركبات الكربون فقط، بل لوحظت هذه العملية في مواد لا عضوية كثيرة. فالكبريت المصهور يحوي نوعين species هما Sλ وSμ (على الأغلب S8 وS6) إضافة إلى نوع أو نوعين آخرين. وللكبريت S8 شكل حلقة تاجية لا تقع في مستو واحد كما هو مبين في الشكل 1.
أما S6 فله شكل سلاسل غير منتظمة كما هو مبيَّن في الشكل 2.
ولأكسيد الكبريت الصلب الصيغة (SO3)n ويعرف له ثلاث بنى على الأقل. ويتكون g - SO3 بتكثيف بخار الكبريت بالدرجة -80ْس أو بدرجة أخفض منها. وله بنية الجليد (ودرجة انصهاره 16.8ْس) وهو على شكل حلقة مؤلفة من ثلاث جزيئات SO3 كما هو مبين في الشكل 3.
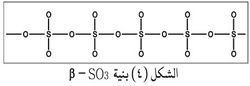
أما ß - SO3 فهو مؤلف من سلاسل لا متناهية لا تقع في مستو واحد helical متصل بعضها ببعض كما هو مبين في الشكل 4.

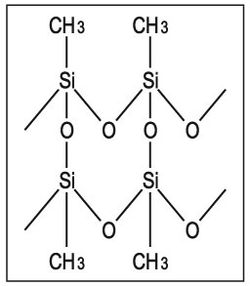
وأكثر أشكال (SO3)n ثباتاً هو γ - SO3 وله مظهر ألياف الأمينت (الأسبِسْتُس) asbestos وله على الأغلب شكل سلاسل مشابهة للشكل ß والسلاسل فيه تتشابك مكونة صفائح. وكذلك السيليكون silicone الاسم التجاري لعائلة من المتبلمرات تحوي سلاسل الجزيئات الكبيرة تكون فيها الروابط Si-O- (الشكل ـ 5).
ويسهم الطرف الفحمي الهدروجيني بإعطاء المركب خواص زيتية أو تشحيمية. وإذا تشابكت السلاسل فهي تكوّن متبلمراً صلباً (الشكل ـ 6).
جرت محاولات كثيرة للحصول على عدد أكبر من المتبلمرات اللاعضوية وذلك بإيجاد ارتباطات أخرى في السلاسل (عدا الارتباطات التي يصنعها الكربون) وقد واجهت هذه المحاولات صعوبات كثيرة لكون الروابط في المركبات اللاعضوية أعقد من روابط الكربون البسيطة σ أو الروابط المضاعفة π - σ.

والصعوبة الأخرى للحصول على المتبلمرات اللاعضوية هو ميل الجمل اللاعضوية إلى تكوين حلقات ذات وزن جزيئي منخفض. وإن الميل إلى تكوين روابط مضاعفة يتناقص بازدياد العدد الذري، ولهذا يصعب في هذه الحالة اللجوء إلى تقنية تبلمر الضم التي تصلح في أحاديات الحد العضوية كالإتلين. ومع هذه الصعوبات، فقد أمكن تحضير متبلمرات لا عضوية كثيرة ويبين الشكل 7 بعضاً منها.
ويمكن من الناحية العلمية تقسيم المتبلمرات إلى قسمين أساسيين: متبلمرات الضم (الإضافة) ومتبلمرات التكاثف condensation polymers.
مقدمة
|
Homopolymers
Co-polymers
|
متبلمرات الضم
وتتلخص آلية التبلمر بالضم في ثلاث مراحل:
1ـ بدء التفاعل initiation الذي يحتاج عادة إلى تسخين وفوق أكسيد.
2ـ الانتشار ونمو السلسلة propagation.
3ـ نهاية التفاعل أو وقف السلسلة termination.
متبلمرات التكاثف
تنتج هذه المتبلمرات من تبلمر أحاديات الحد التي تحوي على الأقل مجموعتين أو زمرتين فعالتين، وذلك لكي يستمر التفاعل فيما بين الجزيئات، فعندما يتفاعل مثلاً أمين مع حمض عضوي يتكون أميد:
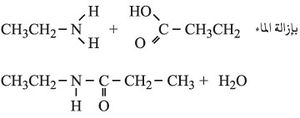
ولا يتكون متبلمر نتيجة هذا التفاعل لأن الناتج من التفاعل لا يحوي COOH أو NH2 لكي يستمر التفاعل. أما تفاعل ثنائي الأمين مع حمض عضوي ثنائي فينتج منه مركب يحوي في جزيئه مجموعتين فعالتين مما يؤدي إلى تكرار التفاعل مرات كثيرة وتكون المتبلمر:
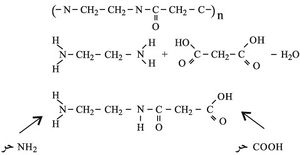
يتم تكون الألياف الاصطناعية بوساطة عملية التكاثف. وتتم عملية التبلمر بالتكاثف بين جزيئات مركبين مختلفين (أحاديي الحد). وينتج من عملية التكاثف إضافة إلى المتبلمر نواتج ثانوية (جزيئات صغيرة مثل H2O وHCl وNH3). وتجب ملاحظة الاختلافين الأساسيين بين متبلمرات الضم ومتبلمرات التكاثف. ففي حالة الضم غالباً ما يكون هناك أحادي حد واحد فقط ولا يكون أي ناتج ثانوي أما في حالة التكاثف فيكون هناك أحاديا حد ويتكون ناتج ثانوي غالباً ما يكون الماء:
ويمكن تمييز المتبلمرات بعضها من بعض حسب التوضع الفراغي stereoregularity للمجموعات الفراغية في السلسلة الجزيئية، فهنالك المتبلمرات المتماثلة التركيب isotactic polymers والمتبلمرات المتناوبة الترتيب syndiotactic polymers والبولميرات اللاترتيبية atactic polymers. وبحسب طبيعة المراكز الفعالة للتبلمر يمكن تمييز التبلمر الأنيوني anionic polymerization، إذ تكون المراكز الفعالة مشحونة بشحنة سالبة، من التبلمر الكاتيوني، إذ تكون المراكز الفعالة مشحونة بشحنة موجبة.
وعندما يكون المتبلمر مكوناً من نوع واحد من الوحدات المتكررة يدعى المركب المتبلمر المتجانس homo polymer، أما عندما يكون المركب الناتج مؤلفاً من نوعين من الوحدات المتكررة فيدعى الناتج عن التبلمر المتبلمر التشاركي copolymer، ويدعى الناتج من ثلاثة أحاديات الحد بالترمتبلمر terpolymer مثال ذلك الستارين ـ البوتاديين ـ أكريل نتريل ABC. وتهدف عملية التبلمر التشاركي إلى:
- تحسين قابلية التلون للمتبلمرات التشاركية.
- تحسين الخاصة الانحلالية للمتبلمرات التشاركية.
- خفض قابلية النفوذية للغازات.
- زيادة المرونة للتبلمر التشاركي.
وضمن هذا المجال تميز المتبلمرات التشاركية المتناوبة alterative copolymers، والمتبلمرات التشاركية المطعمة graff copolymers والمتبلمرات التشاركية العشوائيةrandom copolymers على النحو الآتي:
وقد تحسنت طرائق التقانة لاصطناع المتبلمرات سواء تلك المستخدمة في إنتاج متبلمرات الضم أو التكاثف أو المتبلمرات التشاركية وأهم هذه الطرائق:
- تبلمر الكتلة mass polymerization.
- التبلمر في المحلول solution polymerization.
- التبلمر في المستحلبات emulsion polymerization.
- التبلمر في المعلقات suspension polymerization.
فالتبلمر في الكتلة يتم تحت الضغط العادي أو المرتفع بدرجة حرارة منخفضة أو مرتفعة بوجود مادة بادئة للتفاعل initiator. أما التبلمر في المحلول فيتم بوسط مذيب لكل من أحادي الحد المتبلمر والمادة البادئة للتفاعل مع التحريك. وتستخدم هذه التقانة لإنتاج المواد اللاصقة والطلاء والأصبغة البلاستيكية. والتبلمر في المستحلبات يتم بوجود الماء وأحادي الحد والمادة البادئة للتفاعل والمستحلب ومثبت الاستحلاب ومنظم لنمو السلسلة والتوتر السطحي وذلك باستعمال مواد واقية. وهذا النوع من التقانة يؤدي إلى إجراء التبلمر بسعة كبيرة وبالدرجة العادية من الحرارة، وإن استخدام الماء في هذه التقانة يسهل تنظيم درجة الحرارة والحصول على متبلمر يتصف بدرجة تبلمر أعلى ومن ثم يؤدي إلى خفض سعر التكلفة للمتبلمر الناتج. وتتم التقانة في المعلقات في وسط مائي، ويمكن عندئذ التخلص من الكثير من المشكلات والصعوبات المتعلقة باستخدام التقانة في الكتلة والمحلول كمشكلة التبريد وتفاعلات نقل السلسلة chain transfer reaction.

تأثير العوامل المختلفة في سير عملية التبلمر
1 ـ تأثير درجة الحرارة: يتوقع من الوجهة الحركية أن تزداد سرعة التفاعلات الأولية في عملية التبلمر بازدياد درجة الحرارة من ثم ازدياد نمو السلسلة، إلا أن ذلك يرافقه في الوقت نفسه ازدياد في سرعة تفاعل قطع السلسلة ومن ثم انخفاض في الوزن الجزيئي. وإذا ارتفعت درجة الحرارة أكثر من الحد الضروري تحطمت عملية التبلمر بفعل الحرارة.
2 ـ تأثير الضغط: يعمل الضغط على تنشيط الجذور الحرة في عملية نمو السلسلة وخفض الحرارة لإجراء عملية التبلمر.
3 ـ تأثير المنظمات: تعمل هذه المنظمات على التحكم في نمو السلسلة وعلى توقفها، إذ يتفاعل المنظم مع النهاية الحرة للجذور النشيطة ويؤدي ذلك إلى توقف نمو السلسلة وضبط الوزن الجزيئي.
4 ـ تأثير المركبات المثبِّطة والمعوِّقة inhibitor and retardants وهي مركبات لها القدرة على إيقاف التفاعلات المتسلسلة أو خفض سرعة التفاعل، إذ تعمل على جعل الجذور الحرة مستقرة وضعيفة الفعالية مثال ذلك الهدروكينونات ومركبات النترو.
5 ـ تأثير الـ pH في وسط التفاعل: يعتمد البدء في عملية التبلمر بقدر كبير على سرعة تفكك المادة البادئة للتفاعل والأجسام الوسيطة التي تدخل في عملية التبلمر فمنها ما يتفكك بسرعة في وسط حمضي ومنها ما يتفكك ببطء في وسط قلوي.
انظر أيضا
المصادر
- ^ فواز الديري. "التبلمر". الموسوعة العربية. Retrieved 2011-06-06.