كيمياء حرارية
الكيمياء الحرارية (إنگليزية: thermochemistry) هي دراسة الأفعال الحرارية المرافقة للتفاعلات الكيمياوية.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
ندذة من الأسس
بعض التفاعلات ناشر للحرارة exothermic، مثل احتراق الفحم في الهواء إذ ترتفع درجة حرارته نتيجة للتفاعل الشكل (1)،
(1)
في حين يكون بعضه الآخر ماصاً للحرارة endothermic كتفاعل الفحم المتوهج مع بخار الماء الشكل (2).
(2)
وفي حالات نادرة يكون الفعل الحراري معدوماً تماماً كما في تفاعل الكحول مع حمض الخل لتشكيل الإستر.
تقتضي الدراسة الكمية للفعل الحراري تعريفاً دقيقاً لما يُسمى حرارة تفاعل عند الدرجةt : هي كمية الحرارة، مقدرة بالجول، المنتشرة أو الممتصة في أثناء التفاعل، أي المتبادلة من قبل المواد المتفاعلة والنواتج مع الوسط الخارجي بعد أن تعود هذه المواد كلها إلى الدرجة t التي بدأ بها التفاعل. واصطُلح على اعتبار كمية الحرارة مقداراً جبرياً سالباً للتفاعلات الناشرة للحرارة وموجباً للتفاعلات الماصة للحرارة. الكيمياء الحرارية في الديناميكا الحرارية وفي الكيمياء الطبيعية هي دراسة تولد الحرارة أو امتصاصها في التفاعلات الكيميائية. وتهتم عامة بتبادل الحرارة المرافق للتحولات، مثل الاختلاط وتحول الحالة والتفاعلات الكيميائية وما إلى ذلك، وتشمل حسابات هذه الكميات من حيث سعة الحرارة وحرارة الاحتراق وحرارة التشكيل. تعتمد قوانين الكيمياء الحرارية على قانونين: [1]
|
سبق كلا القانونين أول قانون للديناميكا الحرارية (1850) لكنهما نتيجة مباشرة له.
بعض الكمـّيـّات ذات صلة بتفاعلات كيميائية
إن تطبيق المبدأ الأول في الديناميكا الحرارية على التفاعلات يؤدي إلى قانون هس (Hess)[تعليقة 1] الذي ينص على أن: الحرارة المرافقة لتفاعل ما لا تتعلق إلا بالحالتين الابتدائية والنهائية، وهي مستقلة عن الطريق المسلوك (عدد المراحل وطبيعتها مثلاً) على أن يتم التفاعل إما عند ضغط ثابت أو حجم ثابت.
تتوافق التفاعلات عملياً مع أحد هذين الشرطين، فهي تتم في حجم ثابت إذا أجريت في مفاعل مغلق كمحرك الاحتراق الداخلي، أو إذا كان حجم النواتج مماثلاً لحجم المواد المتفاعلة (جميع المواد الصلبة أو السائلة لها كتل حجمية متقاربة، أو في حالة الغازات إذا كان عدد المولات الداخلة في التفاعل مساوياً لعدد مولات النواتج). أما جميع التفاعلات التي تتم تحت الضغط الجوي فهي تفاعلات تتم تحت ضغط ثابت.
للتمييز بين هاتين الحالتين يمكن الانطلاق من تغير الطاقة الداخلية ΔU لجملة المواد المتفاعلة الذي يُعطى في أثناء التفاعل بالعلاقة: ΔU=W + Q
حيث Q وW: الحرارة والعمل المتبادلان مع الوسط الخارجي، ويكون العمل غالباً ناجماً عن قوى الضغط: W = - P. ΔV وبهذا يكون لكمية الحرارة شكلان للقياس:
1ـ الحجم ثابت: أي إن عمل قوى الضغط معدوم، وحرارة التفاعل بحجم ثابت Qv مساوية لتغير الطاقة الداخلية للجملة: Qv= ΔU.
2ـ الضغط ثابت: في هذه الحالة يرتبط تغير الحرارة Qp بتغير الأنطلبية[ر]:
Qp =ΔU - W= ΔU + P. ΔV ونظراً لثبات الضغط: Qp =ΔU + Δ (P.V)
وبالتالي Qp =ΔH، أي إن كمية حرارة التفاعل تحت ضغط ثابت تساوي تغير أنطلبية الجملة.
يُرى مما سبق أن إشارة كميتي حرارة التفاعل تماثل دوماً إشارة ΔU وΔH فنكتب مثلاً تفاعل احتراق الغرافيت بالشكل:(3)
(3)
اتختلف حرارتا التفاعل السابقتان عموماً إلا إذا اشتركت في التفاعل غازات، وترتبطان عندئذ ببعضهما، في حالة الغازات الكاملة، بالعلاقة: Qp = Qv+ (n2-n1).RT
حيث n1 وn2 عدد مولات الغازات المتفاعلة والناتجة على الترتيب.
يجب الانتباه إلى عدد من الاصطلاحات عند كتابة حرارة تفاعل:
1 - توافِق حرارة التفاعل كمية محددة من المواد المتفاعلة أو المنتَجة، هذه الكمية تظهر في معادلة التفاعل، أي إن مضاعفة أمثال المعادلة يقتضي مضاعفة الحرارة المرافقة أيضاً. وفي حالة تشكل مركّب بدءاً من عناصره تؤخذ أنطلبية التشكل العيارية مول واحد من المركب، والمقصود بعيارية أن القياس تم بالدرجة 298K وبالضغط b1 bar وبالشكل الفيزيائي الأكثر استقراراً للمواد المتفاعلة في هذه الشروط. تعد المراجع القديمة الضغط العياري مساوياً للضغط الجوي (b1.018 bar)، وقد تغير هذا الشرط حديثاً إلى القيمة 1 bar.
2 - بحالة تفاعل عكوس تُكتب القيمة الموافقة للاتجاه المباشر.
3 - يجب تحديد الحالة الفيزيائية لكل مادة في التفاعل، صلبة أم سائلة أم غازية.
4 - إذا لم تُذكر درجة الحرارة التي يتم عندها التفاعل عُدّت مساوية لـِ 298K، والمقصود بذلك أن المواد المتفاعلة أُخذت في هذه الدرجة كما النواتج النهائية. أما في أثناء التفاعل فيمكن أن تتغير درجة حرارة الجملة في أي اتجاه.
التحديد التجريبي لحرارتَي تفاعل
1- التحديد المباشر: يتم ذلك باستخدام مسعر حراري، فحرارة تفاعلات الاحتراق في حجم ثابت تحدد باستعمال ما يسمى «قنبلة حرارية» calorimetric bomb، وهي وعاء فولاذي ذو جدران مقاومة وحجم داخلي لايتجاوز نصف لتر يُدخَل فيه وزن محدد من المادة القابلة للاشتعال والأكسجين تحت ضغط 20 جو تقريباً. تُغمر القنبلة مغلقة في مسعر مائي ويتم إشعال المزيج كهربائياً ثم تُحسب كمية الحرارة المنتشرة من التفاعل من قياس ارتفاع درجة حرارة المسعر. يتم تحديد السعة الحرارية للقنبلة والمسعر وملحقاتهما من تجربة معايرة أولية لاحتراق حمض البنزويك وهو تفاعل حرارته بحجم ثابت Qv معروفة بدقة.
أما كميات حرارة التفاعلات التي تتم بالضغط الجوي بين مواد صلبة أو سائلة ومن دون انطلاق غازات، مثل تفاعل حمض كلور الماء مع ماءات الصوديوم، فتقاس باستخدام المسعر مباشرة عبر قياس ارتفاع درجة حرارة المواد المتفاعلة حين مزجها في المسعر.
2- التحديد غير المباشر: تُستخدَم لهذا الغرض مخططات هِس Hess، فيتم اختيار «طريقين» لتحقيق التفاعل، يتضمن كل منهما مرحلة أو مراحل عدة بحيث يكون التفاعل مجهول الحرارة جزءاً منها، وتكتب أنطلبية التفاعل الكلي في الطريقين، ونظراً لكون الحالتين الابتدائية والنهائية متماثلتين فإن قيمة الأنطلبية أو حرارة التفاعل تحت ضغط ثابت هي نفسها مما يسمح بحساب حرارة التفاعل المجهولة.
مثل للاِستيعاب:
يراد حساب أنطلبية تشكل الأستيلين C2H2 من معرفة كميات حرارة احتراق
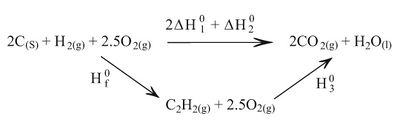
وكلها قابلة للقياس. فيوضع على التوازي احتراق مباشر لمولين من الفحم ومول من الهدروجين ثم تحول غير مباشر يتضمن تشكل مول من الأستيلين ثم احتراقه:الشكل (4),
(4)
وبالتالي يكون: الشكل (5)
(5)
وهي أنطلبية تَشَكُّل مولٍ واحدٍ من الأستيلين بالدرجة العادية من الحرارة (298K) وبالضغط الجوي.
3- تأثير درجة الحرارة:
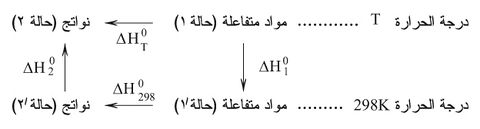
تتأثر كميتا حرارة التفاعل بدرجة الحرارة التي يجري التفاعل عندها، وهي عموماً الدرجة 298K أما التفاعلات التي تجري عند درجات حرارة أخرى فيمكن حساب قيم الأنطلبية أو تغير الطاقة الداخلية المرافقة لها بالاستفادة من مخططات هِس كما سبق:الشكل (6)
(6)
حيث ni عدد مولات المادة i وCi سعتها الحرارية تحت ضغط ثابت مقدرة بـِ Joul.mol-1. K-1 وΔT فرق درجتي الحرارة بين T و298K، توجد السعات الحرارية للمركبات والعناصر المختلفة عادة عند الدرجة k298K، في جداول للاستعانة بها في هذا الحساب. يُلاحظ أن اختلاف السعة الحرارية لمجموعي المواد المتفاعلة والنواتج هو السبب في تغير أنطلبية التفاعل مع تغير درجة الحرارة.
حرارة الرابطة
وتسمى أيضاً طاقة الرابطة أو أنطلبية الرابطة، وهي كمية الحرارة المرافقة لتشكل الرابطة بدءاً من ذرات معزولة وهي في الحالة الغازية تحت ضغط 1 بار. إن تشكل الرابطة الكيميائية ناشر للحرارة دوماً، وهذا يعني أن طاقة تشكل الرابطة سالبة القيمة، وهي مساوية بالقيمة ومعاكسة بالإشارة لطاقة تفكك الرابطة التي تعطى عادة في الجداول.
يمكن إذاً تعيين حرارة تشكل مادة مركبة أو بسيطة بدءاً من طاقات روابطها، فالطرق الفيزيائية المبنية على الدراسة المطيافية للمادة أسهل غالباً من الطرق الكيميائية وتسمح بتحديد بعض حرارات الروابط، مثل تصعّد الغرافيت (j710.6k.J.mo l-1) أو تفكك جزيئة (j493.2k.J.mo l-1). أما أنطلبية تفاعل ما فتُحسب بطرح مجموع طاقات الروابط الموجودة في المواد المتفاعلة من مجموع طاقات روابط المواد الناتجة.
حرارة التفاعل والتوازن الكيميائي
وضع فانت هوف Van’t Hoff عند دراسته لانزياح التوازن الكيميائي بتأثير الحرارة قانونه الذي يشير إلى أن ارتفاع درجة الحرارة يزيح التوازن باتجاه التفاعل الماص للحرارة، والعكس بالعكس، هذا النص يدل على أهمية معرفة حرارة التفاعل عند دراسة توازن كيميائي. أما الصيغة الرياضية للقانون فتعطى سواء للتفاعلات الحاصلة بحجم ثابت أو بضغط ثابت بالعلاقة:الشكل(7)
(7)
وبالتالي يمكن كتابتها في حالة الضغط الثابت بالشكل: الشكل (8)
(8)
وبمكاملة هذه العلاقة بين الدرجتين T1 وT يكون:الشكل (9)
(9)
إيجاد هذه المـُتـَكـَامـِـلَة (integral) يتم عبر استخدام العلاقة المساعدة التالية :
(*)
بـإيجاد المـُتـَكـَامـِـلَة تؤدّي العلاقة (9) إلى :
(10)
أي من الممكن معرفة عبارة K(T) إذا كان DΔH معروفاً بدلالة T، وفي مجال محدود من درجة الحرارة يُعد فيه ΔH ثابتاً تنتج العلاقة في الشكل (10)؛
وعلى العكس، تسمح معرفة قيمة ثابت التوازن عند درجتَي حرارة مختلفتين بتحديد حرارة التفاعل من تطبيق علاقة فانت هوف على مجال صغير:الشكل (11)
(11)
الكيمياء الحرارية والتنبؤ بإمكانية التفاعل
يؤدي المبدأ الثاني في الترموديناميك والقائل بالزيادة الدائمة في أنتروبية[ر] العالَم S إلى تابع حالة جديد هو الأنطلبية الحرة أو تابع جيبس Gibbs (فيزيائي أمريكي 1839-1903):
G = H - TS
إن ΔG هو سالب دوماً في أثناء تفاعل يحدث ذاتياً بضغط ودرجة حرارة ثابتين، أي إن التابع G يسعى إلى قيمة دنيا تتحقق عند الوصول إلى التوازن، فالتنبؤ بالتفاعل وجهته لا تعتمد على معرفة ΔH، وإنما على ΔG = ΔH -TΔS التي تدل وحدها على إمكانية حدوث هذا التفاعل.
توجد جداول تعطي قيم الأنتروبية للمواد المختلفة، بسيطة كانت أم مركبة، مستنتجة من قياسات حرورية (كالوريمترية) ولأنطلبية التشكل بدءاً من حالة مرجعية محددة، وذلك في الشروط النظامية (ضغط 1 بار، الدرجة k298K). فيمكن من هذه المعطيات حساب ΔG في الشروط نفسها:
ΔG0 = ΔH0 -TΔS0
ومنها يمكن استنتاج ثابت التوازن K للتفاعل الحاصل:
ΔG0 = RT.1nK
أما لمعرفة قيمة تغير الأنطلبية الحرة بدلالة درجة الحرارة ΔG (T)، فإن مكاملة علاقة جيبس - هلمهولتز:الشكل (12)
(12)
تسمح من معرفة ΔH بدلالة T بكتابة عبارة ΔG (T) ثم استنتاج K(T) من دون الحاجة إلى إجراء أي قياسات تجريبية للتوازن المدروس. وهكذا تبرز أهمية الكيمياء الحرارية في التنبؤ بالتفاعلات والدراسة المبدئية للتوازنات الكيمياوية.
انظر أيضاً
- Differential scanning calorimetry
- Important publications in thermochemistry
- Isodesmic reaction
- Principle of maximum work
- Reaction Calorimeter
- مبدأ تومسن-برتوليه
- يوليوس تومسن
- Thermodynamic databases for pure substances
- مسعر Calorimetry
تعليقات
- ^ هذا القانون هو منسوب لـگرمن هنري هس Germain Henri Hess (١٨٠٢ - ١٨٥٠م) وهو كيميائي سويسري الأصل ، درس طب بجامعة تارتو بإستونيا وبسبب نتائجه المتميـّزة اِستطاع أن يضيف دراساته بجامعة شتكهولم بالسويد ، ثم درس كيمياء بجامعة تارتو ، ثم اِنتقل مع أسرته إلى روسيا. اِشتغل هناك كطبيب فترة. ولاحقاً حصـّـل على منضب تدريس في مجال الكيمياء. واِستمر فيه حتى وفاته.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
مراجع
- ^ Perrot, Pierre (1998). A to Z of Thermodynamics. Oxford University Press. ISBN 0-19-856552-6.
المصادر
- Skinner, H. A.(ed.) (1975). Thermochemistry and thermodynamics. (MTP international review of science. Physical chemistry ; Ser. 2, Vol. 10) Butterworth, London, ISBN 0-408-70609-0
وصلات خارجية
- Thermochemistry - Britannica (1911)
- Thermochemistry - an overview










![{\displaystyle \int _{T_{1}}^{T}{1\cdot {d(logK_{p})}}=[logK_{p}]{{\Big |}_{T_{1}}^{T}}={logK_{p}}{(T)}-{logK_{p}}{(T_{1})}={\frac {{\Delta }H}{R}}\int _{T_{1}}^{T}{\frac {1}{T^{2}}}{dT}}](https://www.marefa.org/api/rest_v1/media/math/render/svg/21d87aba151dff5b2f90e76a76b1d1a5cab3070a)



