طور (مادة)
في العلوم الفيزيائية ، يطلق مصطلح طور إنگليزية: phase على أي مجموعة من الحالات لنظام فيزيائي جهري يكون عادة ذو تركيب كيمائي متجانس و خواص فيزيائية متجانسة . مثل الكثافة و البنية البلورية crystal structure و قرينة الانكسار refractive index وما إلى ذلك.
والطور هو حالة متوازنة ترموديناميكيّاً للمادة، تختلف عن الحالات المتوازنة الأخرى للمادة نفسها من حيث الخصائص الفيزيائية. ويُعرَف التحول من طور لآخر بالتحول الطوري phase transition، ويرتبط بتغييرات جوهرية لخصائص المادة. وتختلف الأطوار البلورية للمادة بعضها عن بعض بنمط البنية البلورية، والناقلية الكهربائية والخصائص الكهربائية والمغنطيسية، ووجود أو انعدام الناقلية الفائقة superconductivity وغيرها.[1]
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
مفهوم الطور في منظور التحريك الحراري
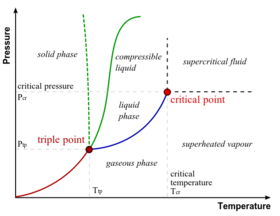
الطور من وجهة نظر التحريك الحراري بتجانس الجملة المدروسة. فالجملة المتجانسة هي أي جزء محاط بسطوح محددة تكون قيم خواصها إما ثابتة أو تتغير تغيرات مستمرة من نقطة إلى أخرى داخل الجملة، أي التي لا يوجد انقطاعات أو قفزات ظاهرة في قيمها عند التنقل داخلها. فوجود الماء مع الجليد مثلاً، يشكل جملة ذات طورين: طور الماء السائل وطور الماء الجامد (الجليد)، أي يوجد في الجملة منطقتان متجانستان متمايزتان ويحدث الانقطاع أو القفزة في قيمة الكتلة الحجمية عند اجتياز السطح الفاصل بين الماء والجليد. وفي الحالة العامة يمكن أن تتكون الجملة من عدة مناطق متجانسة تفصل بينها سطوح واضحة فتسمى جملة متعددة الأطوار multiphase system أو متغايرة التجانس heterogeneous system. تجدر الإشارة إلى أن للطور مفهوماً آخر في الحركات الدورية ومنها التيار الكهربائي المتناوب الذي يؤثر الطور في توليده ونقله، فهناك التيار وحيد الطور والثلاثي الطور أو متعدد الأطوار polyphase.
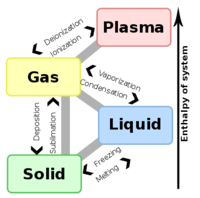
لا تقتصر فكرة الطور في التحريك الحراري على الأطوار المعروفة تقليديا: الغازية والسائلة والصلبة، بل يمكن أن تعمم، وفق هذا التعريف، لتشمل جملاً في الحالة الصلبة تحتوي نظامين بلوريين للمادة نفسها أي في حالة المادة متعددة الأشكال في بعض البلورات، أو في الحالة التي تتغير فيها المقاومة الكهربائية بين نقطة وأخرى فجأة فتنعدم في بعض أجزائها كما في النواقل الفائقة من النوع الثاني، أو في الحالة الصلبة بين منطقة مغنطيسية ومنطقة لا مغنطيسية. وقد يحدث في الحالة السائلة أيضاً أكثر من طور، كما في الهليوم السائل تحت الدرجة 2.4 درجة كلفن إذ تنعدم اللزوجة في بعض أجزائها بينما تبقى محدودة القيمة في أجزاء أخرى.
ومن الناحية الكيمياوية، قد تكون الجملة بسيطة مكونة من عنصر كيمياوي واحد (ذرات حديد مثلاً) أو من مركب كيمياوي (جزيئات أكسيد الحديد) أو عدد من المركبات (أنواع من أكاسيد الحديد). وإذا ما وجدت تحولات بين المركبات فإن عدد المركّبات يدخل في تحديد حالة الجملة المتغايرة التجانس إضافة إلى عدد الأطوار وذلك عبر عدد المتحولات أو الخواص المستقلة اللازمة لوصف حالة الجملة، وتعطي قاعدة جيبس Gibbs في الأطوار هذا العدد بالعلاقة f=n+2-r
( f عدد المتحولات المستقلة وn عدد المركّبات وr عدد الأطوار). وفي حال غياب التفاعلات الكيميائية يكون عدد المركبات مساوياً عدد أنواع الجزيئات الموجودة في الجملة. وقد نضطر من وجهة نظر فيزيائية إلى التمييز بين النظائر مع النظر إلى السلوك الكيمياوي. وتعدّ الجملة متجانسة أحياناً ولو كانت على شكل محلول أو مزيج أو خليط في الحالة الغازية أو السائلة أو الصلبة.
أنواع الطور

طور التوازن
عدد الأطوار
ظواهر بينية
طور الكريستال
الطور الانتقالي
 مقالة مفصلة: الطور الانتقالي
مقالة مفصلة: الطور الانتقالي
تكون الجملة في طور معين إذا خضعت لشروط خارجية محددة من ضغط و درجة حرارة، وهو يقابل الحالة التوازنية ضمن هذه الشروط. وقد يتغير الطور المقابل للحالة التوازنية عند تغير الشروط المطبقة إما بالانتقال إلى طور جديد بالمعنى التقليدي أو بالمعنى المعمم، غير أن سرعة هذا الانتقال تختلف باختلاف الطورين المقابلين فمنها ما يحدث في مدة قصيرة جداً ومنها ما يحدث في مدة طويلة جداً، وكلاهما يصعب قياسهما في الأحوال التجريبية العادية، وبالتالي فإن الوصول إلى الحالة التوازنية ليس متاحاً دائماً مما يغلّب وجود جمل متعددة الأطوار. يفيد تحديد الزمن المميز لانتقال معين كفائدة معرفة سرعة التفاعلات الكيمياوية.
من ناحية أخرى، تصنف الانتقالات تصنيفاً يساعد على تحديد متطلباتها ومنها سرعتها، فإذا احتاج الانتقال كمية من الحرارة ليتم التغير سمي تغيراً من النوع الأول ويحدث الانقطاع في الطاقة الداخلية، كما في حالة الانتقال من الجليد إلى السائل (الماء). أما إذا لم يترافق بتبادل حراري وإنما حدث الانقطاع في السعة الحرارية التي هي مشتق الطاقة الحرارية بالنسبة إلى درجة الحرارة، سمي تغيراً طورياً من النوع الثاني، كما في بعض التغيرات بين الأطوار المغنطيسية، وهكذا يزداد رقم النوع بحسب درجة المشتق الذي يحدث فيه الانقطاع.
تطبيقات
يغير وجود عدة أطوار في جملة معينة من خواص هذه الجملة سواء الميكانيكية أو المغنطيسية أو الكهربائية أو حتى الكيميائية منها. فالجملة ثنائية المركّبة: الحديد والكربون مثلاً تظهر خواص كثيرة تلبي خواص مطلوبة لصناعات مختلفة، بدءاً من الفولاذ غير القابل للصدأ حتى الفولاذ اللامغنطيسي وانتهاءً بالحديد الصب. كما تفيد دراسة التغيرات الطورية التفاعلات الكيمياوية وعلاقاتها الزمنية وضمن شروط مختلفة من الضغط والحرارة في تحديد التاريخ الجيولوجي للأرض أو لصخور منطقة منها. ويمتد ذلك لينطبق على الكواكب والكون.[2]
انظر أيضاً
الهوامش والمصادر
- ^ الطَّور، الموسوعة العربية
- ^ فوزي عوض. "الجمل المتعددة الأطوار". الموسوعة العربية.
وصلات خارجية
| State of aggregation
]].- French physicists find a solution that reversibly solidifies with a rise in temperature – α-cyclodextrin, water, and 4-methylpyridine