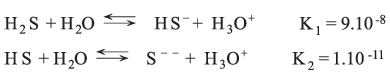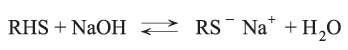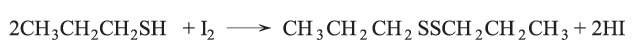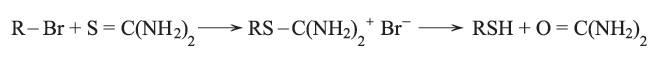كبريتيد الهيدروجين
|
| |||
| الأسماء | |||
|---|---|---|---|
| اسم أيوپاك
Hydrogen sulfide, sulfane
| |||
| أسماء أخرى
Sulfuretted hydrogen; sulfane; Hydrogen Sulfide; sulfur hydride; sour gas; sulfurated hydrogen; hydrosulfuric acid; sewer gas; stink damp; rotten egg gas; brimstone
| |||
| Identifiers | |||
| رقم CAS | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.070 | ||
| رقم EC |
| ||
| رقم RTECS |
| ||
| UN number | 1053 | ||
CompTox Dashboard (EPA)
|
|||
| الخصائص | |||
| الصيغة الجزيئية | H2S | ||
| كتلة مولية | 34.082 g/mol | ||
| المظهر | Colorless gas. | ||
| الكثافة | 1.363 g/L, gas. | ||
| نقطة الانصهار | |||
| نقطة الغليان | |||
| قابلية الذوبان في الماء | 0.25 g/100 mL (40 °C) | ||
| الحموضة (pKa) | 6.89 19±2 (see text) | ||
| البنية | |||
| الشكل الجزيئي | Bent | ||
| Dipole moment | 0.97 D | ||
| المخاطر | |||
تبويب الاتحاد الاوروپي (DSD)
|
Highly Flammable (F+) Very Toxic (T+) Dangerous for the environment (N) | ||
| توصيف المخاطر | R12, R26, R50 | ||
| تحذيرات وقائية | (S1/2), S9, S16, S36, S38, S45, S61 | ||
| NFPA 704 (معيـَّن النار) | |||
| نقطة الوميض | غاز قابل للاشتعال | ||
| حدود الانفجار | 4.3–46% | ||
| مركبات ذا علاقة | |||
ما لم يُذكر غير ذلك، البيانات المعطاة للمواد في حالاتهم العيارية (عند 25 °س [77 °ف]، 100 kPa). | |||
| مراجع الجدول | |||
كبريتيد الهيدروجين إنگليزية: Hygrogen Sulfide أو (هيدروجين مكبرت) H2S هو غاز سام كريه الرائحة تشبه رائحة عفن البيض. وهو غاز أثقل من الهواء ولذلك تجده في الأماكن العميقه في حالة تسربه. يستخرج من الغاز المصاحب للبترول ويتم فصله بالحراره وتتم معالجته وتكثيفه لتسهيل عملية نقله حيث يتم تصديره للخارج. يدخل في صناعة بعض الأدوية.
وكبريتيد الهيدروجين قابل للاشتعال. ويذوب ببطء في الماء مكوناً حمضاً ضعيفاً ثنائي الوظيفة الحمضية يُسمى حمض الهيدروكبريتيك، ويتسبب وجود كميات صغيرة من كبريتيد الهيدروجين في الجو في فقدان المشغولات الفضية لبريقها. ويقوم الكيميائيون عادة بتحضير كبريتيد الهيدروجين في المعمل عن طريق مزج حمض الهيدروكلوريك مع كبريتيد الحديد، ويستخدمون الغاز أساساً في تحليل مركبات المواد الأخرى. ويُستخدم كبريتيد الهيدروجين أيضاً في إنتاج مواد التشحيم ذات الضغط العالي والزيوت.
يُحضر غاز كبريت الهدروجين مخبرياً من تفاعل الحموض مع الكبريتيدات وغالباً ما يستعمل حمض كلور الماء مع كبريتيد الحديد وفق المعادلة:
أو من تسخين مزيج متساو من الكبريت والبارافين. أما صناعياً فيتم الحصول عليه من عمليات فصله عن غاز الاصطناع (يرافق غاز كبريت الهدروجين مزيج غاز الهدروجين مع غاز ثنائي أكسيد الكربون والذي يدعى غاز الاصطناع).
يُستخدم كبريت الهدروجين في التحليل الكيفي والكمي كاشفاً لترسيب الأيونات المعدنية، أما على المستوى الصناعي فيستخدم في تحضير غاز ثنائي أكسيد الكبريت[ر. الكبريت] SO2
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
التواجد
يحتوي البيض والكثير من المواد الأخرى على مركبات عضوية مكونة جزئياً من الكبريت. وعندما تتحلل مثل هذه المركبات يخرج منها كبريتيد الهيدروجين. ولهذا السبب يمكن أن نجد غاز كبريتيد الهيدروجين في الهواء حول أنابيب المجاري تحت الأرض والبالوعات. كما ينتج كبريتيد الهيدروجين عن تحلل الكبريتات المعدنية. وهو مايؤدي بالتالي إلى توافر هذا الغاز في المناجم والعيون المعدنية.
الخصائص
الإنتاج=
الإستخدامات
Production of thioorganic compounds
كبريتيد المعادن القلوية
الكيمياء التحليلية
Precursor to metal sulfides
تطبيقات متنوعة
إزالة الغازات من الوقود
التفاعل مع أكسيد الحديد
السلفرة الهيدروجينية
الأمان
السمية
مشتقات كبريت الهدروجين
مشتقات كبريت الهدروجين مركبات عضوية تحوي الكبريت في بنيتها ممثلاً بالزمرة -SH، وتعد مضاهيات مركبات الأكسجين العضوية الحاوية على الزمرة -OH. وهناك نوعان من هذه المركبات الحاوية على الزمرة -SH، التيولات التي ترتبط فيها الزمرة -SH بجذر أليفاتي، وتيو الفينولات التي ترتبط فيها الزمرة -SH بحلقة عطرية.
ومن مشتقات كبريت الهدروجين الإتيرات الكبريتية (التيوإترات) RSR وهي تعد مضاهيات للإترات ROR.
يعد النفط من أهم المصادر الطبيعية للتيولات، وتتوزع رئيسياً في قطفات النفط الخفيفة مثل الغازولين (بنزين السيارات) وهي المسؤولة عن الرائحة الكريهة في النفط.
لبعض مركبات الكبريت روائح جميلة ومستحبة عندما تكون بتراكيز منخفضة، فعلى سبيل المثال تُعزى رائحة الثوم والبصل الطازجين إلى وجود تيولات وكبريتيدات منخفضة الوزن الجزيئي، كذلك يعد المركب ثنائي متيل الكبريتيد المسؤول عن نكهة الشاي الأخضر، في حين يعد المركب 2-(4-متيل-3-حلقي الهكسينيل)-2- بروبان تيول المسؤول عن الطعم الفريد والمميز للكريفون ولكن في تراكيز ضئيلة جداً من مرتبة جزء من بليون.
1- التيولات الأليفاتية أو تيو الغول:
دعيت قديماً المركبتانات وهي مركبات عضوية للكبريت صيغتها المجملة RSH وترتبط الزمرة -SH فيها بجذر ألكيلي. تُسمى هذه المركبات بأخذ اسم الفحم الهدروجيني متبوعاً بالوسمة تيول، فعلى سبيل المثال يدعى المركب CH3-SH ميتان تيول أو متيل المركبتان .
تتميز التيولات بقوام سائل باستثناء الميتان تيول فهو غاز، ولهذه المركبات درجات غليان أخفض من الأغوال [ر. الغول] الموافقة بسبب قابليتها الضعيفة لتشكيل روابط هدروجينية ولهذا فإن انحلالها ضعيف في الماء مقارنة مع الأغوال. وهي مركبات سامة ذات رائحة كريهة إذ تكفي كميات صغيرة جداً من مركب الإيتان تيول من مرتبة 4.6×10-8 مغ للشعور بها، كما يعد المركب (E) -2-البوتن-1-تيول المسؤول الرئيس عن الرائحة الكريهة الصادرة عن حيوان الراكون الذي يقطن في شمالي القارة الأمريكية.
للثيولات خواص حمضية أقوى من الأغوال فهي تشكل مع ماءات الصوديوم أملاحاً تدعى التيولات أو المركبتيدات
كما تتشكل هذه الأملاح مع العناصر الثقيلة. تُصنف هذه الأملاح (التيولات) بأنها كواشف نوكليوفيلية nucleophilic (النوكليوفيل: هو المركب الشغوف بالشحن الموجبة) قوية فهي تعطي بتفاعلها مع الكيل الهالوجين الإترات التيولية وفق المعادلة:
تختلف التيولات عن الأغوال بسلوكها تجاه المؤكسدات المختلفة فعند تفاعلها مع مؤكسدات متوسطة القوة مثل الماء الأكسجيني أو الهواء ينتج مركبات ثنائي الكبريتيد RSSR. تعطي أكسدة التيولات باليود مركبات ثنائي الكبريتيد:
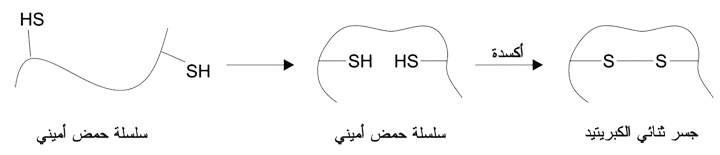
ويمكن الحصول على التيولات من جديد بعمليات إرجاع. يعد هذا التشكل العكوس لمركبات ثنائي الكبريتيد من العمليات البيولوجية إذ يشكل العديد من البروتينات والببتيدات الحاوية على زمرة SH حرة الارتباط ثنائي الكبريتيد. تستخدم الطبيعة هذه الآلية لربط سلاسل الحموض الأمينية.
أما عندما تستخدم مؤكسدات قوية مثل برمنغنات البوتاسيوم أو حمض الآزوت فينتج حموض السلفون R−SO3H.
ومن التفاعلات الأخرى للتيولات التفاعل مع الحموض الكربوكسيلية[ر] فتتشكل استرات تيو الحمض الكربوكسيلي R-−COSR التي يُحفَز تفاعل تشكلها بوجود الحموض القوية وتدعى المركبتالات والتي تعد بدورها الشكل الرئيس الذي يُعتمد عليه في نزع التيولات من النفط إضافة إلى المعالجة الهدروجينية المستخدمة في التخلص من مركبات الكبريت في النفط .
لاصطناع التيولات طرق عدة:
1- تفاعل الكيل الهالوجين [Cl, Br, I :X] RX مع الكبريتيدات مثل:
وتنتج مركبات ثنائي الكبريتيد منتجات ثانوية.
2- تفاعل الكيل الهالوجين مع مركب تيو البولة متبوعاً بحلمهة[ر] الناتج بهدروكسيد البوتاسيوم
3- تفاعل الأغوال مع كبريتيد الهدروجين عند درجات حرارة مرتفعة 300-400 س بوجود أكسيد الألمنيوم فيحل الكبريت محل الأكسجين.
4- تفاعل إضافة كبريت الهدروجين إلى الألكنات alkenes عند درجات حرارة 150-300 س بوجود حفّازات من أكسيد الألمنيوم وكبريتيد النيكل.
2- التيولات العطرية (أو ضروب تيو الفينول)
هي مركبات عضوية تحوي الكبريت في بنيتها ممثلاً بالزمرة -SH المرتبطة مباشرة مع حلقة عطرية، ويعد تيو الفينول أبسط ممثل عن هذه المجموعة. ينحل تيو الفينول في الإتانول والإتر والبنـزن C6H6 ولا ينحل في الماء. وهو يتميز بخواص حمضية إذ يتفاعل مع الهدروكسيدات القلوية مكوِّناً تيو الفينولات. تيو الفينول فعّال كيمياوياً فهو يتأكسد بسهولة بالهواء مشكلاً مركب ثنائي الفنيل ثنائي الكبريتيد في حين يتفاعل تيو الفينول مع الكلور مكوِّناً المركب C6H5SCl كلوريد كبريت الفنيل.
3- تيو الإترات (أو ضروب الكبريتيد العضوية)
هي مركبات عضوية لها الصيغة العامة R-S-R، وR باقية ألكيلية أو أريلية وتعد من مضاهيات الإترات. وتستحصل ضروب تيو الإتر بطرق عدة:
1- تفاعل ألكيل الهالوجين مع التيولات القلوية
أو من تفاعل ألكيل الهالوجين مع ضروب الكبريتيد القلوية
2- تفاعل إضافة التيولات إلى الألكنات بوجود البيروكسيدات والتشعيع بالأشعة فوق البنفسجية
3- تفاعل هالوجين السولفينيل مع الأرينات بوجود حموض لويس
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
استعمالاتها
تستخدم التيولات في تصنيع المبيدات الحشرية وأصبغة الأنديكو، كما تستخدم في فلكنة المطاط. ويستخدم تيو الفينول في اصطناع العديد من مركبات الكبريت وفي اصطناع منظمات البلمرة.
أما ضروب التيو إترات فتتأكسد حسب شروط التفاعل إلى السولفوكسيدات والسولفونات وتشكل أملاح السولفونيوم وتعد بذلك مركبات متوسطة مهمة في الاصطناع العضوي كما تستخدم ملدِّنات.
انظر أيضاً
المصادر
- [1]
- فرانسوا قره بيت. "كبريتيد الهيدروجين". الموسوعة العربية.
مصادر اضافية
- "Hydrogen Sulfide", Committee on Medical and Biological Effects of Environmental Pollutants, University Park Press, 1979, Baltimore. ISBN 0-8391-0127-9
- "Girl's suicide leaves dozens ill from fumes"
وصلات الخارجية
- International Chemical Safety Card 0165
- Concise International Chemical Assessment Document 53
- National Pollutant Inventory - Hydrogen sulfide fact sheet
- NIOSH Pocket Guide to Chemical Hazards
- MSDS safety data sheet
- Abstract of survey article on H2S as used by the body, by P. Kamoun
- Computational Chemistry Wiki
- NACE (National Association of Corrosion Epal)
- Access Safety (Online H2S Awareness Training)
- ECHA InfoCard ID from Wikidata
- Chemical articles with unknown parameter in Chembox
- Articles containing unverified chemical infoboxes
- Short description is different from Wikidata
- Articles containing إنگليزية-language text
- Inorganic sulfur compounds
- مركبات الكبريت
- مركبات الهيدروجين
- كيماويات كريهة الرائحة
- ملوثات
- أحماض
- بذرة كيمياء