أنتيمون
| |||||||||||||||||||||||||
| صفات عامة | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
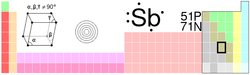
| الإسم, الرقم, الرمز | أنتيمون, Sb, 51 | ||||||||||||||||||||||||
| سلاسل كيميائية | أشباه الفلزات | ||||||||||||||||||||||||
| المجموعة, الدورة, المستوى الفرعي | p , 5 , 15 | ||||||||||||||||||||||||
| المظهر | رمادي ذو بريق فضي 
| ||||||||||||||||||||||||
| كتلة ذرية | 121.760(1) g/mol | ||||||||||||||||||||||||
| شكل إلكتروني | [Kr] 4d10 5s2 5p3 | ||||||||||||||||||||||||
| عدد الإلكترونات لكل مستوى | 2, 8, 18, 18, 5 | ||||||||||||||||||||||||
| خواص فيزيائية | |||||||||||||||||||||||||
| الحالة | صلب | ||||||||||||||||||||||||
| كثافة عندح.غ. | 6.697 ج/سم³ | ||||||||||||||||||||||||
| كثافة السائل عند m.p. | 6.53 ج/سم³ | ||||||||||||||||||||||||
| نقطة الإنصهار | 903.78 ك 630.63 م ° 1167.13 ف ° | ||||||||||||||||||||||||
| نقطة الغليان | 1860 ك 1587 م ° 2889 ف ° | ||||||||||||||||||||||||
| حرارة الإنصهار | kJ/mol 19.79 | ||||||||||||||||||||||||
| حرارة التبخر | kJ/mol 193.43 | ||||||||||||||||||||||||
| السعة الحرارية | (25 25.23 C (م) ° ( J/(mol·K | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| الخواص الذرية | |||||||||||||||||||||||||
| البنية البللورية | rhombohedral | ||||||||||||||||||||||||
| حالة التأكسد | −3, 3, 5 | ||||||||||||||||||||||||
| سالبية كهربية | 2.05 (مقياس باولنج) | ||||||||||||||||||||||||
| طاقة التأين (المزيد) |
1st: 834 kJ/mol | ||||||||||||||||||||||||
| 2nd: 1594.9 kJ/mol | |||||||||||||||||||||||||
| 3rd: 2440 kJ/mol | |||||||||||||||||||||||||
| نصف قطر ذري | 145 pm | ||||||||||||||||||||||||
| نصف قطر ذري (حسابيا) | 133 pm | ||||||||||||||||||||||||
| نصف القطر التساهمي | 138 pm | ||||||||||||||||||||||||
| متفرقة | |||||||||||||||||||||||||
| الترتيب المغناطيسي | no data | ||||||||||||||||||||||||
| مقاومة كهربية | 20 °C 417 nΩ·m | ||||||||||||||||||||||||
| توصيل حراري | (300 K ك ) 24.4 (W/(m·K) | ||||||||||||||||||||||||
| تمدد حراري | (25 °C) 11.0 µm/(m·K) | ||||||||||||||||||||||||
| سرعة الصوت (قضيب رفيع) | (20 °م) 3420 m/s | ||||||||||||||||||||||||
| معامل يونج | 55 GPa | ||||||||||||||||||||||||
| معامل القص | 20 GPa | ||||||||||||||||||||||||
| معاير الحجم | 42 GPa | ||||||||||||||||||||||||
| صلابة موس | 3.0 | ||||||||||||||||||||||||
| رقم برينل للصلادة | 294 MPa | ||||||||||||||||||||||||
| رقم التسجيل | 7440-36-0 | ||||||||||||||||||||||||
| النظائر المهمة | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| المراجع | |||||||||||||||||||||||||
أنتيمون Antimony (ويُنطق: 'æntəməʊni) أو الكحل أو حجر "إثمد" هو عنصر كيميائي في الجدول الدوري يرمز له بالرمز Sb (لاتينية: stibium, تعني "علامة") و رقم ذري 51. وكشبه فلز, فالأنتيمون له أربعة أشكال allotropic. الشكل المستقر للأنتيمون هو معدني أزرق-أبيض. الأنتيمون الأصفر والأسود هم لافلزات غير مستقرة. ويستخدم الأنتيمون في صناعة طلاء مقاومات للهب, الخزف, طلاءات المينا, وتشكيلة واسعة من السبائك, الإلكترونيات, و المطاط.
أنتيمون أو الكحل هو حجر "إثمد" يتواجد في أصفهان والمغرب, وهو يتفتت وأوجهه لماعة.
يطحن الحجر ويستخدم مسحوقه لتكحيل العيون, كان معروفا لدى الفراعنة وكانوا يستخدمونه فتظهر عيونهم واسعة وجميلة.
الإثمد من أشباه الفلزات ورمزه Sb ويدعى بالأنتموان ويوجد في الطبيعة بشكل حر ولكن على الأغلب يوجد بحالة سولفيد أو أكسيد أو أوكسي سولفيد وشكله بحالة سولفيد هو المصدر الرئيسي للمعدن, وهو معدن هشّ سريع التفتت، لامع ذو تركيب رقائقي بلون أبيض فضي.
إذا أخذت قطعة صغيرة منه وثبتت بمسامير صغيرة على قطعة خشبية ولف حول المسامير ملف سلك نحاسي يوصل طرفه إلى هوائي والطرف الآخر إلى دبوس وسماعة يمكن الحصول جهاز راديو بسيط.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
التاريخ
عرف الأنتيمون منذ القديم، فقد كانت العرب وقبائل آسيا البدوية تستعمل حجر الإثمد أو حجر الكحل collyrium stone لمداواة الجروح وكحلاً للعيون، وحجر الكحل هو مركب كبريت الأنتيمون السريع التفتت الذي لِفُتاته بريق ولمعان. استخرج الرومان الأنتيمون ولم يعرفوا استعمالاته وفوائده، كما عرفه الكلدانيون والصينيون والكوريون واليابانيون. وقد أشار برتلو Berthelot إلى أن العرب استعملوا الإثمد أو الأنتيمون في محاولاتهم تحضير الذهب. ويعتقد أن أصل كلمة أنتيمون عربي «أثموند athmond» (هي في الحقيقة إثْمِد ithmid أو أَثْمُد athmod) حمله قسطنطين الإفريقي Constantinos africanus إلى اوروبا، فدخل اللاتينية باسم «اثموديوم athmodium» أو «أثيموديوم athimodium» وغدا في اللاتينية الوسطى «أنتيمونيوم antimonium» ثم استقر على أنْتِموني antimony بالإنگليزية.[1]
وكان العالمان بليني وديوسقوريدس قد أطلقا عليه تسميتي «ستيبي stibi» أو «ستيبيوم stibium» اليونانيتين، ثم أُطلقت هذه التسمية على المعدن نفسه الذي استخرجه بازيل فالانتان Basile Valentin في نهاية القرن الخامس عشر من كبريته المدعو ستيبين stibine، ومن هنا جاء رمزه Sb.
استخداماته
- صناعة البطاريات.
- السبائك قليلة الاحتكاك. يدخل الأنتيمون مع بعض المعادن لتكوين سبائك خليطة متميِّزة، فهو يُكْسبها مزيداً من القساوة والمقاومة، ويكوِّن مع الرصاص الكثير من السبائك الخليطة (الأشابات) المتعددة الاستعمال تبعاً لنسبته فيها، كصنع صفائح المدخرات أو حروف الطباعة (80 % رصاص و20 % أنتيمون)، والمواد المقاومة للائتكال والتحات.
- ويكوِّن مع القصدير سبيكة خليطة تُستعمل في صنع المواعين المنزلية (المعدن الإنكليزي: 90% قصدير و10% أنتيمون) و(المعدن الفضي: 85% قصدير و15% أنتيموان).
- ويستعمل الأنتيمون أيضاً في صنع مهابط الإصدار الضوئي photoemission المؤلفة من طبقة من أنتيمون السيزيوم SbCs3. ويدخل الأنتيمون في تركيب الخلايا الناقلة للضوء photoconductor، والمتكونة من بلورات أحادية من أنتيمون الأنديوم أو الغاليوم، للكشف عن الأشعة تحت الحمراء.
- وتستعمل بعض مشتقات الأنتيموان المعدنية في الطب مقشِّعةً. أما مشتقاته العضوية فتفيد في معالجة داء الليْشمانيات leishmaniasis وداء البلهَرْسيَة bilharziasis.
- صناعة عيدان الكبريت matches .
- أغلفة الكابلات الكهربائية.
- المساند والدحرجات.
- كمواد لحام وسباكة الخالية من الرصاص.
تواجده
لا تتجاوز نسبة الأنتيموان في الطبيعة 5×10-5%، ونادراً ما يوجد حراً كما في منطقة بيلان من لواء اسكندرون، وغالباً ما يكون متحداً بحالة كبريت الأنتيموان Sb2S3، أو متحداً مع الأكسجين Sb2O3 كما في الجزائر.
انصهاره
ينصهر الأنتيمون إلى أشكال متغايرة الصفات allotropic متعددة، وأحد هذه الأشكال ثابت وهو الشكل المعدني القَصِف والمائل إلى الزرقة وذو البريق المعدني والذي يدعى الأنتيمون الفضي؛ أما الآخر فيدعى الأنتيمون الأصفر، وهو غير ثابت إلا تحت الدرجة -90ْ س. تبلغ كثافة الأنتيموان في حالته الصلبة 6.70، وهو ينصهر في الدرجة 630ْس، ويغلي في الدرجة 1640ْس. ويحضر بطرائق عدة، أهمها شيّ الستيبين في الهواء فيتحول إلى الأكسيد الثلاثي الذي يرجع بالكربون أو بالهيدروجين.
إنتاجه
| الدولة | طن | % من إجمالي انتاج العالم |
|---|---|---|
| جمهورية الصين الشعبية | 126 000 | 81.5 |
| روسيا | 12 000 | 7.8 |
| جنوب أفريقيا | 5 023 | 3.3 |
| تاجيكستان | 3 480 | 2.3 |
| بوليفيا | 2 430 | 1.6 |
| أكبر خمسة | 148 933 | 96.4 |
| إجمالي العالم | 154 538 | 100.0 |
Chiffres de 2003, métal contenue dans les minerais et concentrés, source : L'état du monde 2005
مركّباته
- خامس فلوريد الأنتيمون SbF5
- ثالث أكسيد الأنتيمون Sb2O3
- Stibine (antimony trihydride SbH3)
- أنتيمونيد الإنديوم (InSb)
يتحد الأنتيمون بالأكسجين والكبريت والهالوجينات بالتسخين، ويعطي المركبات الموافقة لحالة الأكسدة +3 في الغالب. ولما كان كمون الأكسدة والإرجاع النظامي E0 للجملة Sb3+/Sb يساوي +0.21 فلطاً، فالأنتيمون لا يتأثر بالحموض غير المؤكسدة، لكنه ينحل في حمض الكبريت المركز بالحرارة معطياً كبريتات الأنتيمون III، وينحل في حمض الآزوت معطياً أكسيد الأنتيمون Sb2O3، وينحل أيضاً في الماء الملكي معطياً الشاردة المعقدة [+SbCl6]- (يتألف الماء الملكي من جزيء من حمض الآزوت و3 جزيئات من حمض كلور الماء). انظر أيضاً مركبات الأنتيمون.
مشتقاته الرئيسية
يتميز الأنتيمون في معظم مركباته برقمي أكسدة +3 و+5 كما هي الحال في أكسيدَيْه: Sb2O3 وSb2O5 وفي هاليدَيْه halides: SbX3 وSbX5. أما هيدريدُهُ hydride فمقتصر على حالة الأكسدة +3 (SbH3). ويعد ثلاثي اكسيد الأنتيموان Sb2O3 من الأكاسيد المذبذبة amphoteric. والأنتيمون قليل الذوبان في الماء، لكنه ينحل في الحموض المركزة معطياً الأملاح الموافقة التي تتحلل بالماء hydrolyse بسهولة إلى مركبات الأنتيمونيل . وينحل أيضاً في الأسس (معطياً مركبات الأنتيمونيت SbO3-3)؛ ويتبلمر في الحالة البخارية إلى Sb4O6. وهو يُثَبِّتُ الأكسجين في الدرجات العالية من الحرارة (800ْس) متحولاً إلى الأكسيد Sb2O4، ويعطي مع طرطرات البوتاسيوم مركباً يستعمل في الطب مقيئاً. أما خامس أكسيد الأنتيموان Sb2O5 فهو أكسيد حمضي، ينحل في الأسس وخاصة في هيدروكسيد البوتاسيوم معطياً أنتيمونات البوتاسيوم K[Sb(OH)6]. ولم تعزل الحموض الموافقة للأكسيدين المذكورين مع أن أملاحهما معروفة.
يعرف من هاليدات الأنتيمون كلور الأنتيمون III باسم «زبدة الأنتيمون» وهو سهل التحلل بالماء إلى كلور الأنتيمونيل SbOCl. وكان يُعرف قديماً باسم «مسحوق ألگاروث» Algaroth (طبيب إيطالي عاش في القرن السادس عشر) وقد استعمله هذا الطبيب مادة مطهرة ومقيئة. أما هدريد الأنتيمون (SbH3)III فغاز سام يتميز برائحة كريهة، ويحضر بفعل الهدْروجين الوليد في أكسيد الأنتيمون III. يتفكك هدريد الأنتيموان بسهولة بالحرارة (200ْس) إلى مكوناته، ويصاحب تفككه هذا انفجار، ويقوم SbH3 بدورِ مرجعٍ لكثير من المركبات.
المصادر
- ^ عبد المجيد البلخي. "الأنتيموان". الموسوعة العربية. Retrieved 2012-03-01.
مراجع
- W. F. Albright "Notes on Egypto-Semitic Etymology. II", The American Journal of Semitic Languages and Literatures, Vol. 34, No. 4. (Jul., 1918), pp. 215-255. JSTOR link. esp p.230
- Endlich, F.M. "On Some Interesting Derivations of Mineral Names", The American Naturalist, Vol. 22, No. 253. (Jan., 1888), pp. 21-32. JSTOR link. p.28
- Kirk-Othmer Encyclopedia of Chemical Technology, 5th ed. 2004. Entry for antimony.
- Lippmann, E O von [Edmund Oscar]. 1919. Entstehung und Ausbreitung der Alchemie, teil 1. Berlin: Julius Springer. In German.
- Moorey, PRS. 1994. Ancient Mesopotamian Materials and Industries: the Archaeological Evidence. New York: Clarendon Press.
- Priesner, Claus and Figala, Karin, eds. 1998. Alchemie. Lexikon einer hermetischen Wissenschaft. München: C.H. Beck. 412 p. In German.
- Sarton, George. 1935. Review of Al-morchid fi'l-kohhl, ou Le guide d'oculistique, translated by Max Meyerhof. Isis (Feb. 1935), 22(2):539-542 (The journal Isis is in the JSTOR archive.) In French.
- Shotyk, William; Krachler, Michael; Chen, Bin. Contamination of Canadian and European bottled waters with antimony from PET containers J. Environ. Monit 2006, 8:288-292 DOI: 10.1039/b517844b
- Los Alamos National Laboratory - Antimony
- Public Health Statement for Antimony
- محمد علي المنجد وعبد المجيد البلخي، الكيمياء اللاعضوية 2 (المطبعة التعاونية بدمشق 1988-1989).
- PAUL PASCAL, Traité de chimie minérale (Masson, Paris).
انظر أيضاً
وصلات خارجية
- National Pollutant Inventory - Antimony and compounds
- WebElements.com - Antimony
- انتاج مناجم العالم من الأنتيمون, حسب الدولة
- Chemistry in its element podcast (MP3) from the Royal Society of Chemistry's Chemistry World: Antimony
{clear}}
| الجدول الدوري | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Uub | Uut | Uuq | Uup | Uuh | Uus | Uuo | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||